Флуоцинонид
Fluocinonide
Фармакологическое действие
Флуоцинонид — кортикостероид, обладает противозудным, сосудосуживающим и противовоспалительным эффектом.
Фармакокинетика
Всасывание минимальное (~1 %). Степень всасывания препарата определяется целостностью кожи и использованием окклюзивных перевязок. Наличие воспалительных процессов увеличивает степень всасывания через кожу. Проникая через эпителий, активное вещество распределяется идентично системным кортикостероидам. В большей степени связывается с белками крови. Метаболизируется в печени, затем — в почках. Некоторые метаболиты попадают в желчный пузырь.
Показания
Препарат применяется в лечении воспалительных процессов на коже, которые сопровождаются зудом.
Противопоказания
- Гиперчувствительность,
- беременность,
- лактация (грудное вскармливание).
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — C.
Адекватных и строго контролируемых исследований по безопасности применения флуоцинонида при беременности не проведено. Кортикостероиды проходят через плаценту. Исследования на животных показали, что более сильные кортикостероиды обладают тератогенными свойствами. Потенциальный риск для человека неизвестен.
Необходимо наблюдение за новорождёнными, чьи матери во время беременности получали кортикостероиды (из-за возможного риска развития недостаточности надпочечников у плода и новорождённого).
Применение флуоцинонида во время беременности противопоказано.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения флуоцинонида в период грудного вскармливания не проведено.
Кортикостероиды проникают в грудное молоко.
Рекомендуется прекратить грудное вскармливание в случае необходимости применения препарата.
Способ применения и дозы
Наносить мазь необходимо на место поражения тонким слоем 2–4 раза на день, в зависимости от степени развития болезни. При псориатических поражениях кожи или других острых заболеваниях накладывают поверх мази стерильную повязку. Если инфекция развивается, необходимо прекратить использование окклюзивных повязок и провести комплексную противомикробную терапию.
Побочные действия
Зуд; жжение; раздражение кожи; сухость кожи; фолликулит; стрии; гипертрихоз; дерматит; аллергический контактный дерматит; мацерание кожи; атрофия кожи; вторичная инфекция.
Передозировка
Случаи передозировки не зафиксированы.
Взаимодействие
Не рекомендуется длительное применение актуальных кортикостероидов совместно с окклюзивными повязками при обширном поражении кожи.
Использование препарата возможно в комплексе с антибактериальными и противогрибковыми препаратами. Если комплексное лечение не даёт ожидаемых результатов, необходимо отменить флуоцинонид до тех пор, пока не будет установлен адекватный контроль развития инфекции.
Классификация
-
АТХ
C05AA11, D07AC08
-
Фармакологическая группа
-
Категория при беременности по FDA
C
(риск не исключается)
Информация о действующем веществе Флуоцинонид предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Флуоцинонид, содержатся в инструкции производителя, прилагаемой к упаковке.
ПРЕДУПРЕЖДЕНИЯ
Содержится как часть МЕРЫ ПРЕДОСТОРОЖНОСТИ Раздел.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
Влияние на эндокринную систему
Системная абсорбция актуальных кортикостероидов, включая ванозин, может вызвать обратимое подавление гипофиза гипофиза (HPA) с потенциалом клинической недостаточности глюкокортикостероидов. Это может произойти во время лечения или при прекращении местного кортикостероида. Кроме того, использование крема VANOS может подавлять иммунную систему дольше 2 недель.
Подавление оси HPA наблюдалось с помощью крема VANOS, 0,1% вводили один или два раза в день у 2 из 18 взрослых пациентов с псориазом бляшечного типа, у 1 из 31 взрослого пациента с атопическим дерматитом и у 4 из 123 педиатрических пациентов с применением атопического дерматита.
Из-за потенциальной системной абсорбции использование актуальных кортикостероидов, включая крем ванос, может потребовать регулярного обследования пациентов на предмет подавления оси гПа. Факторы, которые предрасполагают пациента к использованию местного кортикостероида для подавления оси гПа, включают использование более сильных стероидов, использование на больших поверхностях, использование в течение длительных периодов времени, использование под закрытием, использование на измененном кожном барьере и использование у пациентов с печеночной недостаточностью. ,.
Тест стимуляции АКТГ может быть полезен при оценке пациентов на подавление оси гПа. Если подавление оси гПа задокументировано, следует попытаться постепенно вывести препарат, снизить частоту использования или заменить менее мощный стероид. Проявления надпочечников
Отказ может потребовать дополнительных системных кортикостероидов. Восстановление функции оси гПа обычно происходит немедленно и завершается после прекращения применения актуальных кортикостероидов.
Синдром Кушинга, гипергликемия и воздействие скрытого сахарного диабета также могут возникать в результате системного всасывания актуальных кортикостероидов.
Одновременное использование более одного продукта, содержащего кортикостероиды, может увеличить общую системную абсорбцию актуальных кортикостероидов.
Исследования на педиатрических пациентах показали обратимое подавление оси гПа после использования крема VANOS. Из-за их большего соотношения поверхности кожи и массы тела педиатрические пациенты могут быть более восприимчивыми, чем взрослые, к системной токсичности через эквивалентные дозы крема VANOS.
Местные побочные эффекты с актуальными кортикостероидами
Местные побочные эффекты чаще возникают при окклюзионном применении, длительном применении или применении кортикостероидов с более высокой активностью. Реакции могут включать атрофию, бороздки, телеангиэктазы, жжение, зуд, раздражение, сухость, фолликулит, угревые сыпь, гипопигментация, периоральный дерматит, аллергический контактный дерматит, вторичная инфекция и милиария. Некоторые локальные побочные эффекты могут быть необратимыми.
сопутствующие кожные инфекции
Если сопутствующие кожные инфекции присутствуют или развиваются, следует использовать подходящий противогрибковый или антибактериальный агент. Если благоприятная реакция не появляется сразу, использование крема VANOS следует прекратить до тех пор, пока инфекция не будет должным образом контролироваться.
Аллергический контактный дерматит
Если появляется раздражение, крем VANOS следует прекратить и начать соответствующую терапию. Аллергический контактный дерматит с кортикостероидами обычно диагностируется путем наблюдения за не заживлением, а не установления клинического обострения, как большинство актуальных продуктов, которые не содержат кортикостероидов. Такое наблюдение должно быть подтверждено подходящими диагностическими пластырями.
Информация для пациента
Пациенты, использующие крем VANOS, должны получить следующую информацию и инструкции. Эта информация предназначена для обеспечения безопасного и эффективного использования этого препарата. Это не раскрытие всех возможных неблагоприятных или непреднамеренных последствий :
- Крем VANOS следует использовать по указанию врача. Это только для внешнего использования. Избегайте контакта с глазами. Не следует использовать на лице, паху и подмышках.
- Крем VANOS не следует использовать для других, кроме того, для которого он был предписан.
- обработанная область кожи не должна быть перевязана или иным образом покрыта или обернута таким образом, чтобы врач не давал указаний.
- Пациенты должны сообщать о признаках местных побочных эффектов своему врачу.
- Другие продукты кортикостероидов не следует использовать со сливками VANOS без предварительной консультации с врачом.
- Как и в случае других кортикостероидов, терапию следует прекратить при достижении контроля. Если в течение 2 недель улучшение не наблюдается, пациент должен быть проинструктирован обратиться к врачу. Безопасность использования крема VANOS в течение более 2 недель не установлена.
- Пациентам следует информировать не использовать более 60 г крема VANOS в неделю. Не используйте более половины 120 г трубки в неделю.
- Пациенты должны сообщить своим врачам, что вы используете крем VANOS при рассмотрении операции.
- Пациенты должны мыть руки после приема лекарств.
Доклиническая токсикология
Карциногцинцис, мутагенез, нарушение фертильности
Долгосрочное тестирование на животных не проводилось для оценки канцерогенного потенциала ванозина из-за тяжелой иммуносупрессии, вызванной в 13-недельном исследовании на дермальных крысах. Влияние флуоцинонида на фертильность не изучалось.
Флуоцинонид не показал признаков мутагенного или кластогенного потенциала на основании результатов двух in vitro тесты на генотоксичность (тест на выбросы и тест на хромосомную аберрацию с использованием лимфоцитов человека). Тем не менее, флуоцинонид был положительным для кластогенного потенциала, когда он был в in vivo — Анализ микроядер мыши был протестирован.
Актуальное (кожное) использование 0,0003% -0,03% флуоцинонидных сливок у крыс один раз в день в течение 13 недель приводило к профилю токсичности, который обычно ассоциировался с длительным воздействием кортикостероидов, включая снижение толщины кожи, атрофию надпочечников и тяжелую иммуносупрессию. NOAEL не может быть определен в этом исследовании. Дополнительно, актуально (дермальный) Использование 0,1% флуоцинонидного крема плюс воздействие UVR на безволосых мышей в течение 13 недель и 150-900 мг / кг / день 0,1% флуоцинонидного крема для минипигов (модель, это приближается к коже человека в течение 13 недель) привело к подавлению оси HPA, связанной с глюкокортикоидом, некоторые признаки иммуносупрессии были обнаружены в исследовании дермальных минипигов. Хотя клиническая значимость результатов, полученных животными, для человека неясна, постоянная иммуносупрессия, связанная с глюкокортикоидами, может увеличить риск заражения и, возможно, риск канцерогенеза.
Актуальные дозы 0% (свободно-флуоцинонидный носитель), 0,0001%, 0,005% и 0,001% флуоцинонидный крем были исследованы в 52-недельном исследовании кожной фотоканцерогенности (40-недельное лечение с последующим 12-недельным наблюдением) в час. Местное лечение с увеличением концентрации флуоцинонидных сливок не имело побочных эффектов в этом исследовании. Результаты этого исследования показывают, что местное лечение кремом VANOS не улучшит фотоканциногенез.
Используйте в определенных группах населения
Беременность
Тератогенные эффекты: Беременность категории С
Не существует адекватных и контролируемых исследований у беременных женщин. Поэтому крем VANOS следует использовать только во время беременности, если потенциальное использование оправдывает потенциальный риск для плода.
Было показано, что кортикостероиды являются тератогенными у лабораторных животных при системном введении в относительно низких дозах. Было показано, что некоторые кортикостероиды являются тератогенными после кожного применения у лабораторных животных.
Кормящие матери
Системно вводимые кортикостероиды встречаются в грудном молоке и могут подавлять рост, ухудшать выработку эндогенных кортикостероидов или вызывать другие нежелательные эффекты. Неизвестно, может ли местное введение кортикостероидов привести к достаточному системному всасыванию для получения обнаруживаемых количеств в грудном молоке. Тем не менее, принимая во внимание важность препарата для матери, следует решить, следует ли прекратить грудное вскармливание или прекратить прием лекарства.
Педиатрическое использование
Безопасность и эффективность крема VANOS у педиатрических пациентов в возрасте до 12 лет не установлены; поэтому использование у педиатрических пациентов в возрасте до 12 лет не рекомендуется.
Подавление оси HPa было изучено в 4 последовательных когортах педиатрических пациентов с атопическим дерматитом, которые покрывают по меньшей мере 20% поверхности тела и получали крем VANOS один раз в день или два раза в день. Первая когорта из 31 пациента (Среднее 36,3% BSA) От 12 до <18 лет; вторая когорта включала 31 пациента (Среднее 39,0% BSA) 6 <12 лет; третья когорта включала 30 пациентов (Среднее 34,6% BSA) 2 <6 лет; четвертая когорта включала 31 пациента (Среднее 40,0% BSA) 3 месяца <2 года. Крем VANOS вызывал подавление оси HPa у 1 пациента в группе два раза в день в когорте 1, у 2 пациентов в группе два раза в день в когорте 2 и у 1 пациента в группе два раза в день в когорте 3. Последующие тесты через 14 дней после прекращения лечения, которые были доступны для всех 4 угнетенных пациентов, показали обычно привлекательную ось HPA. В начале исследования были признаки атрофии кожи, и тяжесть не была определена, что затрудняет оценку местной безопасности кожи. Таким образом, безопасность крема VANOS не была установлена у пациентов в возрасте до 12 лет.
Подавление оси HPa не изучалось у пациентов с псориазом в возрасте до 18 лет.
Из-за более высокого отношения массы кожи к массе тела педиатрические пациенты подвергаются более высокому риску, чем взрослые, при подавлении оси гПа и синдроме Кушинга, если их лечить местными кортикостероидами. Поэтому у вас более высокий риск надпочечниковой недостаточности во время или после прекращения лечения. Побочные эффекты, включая бороздки, были зарегистрированы при ненадлежащем использовании актуальных кортикостероидов у младенцев и детей.
У детей, получающих актуальные кортикостероиды, было зарегистрировано подавление оси HPa, синдром Кушинга, линейная задержка роста, отсроченное увеличение веса и внутричерепная гипертензия. Проявления подавления надпочечников у детей включают низкий уровень кортизола в плазме и отсутствие реакции на косинтропин (АКТГ1-24) стимуляция. Проявления внутричерепной гипертонии включают в себя бральские роднички, головную боль и двусторонний папиллед.
Гериатрическое применение
Клинические испытания крема VANOS не включали достаточное количество субъектов в возрасте 65 лет и старше, чтобы определить, ответили ли вы иначе, чем более молодые.
These highlights do not include all the information needed to use fluocinonide cream USP, 0.1% safely and effectively. See full prescribing information for fluocinonide cream USP, 0.1%.
Fluocinonide Cream USP, 0.1%
For topical use
Initial U.S. Approval: 1971
INDICATIONS AND USAGE
Fluocinonide cream USP, 0.1% is a corticosteroid indicated for the relief of the inflammatory and pruritic manifestations of corticosteroid responsive dermatoses in patients 12 years of age or older. (1)
Limitation of Use:
- Treatment beyond 2 consecutive weeks is not recommended and the total dosage should not exceed 60 g per week because of the potential for the drug to suppress the hypothalamic-pituitary-adrenal (HPA) axis. (1)
- Avoid use on the face, groin, or axillae. (1.2)
- Avoid use in perioral dermatitis or rosacea.
DOSAGE AND ADMINISTRATION
For topical use only. Fluocinonide cream USP, 0.1% is not for ophthalmic, oral, or intravaginal use. (2)
Psoriasis: apply a thin layer once or twice daily to the affected skin areas. (2)
Atopic Dermatitis: apply a thin layer once daily to the affected skin areas. (2)
Corticosteroid Responsive Dermatoses, other than psoriasis or atopic dermatitis: apply a thin layer once or twice daily to the affected areas. (2)
DOSAGE FORMS AND STRENGTHS
Cream, 0.1% (3)
CONTRAINDICATIONS
None (4)
WARNINGS AND PRECAUTIONS
- Fluocinonide cream USP, 0.1% has been shown to suppress the HPA axis. Systemic absorption of fluocinonide cream USP, 0.1% may produce reversible hypothalamic-pituitary-adrenal (HPA) axis suppression, Cushing’s syndrome, hyperglycemia and unmask latent diabetes (5.1)
- Systemic absorption may require evaluation for HPA axis suppression (5.1)
- Modify use should HPA axis suppression develop (5.1)
- Potent corticosteroids, use on large areas, prolonged use or occlusive use may increase systemic absorption (5.3)
- Local adverse reactions with topical steroids may include atrophy, striae, irritation, acneiform eruptions, hypopigmentation and allergic contact dermatitis and may be more likely to occur with occlusive use or more potent corticosteroids (5.3)
- Children may be more susceptible to systemic toxicity when treated with topical corticosteroids. (5.1, 8.4)
ADVERSE REACTIONS
The most commonly reported adverse reactions (≥1%) were headache, application site burning, nasopharyngitis, and nasal congestion. (6)
To report SUSPECTED ADVERSE REACTIONS, contact Taro Pharmaceuticals U.S.A., Inc., at 1-866-923-4914 or FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
See 17 for PATIENT COUNSELING INFORMATION and FDA-approved patient labeling.
Revised: 2/2016
FULL PRESCRIBING INFORMATION: CONTENTS*
1 INDICATIONS AND USAGE
1.1 Indication
1.2 Limitation of Use
2 DOSAGE AND ADMINISTRATION
3 DOSAGE FORMS AND STRENGTHS
4 CONTRAINDICATIONS
5 WARNINGS AND PRECAUTIONS
5.1 Effect on Endocrine System
5.2 Local Adverse Reactions with Topical Corticosteroids
5.3 Concomitant Skin Infections
5.4 Allergic Contact Dermatitis
6 ADVERSE REACTIONS
6.1 Clinical Trials Experience
6.2 Postmarketing Experience
8 USE IN SPECIFIC POPULATIONS
8.1 Pregnancy
8.3 Nursing Mothers
8.4 Pediatric Use
8.5 Geriatric Use
10 OVERDOSAGE
11 DESCRIPTION
12 CLINICAL PHARMACOLOGY
12.1 Mechanism of Action
12.2 Pharmacodynamics
12.3 Pharmacokinetics
13 NONCLINICAL TOXICOLOGY
13.1 Carcinogenesis, Mutagenesis, Impairment of Fertility
14 CLINICAL STUDIES
16 HOW SUPPLIED/STORAGE AND HANDLING
17 PATIENT COUNSELING INFORMATION
- *
- Sections or subsections omitted from the full prescribing information are not listed.
1.1 Indication
Fluocinonide cream USP, 0.1% is indicated for the relief of the inflammatory and pruritic manifestations of corticosteroid responsive dermatoses in patients 12 years of age or older [see Use in Specific Populations (8.4)].
1.2 Limitation of Use
Treatment beyond 2 consecutive weeks is not recommended and the total dosage should not exceed 60 g per week because the safety of fluocinonide cream USP, 0.1% for longer than 2 weeks has not been established and because of the potential for the drug to suppress the hypothalamic-pituitary-adrenal (HPA) axis. Therapy should be discontinued when control of the disease is achieved. If no improvement is seen within 2 weeks, reassessment of the diagnosis may be necessary. Do not use more than half of the 120 g tube per week.
Fluocinonide cream USP, 0.1% should not be used in the treatment of rosacea or perioral dermatitis, and should not be used on the face, groin, or axillae.
For topical use only. Fluocinonide cream USP, 0.1% is not for ophthalmic, oral, or intravaginal use.
For psoriasis, apply a thin layer of fluocinonide cream USP, 0.1% once or twice daily to the affected skin areas as directed by a physician. Twice daily application for the treatment of psoriasis has been shown to be more effective in achieving treatment success during 2 weeks of treatment.
For atopic dermatitis, apply a thin layer of fluocinonide cream USP, 0.1% once daily to the affected skin areas as directed by a physician. Once daily application for the treatment of atopic dermatitis has been shown to be as effective as twice daily treatment in achieving treatment success during 2 weeks of treatment [see Clinical Studies (14)].
For corticosteroid responsive dermatoses, other than psoriasis or atopic dermatitis, apply a thin layer of fluocinonide cream USP, 0.1% once or twice daily to the affected areas as directed by a physician.
Cream, 0.l%.
Each gram of fluocinonide cream USP, 0.1% contains 1 mg of fluocinonide in a white to off-white cream base.
5.1 Effect on Endocrine System
Systemic absorption of topical corticosteroids, including fluocinonide cream USP, 0.1%, can produce reversible hypothalamic-pituitary-adrenal (HPA) axis suppression with the potential for clinical glucocorticosteroid insufficiency. This may occur during treatment or upon withdrawal of the topical corticosteroid. In addition, the use of fluocinonide cream USP, 0.1% for longer than 2 weeks may suppress the immune system [see Nonclinical Toxicology (13.1)].
HPA axis suppression has been observed with fluocinonide cream USP, 0.1% applied once or twice daily in 2 out of 18 adult patients with plaque-type psoriasis, 1 out of 31 adult patients with atopic dermatitis and 4 out of 123 pediatric patients with atopic dermatitis [see Use in Specific Population (8.4) and Clinical Pharmacology (12.2)].
Because of the potential for systemic absorption, use of topical corticosteroids, including fluocinonide cream USP, 0.1%, may require that patients be periodically evaluated for HPA axis suppression. Factors that predispose a patient using a topical corticosteroid to HPA axis suppression include the use of more potent steroids, use over large surface areas, use over prolonged periods, use under occlusion, use on an altered skin barrier, and use in patients with liver failure.
An ACTH stimulation test may be helpful in evaluating patients for HPA axis suppression. If HPA axis suppression is documented, an attempt should be made to gradually withdraw the drug, to reduce the frequency of application, or to substitute a less potent steroid.
Manifestations of adrenal insufficiency may require supplemental systemic corticosteroids. Recovery of HPA axis function is generally prompt and complete upon discontinuation of topical corticosteroids.
Cushing’s syndrome, hyperglycemia, and unmasking of latent diabetes mellitus can also result from systemic absorption of topical corticosteroids.
Use of more than one corticosteroid-containing product at the same time may increase the total systemic absorption of topical corticosteroids.
Studies conducted in pediatric patients demonstrated reversible HPA axis suppression after use of fluocinonide cream USP, 0.1%. Pediatric patients may be more susceptible than adults to systemic toxicity from equivalent doses of fluocinonide cream USP, 0.1% due to their larger skin surface-to-body-mass ratios [See Use in Specific Populations (8.4)].
5.2 Local Adverse Reactions with Topical Corticosteroids
Local adverse reactions may be more likely to occur with occlusive use, prolonged use or use of higher potency corticosteroids. Reactions may include atrophy, striae, telangiectasis, burning, itching, irritation, dryness, folliculitis, acneiform eruptions, hypopigmentation, perioral dermatitis, allergic contact dermatitis, secondary infection, and miliaria. Some local adverse reactions may be irreversible.
5.3 Concomitant Skin Infections
If concomitant skin infections are present or develop, an appropriate antifungal or antibacterial agent should be used. If a favorable response does not occur promptly, use of fluocinonide cream USP, 0.1% should be discontinued until the infection has been adequately controlled.
5.4 Allergic Contact Dermatitis
If irritation develops, fluocinonide cream USP, 0.1% should be discontinued and appropriate therapy instituted. Allergic contact dermatitis with corticosteroids is usually diagnosed by observing failure to heal rather than noting a clinical exacerbation as with most topical products not containing corticosteroids. Such an observation should be corroborated with appropriate diagnostic patch testing.
6.1 Clinical Trials Experience
Because clinical studies are conducted under widely varying conditions, adverse reaction rates observed in the clinical studies of a drug cannot be directly compared to rates in the clinical studies of another drug and may not reflect the rates observed in practice.
In clinical trials, a total of 443 adult subjects with atopic dermatitis or plaque-type psoriasis were treated once daily or twice daily with fluocinonide cream USP, 0.1% for 2 weeks. The most commonly observed adverse reactions in these clinical trials were as follows:
Safety in patients 12 to 17 years of age was similar to that observed in adults.
6.2 Postmarketing Experience
The following adverse reactions have been identified during post approval use of fluocinonide cream USP, 0.1%:
Administration Site Conditions: discoloration, erythema, irritation, pruritus, swelling, pain and condition aggravated.
Immune System Disorders: hypersensitivity.
Nervous System Disorders: headache and dizziness.
Skin and Subcutaneous Tissue Disorders: acne, dry skin, rash, skin exfoliation and skin tightness.
Because these reactions are reported voluntarily from a population of uncertain size, it is not always possible to reliably estimate their frequency or establish a causal relationship to drug exposure.
8.1 Pregnancy
Teratogenic Effects: Pregnancy Category C
There are no adequate and well-controlled studies in pregnant women. Therefore, fluocinonide cream USP, 0.1% should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus.
Corticosteroids have been shown to be teratogenic in laboratory animals when administered systemically at relatively low dosage levels. Some corticosteroids have been shown to be teratogenic after dermal application in laboratory animals.
8.3 Nursing Mothers
Systemically administered corticosteroids appear in human milk and could suppress growth, interfere with endogenous corticosteroid production, or cause other untoward effects. It is not known whether topical administration of corticosteroids could result in sufficient systemic absorption to produce detectable quantities in breast milk. Nevertheless, a decision should be made whether to discontinue nursing or to discontinue the drug, taking into account the importance of the drug to the mother.
8.4 Pediatric Use
Safety and efficacy of fluocinonide cream USP, 0.1% in pediatric patients younger than 12 years of age have not been established; therefore use in pediatric patients younger than 12 years of age is not recommended.
HPA axis suppression was studied in 4 sequential cohorts of pediatric patients with atopic dermatitis covering at least 20% of the body surface area, treated once daily or twice daily with fluocinonide cream USP, 0.1%. The first cohort of 31 patients (mean 36.3% BSA) 12 to < 18 years old; the second cohort included 31 patients (mean 39.0% BSA) 6 to < 12 years old; the third cohort included 30 patients (mean 34.6% BSA) 2 to < 6 years old; the fourth cohort included 31 patients (mean 40.0% BSA) 3 months to < 2 years old. Fluocinonide cream USP, 0.1% caused HPA-axis suppression in 1 patient in the twice daily group in Cohort 1, 2 patients in the twice daily group in Cohort 2, and 1 patient in the twice daily group in Cohort 3. Follow-up testing 14 days after treatment discontinuation, available for all 4 suppressed patients, demonstrated a normally responsive HPA axis. Signs of skin atrophy were present at baseline and severity was not determined making it difficult to assess local skin safety. Therefore, the safety of fluocinonide cream USP, 0.1% in patients younger than 12 years of age has not been demonstrated [see Warnings and Precautions (5.2)].
HPA axis suppression has not been evaluated in patients with psoriasis who are less than 18 years of age.
Because of a higher ratio of skin surface area to body mass, pediatric patients are at a greater risk than adults of HPA-axis suppression and Cushing’s syndrome when they are treated with topical corticosteroids. They are therefore also at greater risk of adrenal insufficiency during or after withdrawal of treatment. Adverse effects including striae have been reported with inappropriate use of topical corticosteroids in infants and children.
HPA-axis suppression, Cushing’s syndrome, linear growth retardation, delayed weight gain, and intracranial hypertension have been reported in children receiving topical corticosteroids. Manifestations of adrenal suppression in children include low plasma cortisol levels and absence of response to cosyntropin (ACTH1-24) stimulation. Manifestations of intracranial hypertension include bulging fontanelles, headaches, and bilateral papilledema.
8.5 Geriatric Use
Clinical studies of fluocinonide cream USP, 0.1% did not include sufficient numbers of subjects aged 65 and over to determine whether they respond differently from younger subjects.
Topically applied fluocinonide cream USP, 0.1% can be absorbed in sufficient amounts to produce systemic effects [see Warnings and Precautions (5.1)].
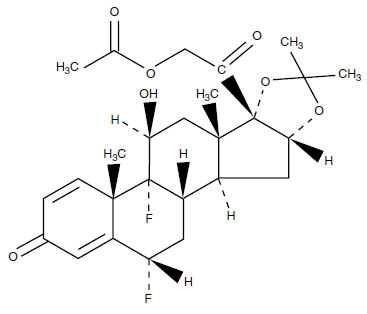
Fluocinonide cream USP, 0.1% contains fluocinonide, a synthetic corticosteroid for topical dermatologic use. The corticosteroids constitute a class of primarily synthetic steroids used topically as anti-inflammatory and antipruritic agents. Fluocinonide has the chemical name 6 alpha, 9 alpha-difluoro-11 beta, 21-dihydroxy-16 alpha, 17 alpha-isopropylidenedioxypregna-1, 4-diene-3,20-dione 21-acetate. Its chemical formula is C26H32F2O7 and it has a molecular weight of 494.58.
It has the following chemical structure:
Fluocinonide, USP is an almost odorless white to creamy white crystalline powder. It is practically insoluble in water and slightly soluble in ethanol.
Each gram of fluocinonide cream USP, 0.1% contains 1 mg micronized fluocinonide in a cream base of carbomer 940 (carbopol 980), ceteareth-20, citric acid, diethylene glycol monoethyl ether (transcutol P), polyethylene glycol, propylene glycol, sorbitan monostearate, and trolamine.
12.1 Mechanism of Action
Corticosteroids play a role in cellular signaling, immune function, inflammation, and protein regulation; however, the precise mechanism of action of fluocinonide cream USP, 0.1% in corticosteroid responsive dermatoses is unknown.
12.2 Pharmacodynamics
Vasoconstrictor studies performed with fluocinonide cream USP, 0.1% in healthy subjects indicate that it is in the super-high range of potency as compared with other topical corticosteroids; however, similar blanching scores do not necessarily imply therapeutic equivalence.
Application of fluocinonide cream USP, 0.1% twice daily for 14 days in 18 adult subjects with plaque-type psoriasis (10–50% BSA, mean 19.6% BSA) and 31 adult subjects (17 treated once daily; 14 treated twice daily) with atopic dermatitis (2-10% BSA, mean 5% BSA) showed demonstrable HPA-axis suppression in 2 subjects with psoriasis (with 12% and 25% BSA) and 1 subject with atopic dermatitis (treated once daily, 4% BSA) where the criterion for HPA-axis suppression is a serum cortisol level of less than or equal to 18 micrograms per deciliter 30 minutes after stimulation with cosyntropin (ACTH1-24) [see Warnings and Precautions (5.1)].
HPA-axis suppression following application of fluocinonide cream USP, 0.1% (once or twice daily) was also evaluated in 123 pediatric patients from 3 months to < 18 years of age with atopic dermatitis (mean BSA range 34.6 % — 40.0 %). HPA-axis suppression was observed in 4 patients in the twice daily groups. Follow-up testing 14 days after treatment discontinuation demonstrated a normally responsive HPA axis in all 4 suppressed patients [see Warnings and Precautions (5.1) and Use in Specific Populations (8.4)].
12.3 Pharmacokinetics
The extent of percutaneous absorption of topical corticosteroids is determined by many factors including the vehicle and the integrity of the epidermal barrier. Topical corticosteroids can be absorbed from normal intact skin. Inflammation and/or other disease processes in the skin may increase percutaneous absorption.
13.1 Carcinogenesis, Mutagenesis, Impairment of Fertility
Long-term animal studies have not been performed to evaluate the carcinogenic potential of fluocinonide cream USP, 0.1% because of severe immunosuppression induced in a 13-week dermal rat study. The effects of fluocinonide on fertility have not been evaluated.
Fluocinonide revealed no evidence of mutagenic or clastogenic potential based on the results of two in vitro genotoxicity tests (Ames test and chromosomal aberration assay using human lymphocytes). However, fluocinonide was positive for clastogenic potential when tested in the in vivo mouse micronucleus assay.
Topical (dermal) application of 0.0003%-0.03% fluocinonide cream to rats once daily for 13 weeks resulted in a toxicity profile generally associated with long term exposure to corticosteroids including decreased skin thickness, adrenal atrophy, and severe immunosuppression. A NOAEL could not be determined in this study. In addition, topical (dermal) application of 0.1% fluocinonide cream plus UVR exposure to hairless mice for 13 weeks and 150-900 mg/kg/day of 0.1% fluocinonide cream to minipigs (a model which more closely approximates human skin) for 13 weeks produced glucocorticoid-related suppression of the HPA axis, with some signs of immunosuppression noted in the dermal minipig study. Although the clinical relevance of the findings in animals to humans is not clear, sustained glucocorticoid-related immune suppression may increase the risk of infection and possibly the risk for carcinogenesis.
Topical doses of 0% (fluocinonide cream vehicle), 0.0001%, 0.005% and 0.001% fluocinonide cream were evaluated in a 52 week dermal photocarcinogenicity study (40 weeks of treatment followed by 12 weeks of observation) conducted in hairless albino mice with concurrent exposure to low level ultraviolet radiation. Topical treatment with increasing concentrations of fluocinonide cream did not have an adverse effect in this study. The results of this study suggest that topical treatment with fluocinonide cream would not enhance photocarcinogenesis.
Two adequate and well-controlled efficacy and safety studies of fluocinonide cream USP, 0.1% have been completed, one in adult subjects with plaque-type psoriasis (Table 2), and one in adult subjects with atopic dermatitis (Table 3). In each of these studies, subjects with between 2% and 10% body surface area involvement at baseline treated all affected areas either once daily or twice daily with fluocinonide cream USP, 0.1% for 14 consecutive days. The primary measure of efficacy was the proportion of subjects whose condition was cleared or almost cleared at the end of treatment. The results of these studies are presented in the tables below as percent and number of patients achieving treatment success at Week 2.
No efficacy studies have been conducted to compare fluocinonide cream USP, 0.1% with any other topical corticosteroid product, including fluocinonide cream 0.05%.
Fluocinonide cream USP, 0.1% is white to off-white in color and is supplied in tubes as follows:
120 g (NDC 45861-064-01)
Store at 20° to 25°C (68° to 77°F) [see USP Controlled Room Temperature].
Keep the tube tightly closed.
[See FDA-approved patient labeling (Patient Information)]
Patients using fluocinonide cream USP, 0.1% should receive the following information and instructions. This information is intended to aid in the safe and effective use of this medication. It is not a disclosure of all possible adverse or unintended effects:
- Fluocinonide cream USP, 0.1% is to be used as directed by the physician. It is for external use only. Avoid contact with the eyes. It should not be used on the face, groin, and underarms.
- Fluocinonide cream USP, 0.1% should not be used for any disorder other than that for which it was prescribed.
- The treated skin area should not be bandaged or otherwise covered or wrapped, so as to be occlusive unless directed by the physician.
- Patients should report to their physician any signs of local adverse reactions.
- Other corticosteroid-containing products should not be used with fluocinonide cream USP, 0.1% without first talking to the physician.
- As with other corticosteroids, therapy should be discontinued when control is achieved. If no improvement is seen in 2 weeks, the patient should be instructed to contact a physician. The safety of the use of fluocinonide cream USP, 0.1% for longer than 2 weeks has not been established.
- Patients should be informed to not use more than 60 g per week of fluocinonide cream USP, 0.1%. Do not use more than half of the 120 g tube per week.
- Patients should inform their physicians that they are using fluocinonide cream USP, 0.1% if surgery is contemplated.
- Patients should wash their hands after applying medication.
Manufactured for: Pharmaceutica North America, Inc., Glendale, CA 91204
Made in Canada
Revised: January, 2016
PK-8060-0
125
Read the Patient Information that comes with Fluocinonide Cream USP, 0.1% before you start using it and each time you get a refill. There may be new information. This leaflet does not take the place of talking to your doctor about your condition or treatment.
What is Fluocinonide Cream USP, 0.1%?
Fluocinonide Cream USP, 0.1% is a prescription corticosteroid medicine used on the skin (topical) to treat adults and children 12 years and older with certain skin conditions that cause red, flaky, and itchy skin.
- You should not use Fluocinonide Cream for longer than 2 weeks in a row.
- You should not use more than 60 grams of Fluocinonide Cream or more than half of the 120 gram tube in 1 week.
- Fluocinonide Cream should not be used:
- if you have skin swelling or redness on the nose of face (rosacea)
- for a scaly or bumpy rash around your mouth (perioral dermatitis)
- on your face, underarms, or groin area
It is not known if Fluocinonide Cream USP, 0.1% is safe and effective in children under 12 years of age.
What should I tell my doctor before using Fluocinonide Cream USP, 0.1%?
Before using Fluocinonide Cream USP, 0.1%, tell your doctor if you:
- have had irritation or other skin reaction to a steroid medicine in the past
- adrenal gland problems
- plan to have surgery
- are pregnant or plan to become pregnant. It is not known if Fluocinonide Cream will harm your unborn baby. Talk to your doctor if you are pregnant or plan to become pregnant.
- are breast-feeding or plan to breastfeed. It is not known if Fluocinonide Cream passes into your breast milk. Talk to your doctor about the best way to feed your baby if you use Fluocinonide Cream.
Tell your doctor about all the medicine you take including prescriptions and non-prescriptions medicines, vitamins, and herbal supplements. Especially tell your doctor if you take a corticosteroid medicine by mouth or use other products on your skin that contain corticosteroids. Ask your doctor or pharmacist if you are not sure.
Know the medicines you take. Keep a list of your medicines with you to show your doctor and pharmacist when you get a new medicine.
How should I use Fluocinonide Cream USP, 0.1%?
- See «What is Fluocinonide Cream USP, 0.1%?»
- Use Fluocinonide Cream exactly as your doctor tells you.
- This medicine is for use on the skin only. Do not use Fluocinonide Cream in your eyes, mouth or vagina.
- Wash your hands after you use Fluocinonide Cream.
- Do not use Fluocinonide Cream for longer than 2 weeks in a row.
- Talk to your doctor if your skin does not get better after 2 weeks of treatment with Fluocinonide Cream.
- Do not bandage or cover the skin treated with Fluocinonide Cream unless your doctor tells you to.
What are the possible side effects with Fluocinonide Cream USP, 0.1%?
Fluocinonide Cream may cause side effects, including:
-
Symptoms of a disorder where the adrenal gland does not make enough of certain hormones (adrenal insufficiency) during treatment or after stopping treatment. Your doctor may do blood tests to check you for adrenal insufficiency while you are using Fluocinonide Cream. Tell your doctor if you have any of these symptoms of adrenal insufficiency:
- tiredness that worsens and does not go away
- nausea or vomiting
- dizziness or fainting
- muscle weakness
- irritability and depression
- loss of appetite
- weight loss
-
Cushing’s syndrome, when the body is exposed to too much of the hormone cortisol. Your doctor may do tests to check for this. Symptoms can include:
- weight gain, especially around your upper back and midsection
- slow healing of cuts, insect bites and infections
- tiredness and muscle weakness
- depression, anxiety and irritability
- roundness of your face (moon face)
- new or worsening high blood pressure
The most common side effect of Fluocinonide Cream USP, 0.1% is burning of your skin treated with Fluocinonide Cream USP, 0.1%.
Talk to your doctor about any side effect that bothers you or that does not go away. These are not all the side effects with Fluocinonide Cream USP, 0.1%. Ask your doctor or pharmacist for more information.
Call your doctor for medical advice about side effects. You may report side effects to FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
You may also report side effects to Taro at 1-866-923-4914.
How should I store Fluocinonide Cream USP, 0.1%?
- Store Fluocinonide Cream at 20°C to 25°C (68°F to 77°F).
- Keep the tube tightly closed.
Keep Fluocinonide Cream USP, 0.1% and all medicines out of the reach of children.
General information about Fluocinonide Cream USP, 0.1%
Medicines are sometimes prescribed for purposes other than those listed in the Patient Information leaflet. Do not use Fluocinonide Cream for a condition for which it was not prescribed. Do not give Fluocinonide Cream to other people, even if they have the same symptoms you have. It may harm them.
This Patient Information leaflet summarizes the most important information about Fluocinonide Cream. If you would like more information, talk with your doctor. You can also ask your pharmacist or doctor for information about Fluocinonide Cream that is written for healthcare professionals.
What are the ingredients in Fluocinonide Cream USP, 0.1%?
Active ingredient: fluocinonide 0.1%
Inactive ingredients: carbomer 940 (carbopol 980), ceteareth-20, citric acid, diethylene glycol monoethyl ether (transcutol P), polyethylene glycol, propylene glycol, sorbitan monostearate, and trolamine.
This Patient Information has been approved by the U.S. Food and Drug Administration.
Manufactured for: Pharmaceutica North America, Inc., Glendale, CA 91204
Made in Canada
Revised: January, 2016
PK-8060-0
125
NDC 45861-064-01
120 g
Fluocinonide
Cream USP, 0.1%
FOR TOPICAL USE ONLY
NOT FOR OPHTHALMIC, ORAL, OR INTRAVAGINAL USE
Rx only
Keep this and all medications out of the reach of children.
Fluocinonide Cream Description
Fluocinonide Cream, USP 0.05% is intended for topical administration. The active component is the corticosteroid fluocinonide, which is the 21-acetate ester of fluocinolone acetonide and has the chemical name pregna-1,4-diene-3,20-dione, 21-(acetyloxy)-6,9-difluoro-11-hydroxy-16,17-[(1-methylethylidene)bis(oxy)]-, (6∝,11ß,16∝). Its molecular formula is C
26H
32F
2O
7, and has the molecular weight of 494.53. It has the following chemical structure:
Fluocinonide Cream, USP 0.05% contains fluocinonide 0.5 mg/g in a cream base consisting of citric acid, 1,2,6-hexanetriol, polyethylene glycol-8000, propylene glycol and stearyl alcohol. This white cream vehicle is greaseless, non-staining, anhydrous and completely water miscible. The base provides emollient and hydrophilic properties.
In the Fluocinonide Cream, USP 0.05% formulation, the active ingredient is totally in solution.
Fluocinonide Cream — Clinical Pharmacology
Topical corticosteroids share anti-inflammatory, antipruritic and vasoconstrictive actions.
The mechanism of anti-inflammatory activity of the topical corticosteroids is unclear. Various laboratory methods, including vasoconstrictor assays, are used to compare and predict potencies and/or clinical efficacies of the topical corticosteroids. There is some evidence to suggest that a recognizable correlation exists between vasoconstrictor potency and therapeutic efficacy in man.
Pharmacokinetics: The extent of percutaneous absorption of topical corticosteroids is determined by many factors including the vehicle, the integrity of the epidermal barrier, and the use of occlusive dressings.
Topical corticosteroids can be absorbed from normal intact skin. Inflammation and/or other disease processes in the skin increase percutaneous absorption. Occlusive dressings substantially increase the percutaneous absorption of topical corticosteroids. Thus, occlusive dressings may be a valuable therapeutic adjunct for treatment of resistant dermatoses. (See
DOSAGE AND ADMINISTRATION.)
Once absorbed through the skin, topical corticosteroids are handled through pharmacokinetic pathways similar to systemically administered corticosteroids.
Corticosteroids are bound to plasma proteins in varying degrees. Corticosteroids are metabolized primarily in the liver and are then excreted by the kidneys. Some of the topical corticosteroids and their metabolites are also excreted into the bile.
Indications and Usage for Fluocinonide Cream
Fluocinonide Cream, USP 0.05% is indicated for the relief of the inflammatory and pruritic manifestations of corticosteroid-responsive dermatoses.
Contraindications
Fluocinonide cream is contraindicated in those patients with a history of hypersensitivity to any of the components of the preparation.
Precautions
General: Systemic absorption of topical corticosteroids has produced reversible hypothalamic-pituitary-adrenal (HPA) axis suppression, manifestations of Cushing’s syndrome, hyperglycemia, and glucosuria in some patients.
Conditions which augment systemic absorption include the application of the more potent steroids, use over large surface areas, prolonged use, and the addition of occlusive dressings.
Therefore, patients receiving a large dose of a potent topical steroid applied to a large surface area or under an occlusive dressing should be evaluated periodically for evidence of HPA axis suppression by using the urinary free cortisol and ACTH stimulation tests. If HPA axis suppression is noted, an attempt should be made to withdraw the drug, to reduce the frequency of application, or to substitute a less potent steroid.
Recovery of HPA axis function is generally prompt and complete upon discontinuation of the drug. Infrequently, signs and symptoms of steroid withdrawal may occur, requiring supplemental systemic corticosteroids.
Children may absorb proportionally larger amounts of topical corticosteroids and thus be more susceptible to systemic toxicity. (See
PRECAUTIONS-Pediatric Use.) If irritation develops, topical corticosteroids should be discontinued and appropriate therapy instituted.
As with any topical corticosteroid product, prolonged use may produce atrophy of the skin and subcutaneous tissues. When used on intertriginous or flexor areas, or on the face, this may occur even with short term use.
In the presence of dermatological infections, the use of an appropriate antifungal or antibacterial agent should be instituted. If a favorable response does not occur promptly, the corticosteroid should be discontinued until the infection has been adequately controlled.
Information for the Patient: Patients using topical corticosteroids should receive the following information and instructions:
1. This medication is to be used as directed by the physician. It is for external use only. Avoid contact with the eyes.
2. Patients should be advised not to use this medication for any disorder other than for which it was prescribed.
3. The treated skin area should not be bandaged or otherwise covered or wrapped as to be occlusive unless directed by the physician.
4. Patients should report any signs of local adverse reactions especially under occlusive dressing.
5. Parents of pediatric patients should be advised not to use tight-fitting diapers or plastic pants on a child being treated in the diaper area, as these garments may constitute occlusive dressings.
Laboratory Tests: The following tests may be helpful in evaluating HPA axis suppression:
Urinary free cortisol test
ACTH stimulation test
Carcinogenesis, Mutagenesis, and Impairment of Fertility: Long-term animal studies have not been performed to evaluate the carcinogenic potential or the effect on fertility of topical corticosteroids.
Studies to determine mutagenicity with prednisolone and hydrocortisone have revealed negative results.
Pregnancy Category C: Corticosteroids are generally teratogenic in laboratory animals when administered systemically at relatively low dosage levels. The more potent corticosteroids have been shown to be teratogenic after dermal application in laboratory animals. There are no adequate and well-controlled studies in pregnant women on teratogenic effects from topically applied corticosteroids. Therefore topical corticosteroids should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus. Drugs of this class should not be used extensively on pregnant patients, in large amounts, or for prolonged periods of time.
Nursing Mothers: It is not known whether topical administration of corticosteroids could result in sufficient systemic absorption to produce detectable quantities in breast milk. Systemically administered corticosteroids are secreted into breast milk in quantities
not likely to have a deleterious effect on the infant. Nevertheless, caution should be exercised when topical corticosteroids are administered to a nursing woman.
Pediatric Use: Pediatric patients may demonstrate greater susceptibility to topical corticosteroid-induced hypothalamic-pituitary-adrenal (HPA) axis suppression and Cushing’s syndrome than mature patients because of a larger skin surface area to body weight ratio.
HPA axis suppression, Cushing’s syndrome, and intracranial hypertension have been reported in children receiving topical corticosteroids. Manifestations of adrenal suppression in children include linear growth retardation, delayed weight gain, low plasma cortisol levels, and absence of response to ACTH stimulation. Manifestations of intracranial hypertension include bulging fontanelles, headaches, and bilateral papilledema.
Administration of topical corticosteroids to children should be limited to the least amount compatible with an effective therapeutic regimen. Chronic corticosteroid therapy may interfere with the growth and development of children.
Adverse Reactions/Side Effects
The following local adverse reactions are reported infrequently with topical corticosteroids, but may occur more frequently with the use of occlusive dressings. These reactions are listed in an approximate decreasing order of occurrence: burning, itching, irritation, dryness, folliculitis, hypertrichosis, acneiform eruptions, hypopigmentation, perioral dermatitis, allergic contact dermatitis, maceration of the skin, secondary infection, skin atrophy, striae, miliaria.
To report SUSPECTED ADVERSE REACTIONS, contact Cosette Pharmaceuticals, Inc. at 1-800-922-1038 or FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
Overdosage
Topically applied corticosteroids can be absorbed in sufficient amount to produce systemic effects (see
PRECAUTIONS).
Fluocinonide Cream Dosage and Administration
Fluocinonide cream 0.05% is generally applied to the affected area as a thin film from two to four times daily depending on the severity of the condition.
Occlusive dressings may be used for the management of psoriasis or recalcitrant conditions.
If an infection develops, the use of occlusive dressings should be discontinued and appropriate antimicrobial therapy instituted.
How is Fluocinonide Cream supplied
Fluocinonide Cream, USP 0.05% is supplied in 15 g (NDC 0713-0663-15), 30 g (NDC 0713-0663-31), and 60 g (NDC 0713-0663-60) tubes.
Store at 20°-25°C (68°-77°F) [see USP Controlled Room Temperature].
Distributed by:
Cosette Pharmaceuticals, Inc.
South Plainfield, NJ 07080
Iss. 09/2021
8-0663CPLNC1 VC7594
PRINCIPAL DISPLAY PANEL
NDC 0713-
0663-15
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
15 g
NDC 0713-
0663-15
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
15 g
NDC 0713-
0663-31
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
30 g
NDC 0713-
0663-31
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
30 g
NDC 0713-
0663-60
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
60 g
NDC 0713-
0663-60
Rx Only
Fluocinonide Cream, USP
0.05%
FOR EXTERNAL USE ONLY. NOT FOR OPHTHALMIC USE.
60 g
Fluocinonide ointment (Flostlike)
Средство создано целенаправленно для устранения дерматита (контактного, аллергического, себорейного). Помогает при псориазе, экземе, зуде разной этиологии. Используется при лечении аллергических высыпаний, потницы, других кожных заболеваний.
Крем не имеет запаха. Обладает легкой текстурой и хорошо впитывается.
Состав
Основной активный компонент крема — флюоцинонид. Это мощный антисептик, для которого характерны также противовоспалительные свойства. Эффективен против грибка, дерматологических расстройств кожи. Приводит в норму местный иммунитет. Также средство содержит кортикостероидные гормоны.
В каких случаях используют
Применение крема рекомендовано в следующих случаях:
- экзема различной локализации (для нее характерны мокнущие, зудящие воспаления);
- прикрывающие дефекты кожи струпья;
- нейродермиты (обусловленные нарушениями функций ЦНС заболевания кожи);
- плоский красный лишай;
- псориаз в период обострений;
- себорея головы, лица, груди, спины;
- зуд в заднем проходе и половых органах.
Способ применения
Крем наносят на чистую кожу. Небольшой объем средства распределяют по проблемному участку, слегка втирая в кожу. Используют 2-3 раза в день на протяжении 5-10 дней. Если заболевание не купировано, курс продлевают до 25 дней. При этом дозировка средства в неделю не должна превышать 5 г (примерно ½ тюбика).
Для терапевтического эффекта препарат наносят на кожу 1-2 раза в день. Противопоказания — возраст до 18 лет.
НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ!
Производство: Китай.
Флуоцинолон-Брингер (Fluocinolon-Bringer)
💊 Состав препарата Флуоцинолон-Брингер
✅ Применение препарата Флуоцинолон-Брингер
Описание активных компонентов препарата
Флуоцинолон-Брингер
(Fluocinolon-Bringer)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2021.11.10
Владелец регистрационного удостоверения:
Код ATX:
D07AC04
(Флуоцинолона ацетонид)
Лекарственная форма
| Флуоцинолон-Брингер |
Мазь д/наружного применения 0.025%: тубы 20 г рег. №: ЛП-007971 |
Форма выпуска, упаковка и состав
препарата Флуоцинолон-Брингер
Мазь для наружного применения однородная, от желтовато-белого до желтого цвета.
Вспомогательные вещества: пропиленгликоль — 49.75 мг, ланолин безводный — 50 мг, парафин жидкий — 50 мг, парафин мягкий белый — до 1 г.
20 г — тубы алюминиевые (1) — пачки картонные.
Фармакологическое действие
ГКС для наружного применения; тормозит высвобождение медиаторов воспаления. При воздействии на кожу происходит предупреждение краевого скопления нейтрофилов, что приводит к уменьшению воспалительного экссудата и продукции цитокинов; торможению миграции макрофагов, уменьшению процессов инфильтрации и грануляции. Оказывает противовоспалительное, противоаллергическое, антиэкссудативное и противозудное действие. Уменьшает проявления или устраняет воспалительную кожную реакцию.
Фармакокинетика
Флуоцинолона ацетонид легко проникает в роговой слой эпидермиса при наружном применении, не подвергается биотрансформации, кумулирует. Всасывание флуоцинолона усиливается при применении на тонкой коже в области складок или на лице, а также на участках с поврежденным эпидермисом или на коже, пораженной воспалительным процессом. При применении окклюзионной повязки, частом нанесении или при применении на большой поверхности кожи увеличивается чрескожная абсорбция флуоцинолона. У детей всасывание флуоцинолона через кожу выражено в большей степени, чем у взрослых. Метаболизируется в печени с образованием неактивных метаболитов. Выводится почками и, в меньшей степени, через кишечник с желчью, преимущественно в виде соединений с глюкуроновой кислотой, а также в небольшом количестве — в неизмененном виде.
Показания активных веществ препарата
Флуоцинолон-Брингер
Острые и хронические воспалительные и аллергические заболевания кожи немикробной этиологии, чувствительные к ГКС, в т.ч. себорейный дерматит, атопический дерматит, экзема различного генеза и локализации, кожный зуд, псориаз; солнечные ожоги; укусы насекомых.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Применяют наружно 1-3 раза/сут, в зависимости от возраста пациента и применяемой лекарственной формы. Продолжительность лечения зависит от характера заболевания и эффективности терапии.
Побочное действие
Возможно: жжение, кожный зуд, сухость кожи, стероидные угри, фолликулиты; развитие вторичных инфекционных поражений кожи и атрофических изменений в ней.
При длительном применении — вторичный иммунодефицит, гипертрихоз, алопеция, особенно у женщин, атрофия кожи, гирсутизм, телеангиэктазии, пурпура, нарушение пигментации.
При нанесении на обширные поверхности возможны системные проявления (гастрит, стероидная язва желудка, надпочечниковая недостаточность, синдром Иценко- Кушинга, стероидный сахарный диабет, стрии, замедление репаративных процессов); при местном применении ГКС отмечались такие системные реакции как нечеткость зрения. В случае применения на коже век возможно развитие глаукомы или катаракты; редко — центральная серозная хориоретинопатия.
Противопоказания к применению
Повышенная чувствительность к флуоцинолона ацетониду или другим ГКС; бактериальные, грибковые и вирусные инфекции, кожные проявления сифилиса, акне, розацеа, периоральный дерматит, аногенитальный зуд, туберкулез кожи, рак кожи, ожоги, раны, трофические язвы голени; поствакцинальные реакции; беременность, период грудного вскармливания; детский возраст до 2 лет.
С осторожностью
Нанесение на большие участки кожи, поврежденную кожу, применение больших доз, длительная терапия (особенно у детей старше 2 лет); нанесение на кожу лица, участки с тонкой кожей и интертригинозную кожу (складки кожи, подмышечные впадины, паховая область, сгибы рук и ног); нанесение на кожу вокруг глаз или веки (риск развития глаукомы, катаракты), в т.ч. у пациентов с глаукомой или катарактой. Атрофические изменения подкожной клетчатки, особенно у лиц пожилого возраста. Применение у девушек в период полового созревания.
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности и в период лактации (грудного вскармливания). При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания. Не рекомендуют применять средство на коже молочных желез.
Применение у детей
Противопоказано применение у детей в возрасте до 2 лет. У детей старше 2 лет следует применять с осторожностью, под контролем врача, минимальными эффективными дозами, на небольших участках кожи, короткими курсами (не более 5 дней); не следует применять на коже лица. С осторожностью следует применять у девушек в период полового созревания.
Применение у пожилых пациентов
С осторожностью следует назначать пожилым пациентам из-за атрофических изменений подкожной клетчатки у данной категории пациентов.
Особые указания
Флуоцинолона ацетонид рекомендуется применять короткими курсами на небольших участках кожи. При длительном применении и/или нанесении на большие поверхности кожи, поврежденную кожу, при применении больших доз, при использовании окклюзионных повязок и при терапии у детей возможна системная абсорбция флуоцинолона ацетонида; возможно подавление функции гипоталамо-гипофизарно-надпочечниковой системы и развитие симптомов гиперкортицизма.
На коже лица чаще, чем на других поверхностях тела, после длительного местного применения ГКС могут проявляться атрофические изменения.
При длительной терапии ГКС внезапное прекращение терапии может привести к развитию «синдрома рикошета», проявляющегося в форме дерматита с интенсивным покраснением кожи и ощущение жжения. Поэтому после длительного лечения отмену флуоцинолона ацетонида следует проводить постепенно, например, переходя на интермиттирующую схему лечения перед тем, как его полностью прекратить.
Во время терапии флуоцинолона ацетонидом необходим периодический контроль функции коры надпочечников, с определением уровня кортизола в крови и моче после стимуляции надпочечников АКТГ.
У пациентов с обыкновенными или розовыми угрями на фоне терапии флуоцинолона ацетонидом возможно обострение заболевания. Для предупреждения местных инфекционных осложнений рекомендуется назначать в сочетании с противомикробными средствами.
Если на фоне применения флуоцинолона ацетонида у пациента возникают такие симптомы как нечеткость зрения либо другие зрительные нарушения, рекомендуется консультация офтальмолога для выяснения возможных причин нарушений, к которым может относиться катаракта, глаукома или редкие заболевания, такие как центральная серозная хориоретинопатия.
С особой осторожностью следует применять флуоцинолона ацетонид у пациентов с псориазом вследствие возможного рецидива заболевания, вызванного развитием толерантности, риска генерализованного пустулезного псориаза и общей токсичности из-за пролежней.
Флуоцинолона ацетонид совместим с противомикробными средствами.
Использование в педиатрии
Флуоцинолона ацетонид можно применять у детей старше 2 лет. Необходимо учитывать, что у детей младшего возраста кожные складки, пеленки, подгузники могут оказывать действие, сходное с действием окклюзионной повязки, и повысить системную абсорбцию флуоцинолона ацетонида. Кроме того, у детей возможна большая степень системной абсорбции из-за соотношения между поверхностью кожных покровов и массой тела, а также в связи с недостаточной зрелостью кожи. Длительное применение ГКС у детей может привести к нарушениям их роста и развития. С осторожностью применяют флуоцинолона ацетонид у девушек в период полового созревания.
Длительное применение флуоцинолона ацетонида у детей возможно только под контролем врача, в минимальной дозе, достаточной для достижения эффекта. У детей курс лечения не должен превышать 5 дней.
Лекарственное взаимодействие
При одновременном применении флуоцинолона ацетонид снижает активность гипотензивных, диуретических, антиаритмических лекарственных средств, препаратов калия.
При одновременном применении диуретиков (кроме калийсберегающих) повышается риск развития гипокалиемии.
Во время лечения ГКС не следует проводить вакцинацию и иммунизацию, в связи с иммунодепрессивным эффектом данных средств. Флуоцинолона ацетонид может усиливать действие иммуносупрессивных препаратов и ослаблять действие иммуностимулирующих.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Синафлан
(МУРОМСКИЙ ПРИБОРОСТРОИТЕЛЬНЫЙ ЗАВОД, Россия)
Синафлан
(ПРОМОМЕД РУС, Россия)
Синафлан
(НИЖФАРМ, Россия)
Синафлан
(АТОЛЛ, Россия)
Синафлан
(ТУЛЬСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА, Россия)
Синафлан
(АЛТАЙВИТАМИНЫ, Россия)
Синафлан
(МУРОМСКИЙ ПРИБОРОСТРОИТЕЛЬНЫЙ ЗАВОД, Россия)
Синафлан
(ЗЕЛЕНАЯ ДУБРАВА, Россия)
Синафлан-Акрихин
(Химико-фармацевтический комбинат АКРИХИН, Россия)
Синафлана мазь 0.025…
(АЛТАЙВИТАМИНЫ, Россия)
Все аналоги