В наблюдениях, проведенных на 37 больных диффузным токсическим зобом, показано, что применение тимомиметика вилона (Lys-Glu) в дозе 10 мкг на инъекцию на протяжении 8-10 дн. приводит к более быстрому наступлению клинического эутиреоза, а также нормализации уровня тиреоидных гормонов ТЗ и Т4.
УДК 615.37: 616 089
О.В. Гвоздева, Б.И. Кузник
ОПЫТ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ ТИМОМИМЕТИКА
ВИЛОНА В ЛЕЧЕНИИ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА
Читинская государственная медицинская академия;
эндокринологическое отделение областной клинической больницы, г. Чита
Известно, что в патогенезе диффузного токсического зоба (ДТЗ) большую роль играют иммунологические нарушения. Традиционная терапия не является патогенетической, а блокирует выработку гормонов щитовидной железой и их периферические эффекты. Именно с этим связано то, что при проведении консервативной терапии только приблизительно у 30% больных достигается стойкая ремиссия заболевания [1, 3, 4, 14-16|.
Вместе с тем, исследованиями, проведенными Е.Б. Жигжитовой [6], установлено, что использование иммуномодулятора тималина при ДТЗ способствует не только ликвидации нарушений иммунитета, но и приводит к более быстрой нормализации уровня гормонов щитовидной железы. В настоящее время, на оснований изучения аминокислотного состава тималина, путем целенаправленного химического синтеза был сконструирован и синтезирован тимомиметик дипептид вилон — Lys-Glu [17, 18, 19]. Вилон является фрагментом многих цитокинов (IL-1 сх, IL-2, IL-3, IL-4, IL-5,1L-6, интерферона), а также целого ряда биологически активных веществ, в том числе тимозинов, тимопоэтина и др. [11,17,19]. В результате многочисленных экспериментальных и клинических исследований [7-9, 10, 11, 17-19] установлено, что вилон обладает теми же свойствами, что и тималин. Под его воздействием у больных с вторичными иммунодефицитами и аутоиммуноагрессией происходит нормализация клеточного и гуморального иммунитета, а также ликвидация хронической формы ДВС- синдрома [8-10, 12]. Более того, оказалось, что вилон способен нормализовать гормональный статус у больных сахарным диабетом 1 типа [8]. Следует напомнить, что между патогенезом аутоиммунных заболеваний щитовидной железы и сахарного диабета 1 типа имеется значительное сходство [ 1, 2, 5[.
Целью настоящей работы явилось изучение эффективности применения вилона для лечения больных с диффузным токсическим зобом.
Влияние применяемой терапии на состояние сердечно-сосудистой системы и уровень гормонов у больных ДТЗ (М±ш)
|
Показатель |
Норма |
1 группа(традиционная терапия) |
2 группа (традиционная терапия + вилон) |
||
|
до лечения |
после лечения |
до лечения |
после лечения |
||
|
Частота пульса, уд./мин |
60-80 |
95,6±14,4 |
76,8±8,9* |
100,1+9,1 |
72,9±2,3* |
|
Артериал. давл., мм рт.ст. |
110-120 65-75 |
133,2+2,9 75,0±2,8 |
120+2,5* 78,4± 1,6 |
140,7±5,6 75,7±4,8 |
116±3,7* 72,9±1,8 |
|
Уровень ТЗ, пмоль/л |
1,0-2,8 |
8,8+0,5 |
6,4±0,5* |
8,9+1,6 |
2,3±0,3* ** |
|
Уровень Т4, пмоль/л |
10,2-23,2 |
96,0+28.4 |
24,6±7,8* |
85,8± 14* |
18,6+3,7* |
|
Уровень ТТГ, нмоль/л |
0,23-3,4 |
0,1 ±0,04 |
0,4±0,2 |
0,07±0,03 |
0,1 ±0,03 |
|
АТ к тиреоидной пероксидазе, ЕД/мл |
0,0-30,0 |
229,0±202,7 |
269+195 |
435,8+108,5 |
391 + 118,2 |
|
Сроки достижения клинич. эутиреоза |
— |
9,0±2,0 |
6,4 ± 1,27 |
Примечания. * достоверность различий до и после применяемой терапии; ** — достоверность различий между 1 и 2 группой.
Методы исследования
Под наблюдением находилось 37 чел., у 15 из которых совместно с традиционной терапией применялся вилон из расчета 10 мкг 1 раз в сут внутримышечно на протяжении 8-10 дн. Группу контроля составляло 22 чел., у 18 из них наблюдался рецидив тиреотоксикоза, и проводимое традиционное лечение являлось подготовкой к проведению терапии I131 или к оперативному вмешательству. Традиционная терапия включала в себя тиреостатики (мерказолил), бетаблокаторы и седативные препараты.
Всем больным проводилось клиническое обследование, включающее общий осмотр, измерение частоты сердечных сокращений, артериального давления, проведение ультразвукового исследования щитовидной железы и электрокардиографии. Гормоны щитовидной железы (ТЗ и Т4), уровень тиреотропного гормона (ТТГ) и аутоантител (аАТ) к тиреоидной пероксидазе определялись методом иммуноферментного анализа в момент поступления больного в стационар и на фоне достигнутого эутиреоза по ТЗ.
Больные, получавшие вилон, исходно имели более выраженный тиреотоксикоз, что подтверждалось более высоким уровнем ТЗ и аутоантител (аАТ) к тиреоидной пероксидазе. Известно, что тяжесть клинических проявлений ДТЗ находится в прямой корреляционной зависимости от уровня ТЗ, являющегося независимым предиктором рецидива тиреотоксикоза [20, 21]. Статистическая обработка данных проведена с использованием критерия Стьюдента.
Результаты исследований
Заключение о достижении эутиреоза выносилось на основании клинико-лабораторных данных (уровень ТЗ, Т4), а также функциональных методов обследования (частота сердечных сокращений, артериальное давление, ЭКГ). После используемой терапии у больных нормализовывалось общее самочувствие — исчезала потливость, суетливость, беспокойство, бессонница. Частота сердечных сокращений при достижении эутиреоза возвращалась к норме, что подтверждалось ЭКГ; одновременно купировалась артериальная гипертензия. Вместе с тем, при использовании вилона систолическое кровяное давление снижалось более значительно (на 25±4,3 мм рт.ст. при использовании вилона и на 12,8+2,3 мм рт.ст. при традиционной терапии, р<0,01). Изначально повышенный уровень ТЗ и Т4 при поступлении больных в стационар в процессе терапии вилоном возвращался к норме. У больных, леченных традиционным методом, к норме показатели гормонов щитовидной железы, как правило, не возвращались. Содержание ТТГ при терапии как вилоном, так и с использованием лишь традиционных методов лечения не изменялось, что, безусловно, связано со слишком коротким сроком наблюдения. Также оставались стабильно высокими в процессе применяемой терапии аАТ к тиреоидной пероксидазе.
В то же время при добавлении к традиционной терапии вилона, по сравнению с контрольной группой, значительно снижались сроки достижения клинического эутиреоза.
Следует особо отметить, что при использовании вилона в течение года не отмечено рецидивов заболевания. Не вызывает сомнений, что достигнутый положительный результат при добавлении к традиционной терапии вилона больным ДТЗ в первую очередь связан с его нормализующим действием на состояние клеточного и гуморального иммунитета [7-10].
Представленные нами данные свидетельствуют о том, что при включении в комплексную терапию диффузного токсического зоба вилона наблюдается более быстрое достижение ремиссии, сопровождающееся нормализацией уровня гормонов щитовидной железы и восстановлением деятельности сердечно-сосудистой системы.
Резюме
В наблюдениях, проведенных на 37 больных диффузным токсическим зобом, показано, что применение тимомиметика вилона (Lys-Glu) в дозе 10 мкг на инъекцию на протяжении 8-10 дн. приводит к более быстрому наступлению клинического эутиреоза, а также нормализации уровня тиреоидных гормонов ТЗ и Т4.
Литература
1. Балаболкин М.И Эндокринология. М., 1989.416 с.
2. Балаболкин М.И. // Тер. архив. 1997. № 10. С. 5-11.
3. Браверман Л.И. Болезни щитовидной железы / Пер. с англ. М.: Медицина, 2000. 418 с.
4. Бузиашвили И., Фадеев В., Мельниченко Р. // Врач. 2005. № 3. С. 32-36.
5. Дедов И.И., Балаболкин М.И., Морова С.И. Болезни органов эндокринной системы. М.: Медицина, 2000. 568 с.
6. Дедов И.И., Трошина Е.А., Антонова С.С. и др. // Проблемы эндокринологии. 2002. № 2. С. 6-13.
7. Жигжитова Е.Б. Патогенетическая иммунокоррекция тималином у больных диффузным токсическим зобом и аутоиммунным тиреоидитом: Автореф. дис…. канд. мед.наук. Чита, 2002. 22 с.
8. Кузник Б.И., Гаймоленко И.Н., Цыбенова Б.Ц. // Цитокины и воспаление. 2003. Т.2. №4. С. 21-26.
9. Кузник Б.И., Колесниченко Л.Р., Ключерева Н.Н. и др. // Успехи геронтологии. 2006. Вып. 19. С. 107-115.
10. Кузник Б.И., Хавинсон В.Х., Витковский Ю.А. и др. Пептидные биорегуляторы. Применение в хирургии, травматологии, стоматологии и онкологии. М.: Вузовская книга, 2004. 400 с.
11. Малинин В.В. Механизмы действия синтетических пептидных тимомиметиков: Автореф. дис. … д-ра мед. наук. СПб., 2001. 32 с.
12. Морозов В.Г., Хавинсон В.Х., Малинин В.В. Пептидные тимомиметики. СПб.: Наука, 2000. 158 с.
13. Старкова Н.Т. Клиническая эндокринология. М.: Медицина, 1991. 510 с.
14. Фадеев В.В. Болезнь Грейвса // РМЖ. 2002. Т.10. №27. С. 1262-1265.
15. Фадеев В.В., Абрамова Н.А. // Проблемы эндокринологии. 2005. Т.51. №6. С. 44-49.
16. Фадеев В.В., Бузиашвили И.И., Абрамова Н.А. и др. // Проблемы эндокринологии. 2004. Т. 50, № 6. С. 3-9.
17. Хавинсон В.Х., Анисимов В.Н., Заварзина Н.Ю. // Бюл. экснерим. биол. и мед. 2000. №7. С. 88-91.
18. Хавинсон В.Х., Анисимов С.В., Малинин В.В. Пептидная регуляция генома и старение. М.: Из-во РАМН, 2005. 208 с.
19. Хавинсон В.Х., Морозов В.Г. Пептиды эпифиза и тимуса в регуляции старения. СПб.: Фолиант, 2001.159 с.
20. Glinoer D., de Nayer Р., Вех М. // Eur. J. Endokrinol. 2001. Vol. 144, Р. 475-483.
21. Young Е.Т., Steel N.R., Talor G.G. et al. // Quart. J. Med. 1998. Vol. 250, P. 175-189.
Клиническая фармакология Тимогена®. Глава 2
Долгов Г.В., Куликов С.В., Легеза В.И., Малинин В.В., Морозов В.Г., Смирнов В.С., Сосюкин А.Е.
УДК 61.438.1:577.115.05
Под редакцией проф. В.С. Смирнова.
Авторский коллектив:
- Долгов Г.В. — д.м.н., профессор кафедры акушерства и гинекологии Военно-медицинской академии
- Куликов С.В. — к.м.н., старший научный сотрудник отдела нейрофармакологии Института экспериментальной медицины РАМН
- Легеза В.И.— д.м.н., профессор ведущий научный сотрудник кафедры Военно-полевой терапии Военно-медицинской академии
- Малинин В.В. — д.м.н., начальник отдела Института биорегуляции и геронтологии СЗО РАМН
- Морозов В.Г. — д.м.н., профессор заместитель директора Института биорегуляции и геронтологии СЗО РАМН
- Смирнов В.С. — д.м.н., профессор ведущий научный сотрудник кафедры военно-полевой терапии Военно-медицинской академии
- Сосюкин А.Е. — д.м.н., профессор начальник кафедры военно- полевой терапии Военно-медицинской академии
Опубликовано в СПб, 2003. — 103 с.
2003
Тимоген
Скачать PDF
Введение
Глава 1. Механизмы пептидной регуляции гомеостаза (В.В. Малинин, В.Г. Морозов)
Глава 2. Регуляторные пептиды тимуса (В.С. Смирнов)
Глава 3. Тимоген®: структура, химический синтез, свойства (С.В. Куликов, В.С. Смирнов)
Глава 4. Тимоген® в профилактике и комплексной терапии инфекционных заболеваний (В.С. Смирнов)
Глава 5. Тимоген® в терапии бронхолегочных заболеваний (В.С. Смирнов)
Глава 6. Применение тимогена в комплексной терапии внутренних болезней (В.С. Смирнов, А.Е. Сосюкин)
Глава 7. Тимоген® в дерматологии (В.С. Смирнов)
Глава 8. Применение Тимогена® для профилактики и лечения радиационных поражений (В.И.Легеза, В.С. Смирнов)
Глава 9. Применение Тимоген® в комплексном лечении механических и термических травм (В.С. Смирнов)
Глава 10. Тимоген® в акушерско-гинекологической практике (Г.В. Долгов, В.С. Смирнов)
Глава 11. Особенности применения Тимогена® в педиатрии (В.С. Смирнов)
Заключение
Глава 2. Пептиды тимуса и пептидные тимомиметики
В.С. Смирнов
Среди различных регуляторных структур организма иммунная система по своей сложности и многофункциональности занимает особое место. Значительная дифференциация функций иммунокомпетентных клеток, большое число их субпопуляций, клонов и способов взаимодействия требуют высокоразвитых селективных и неселективных механизмов передачи информации, обеспечивающих скоординированную работу системы в целом. Большинство эффекторных и вспомогательных функций клеток иммунной системы осуществляются при участии особых эндогенных структур внутрисистемных гормонов и медиаторов. Именно эти молекулы обеспечивают созревание и дифференцировку разных типов клеток, служат передатчиками межклеточных регуляторных сигналов, образуя уже упоминавшуюся APUD-систему, осуществляют контроль над интенсивностью и длительностью иммунного ответа.
Экстракты ткани тимуса
Уникальные свойства эндогенных медиаторов давно уже привлекали к себе пристальное внимание в плане разработки средств коррекции тех или иных изменений в работе системы иммунитета. Наибольшие успехи в этом направлении стали возможны после открытия регуляторных пептидов центральных органов иммунитета: тимуса и костного мозга. В 60-70 гг. прошлого столетия в различных лабораториях мира из центральных органов иммунитета было получено около десятка различных пептидов. Использовались различные технологии выделения: экстрагирование изотоническим раствором хлорида натрия, автолиз и последующая экстракция, экструзионная деструкция, кислотный гидролиз, ультрафильтрация, препаративный электрофорез и др. (Никольский, Гриневич, 1989). Одним из самых первых был препарат гомеостатического тимусного гормона, выделенный еще в 1938 году (Coomsa, 1971). В 70-х годах прошлого столетия были получены тимозины, тимический гуморальный фактор, тимопоэтин, тимостерин, тимический полипептидный препарат, растворимый фактор тимуса, тимостимулин, вилозен, тактивин, тималин и др. Дальнейшая судьба этих соединений различна: одни экстракты так и остались объектом экспериментальных исследований, другие были внедрены в медицинскую практику. Некоторые экстракты подвергли аналитическому и препаративному фракционированию, в результате которого были выделены регуляторные пептиды различной длины. Часть этих пептидов обладала иммуномодулирующими и биорегулирующими активностями, присущими нативным экстрактам тимуса. Для российского читателя наибольший интерес представляют три из них: тимозин, тактивин, тималин; два их которых: тактивин и тималин являются официально зарегистрированными в Российской Федерации лекарственными средствами.
Одним из первых полипептидных экстрактов тимуса был тимозин, выделенный А. Гольдстайном и соавторами (Goldstein) в 1966 году. Гомогенная фракция 8 тимозина, представлявшая собой, агрегат полипептидных цепей, включавших 108 аминокислотных остатков, стимулировала образование антител и способствовала дифференцировке клеток костного мозга в антителообразующие клетки. Было высказано предположение о том, что тимозин активирует хелперную функцию Т-лимфоцитов в кооперативном иммунном ответе на тимуснезависимые антигены. Наименее очищенная фракция 3 тимозина уменьшала проявления вастинг-синдрома, увеличивала выживаемость животных, частично восстанавливала структуру лимфоидных тканей и количество циркулирующих лимфоцитов, а также способность к отторжению кожных трансплантатов (Goldstein et al., 1966; Bach et al., 1971).
Фракция 5 тимозина (тимозин Ф5) – гликопептид, состоящий примерно из 30-ти полипептидов с молекулярной массой от 1 до 15 кД. Препарат усиливал реакцию тимоцитов в смешанной культуре и активность в тесте розеткообразования, а также индуцировал цитотоксичность лимфоцитов и их чувствительность к анти-TL и анти-Thy-1 сывороткам (Pahwa et al., 1979). Эта фракция тимозина стимулировала активность гипоталамо-гипофизарно-адреналовой оси и продукцию ИЛ-6 глиальными клетками (Tijerina et al., 1997). Добавление тимозина Ф5 к культуре спленоцитов, сопровождалось активной выработкой ИЛ-6 (Attia, et al. 1993).
Наиболее широко тимозин применяли при бактериальных, вирусных и грибковых инфекциях (Mutchnic, 1991; Serrate et al., 1987; Reddy, Grieco, 1987; Spangelo et al., 1987). М. Мучник и соавторы (Mutchnick et al., 1991) в двойном слепом плацебоконтролируемом опыте показали, что у больных хроническим вирусным гепатитом В курсовое применение тимозина Ф5 или тимозинаα1 дважды в неделю на протяжении 6 месяцев сопровождалось достоверным увеличением содержания CD3 и CD4 лимфоцитов в периферической крови и активацией выработки интерферонаγ. На фоне применения иммуномодулятора достоверно уменьшалась активность аминотрансфераз. Авторы считают, что терапия тимозином Ф5 способствует наступлению ремиссии или даже выздоровлению больных хроническим вирусным гепатитом В.
Неоднократно предпринимались попытки применения Ф5 в терапии злокачественных опухолей (Wada et al., 1996; Ikemoto et al., 1999; Scher et al., 1988 и др.). Однако однозначных выводов о его эффективности не получено. Так, применение тимозина Ф5 у больных с мелкоклеточным раком легкого на фоне радио- и/или химиотерапии не выявило достоверного влияния иммуномодулятора на течение заболевания и эффективность базисного лечения (Scher et al., 1988).
Применение тимозина у крыс и мышей с раком мочевого пузыря, индуцированным бутил-N-(4-гидроксибутил)-нитрозамином, сопровождалось замедлением скорости развития опухоли на фоне сохранения нормальной активности естественных киллеров (Wada, 1966). В другом исследовании на аналогичной опухолевой модели было показано, что тимозин Ф5 потенцирует действие противораковых химиопрепаратов, в частности деокси-5-флюороуридина (Ikemoto et al., 1999). Применение тимозина после лучевой терапии способствовало более быстрому восстановлению иммунологической реактивности (Wara et al., 1978). Таким образом, в онкологической практике тимозин Ф5 показан в качестве иммунокорректора, применяемого в составе комплексной противоопухолевой терапии с целью восстановления подавленной иммунореактивности. На основе полипептидного экстракта тимуса, аналогичного тимозину Ф5, был получен препарат ТР-1, зарегистрированный в качестве лекарственного средства фирмой «Сероно» (Falchetti et al., 1977).
В 1981 году В.Я. Арионом и соавторами из аутолизата тимуса был получен тактивин – комплексный препарат, содержащий пептиды с молекулярной массой от 1,5 до 6 кДа. В экспериментальных исследованиях и клинических наблюдениях тактивин эффективно восстанавливал сниженную или подавленную иммунологическую реактивность. Введение препарата мышам СВА с индуцированной бензолом депрессией иммунитета, восстанавливало количество ЕК-клеток и Т-киллеров до исходного уровня. Под влиянием тактивина повышалось содержание тимического сывороточного фактора, повышалась активность экспрессии дифференцировочных рецепторов лимфоцитов.
За время, прошедшее с момента создания препарата его использовали для лечения широкого круга заболеваний, сопровождавшихся формированием вторичного иммунодефицитного состояния. Наилучшие результаты были получения при применении тактивина в составе комплексной терапии при радиационной иммунодепрессии кроветворения, при первичных иммунодефицитных состояниях (атаксия-телеангиэктазия, врожденные нарушения тимической регуляции), при лечении генерализованных форм герпеса (Арион, 1989). Клинико-иммунологического эффекта удавалось достичь при рассеянном склерозе, острой септической и гнойно-воспалительной патологии, при острых и хронических инфекционных процессах. Во всех этих случаях после курса тактивина отмечена нормализация состояния иммунной системы, сокращение продолжительности заболевания и повышение эффективности специфической терапии.
Близкий по иммунологическим свойствам пептидный препарат тималин получен путем кислотного гидролиза тимуса крупного рогатого скота (Морозов, Хавинсон, 1978). При экспериментальном изучении тималина показана его способность модулировать процессы репопуляции дифференцировочных рецепторов лимфоцитов (Смирнов и др., 1992). В клинических целях тималин применяли при широком круге заболеваний. Так, парентеральные инъекции препарата в дозе 10-20 мг ежедневно в течение 5-20 сут. у больных с хроническими неспецифическими заболеваниями легких способствовали нормализации большинства показателей клеточного иммунитета и неспецифической защиты организма (Яковлев и др., 1992). Одновременно наблюдалось уменьшение или исчезновение воспалительных явлений в легких. Срок лечения больных сокращался в среднем на 21%. Среди других клинических аспектов иммунотерапии тималином заслуживает внимания его эффективность при лечении различных воспалительных заболеваний, сопровождающихся формированием вторичных иммунодефицитных состояний. Чаще всего при этом наблюдается снижение количества лимфоцитов, экспрессирующих CD2+DR+, CD3+, CD4+, CD8+ рецепторы, на фоне достоверного возрастания индекса миграции лейкоцитов периферической крови. Со стороны системы неспецифической защиты отмечается угнетение экспрессии ОКМ1+ рецепторов на макрофагах, снижение содержания катионных белков, фагоцитарного индекса и активности пероксидазы. Применение тималина в составе комплексной терапии по 10 мг ежедневно на протяжении 5-10 сут. сопровождалось восстановлением сниженных показателей иммунной системы, уменьшением интенсивности внутрисосудистого свертывания и сокращением продолжительности воспаления (Морозов, Хавинсон, 1989; Яковлев и др., 1992). Улучшение клинического состояния наблюдалось в 80-93% случаев. Показатель летальности при таком тяжелом состоянии как перитонит на фоне иммуномодулирующей терапии тималином составил 0,08, в то время как у лиц, получавших стандартную терапию, он был почти в 4 раза выше.
Применение тималина при бронхиальной астме, тимомегалии, системной красной волчанке, саркоидозе, острой пневмонии, псориазе, ревматоидном артрите сопровождалось восстановлением содержания основных субпопуляций Т- и В-лимфоцитов, улучшением клинического течения заболевания, сокращением периода реабилитации. При хронических процессах отмечено увеличение продолжительности периодов ремиссии, а в некоторых случаях и полное выздоровление (Яковлев и др., 1992). Профилактическое назначение тималина ликвидаторам аварии на Чернобыльской АЭС позволяло уменьшить риск формирования вторичного иммунодефицитного состояния (Смирнов и др., 1992).
Тималин применяли при лечении инфекционных заболеваний, в частности, вирусных гепатитов. Показано, что у 50% больных вирусным гепатитом В после 2-х курсов тималина исчезали маркеры возбудителя и наступала стойкая ремиссия, продолжавшаяся 3 и более мес. (Векслер и др., 1987).
Сравнительное исследование влияния экстрактов тимуса показало, что независимо от методики их получения все они обладают близкими иммунобиологическими свойствами. Так, например, в тесте репопуляции мембранных рецепторов у Т-лимфоцитов, обработанных трипсином, все исследованные препараты тимуса оказывали идентичное действие на скорость экспрессии рецепторов, определявшуюся по приросту количества «активных» розеткообразующих клеток (табл. 2.1).
Таблица 2.1. Влияние некоторых пептидных экстрактов тимуса на содержание «активных» Т-лимфоцитов (Еа-РОК) ( Яковлев и др., 1992)
|
Препарат |
Еа-РОК, % |
Р |
|
Контроль: I II Тимостимулин Тактивин Тималин Тимунокс |
45,7±3,1 19,3±1,2 31,5±1,6 34,2±2,7 34,7±2,8 31,0±3,3 |
– – <0,05 <0,05 <0,05 <0,05 |
Примечание. В каждом случае n=12. Контроль I – содержание Еа-РОК в исходной суспензии лимфоцитов; контроль II – после инкубации лимфоцитов в растворе трипсина.
Таким образом, можно с достаточным основанием утверждать, что пептидные препараты, выделяемые из вилочковой железы, оказывают одинаковое иммуномодулирующее действие, независимо от методики их выделения. Это обстоятельство свидетельствует о том, что пептидные последовательности, содержащиеся в экстракте, имеют высокую степень гомологии.
Регуляторные пептиды тимуса
Исследования тимозина Ф5 проведенные А. Гольдстайном (A. Goldstein, 1972), показали, что тимозин Ф5 содержит в своем составе большое количество пептидов, разделенных по миграционным свойствам на 3 группы, отличавшихся по изоэлектрической точке. Среди них наиболее активными оказались тимозины α1, β4 и протимозин-α (Han- nappel, Huff, 2003).
Было установлено, что тимозин-α1 представляет собой полипептид с молекулярной массой 3108 Да, состоящий из 28 аминокислотных остатков. Отмечено, что аминокислотная последовательность пептида не имеет видовой специфичности. Тимозин-β4 включает в себя 43 аминокислотных остатка и имеет молекулярную массу 4863 Да. Пептидная цепь протимозина-α состоит из 112 аминокислотных остатков. Ниже приведены аминокислотные последовательности молекул тимозина-α1и тимозина-β4:
Молекула тимозина-α1
Ser-Asp-Ala-Val-Asp-Thr-Ser-Ser-Ile-Thr-Thr-Lys-Asp-Leu-Lys-Glu-Lys-Lys-Glu-Val-Val-Glu-Glu-Ala-Glu- Asn-COOH
Молекула тимозина-β4
Ser-Asp-Lys-Pro-Asp-Met-Ala-Glu-Ile-Glu-Lys-Phe-Asp-Lys-Ser-Lys-Leu-Lys-Thr-Glu-Thr-Gln-Glu-Lys-Asn- Pro-Leu-Pro-Ser-Lys-Glu-Thr-Ile-Glu-Gln-Glu-Lys-Gln-Ala-Glu-Glu-Ser-OH
Отметим, что все эти полипептиды включают в себя большое количество остатков лизина и глутаминовой кислоты. Особенно это заметно в молекуле тимозина-β4, где многократно встречается последовательность Lys-Glu. Данное обстоятельство имеет большое значение и, как будет отмечено далее, послужило основанием для конструирования минимальных молекул тимомиметиков.
Молекула тимозина-α1 увеличивает экспрессию дифференцировочных рецепторов на Т-лимфоцитах, активирует СD4-лимфоциты, усиливает экспрессию Lyt-1+, Lyt-2+, Lyt- 3+ антигена лимфоцитов, а также усиливает зависимый от активности Т-лимфоцитов IgG-, IgM- и IgA-иммунный ответ (Никольский, Гриневич, 1989). Показана способность тимозина-α1 отменять фазу рефрактерности в процессе синтеза эндогенного интерферона (Носик и др., 1985). Эта способность пептида была использована при изучении эффективности биорегулирующей терапии вирусных гепатитов. Во всех случаях применяли комбинированную схему, в состав которой могли включаться препараты интерферона, противовирусные средства и тимозин-α1. В процессе лечения больных активным HBe-позитивным вирусным гепатитом В тимозин-α1 вводили 2 раза в неделю в дозе 1,6 мг подкожно 2 раза в неделю, интерферон-α применяли подкожно в дозе 10 млн. ед. 3 раза в неделю. Продолжительность курса терапии составляла 26 недель. Катамнестическое наблюдение за больными осуществляли в течение 26 недель. Итого, общий срок наблюдения составил 52 недели. Обследование больных проводили на 52-й и 78-й неделях (Saruc et al., 2002). К концу 52-й недели нормализация уровня трансаминаз была отмечена у 87,7% наблюдавшихся больных. У 76,2% больных нормальный уровень трансаминаз и негативная реакция на HBV-ДНК сохранялись на протяжении 78 недель. Близкие по эффективности результаты получены при лечении больных вирусным гепатитом В сочетанием тимозина-α1 с аномальными нуклеозидами (Yuen, Lai, 2001). Положительные результаты, хотя может быть и не столь значительные, отмечены и при комбинированном лечении больных вирусным гепатитом С (Ideo, Bellobuono, 2002; Kullavanuaya et al., 2001). Наконец, также, как и экстракты тимуса, тимозин-α1 применяли на фоне радио- и химиотерапии злокачественных процессов с целью повышения активности иммунной системы, подавленной противоопухолевыми препаратами (Garachi et al., 1995).
Выделенный из β-области тимозина Ф5 тимозин-β4 в отличие от тимозина-α1 индуцировал появление терминальной дезоксинуклеотидилтрансферазы в негативных по этому признаку клетках костного мозга у бестимусных мышей (Hu et al., 1981). Эти данные подтвердили, что тимозины влияют на ранние стадии Т-клеточной дифференцировки, причем это влияние зависит от вида тимозина. Тимозин-β4 ингибирует, а тимозин-α1 усиливает пролиферативный ответ. Отмечено неодинаковое воздействие на экспрессию дифференцировочных рецепторов: тимозин-β4 увеличивал количество клеток с фенотипами CD8+ и CD11+, но не влиял на экспрессию CD3+-, CD6+- и CD9+ – рецепторов (Kokki- nopoulos et al., 1985).
С другой стороны, тимозин-β4 оказывает выраженное действие на процессы регенерации. Установлено, что интраперитонеальное введение пептида сопровождается усилением процессов реэпителизации раны на 4-й день после травмы на 42%, а на 7-й – на 61% относительно контроля. Показано также, что тимозин-β4 существенно увеличивает скорость миграции кератиноцитов в камере Бойдена (Malinda et al., 1999).
Анализ биологических эффектов семейства тимозинов свидетельствует о том, что каждый из пептидов, образующих комплекс тимозин Ф5, активен на определенном этапе дифференцировки лимфоцитов. Так, тимозины β3, β4 индуцируют дифференцировку предшественников Т-лимфоцитов, тимозин-α1 контролирует превращение преТ-клеток в тимоциты, а тимозины α5 и α7 оказывают влияние на дифференцировку и функциональную активность предшественников Т-лимфоцитов в периферических лимфоидных органах (Low, Goldstein, 1985).
Тимусный гуморальный фактор был выделен из диализатов гомогенизированной ткани тимуса (Traini et al., 1979). Он представляет собой термостабильный олигопептид с молекулярной массой около 3000 Да и состоит из 31 аминокислотного остатка. Пептид восстанавливал способность клеток селезенки новорожденных тимэктомированных мышей вызывать реакцию «трансплантат против хозяина», а также увеличивал количество антителобразующих клеток в селезенке у тимэктомированных и облученных животных (Rotter et al., 1973). Применение этого фактора у детей с лимфопролиферативными заболеваниями (лимфогранулематоз, лимфосаркома, лимфома) после курса химиотерапии сопровождалось выраженным иммуномодулирующим эффектом, сходным с таковым у тимозинов (Traini et al., 1979).
Другим хорошо изученным тимическим иммуномодулятором является тимопоэтин, впервые выделенный в 1971 году (Goldstein, Manarano, 1971). Из вводно-солевого экстракта тимуса получены два пептида – тимопоэтин I и тимопоэтин II. Дальнейшее изучение тимопоэтина II показало, что это полипептид с молекулярной массой 5562 Да и изоэлектрической точкой 5,5, состоящий из 49 аминокислотных остатков. Биологическую активность тимопоэтина II связывают с пентапептидом, названным тимопентин (ТП-5), соответствующим 32-36 аминокислотным остаткам нативной молекулы тимопоэтина: Arg- Lys-Asp-Val-Tyr. Вместе с тем было показано, что некоторые проявления активности тимопоэтина сохраняются и у более коротких пептидов, состоящих из 4-х и даже 3-х аминокислотных остатков (Denes и др., 1986).
Основной функцией тимопоэтина является регуляция лимфопоэза. Применение пентапептида в дозе 0,5 мг/кг ежедневно в течение 2-х недель, а затем 3 раза в неделю в течение 10 недель способствовало улучшению клинического состояния и показателей Т- системы иммунитета у ряда больных с первичными иммунодефицитами (Goldstein at al., 1979).
Пептидные тимомиметики
Цитированные выше исследования имели весьма важное значение в развитии проблемы пептидных тимомиметиков. Они подтвердили актуальность пептидного процессинга и показали, что информация, необходимая для реализации иммунорегуляторных эффектов, может содержаться в небольших по размерам олигопептидах, содержащих 5-6 аминокислотных остатков. Примером такого олигопептида является тимогексин (иммунофан), структура которого отличается от тимопентина наличием аминокислотных замен с элонгированием цепи концевым аргинином: Arg-Asp-Lys-Val-Tyr-Arg. Применение препарата способствовало достижению сероконверсии у больных хроническим вирусным гепатитом и оказывало положительное влияние на продукцию специфических антител при хроническом бруцеллезе (Покровский и др., 1992). Позднее было установлено, что тимогексин при патологическом изменении синтеза иммуноглобулинов, вызванном врожденным иммунодефицитом IgA или атопическим дерматитом с гиперпродукцией IgE, оказывает иммунокорригирующее действие на продукцию обоих классов иммуноглобулинов. Механизм этого действия обусловлен межклеточным взаимодействием иммунокомпетентных клеток и реализуется вне зависимости от дополнительного введения ИЛ-4 (Лебедев и др., 1994).
Дальнейшее развитие идеи пептидных тимомиметиков привело к пониманию того факта, что для индукции регуляторного сигнала и системе может быть достаточно минимального пептида, состоящего всего из 2-х аминокислотных остатков.
Если проанализировать аминокислотную последовательность тимозинов, тимопо- этинов и других типических пептидов, а также ряда интерлейкинов можно видеть, что в их структуре часто встречается дипептид, состоящий из остатков лизина и глутаминовой кислоты. Этот факт был использован В.Х Хавинсоном и сотрудниками для создания нового иммуномодулятора Lys-Glu, получившего наименование «Вилон» (Хавинсон и др., 1997). Экспериментальное изучение Вилона показало его способность усиливать реакцию гиперчувствительности замедленного типа у мышей, индуцированную тринитробензо-сульфокислотой (Морозов и др., 2000). Вилон стимулирует образование антителобразующих клеток в селезенке мышей, иммунизированных эритроцитами барана, а также активирует репаративные процессы в тимусе облученных животных.
В клинических наблюдениях, опубликованных В.Г. Морозовым и соавторами (2000), показана способность Вилона стимулировать репаративные процессы при механической травме, остеомиелите, при различных заболеваниях роговицы. У больных кавернозным туберкулезом наблюдали стимулирующее действие Вилона на процессы заживления каверн на фоне увеличения экспрессии CD4+ и уменьшения экспрессии CD8+ рецепторов Т-лимфоцитов. У больных обструктивным бронхитом назначение Вилона способствовало снижению частоты бронхоспазмов, нормализации температуры и улучшению аппетита. Одновременно наблюдалось увеличение количества лимфоцитов в периферической крови и усиление фагоцитарной активности лейкоцитов
Другим дипептидом, обладающим тимомиметическими свойствами, является Glu- Trp, известный под названием «Тимоген». Первоначально дипептид был выделен из тималина методом высокоэффективной жидкостной хроматографии, а затем синтезирован несколькими методами, один из которых подробно описан в 3-й главе данной монографии. Долгое время считалось, что этот дипептид может содержаться в молекуле гормона тимуса. К сожалению, выделить и идентифицировать полную молекулу этого гормона так и не удалось, но в тех ее фрагментах, которые на сегодняшний день известны, такой дипептид не найден, зато его можно обнаружить в молекуле фактора некроза опухоли, некоторых интерлейкинах и пр.
Подробное изучение и опыт более чем 16-летнего опыта клинического применения убедительно показали, что Тимоген® является классическим тимомиметиком, обладающим всей совокупностью иммуномодулирующих реакций. Это обстоятельство имеет важное методическое значение, поскольку показало, что способность регулировать клеточные иммунные реакции не является исключительным свойством тимических пептидов. Аналогичными свойствами могут обладать короткие пептиды иного происхождения. Анализ накопленной информации позволяет определенно утверждать, что фактором, определяющим свойства того или иного пептида, является его структура, а не происхождение. С этих позиций распространенная до настоящего времени точки зрения, согласно которой Тимоген® является синтетическим аналогом пептидного экстракта тимуса – тималина, а, равно как и иных, идентифицированных пептидов тимуса, является ошибочной и не имеет под собой научных оснований. Тимоген® является самостоятельным дипептидом, воспроизводящим некоторые свойства тимозинов, но не имеющим с ними структурных аналогий. С этой точки зрения логично было ожидать появления других коротких пептидов, способных регулировать те или иные реакции иммунной системы. Определенными свойствами, присущими тимическим иммуномодуляторам, обладают некоторые аминокислоты, в частности, глутаминовая кислота, глицин, триптофан и их простые смеси (Белокрылов и др., 1999).
Эти данные лишний раз подчеркивают многокомпонентность регуляторных структур системы иммунитета, которые нельзя втиснуть в прокрустово ложе тимических пептидов. Более того, нет никаких оснований идентифицировать пептидные тимомиметики как фракции или активные центры гормона тимуса. Это самостоятельные соединения, обладающие иммунорегулирующими свойствами, которые могут быть использованы в терапевтической практике. Опыт 15-летнего исследования Тимогена®, обобщенный на страницах данной работы, полностью подтвердил правомерность такого подхода.
Введение
Глава 1. Механизмы пептидной регуляции гомеостаза (В.В. Малинин, В.Г. Морозов)
Глава 2. Регуляторные пептиды тимуса (В.С. Смирнов)
Глава 3. Тимоген®: структура, химический синтез, свойства (С.В. Куликов, В.С. Смирнов)
Глава 4. Тимоген® в профилактике и комплексной терапии инфекционных заболеваний (В.С. Смирнов)
Глава 5. Тимоген® в терапии бронхолегочных заболеваний (В.С. Смирнов)
Глава 6. Применение тимогена в комплексной терапии внутренних болезней (В.С. Смирнов, А.Е. Сосюкин)
Глава 7. Тимоген® в дерматологии (В.С. Смирнов)
Глава 8. Применение Тимогена® для профилактики и лечения радиационных поражений (В.И.Легеза, В.С. Смирнов)
Глава 9. Применение Тимоген® в комплексном лечении механических и термических травм (В.С. Смирнов)
Глава 10. Тимоген® в акушерско-гинекологической практике (Г.В. Долгов, В.С. Смирнов)
Глава 11. Особенности применения Тимогена® в педиатрии (В.С. Смирнов)
Заключение
Скачать PDF
Назад к списку
Пептидный крем для ускоренной полной репаративной регенерации кожных тканей
Основная цена: 47,00 €
47,00 €
Скидка:

Описание
Восстанавливающий крем с пептидами для наружного применения PAN VILON® — последняя научная разработка в области восстановительной косметологии. Крем для ускоренной полной репаративной регенерации тканей кожи. Инновационная формула крема, созданная на основе многолетних исследований, содержит специальные пептиды, активирующие обновление клеток на молекулярном уровне.
Крем PAN VILON® содержит пептидный биорегулятор ВИЛОН®, уникальный ультракороткий пептид, состоящий из комбинации двух аминокислот, включая лизин. Лизин используется клетками в производстве коллагена и эластина для здоровья и упругости кожи. Дипептид VILON® активирует выработку собственного коллагена и эластина, необходимых элементов для полной физиологической регенерации кожи. При полной репаративной регенерации коллаген и эластин помогают избежать образования рубцовой ткани (рубцов). Пептиды, проникая в ядро клетки, запускают процессы регенерации и активируют синтез новых клеток. Это приводит к максимально ускоренному полному заживлению ран и повреждений кожи, а также к обновлению и омоложению кожи. Поэтому действие крема Pan Vilon можно сравнить с эффектом профессиональных аппаратных процедур. Крем PAN VILON® создан по технологии регулирующих пептидов профессора Хавинсона.
Пептиды кожи VILON® являются строительным материалом для нашего тела, в том числе кожи. Благодаря небольшому размеру они легко проникают в глубокие слои и запускают процессы восстановления и заживления в клетках. Пептиды — это естественный компонент, и организм воспринимает их как связанные компоненты. Поэтому крем Пан Вилон не вызывает аллергии и раздражения. Крем PAN VILON® содержит пептидный биорегулятор ВИЛОН®. Это уникальный ультракороткий пептид, состоящий из комбинации двух аминокислот. Комбинация наиболее положительно заряженных и наиболее отрицательно заряженных аминокислот оказывает уникальное регенерирующее действие на ткани кожи.
Эстетическое применение ПАН ВИЛОН рекомендуется при возрастных деформациях кожи, в том числе:
- потеря тургора и тонуса
- дряблость, дряблость
- снижение скорости регенерации и др.
Восстанавливающее и регенерирующее применение ПАН ВИЛОН рекомендуется при любых повреждениях кожи, в том числе:
- при любых ранах на коже, в том числе открытых
- послеоперационные раны
- растяжки кожи
- с ожогами, в том числе от солнца
- после травматических косметических процедур (пилинг, лазерная шлифовка, механическая чистка и др.)
- после аллергии (зуд, покраснение)
- после татуажа и перманентного макияжа и др.
Только для наружного применения. Храните в недоступном для детей месте. Избегайте попадания в глаза. Прекратите использование при появлении раздражения.
Ингредиенты:
Вода, петролатум, глицерин, каприловый / каприновый триглицерид, изопропилмиристат, цетеариловый спирт, полисорбат 60, глицерилстеарат, бисаболол, феноксиэтанол, этилгексилглицерин, облепиховое масло, дипептид-9, трипептид-62
Способ применения:
Равномерно распределите крем PAN VILON® по коже и нежно помассируйте. Допускается нанесение на пораженный участок кожи.
Форма выпуска:
20 мл
Гарантированная подлинность и качество:
100% оригинал от NANOPEP (Франция).
Разработка и производство:
NANOPEP создает оригинальные продукты нового поколения, которые значительно улучшают качество жизни.
Khavinson Peptides® (Международный исследовательский фонд)
Лечение и оздоровление пептидами Хавинсона
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Щербак В.А.
1
1 Читинская государственная медицинская академия Минздрава России
Цель работы – исследовать возможности вилона воздействовать на морфологию селезенки в условиях экспериментальной патологии, вызванной гиподинамическим стрессом. Исследования проведены на 58 беспородных белых крысах-самцах (возраст 3-5 мес.) весом 160 – 200 гр. Использовали острый иммобилизационный стресс. Микроморфометрию проводили под микроскопом МБР-1 методом точечного счета с помощью окулярной стереометрической сетки Г.Г. Автандилова. Селезенка интактных животных имела массу 1079,7 ± 11,6 мг и с поверхности была покрыта фиброзной капсулой. Острый иммобилизационный стресс вызывал значительные изменения морфофункционального состояния селезенки, а их восстановление происходило неодинаково у крыс разных экспериментальных групп. Пептидный тимомиметик вилон (Lys-Glu) получен путем направленного химического синтеза на основании аминокислотного анализа комплексного препарата тимуса – тималина. Введение терапевтических доз вилона усиливало функциональную активность лимфоидной ткани и уровень лимфопоэза в ней, что является морфологическим отражением усиления функции гуморального звена иммунитета. Таким образом, вилон оказывают нормализующее влияние на структуру селезенки и, в конечном итоге, на иммунный ответ, усиливая его в случае подавления действием чрезмерных повреждающих факторов. Тимомиметик вилон ликвидирует иммунные нарушения, вызванные стрессом, и оказывает протекторное действие при введении его до стресса.
селезенка
стресс
вилон
тимомиметик
крысы
белая пульпа
красная пульпа
1. Кузник Б.И., Линькова Н.С., Тарновская С.И., Хавинсон В.Х. Цитокины и регуляторные пептиды: возрастные изменения, развитие атеросклероза и тромботических заболеваний (обзор литературы и собственных данных) // Успехи геронтологии. – 2013. – 2013. – Т. 26, № 1. – С. 038-051.
2. Степанов А.В., Цепелев В.Л., Мельникова С.Л. Иммуностимулятор из центрального органа гуморального иммунитета — сумки Фабрициуса // Сибирский медицинский журнал. – 2013. – № 2. – С. 32-34.
3. Степанов А.В., Цепелев В.Л. Влияние синтетических пептидов сумки Фабрициуса на функциональную активность макрофагов. // Забайкальский медицинский вестник. – 2014. – № 2. – С. 44-47.
4. Степанов А.В., Цепелев В.Л., Цепелев С.Л. Результаты исследования эффективности синтетического иммуностимулятора нового поколения. // Фундаментальные исследования. – 2012. – № 12-1. – С. 142-145.
5. Хавинсон В.Х., Кузник Б.И., Рыжак Г.А. Пептидные биорегуляторы – новый класс геропротекторов. Сообщение 2. // Успехи геронтологии. – 2013. – 2013. – Т. 26, № 1. – С. 020-037.
6. Щербак В.А. Динамика интерлейкинов при лечении детей, больных хроническим гастродуоденитом // Экспериментальная и клиническая гастроэнтерология. – 2003. – № 1. – С. 120-121.
7. Щербак В.А., Щербак А.И., Щербак А.Г. Морфологические изменения тимуса при остром стрессе у крыс // Морфология. – 2004. – Том 126, № 4. – С. 145.
8. Щербак В.А. Роль иммуномодуляторов в комплексной терапии детей с хроническим гастродуоденитом, ассоциированным с Helicobacter pylori // Вопросы практической педиатрии.- 2008. – Т.3, № 1. – С. 30-35.
9. Щербак В.А. Терапия Helicobacter pylori-ассоциированного эрозивного гастродуоденита у детей с использованием цитаминов // Экспериментальная и клиническая гастроэнтерология. – 2004. – № 1. – С.180-187.
10. Щербак В.А., Витковский Ю.А. Влияние вилона на лимфоцитарно-тромбоцитарную адгезию в эксперименте // Дальневосточный медицинский журнал. – 2006. – № 2. – 71-73.
11. Щербак В.А., Малежик Л.П., Аксенова Т.А., Патеюк А.В. Влияние цитомединов желудка на иммунный ответ при остром иммобилизационном стрессе у крыс // Патологическая физиология и экспериментальная терапия. – 2005. – № 3. – С. 6-7.
12. Щербак В.А., Цапп А.В. Эндогенная интоксикация и экстракорпоральные методы ее коррекции у детей с хроническим гастродуоденитом // Вопросы детской диетологии. – 2014. – Т. 12, № 4. – С. 15-20.
13. Shcherbak V.A. Lymphocyte-thrombocyte rosette adhesion in children with chronic gastritis //Journal of Thrombosis and Haemostasis. – 2005. – Vol. 3, Suppl. 1. – P. 1559.
Изучение последствий воздействия на организм стресса приобретает особое значение, так как он инициирует комплекс разнообразных реакций. При чрезмерном или длительном воздействии стресса или неполноценности какого-либо звена системы адаптации нарушения могут быть обнаружены на уровне соматических функций [7, 11]. Последствия стресса могут трансформироваться в ведущий фактор патогенеза ряда болезней, в том числе, связанных с нарушением иммунной системы.
Цель работы – исследовать возможности вилона воздействовать на морфологию селезенки в условиях экспериментальной патологии, вызванной гиподинамическим стрессом.
Материалы и методы исследования
Наши исследования проведены на 58 беспородных белых крысах-самцах (возраст 3-5 мес.) весом 160 – 200 гр. Использовали острый иммобилизационный стресс (ОИС). За основу взят метод О.Н. Забродина (1982), модифицированный соответственно нашим условиям [82]. За сутки до эксперимента крысы лишались пищи при свободном доступе к воде. Затем животных фиксировали на деревянных станках в положении на спине, привязывая конечности. Для профилактики некрозов через каждые 2 часа конечность (последовательно по одной) освобождалась от лигатур на 5 минут. Фиксация продолжалась 24 часа. В течение этого времени наблюдалось двигательное беспокойство животных, попытки освободиться.
Для гистологического исследования материал фиксировали при + 4 °С в жидкости Карнуа, 10 % нейтральном формалине, заливали в парафин и целлоидин. Срезы парафиновых и целлоидиновых блоков толщиной 5 и 10 мкм соответственно окрашивали общеморфологическими методиками: гематоксилин-эозином, азур II-эозином, по ван Гизону. Углеводный компонент окрашивали ШИК-реакцией по Мак-Манусу в прописи Лилли, ДНК – по методу Фельгена. Для элективного выявления лаброцитов использована окраска бисмарк-брауном по Шубичу, а для определения плазматических клеток в стенке желудка – пиронином-метиленовым зеленым по Браше. Аргирофильные ретикулиновые волокна выявляли импрегнацией серебром по Футу.
Микроморфометрию проводили под микроскопом МБР-1 методом точечного счета с помощью окулярной стереометрической сетки Г.Г. Автандилова и окуляр-микрометра МОВ-15. Число лаброцитов подсчитывали при увеличении микроскопа х600 на 1 мм2 слизистой оболочки в 10 полях зрения. Масса органов всех животных определялась с точностью до 1 мг.
После создания острого иммобилизационного стресса (ОИС) животные были разделены на 2 группы: 1- получала физраствор (1,0 мл) , 2 – вилон в дозе 10 мкг. Пептидный тимомиметик вилон (Lys-Glu) получен путем направленного химического синтеза на основании аминокислотного анализа комплексного препарата тимуса – тималина [1, 5]. Вилон или физраствор вводили внутримышечно 1 раз в сутки на протяжении 10 дней подряд. Забор материала проводили на вторые, девятые и двадцать первые сутки эксперимента. Сравнение проводили с интактными крысами. Для изучения протекторного действия вилон вводили 1 раз в сутки в течение 3 дней, предшествующих эксперименту, и во время стресса каждые 6 часов по 10 мкг внутримышечно. Значимость различий оценивали по t-критерию Стьюдента и χ2 Пирсона.
Результаты исследования и их обсуждение
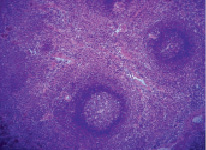
В первые сутки после ОИС у крыс наблюдалась общая реакция в виде заторможенности, снижения аппетита, жажды, у некоторых животных отмечалось затруднение движений вследствие синюшности и отека дистальных отделов конечностей. Селезенка интактных животных имела массу 1079,7 ± 11,6 мг и с поверхности была покрыта фиброзной капсулой. От капсулы внутрь органа отходили трабекулы, между которыми залегала белая и красная пульпа (рис. 1).
Рис. 1. Селезенка интактных животных. Окраска гематоксилин-эозин. Увеличение 120
Белая пульпа была представлена лимфоидными узелками и периартериальными лимфоидными влагалищами (ПАЛВ). Лимфоидный узелок состоял из плотно расположенных мелких лимфоцитов, имел округлую или овальную форму. Его площадь у интактных животных равнялась 585,2 ± 9,4 мкм2.
В зависимости от функционального состояния фолликул мог содержать герминативный центр или не иметь его, так как образование герминативного центра происходит только при антигенной стимуляции. Центр размножения повторял форму лимфоидного узелка, имел светлую окраску и был образован крупными клетками со светлыми ядрами и базофильной цитоплазмой. Его площадь составляла 234,7 ± 2,5 мкм2.
С поверхности герминативный центр был окружен более темноокрашенной мантийной зоной, образованной 2-4 слоями компактно расположенных мелких и средних лимфоцитов, формирующих корону узелка. Периартериальные лимфоидные влагалища располагались вокруг центральной артерии и были построены достаточно однородно. Они были образованы 2-4 рядами мелких и средних лимфоцитов, разделенных концентрическими слоями ретикулярных волокон. Большинство лимфоцитов имели фенотип Т-хелперов.
Маргинальная (пограничная) зона лежала на границе с красной пульпой и являлась общей для лимфатического узелка и ПАЛВ. Она была образована рыхло расположенными клетками и многочисленными капиллярами. Ее площадь составляла 46,83 ± 1,68 мкм2. Маргинальная зона всегда является местом формирования иммунного ответа независимо от вида антигена и способа его внедрения. Кроме того, маргинальная зона служит местом поступления из центральных органов кроветворения предшественников Т- и В-лимфоцитов, расселяющихся в соответствующие зоны.
Красная пульпа была образована ретикулярными клетками, ретикулиновыми волокнами и венозными синусами. Из клеточных элементов в ней находились эритроциты и небольшое количество равномерно расположенных мононуклеарных лейкоцитов. Процентное соотношение белой и красной пульпы составляло 14,6 % и 81,3 % соответственно.
На вторые сутки после стресса аргирофильные волокна капсулы были неравномерно импрегнированы серебром, по ходу волокон наблюдались утолщения, чередующиеся с истонченными участками. Масса органа снижалась до 930,8 ± 13,9 мг в первой и 978,5 ± 12,3 мг во второй группах соответственно.
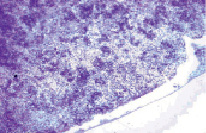
Четко выявлялась неравномерная плотность в расположении клеточных элементов красной пульпы. Сразу под капсулой формировалась светлоокрашенная зона, бедная лимфоцитами (рис. 2). Ширина её в разных отделах колебалась от 50 до 75 мкм, а в области ворот зона, практически лишенная лимфоцитов, достигала 300 мкм. Вместо диффузного расположения клеток, характерного для контрольных животных, лимфоциты формировали многочисленные скопления различной величины и формы. В отдельных участках красной пульпы наблюдались мелкоочаговые кровоизлияния. Венозные синусы расширены и полнокровны.
Рис. 2. Группы лимфоцитов в красной пульпе селезенки. Крысы, получавшие физиологический раствор. Вторые сутки после острого иммобилизационного стресса. Окраска гематоксилин-эозин. Увеличение 120
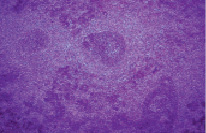
Значительные изменения претерпевала белая пульпа. Площадь лимфоидных фолликулов и плотность расположения в них лимфоцитов уменьшалась в 2,1 раза, что наряду с локальным расширением межклеточных щелей свидетельствовало о нарастающей делимфатизации. Это приводило к появлению бледноокрашенных телец-теней (рис. 3).
Рис. 3. Делимфатизация белой пульпы и формирование телец-«теней» (стрелка). Крысы, получавшие физиологический раствор. Вторые сутки после острого иммобилизационного стресса. Окраска гематоксилин-эозин. Увеличение 120
В 3,25-3,5 раза снижалась площадь герминативных центров, вплоть до полного исчезновения некоторых из них (таблица). Поэтому количество лимфатических узелков, имеющих герминативные центры, была в 1,3 раза меньше, чем у контрольных животных. В тоже время площадь, занимаемая маргинальной зоной, возрастала достигая 67,1 ± 3,64 мкм2 и 69,4 ± 2,21 мкм2 у крыс 1 и 2 групп соответственно.
Площадь некоторых структур белой пульпы селезенки (мкм2)
|
Лимфоидный узелок |
Герминативный центр |
Маргинальная зона |
|
|
Интактные животные |
585,24 ± 3,62 |
234,75 ± 2,51 |
46,8 ± 2,68 |
|
Вторые сутки |
|||
|
1 группа |
288,87 ± 9,05 р1 < 0,05 |
66,24 ± 3,18 р1 < 0,05 |
67,17 ± 3,64 р1 < 0,05 |
|
2 группа |
281,98 ± 7,12 p1 < 0,05; p2 < 0,01 |
72,83 ± 3,49 p1 < 0,05; p2 < 0,01 |
69,41 ± 2,21 p1 < 0,05; p2 < 0,01 |
|
Девятые сутки |
|||
|
1 группа |
402,71 ± 4,28 р1 < 0,05 |
102,51 ± 2,75 р1 < 0,05 |
58,17 ± 1,93 р1 < 0,05 |
|
2 группа |
456,65 ± 5,32 p1 < 0,05; p2 < 0,01 |
139,68 ± 4,92 p1 < 0,05; p2 < 0,01 |
48,36 ± 2,16 p1 < 0,05; p2 < 0,01 |
|
Двадцать первые сутки |
|||
|
1 группа |
509,76 ± 3,14 р1 < 0,05 |
184,45 ± 2,92 р1 < 0,05 |
51,62 ± 2,46 р1 < 0,05 |
|
2 группа |
594,14 ± 9,15 p1 < 0,05; p2 < 0,01 |
240,45 ± 3,18 p1 < 0,05; p2 < 0,01 |
45,43 ± 2,21 p1 < 0,05; p2 < 0,01 |
|
Протекторное действие |
|||
|
1 группа |
296,90 ± 9,05 р1 < 0,05 |
92,14 ± 6,22 р1 < 0,05 |
71,56 ± 4,95 р1 < 0,05 |
|
2 группа |
562,24 ± 8,69 p1 > 0,05; p2 < 0,01 |
224,52 ± 7,53 p1 > 0,05; p2 < 0,01 |
44,7 ± 3,69 p1 > 0,05; p2 < 0,01 |
Примечания: p1 – значимость различий по сравнению с интактными крысами; p2 – значимость различий между группами животных, получавших вилон и физраствор.
Увеличение ширины маргинальной зоны по сравнению с контролем могло свидетельствовать о том, что, несмотря на существенно больший приток лимфоцитов и макрофагов к белой пульпе не все поступившие лимфоциты проходят стадию пролиферации и дифференцировки вплоть до образования плазмоцитов, продуцирующих иммуноглобулины.
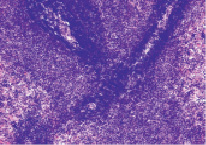
У стрессированных крыс увеличивалась ширина ПАЛВ и плотность расположения в ней лимфоцитов в 1,2 раза у крыс 1 группы и в 1,6 раза у крыс 2 группы. На поперечных и продольных срезах селезенки лимфоидные муфты имели интенсивную окраску и были образованы малыми и средними лимфоцитами, формирующими 6-9 рядов радиально расположенных цепочек (рис. 4).
Рис. 4. Периартериальное лимфоидное влагалище (стрелка). Крысы, получавшие вилон. Вторые сутки после острого иммобилизационного стресса. Окраска гематоксилин-эозин. Увеличение 200
В ответ на стресс-реакцию изменялись кровеносные сосуды. Ядра эндотелиальных клеток часто деформированы, располагались на вершинах складок. Внутренняя эластическая мембрана утолщена, растянута. Эластические волокна средней оболочки извиты и фрагментированы. Гладкомышечные клетки уплощены, их ядра спиралевидно скручены.
При гистохимическом исследовании найдено усиленное периваскулярное накопление ШИК-позитивных веществ вокруг сосудов микроциркуляторного русла и очаговая метахромазия, что свидетельствовало об увеличении проницаемости сосудистой стенки и развитии отека. В просвете сосудов формировались агрегаты форменных элементов крови и пристеночные тромбы.
Морфометрические параметры, полученные на 9 сутки после острого иммобилизационного стресса, свидетельствовали о повышении функциональной активности органа. У крыс обеих экспериментальных групп увеличивалась масса селезенки, снижалась толщина капсулы, хотя в ней сохранялось некоторое количество деформированных аргирофильных волокон. В красной пульпе мононуклеарные элементы были распределены преимущественно равномерно, поэтому сохранялись лишь единичные очаговые клеточные скопления.
Иммунный аппарат белой пульпы восстанавливался, но динамика его активизации была неодинакова у крыс разных экспериментальных групп. Более выраженная лимфатизация происходила у крыс, получавших вилон, о чем свидетельствовало увеличение размеров лимфоидных фолликулов на 61,9 % (р < 0,001) и практически вдвое на 91,8 % площади герминативного центра с одновременным ростом числа фолликулов, имеющих эту структуру. Дополнительным признаком стабилизации органа являлось сокращение площади маргинальной зоны, которая у крыс 1 и 2 групп уменьшалась на 15,4 % и 43,5 % соответственно.
ПАЛВ были четко выражены, образованы радиальными цепочками лимфоцитов. Согласно данным литературы образование «цепочек», состоящих из различных типов Т-лимфоцитов, свидетельствует о кооперации клеток, участвующих в иммунном ответе [428, 608]. Просветы сосудов у крыс 1 группы были умеренно спавшиеся, в части из них обнаруживались сладжи эритроцитов. Аргирофильные волокна имели вид нежной сеточки, контурирующей трабекулярные и пульпарные артерии и вены.
Динамика морфологических изменений белой пульпы на 21 день свидетельствовала об увеличение объема лимфоидной ткани в органе, поэтому масса селезенки практически достигала контрольных цифр, особенно у крыс 2 группы. Это подтверждалось тем, что к 21 дню размеры лимфатических узелков на фоне введения вилона возросли в 2,1 раза, что на 51,3 % больше, чем у крыс 1 группы. Важным моментом в ответ на введение вилона явилось увеличение в 1,5 раза числа фолликулов с герминативным центром, что на морфологическом уровне свидетельствует об активации иммунной реакции селезенки. Восстановление структурной организации и цитоархитектоники органа, начинающееся с 9 суток, на фоне введения вилона достигало контрольных цифр к 21 дню. У нелеченых крыс к этому сроку полностью восстановились не все морфологические показатели.
Полученные данные свидетельствуют о том, что ОИС вызывал значительные изменения морфофункционального состояния селезенки, а их восстановление происходило неодинаково у крыс разных экспериментальных групп. Введение терапевтических доз вилона усиливало функциональную активность лимфоидной ткани и уровень лимфопоэза в ней, что является морфологическим отражением усиления функции гуморального звена иммунитета. Вилон ликвидирует нарушения иммунитета при различных патологических состояниях [6, 8, 9, 12, 13]. Показано положительное действие других синтетических пептидов в эксперименте [2, 3, 4].
Таким образом, вилон оказывают нормализующее влияние на структуру селезенки и, в конечном итоге, на иммунный ответ, усиливая его в случае подавления действием чрезмерных повреждающих факторов. Тимомиметик вилон ликвидирует иммунные нарушения, вызванные стрессом, и оказывает протекторное действие при введении его до стресса.
Библиографическая ссылка
Щербак В.А. ВЛИЯНИЕ ВИЛОНА НА МОРФОМЕТРИЧЕСКИЕ ПОКАЗАТЕЛИ СЕЛЕЗЕНКИ В ЭКСПЕРИМЕНТЕ // Научное обозрение. Медицинские науки. – 2016. – № 5.
– С. 123-127;
URL: https://science-medicine.ru/ru/article/view?id=937 (дата обращения: 28.11.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Вилон — это короткий пептид. Он используется в комплексной терапии для предотвращения возникновения гнойных осложнений в послеоперационный период, при ожогах, открытых ранах на коже. Применяется как иммуномодулятор, то есть активатор иммунных процессов в организме.
Что собой представляют пептиды? Основной «строительный» материал наших клеток — аминокислоты. Соединенные в определенной последовательности, они образуют белки. Пептиды — это короткие цепочки аминокислот, в дипептидах их две. Именно они содержатся в PAN VILON — восстановительном креме.
Процессы в организме при возникновении раны или ожога
В области ожога или раны всегда возникает типичный воспалительный процесс, сопровождаемый рядом признаков:
- разрушение и закупорка сосудов;
- инфильтрация и отек тканей;
- отмирание поврежденных участков.
В этот период в организме запускается сложный механизм регенерации.
Методика исследований
Клинические исследования вилона проводились несколькими медицинскими академиями и университетами. Обследовались как здоровые люди, получившие раны, ожоги или переломы, так и больные с различными патологиями, в том числе сахарным диабетом.
Обследовано 90 больных в возрасте от 16 до 46 лет. В контрольную группу вошло 30 здоровых людей в возрасте от 17 до 32 лет.
Исследовались следующие показатели в сыворотки крови:
- концентрация цитокинов;
- количество диеновых конъюгатов;
- содержание ТБК-активных продуктов;
- антиоксидантная активность.
Кроме того, экспресс-методом определялась степень микробной обсемененности раны.
Результаты
У пациентов, получавших вилон, микробная обсемененность была ниже 105
на 1 г ткани. На вторые сутки у них повысилось количество противовоспалительных цитокинов — пептидов-информаторов. В последующие дни их количество упало, что свидетельствует о затухании воспаления и нормальной регенерации.
Выводы
Клинические исследования привели к однозначному выводу, что применение вилона сокращает длительность воспалительного процесса и регенерации тканей, к тому же он снижает активность стресс-системы надпочечников, увеличивает количество лимфоцитов, восстанавливает структуру тимуса.
Результаты клинических исследований пептида позволили создать уникальную формулу крема PAN VILON. Он относится к восстановительным косметическим средствам с основным действующим веществом в виде короткого пептида. Используется при царапинах, ранах, ожогах на коже, значительно сокращая время регенерации и препятствуя развитию гнойных процессов.
Литература:
1. Севостьянова Н. Н., Линькова Н.С., Полякова В.О. Иммуномодулирующее действие вилона и его аналога в культурах клеток тимуса человека и животного. Институт физиологии им. И.П. Павлова РАН, Санкт-Петербург, 2012. – 4 с.
2. Мироманов А.М., Намоконов Е.В., Патогенетическое обоснование использования вилона в профилактике послеоперационных гнойных осложнений при открытых переломах конечностей. Читинская государственная медицинская академия. Чита, 2008. – 4с.
3. Обыденко В.И., Патеюк А.В., Кузник Б.И., Влияние вилона на регенерацию ожоговой раны, морфологию тимуса и надпочечников у животных в условиях эксперимента. — Читинская государственная медицинская академия. Чита, 2009. – 4с.
4. Кузник В.И., Колесниченко Л.Р., Ключерева Н.Н. Влияние тимомиметика вилона на состояние свертывающей системы крови и фибринолиза у больных сахарным диабетом I типа разного возраста.- Читинская государственная медицинская академия. Чита, 2006. – 9 с.
В разделе собраны статьи об эффективности применения пептидов, а также с информацией о CLUB120
Велсон® (Velson) инструкция по применению
📜 Инструкция по применению Велсон®
💊 Состав препарата Велсон®
✅ Применение препарата Велсон®
📅 Условия хранения Велсон®
⏳ Срок годности Велсон®
Описание лекарственного препарата
Велсон®
(Velson)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2020 года.
Дата обновления: 2020.03.18
Активное вещество:
мелатонин
(melatonin)
BP
Британская Фармакопея
Лекарственная форма
| Велсон® |
Таб., покр. пленочной оболочкой, 3 мг: 30, 60 или 90 шт. рег. №: ЛП-005391 |
Форма выпуска, упаковка и состав
препарата Велсон®
Таблетки, покрытые пленочной оболочкой белого цвета, круглые, двояковыпуклые; на поперечном разрезе ядро от белого до почти белого цвета с коричневатым оттенком.
Вспомогательные вещества: кальция гидрофосфата дигидрат — 64.67 мг, целлюлоза микрокристаллическая — 25 мг, повидон К25 — 3.33 мг, кроскармеллоза натрия — 2 мг, тальк — 1 мг, кремния диоксид коллоидный — 0.5 мг, кальция стеарат — 0.5 мг.
Состав оболочки: опадрай белый (03A280002) — 3 мг (гипромеллоза (гидроксипропилметилцеллюлоза) — 40%, целлюлоза микрокристаллическая — 32%, титана диоксид — 20%, макрогол (полиэтиленгликоль) — 8%).
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
10 шт. — упаковки ячейковые контурные (6) — пачки картонные.
10 шт. — упаковки ячейковые контурные (9) — пачки картонные.
Фармакологическое действие
Синтетический аналог гормона шишковидного тела (эпифиза). В норме синтез мелатонина в эпифизе имеет определенный суточный ритм. Выработка мелатонина синхронизирована с циклом день/ночь, при этом пик концентрации в плазме приходится на ночное время, а минимум – на дневное. Информация об отсутствии света воспринимается сетчаткой глаза, откуда сигнал по ретиногипоталамическому тракту направляется в супрахиазматическое ядро, и далее — в верхний шейный ганглий. Из окончаний симпатических нервов, отходящих от нейронов верхнего шейного ганглия, в паренхиму эпифиза выделяется норадреналин, который запускает синтез мелатонина. Свет тормозит выработку мелатонина.
Воздействие на любое звено процесса синтеза мелатонина может привести к снижению выработки данного гормона и нарушению циркадных ритмов. Снижение выработки мелатонина может наблюдаться на фоне следующих состояний:
- избыточное воздействие искусственных источников света в темное время суток (особенно голубого спектра — экран телевизора, смартфона, компьютера);
- расстройства цикла сон-бодрствование (десинхроноз), которые могут возникать под влиянием эндогенных (например, при синдроме задержки фазы сна, синдроме опережения фазы сна) и экзогенных факторов (например, нарушения режима сна при сменном графике работы, смене часовых поясов);
- пожилой и старческий возраст;
- перименопауза и постменопауза у женщин;
- наличие вредных привычек (активное курение и употребление алкоголя);
- прием некоторых лекарственных средств (НПВП, бета-адреноблокаторов, бензодиазепинов).
Мелатонин нормализует циркадные ритмы. Оказывает адаптогенное, седативное, снотворное действие. Увеличивает концентрацию ГАМК и серотонина в среднем мозге и гипоталамусе, изменяет активность пиридоксалькиназы, участвующей в синтезе ГАМК, допамина и серотонина. Регулирует цикл сон-бодрствование, суточные изменения локомоторной активности и температуры тела, положительно влияет на интеллектуально-мнестические функции мозга, на эмоционально-личностную сферу.
Способствует организации биологического ритма и нормализации ночного сна. Улучшает качество сна, ускоряет засыпание, снижает число ночных пробуждений, улучшает самочувствие после утреннего пробуждения, не вызывает ощущения вялости, разбитости и усталости при пробуждении, регулирует нейроэндокринные функции, снижает стрессовые реакции. Адаптирует организм метеочувствительных людей к изменениям погодных условий.
Не вызывает привыкания и зависимости.
Фармакокинетика
Всасывание
Мелатонин после приема внутрь быстро всасывается из ЖКТ. Кинетика мелатонина в диапазоне 2-8 мг линейна. При приеме внутрь в дозе 3 мг Сmax в плазме крови и слюне достигается соответственно через 20 мин и 60 мин. Тmax в сыворотке крови — 60 мин (нормальный диапазон 20-90 мин). После приема мелатонина в дозе 3-6 мг Сmax в сыворотке крови, как правило, в 10 раз больше эндогенного мелатонина в сыворотке крови ночью. Сопутствующий прием пищи задерживает абсорбцию мелатонина.
Биодоступность мелатонина при пероральном приеме колеблется в диапазоне от 9 до 33% (приблизительно составляет 15%).
Распределение
В исследованиях in vitro связывание мелатонина с белками плазмы составляет 60%. В основном мелатонин связывается с альбумином, α1-кислым гликопротеином и ЛПВП. Vd около 35 л. Быстро распределяется в слюну и проникает через ГЭБ, определяется в плаценте. Концентрация в спинномозговой жидкости в 2.5 раза ниже, чем в плазме.
Метаболизм
Мелатонин метаболизируется преимущественно в печени. После приема внутрь мелатонин подвергается существенному преобразованию при «первом прохождении» через печень, где происходит его гидроксилирование и конъюгация с сульфатом и глюкуронидом с образованием 6-сульфатоксимелатонина; уровень пресистемного метаболизма может достигать 85%. Экспериментальные исследования позволяют предположить, что в процессе метаболизма мелатонина принимают участие изоферменты CYP1A1, CYP1A2 и, возможно, CYP2C19 системы цитохрома Р450. Основной метаболит мелатонина — 6-сульфатоксимелатонин, неактивен.
Выделение
Мелатонин выделяется из организма почками. Средний Т1/2 мелатонина составляет 45 мин. Выведение осуществляется с мочой, около 90% в виде сульфатного и глюкуронового конъюгатов 6-гидроксимелатонина, а около 2-10% выводился в неизмененном виде.
Фармакокинетика у особых групп пациентов
На фармакокинетические показатели влияют возраст, прием кофеина, курение, прием пероральных контрацептивов. У критически больных пациентов наблюдается ускоренная абсорбция и нарушенная элиминация.
У пациентов пожилого возраста скорость всасывания может быть снижена на 50%. Метаболизм мелатонина замедляется с возрастом. При разных дозах мелатонина более высокие значения показателей AUC и Сmax получены у пациентов пожилого возраста, что отражает сниженный метаболизм мелатонина у этой группы пациентов.
У пациентов с нарушением функции почек при длительном лечении кумуляции мелатонина не отмечено. Эти данные согласуются с коротким Т1/2 мелатонина у человека.
Печень является основным органом, участвующим в метаболизме мелатонина, поэтому заболевания печени приводят к повышению концентрации эндогенного мелатонина. У пациентов с циррозом печени плазменная концентрация мелатонина в дневное время суток существенно увеличивалась.
Показания препарата
Велсон®
- при расстройствах сна, в т.ч. обусловленных нарушением ритма «сон-бодрствование», таких как десинхроноз.
Режим дозирования
Препарат принимают внутрь, запивая достаточным количеством жидкости.
При нарушении сна, десинхронозе принимают 3 мг 1 раз/сут за 30-40 мин до сна.
При применении в качестве адаптогена при смене часовых поясов принимают за 1 день до перелета и в последующие 2-5 дней по 3 мг за 30-40 мин до сна.
Максимальная суточная доза — 6 мг.
С возрастом происходит снижение метаболизма мелатонина, что необходимо учитывать при выборе режима дозирования для пациентов пожилого возраста. С учетом этого у пациентов пожилого возраста возможен прием препарата за 60-90 мин до сна.
Побочное действие
Классификация побочных реакций по органам и системам с указанием частоты их возникновения: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000), очень редко (<1/10000), в т.ч. отдельные сообщения, частота неизвестна (частота не может быть оценена на основе имеющихся данных).
Инфекционные и паразитарные заболевания: редко — опоясывающий герпес.
Со стороны системы кроветворения: редко — лейкопения, тромбоцитопения.
Со стороны иммунной системы: частота неизвестна — реакции гиперчувствительности.
Со стороны обмена веществ: редко — гипертриглицеридемия, гипокалиемия, гипонатриемия.
Нарушения психики: нечасто — раздражительность, нервозность, беспокойство, бессонница, необычные сновидения, ночные кошмары, тревога; редко — перемены настроения, агрессия, ажитация, плаксивость, симптомы стресса, дезориентация, раннее утреннее пробуждение, повышение либидо, пониженное настроение, депрессия.
Со стороны нервной системы: нечасто — мигрень, головная боль, вялость, психомоторная гиперактивность, головокружение, сонливость; редко — обморок, нарушение памяти, нарушение концентрации внимания, делирий, синдром «беспокойных ног», плохое качество сна, парестезии.
Со стороны органа зрения: редко — снижение остроты зрения, нечеткость зрения, повышенное слезотечение.
Со стороны органа слуха и лабиринтные нарушения: редко — вертиго, позиционное вертиго.
Со стороны сердечно-сосудистой системы: нечасто — артериальная гипертензия; редко — «приливы», стенокардия напряжения, ощущение сердцебиения.
Со стороны пищеварительной системы: нечасто — абдоминальная боль, боль в верхней части живота, диспепсия, язвенный стоматит, сухость во рту, тошнота; редко — гастроэзофагеальная болезнь, желудочно-кишечное нарушение или расстройство, буллезный стоматит, язвенный глоссит, рвота, усиление перистальтики, вздутие живота, гиперсекреция слюны, неприятный запах изо рта, абдоминальный дискомфорт, дискинезия желудка, гастрит.
Со стороны печени и желчевыводящих путей: нечасто — гипербилирубинемия.
Со стороны кожи и подкожных тканей: нечасто — дерматит, потливость по ночам, зуд и генерализованный зуд, сыпь, сухость кожи; редко — экзема, эритема, дерматит рук, псориаз, генерализованная сыпь, зудящая сыпь, поражение ногтей; частота неизвестна — отек Квинке, отек слизистой оболочки полости рта, отек языка.
Со стороны костно-мышечной системы: нечасто — боль в конечностях; редко — артрит, мышечный спазм, боль в шее, ночные судороги.
Со стороны мочевыделительной системы: нечасто — глюкозурия, протеинурия; редко — полиурия, гематурия, никтурия.
Со стороны половых органов и молочной железы: нечасто — менопаузальные симптомы; редко — приапизм, простатит; частота неизвестна — галакторея.
Общие расстройства и нарушения в месте введения: нечасто — астения, боль в груди; редко — утомляемость, боль, жажда.
Влияние на результаты лабораторных и инструментальных исследований: нечасто — отклонение от нормы лабораторных показателей функции печени, увеличение массы тела; редко — повышение активности печеночных трансаминаз, отклонение от нормы содержания электролитов в крови, отклонение от нормы результатов лабораторных тестов.
Если любые из указанных в инструкции побочных эффектов усугубляются или отмечаются любые другие побочные эффекты, не указанные в инструкции, пациенту необходимо сообщить об этом врачу.
Противопоказания к применению
- повышенная чувствительность к компонентам препарата;
- аутоиммунные заболевания;
- печеночная недостаточность;
- тяжелая почечная недостаточность;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (эффективность и безопасность препарата не установлена).
С осторожностью
Влияние различной степени почечной недостаточности на фармакокинетику мелатонина не изучено, поэтому применять препарат у пациентов с данной патологией следует с осторожностью.
Применение при беременности и кормлении грудью
Препарат Велсон® противопоказан к применению при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
Противопоказано применение препарата при печеночной недостаточности.
Применение при нарушениях функции почек
Противопоказано применение препарата при тяжелой почечной недостаточности.
С осторожностью следует применять препарат пациентам с различной степенью почечной недостаточности.
Применение у детей
Противопоказано применение препарата в возрасте до 18 лет.
Применение у пожилых пациентов
С возрастом происходит снижение метаболизма мелатонина, что необходимо учитывать при выборе режима дозирования для пациентов пожилого возраста. С учетом этого у пациентов данной группы возможен прием препарата за 60-90 мин до сна.
Особые указания
Пребывание на ярком свету может привести к снижению эффективности препарата Велсон®. В связи с этим, после приема препарата Велсон® рекомендуется избегать яркого освещения.
Необходимо проинформировать женщин, желающих забеременеть, о наличии у препарата слабого контрацептивного действия.
Отсутствуют клинические данные о применении мелатонина у пациентов с аутоиммунными заболеваниями, в связи с чем применение препарата у данной категории пациентов не рекомендуется.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат Велсон® вызывает сонливость, в связи с этим в период лечения следует воздержаться от вождения автотранспорта и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Передозировка
По имеющимся литературным данным, применение мелатонина в суточной дозе до 300 мг не вызывало клинически значимых нежелательных реакций. Наблюдались гиперемия, спазмы в брюшной полости, диарея, головная боль и скотома при применении мелатонина в дозах 3000-6600 мг в течение нескольких недель. При применении мелатонина в очень высоких дозах (до 1 г) наблюдалась потеря сознания.
Симптомы: при передозировке возможно развитие сонливости.
Лечение: промывание желудка, активированный уголь, симптоматическая терапия. Клиренс активного вещества предполагается в пределах 12 ч после приема внутрь.
Лекарственное взаимодействие
Фармакокинетическое взаимодействие
В концентрациях, значительно превышающих терапевтические, мелатонин индуцирует изофермент CYP3A in vitro. Клиническое значение этого явления до конца не выяснено. В случае развития признаков индукции следует рассмотреть вопрос о снижении дозы одновременно применяемых лекарственных средств.
Следует избегать комбинации с флувоксамином, который повышает концентрацию мелатонина (увеличение AUC в 17 раз и Cmax в 12 раз) за счет ингибирования его метаболизма изоферментами цитохрома Р450 (CYP): CYP1A2 и CYP2C19.
Следует соблюдать осторожность при одновременном приеме следующих лекарственных средств:
- 5- и 8-метоксипсоралена, который повышает концентрацию мелатонина вследствие ингибирования его метаболизма;
- циметидина (ингибитор изоферментов CYP2D), который повышает содержание мелатонина в плазме за счет ингибирования последнего;
- эстрогенов, которые увеличивают концентрацию мелатонина путем ингибирования его метаболизма изоферментами CYP1A1 и CYP1A2;
- ингибиторов изофермента CYPA2 (например, хинолоны), которые способны повышать экспозицию мелатонина;
- индукторов изофермента CYP1A2 (например, карбамазепина и рифампицина), которые способны снижать плазменную концентрацию мелатонина.
Курение способно снизить концентрацию мелатонина за счет индукции изофермента CYP1A2.
Опубликовано множество данных о влиянии агонистов/антагонистов адренергических и опиоидных рецепторов, антидепрессантов, ингибиторов простагландинов, бензодиазепинов, триптофана и этанола на секрецию эндогенного мелатонина. Изучение взаимного влияния этих препаратов на динамику или кинетику мелатонина не проводилось.
Фармакодинамическое взаимодействие
Во время приема мелатонина следует воздержаться от употребления алкоголя, т.к. он снижает эффективность препарата.
Мелатонин усиливает седативное действие бензодиазепиновых и небензодиазепиновых снотворных средств, таких как залеплон, золпидем и зопиклон. Комбинированное применение может приводить к прогрессирующему расстройству внимания, памяти и координации в сравнении с монотерапией золпидемом.
Применение мелатонина совместно с тиоридазином и имипрамином может привести к повышению ощущения спокойствия и затруднениям при выполнении определенных заданий по сравнению с монотерапией имипрамином, а также к усилению чувства «помутнения в голове» по сравнению с монотерапией тиоридазином.
Условия хранения препарата Велсон®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре не выше 25°С.
Срок годности препарата Велсон®
Срок годности — 4 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается без рецепта.
Контакты для обращений
НПО ПЕТРОВАКС ФАРМ ООО
(Россия)

|
|
142143 Московская обл., г. Подольск |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Мелагив
(ЗВЕЗДА МЕДИА, Россия)
Меладапт
(АТОЛЛ, Россия)
Меладрим®
(ЮНИФАРМ, Россия)
Мелаксен
(UNIPHARM, США)
Меларена®
(НИЖФАРМ, Россия)
Меларитм®
(АЛИУМ, Россия)
Мелатонин
(РИФ, Россия)
Мелатонин Авексима
(АВЕКСИМА, Россия)
Мелатонин Эвалар
(ЭВАЛАР, Россия)
Мелатонин-СЗ
(СЕВЕРНАЯ ЗВЕЗДА, Россия)
Все аналоги