Тривирон форте-ТРВ
Механизм действия препарата Тривирон форте-ТРВ основан на разрушении РНК-вирусных частиц с помощью низкомолекулярной искусственной рибонуклеазы (artificial ribonucleases).
Показания к применению:
Для борьбы с инфекционными заболеваниями, вызванными РНК-вирусами; используется для профилактики секундарных инфекций вирусной этиологии.
Состав и действующее вещество :
В состав противовирусного препарата Тривирон форте-ТРВ входит искусственно синтезированный фермент (рибонуклеаза), муравьиная кислота. Искусственно синтезированные рибонуклеазы, входящие в состав препарата Тривирон форте-ТРВ, благодаря своему малому размеру, способны эффективнее проникать в капсиды вирусных частиц и разрушать РНК вирусы, а благодаря их небелковой природе, устойчивы к действию желудочного сока и пищеварительных ферментов.
Экономическое обоснование применения Тривирона форте-ТРВ
Важным моментом является каталитический характер действия препарата т.е. Тривирон форте-ТРВ действует многократно: одна молекула действующего вещества разрушает много вирусных частиц (вирусного РНК).
В результате препарат может быть использован в низких дозах, что делает экономически возможным его использование в промышленном птицеводстве и свиноводстве.
Порядок применения препарата
Тривирон форте-ТРВ вводится в систему поения через медикатор.
- Птицеводство — 0,00125-0,005 мл препарата на 1 кг массы тела. Курс 2-10 дней.
- Свиноводство — 0,05-0,1 мл препарата на 1 кг массы тела. Курс 2-10 дней.
- Крупный рогатый скот — 0,05-0,1 мл препарата на 1 кг массы тела. Перед выпойкой препарат обязательно разводят в питьевой воде в соотношении 1:1000. Курс 2-10 дней.
Произведено по заказу ООО «Трионис Вет»
Доставка осуществляется собственным транспортом или транспортными компаниями в кратчайшие сроки с соблюдением всех мер безопасности и сохранности качества товара.
Вернуться к списку
|
ООО «Трионис Вет»
Россия, Московская обл., Королев, ул. Лесная, 14/5
Тривирон
×
|
|||||||||||||||||
|
2009-2023 © All Rights Reserved |
D. Khlyp
Несмотря на существенное расширение арсенала средств специфической профилактики (живые, инактивированные и векторные вакцины), распространение РНК-содержащих вирусов, вызывающих различные заболевания (инфекционный энцефаломиелит, ньюкаслская болезнь, грипп птиц, инфекционный бронхит кур, метапневмовирус, инфекционная бурсальная болезнь и др.), в последние годы нисколько не уменьшилось, а тема защиты поголовья от инфицирования не потеряла своей актуальности.
Следует отметить, что даже после качественной вакцинации и при высокой иммунной защите всего поголовья птица может заразиться данными вирусными заболеваниями. Благодаря тому что уровень антител в организме птицы достаточно высокий, болезнь будет протекать в более легкой форме и производственные показатели снизятся незначительно.
Основные причины вспышек вирусных заболеваний, которые периодически регистрируют в хозяйствах, — ошибки, допущенные при составлении схемы иммунизации и при вакцинации (например, неправильное применение вакцин), недостаточная концентрация материнских и поствакцинальных антител, высокая вирулентность и давление полевых вирусов. Таким образом, эффективность иммунизации птицы напрямую зависит от используемого вакцинного штамма, однородности иммунного ответа, кратности вакцинации и способа введения вакцины.
Для связывания и уничтожения вирусов, попадающих в организм птицы и циркулирующих в нем, специалисты компании «Трионис Вет» рекомендуют применять противовирусный препарат Тривирон. Он принадлежит к новой фармакологической группе синтетических рибонуклеаз. В качестве действующего вещества Тривирон содержит химически синтезированные небольшие молекулы (они меньше, чем молекулы природных рибонуклеаз), которые благодаря малому размеру способны проникать в капсиды вирусных частиц и оказывать ингибирующее действие на основные структурные компоненты вируса. Следует отметить, что вырабатываемые макроорганизмом антитела и защитные клетки не подвергаются воздействию синтетических рибонуклеаз. К тому же одна молекула рибонуклеазы может разрушить несколько молекул РНК-содержащих вирусов. Это — важное свойство искусственных рибонуклеаз.
Мы провели исследования, в ходе которых определили активность противовирусного препарата Тривирон в отношении РНК-содержащих вирусов (типичные представители: вирусы семейства Coronaviridae — возбудители инфекционного бронхита кур и Paramyxoviridae — возбудители ньюкаслской болезни), циркулирующих в организме бройлеров. Для связывания и инактивации вирусных частиц противовирусный препарат Тривирон вводили путем распыления (в лаборатории) и методом выпойки (производственный опыт).
Исследования проходили на базе лаборатории фармакогеномики Института химической биологии и фундаментальной медицины и сектора молекулярной биологии Сибирского федерального научного центра агробиотехнологий. Вирусы выделяли по общепринятой методике.
Идентификацию вируса ньюкаслской болезни осуществляли методом РТГА (РЗГА) (реакция торможения гемагглютинации).
В исследованиях задействовали бройлеров кроссов Hubbard F15 и Cobb 500. Для проведения первого эксперимента двухнедельных цыплят кросса Hubbard F15 разделили на четыре группы — контрольную (семь голов) и три опытные (по шесть голов в каждой). Птицу опытных групп обработали аэрозольной живой аттенуированной вакциной на основе штамма IB 4-91 вируса инфекционного бронхита кур из расчета 10 доз на голову при экспозиции 30 минут. Через три часа после введения вакцинного штамма молодняк первой, второй и третьей опытных групп обработали противовирусным препаратом Тривирон. Экспозиция составила 10, 20 и 40 минут соответственно. Эту процедуру повторяли дважды с интервалом в 24 часа. Расход препарата — 3 мл/м3.
Для приготовления рабочего раствора брали 890 мл дистиллированной воды, 100 мл глицерина, 6 г натрия гидрокарбоната и 10 мл противовирусного препарата, pH полученного раствора варьировал в пределах 4,5–5,2.
Было установлено, что аэрозольная обработка цыплят противовирусным препаратом Тривирон (экспозиция — 40 минут) способствовала снижению числа случаев возникновения пневмонии и повышению сохранности цыплят (табл. 1).
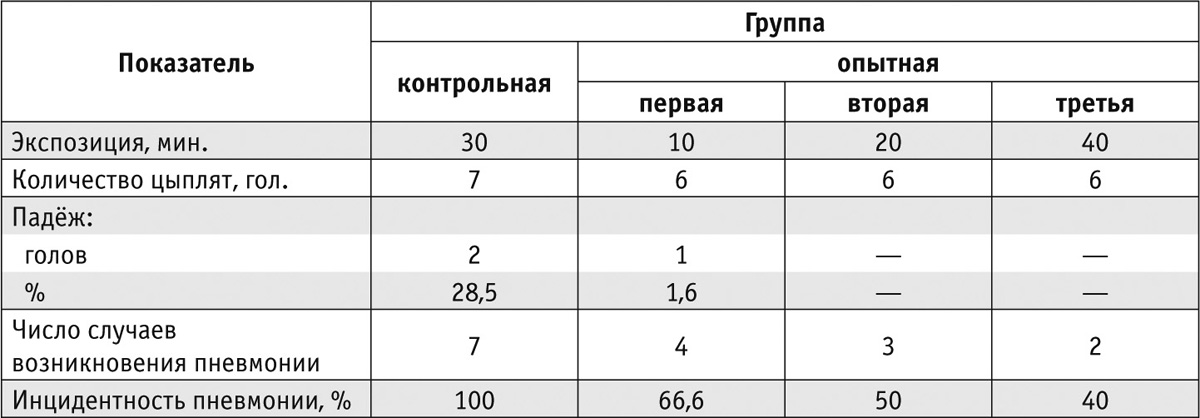
Второй эксперимент проходил в одном из птицеводческих хозяйств. Бройлеров кросса Cobb 500 содержали в двух корпусах, расположенных на одной площадке. В первом корпусе насчитывалось 16 420 цыплят, во втором — 15 930.
Первая иммунизация была проведена в инкубатории. Птицу вакцинировали против болезни Марека (вирусвакцину вводили подкожно в область шеи в дозе 0,2 мл на голову), ньюкаслской болезни (живую сухую вакцину распыляли из расчета 1 доза на голову) и инфекционного бронхита кур (распыляли вакцины, содержащие классический и вариантный штаммы инфекционного бронхита кур из расчета 1 доза на голову).
Бройлеров в процессе выращивания вакцинировали методом выпойки, применяя по 1 дозе на голову: на 10‑й день — против болезни Гамборо (живая вакцина), на 14‑й день — против ньюкаслской болезни и инфекционного бронхита кур (живая двухвалентная вакцина), на 21‑й день — против болезни Гамборо (живая вакцина).
Первые признаки заболевания бройлеров, содержавшихся в первом и во втором корпусах, зарегистрировали соответственно на 23‑й и 25‑й дни.
По мере прогрессирования болезни фиксировали следующие симптомы:
- снижение потребления корма;
- вялость и апатию;
- выделение слизи из носовой полости;
- воспаление конъюнктивы глаз и слезотечение;
- появление свистящих, хрипящих, клокочущих и каркающих звуков;
- расстройства нервной системы;
- жидкий, водянистый помет ярко-зеленого или белого цвета, иногда с кровяными включениями.
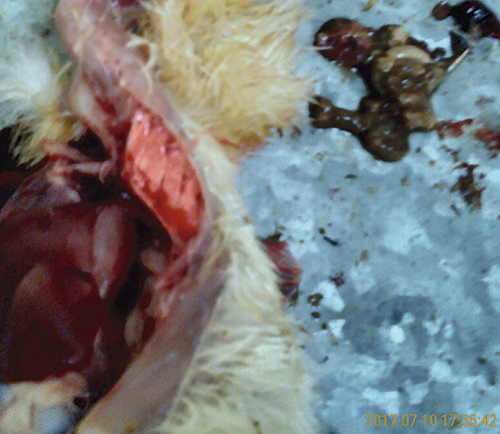
Патолого-анатомическое вскрытие и исследование желудочно-кишечного тракта павшей птицы показали, что в организме заболевших бройлеров протекали воспалительные процессы (мультифокальный некротический стоматит, фарингит, эзофагит и т. д.). Кроме того, зафиксированы патологические изменения тканей и органов, а именно:
отек слизистой оболочки железистого желудка, наличие кровоизлияний на верхушке конусовидных возвышений — сосочков;
поражения в виде геморрагического ободка на границе между железистым и мышечным желудком (Марусин поясок);
кровоизлияния и появление язв-бутонов (некротические очаги) в цекальных миндалинах слепых отростков кишечника;
пятнистые и полосчатые кровоизлияния в слизистой оболочке прямой кишки.
Исследование методом РТГА позволяет обнаружить в сыворотке крови специфические антитела (антигемагглютинины). Таким способом осуществляют серологический контроль эпизоотической ситуации в конкретном хозяйстве. Результаты анализа, проведенного методом РТГА, представлены в таблице 2.
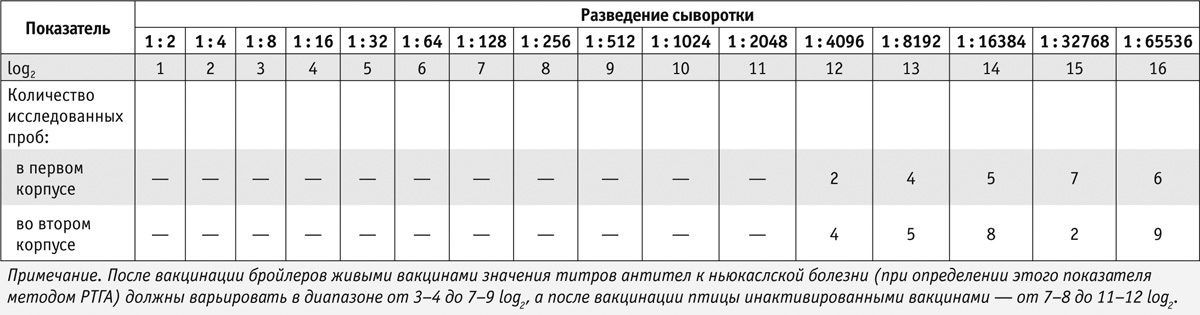
При постановке окончательного диагноза учитывали такие параметры, как результаты клинических и патолого-анатомических исследований, титры антител к ньюкаслской болезни и эпидемиологическая обстановка в данном регионе.
По субъективным причинам противовирусный препарат Тривирон в хозяйстве начали применять только с 32‑го дня. Уровень падежа на 32‑й день в первом корпусе достиг 1516 голов (9,23%), во втором — 620 голов (3,9%). После курса лечения бройлеров с использованием противовирусного препарата Тривирон (выпойка на протяжении семи дней в течение шести часов в сутки) на 38‑й день уровень падежа в первом корпусе составил 86 голов (0,52%), во втором — 80 голов (0,5%).
Данные эксперимента показали, что эффективность противовирусного препарата Тривирон была высокой (табл. 3).
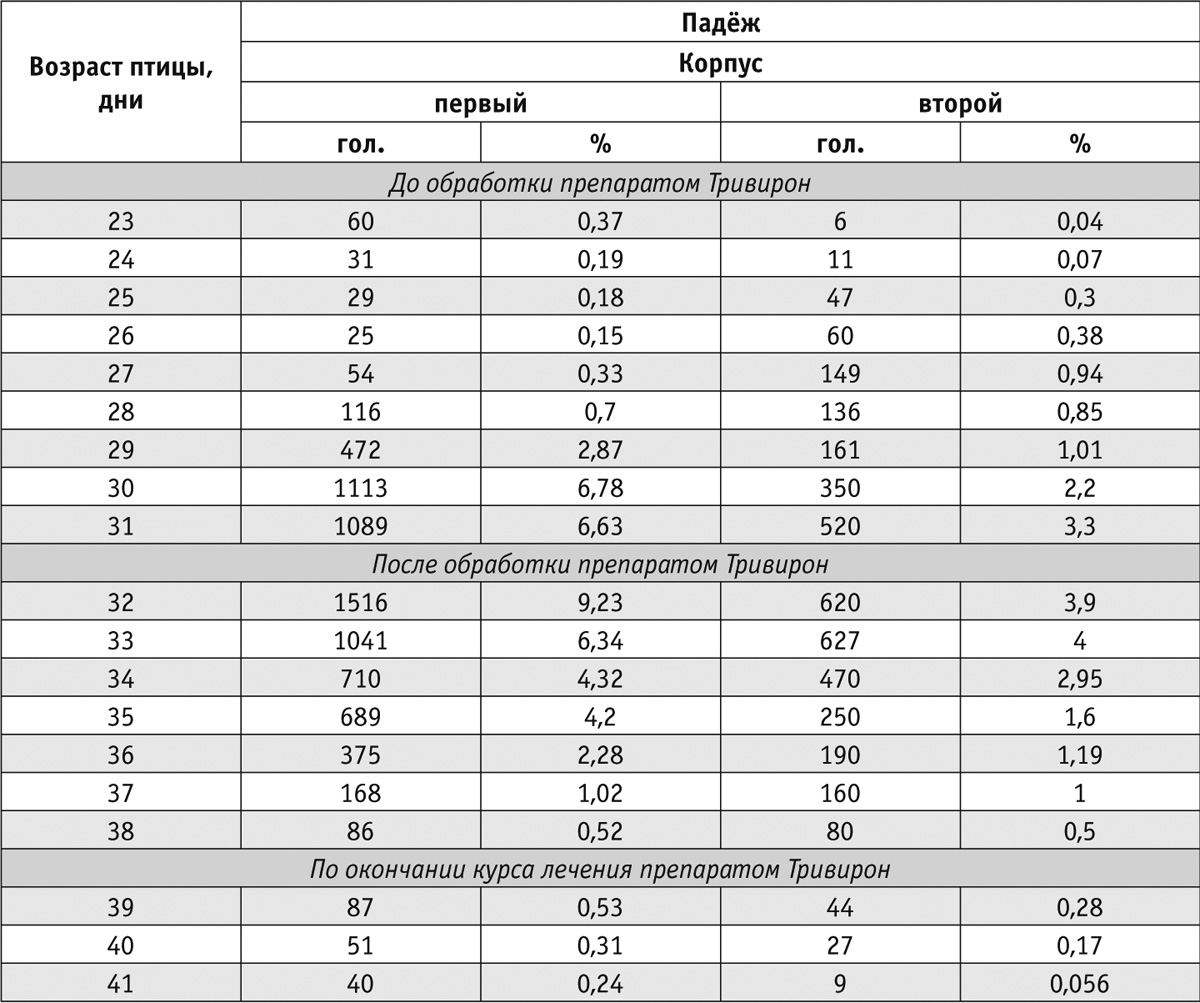
Результаты исследований, данные наших наблюдений и статьи, опубликованные в научной литературе, позволяют, не вдаваясь в детали относительно механизма реализации собственного потенциала, присущего типичным представителям семейств Coronaviridae и Paramyxoviridae и другим вирусам, сделать вывод, что способность колонизировать клетки-мишени и персистировать с током крови в органы и ткани организма — общее свойство всех вирусов. Стоит отметить, что этим свойством обладают не только полевые вирусы, внедряющиеся в макроорганизм, но и вирусы вакцинных штаммов, которые разными способами вводят в организм птицы.
При вспышках вирусных заболеваний или появлении поствакцинальных осложнений лечебно-профилактические мероприятия должны быть комплексными:
- связывание, уничтожение и выведение вирусов;
- снижение давления вирусного фактора на птицекомплексах путем использования йодсодержащих препаратов, распыления молочной кислоты или дезинфицирующих средств;
- подавление патогенной и условно-патогенной микрофлоры при помощи различных антибактериальных препаратов.
Между периодически регистрируемыми вспышками вирусных заболеваний (при обязательной вакцинации против большинства из них) и активизацией патогенной и условно-патогенной микрофлоры существует взаимосвязь. Этому есть объяснение.
В первом случае микоплазмы [Mycoplasma gallisepticum и (или) Mycoplasma synoviae], взаимодействуя с респираторными вирусами и оппортунистическими бактериями, вызывали обострение респираторных заболеваний. При этом разрушалась защитная система респираторного тракта птицы, вследствие чего респираторные патогены более интенсивно воздействовали на организм. Наглядный пример — поствакцинальная реакция, которая на фоне микоплазменной инфекции проявляется в более поздние сроки (в норме период возникновения поствакцинальной реакции составляет 3–10 дней). Применение (особенно аэрозольное введение) живых вирусвакцин против инфекционных респираторных заболеваний может спровоцировать обострение микоплазмозов, что в свою очередь не позволит получить хороший поствакцинальный иммунный ответ.
Во втором случае вследствие внедрения в слизистые оболочки респираторного или пищеварительного тракта птицы различных вирусов и их размножения (репликация генома и репродукция других структурных компонентов вириона) первоначально повышается распад эпителиальных клеток, граничащих с внешней средой. Время этого распада значительно превышает время, требующееся для естественного отмирания клеток.
Скорость распада эпителиальных клеток (сверх нормы) прямо пропорциональна скорости течения инфекционного процесса. Другими словами, при сверхусиленном распаде эпителиальных клеток течение болезни окажется сверхострым.
При молниеносном течении болезни, естественно, не идут токсические процессы (они просто не успевают развиться) и не проявляются клинические и патолого-анатомические изменения. В зависимости от заболевания при молниеносном течении болезни определенная часть бройлеров погибает. Остальная птица переболевает в острой, подострой или хронической форме (в этом случае могут проявляться клинические и патолого-анатомические изменения).
Из-за увеличения скорости распада эпителиальных клеток увеличивается нагрузка на печень, селезенку, почки, лейкоцитарную и другие системы организма. В такой ситуации он либо справляется с нагрузкой с большим трудом, либо вообще не справляется. Тогда начинается эндотоксикоз из-за отравления продуктами распада собственных клеток.
Открытие ворот первичным агентом, питательная среда, образовавшаяся за счет распада тканей, и подавленный иммунитет способствуют внедрению и размножению патогенных и условно-патогенных бактерий. Вследствие этого развиваются местные воспалительные процессы. Очень часто воспаление затрагивает прилегающие ткани. Если болезнетворные микроорганизмы попадают в кровь, развивается септицемия.
Результаты проведенных лабораторных и производственных исследований позволяют рекомендовать противовирусный препарат Тривирон для профилактики и лечения (методом выпойки и путем распыления) бройлеров от инфекционного бронхита кур и ньюкаслской болезни.
Синтетические рибонуклеазы лучше всего применять в течение шести часов в сутки на протяжении 2–10 дней. Использование противовирусного препарата Тривирон может быть оправданно при возрастном иммунодефиците. Это обусловлено тем, что формирование иммунной системы в онтогенезе имеет свои особенности.
В жизни цыплят и кур родительских стад можно выделить пять критических периодов, когда иммунная защита организма ослабевает: первый — с 3‑го по 5‑й день, второй — с 12‑го по 28‑й, третий — с 50‑го по 60‑й, четвертый — с 110‑го по 130‑й, пятый — с 240‑го по 300‑й день.
Применять противовирусный препарат Тривирон целесообразно и при опасности заноса в хозяйство полевых вирусов до того, как в организме птицы начнут циркулировать вирусы соответствующих вакцинных штаммов. Следует отметить, что за 1–2 суток до введения вакцин использование синтетических рибонуклеаз нужно полностью прекратить.
ООО «Трионис Вет»
141092, Московская обл., г. Королёв, мкр-н Юбилейный, ул. Лесная, д. 14, оф. 5
Тел.: +7 (499) 753‑83‑93
E-mail: info@trionisvet.ru
www.trionisvet.ru
Племенное свиноводство
Genesus
Башкирская мясная компания
Генетика ПИК
Топигс Норсвин
Ветеринарные препараты для животных и птиц
KRKA Фарма
Группа компаний ВИК
СЕВА Санте Анималь
Корма для животных и птиц
ANCORE
Мустанг Технологии Кормления
Оллтек
Провими
Фабрика Кормов
Оборудование для ферм
Comax-FTG
Биг Дачмен
Лаборатория
Агроплем
Механизм противовирусного действия препарата «Тривирон» основан на разрушении РНК вирусных частиц с помощью низкомолекулярной искусственной рибонуклеазы (artificial ribonucleases).
Доказано, что гидролиз РНК под действием химически синтезированных рибонуклеаз протекает аналогично гидролизу РНК под действием панкреатических РНК-аз. Свойства таких искусственных РНК-аз используются в препарате «Тривирон», обуславливая его противовирусную активность. Еще одним важным свойством, которым обладают искусственные рибонуклеазы, является каталитический характер их действия, т. е. искусственные рибонуклеазы могут действовать многократно – одна молекула РНК-азы может разрушить много молекул РНК, что позволяет использовать противовирусный препарат «Тривирон» в низких дозах.
Для борьбы с респираторными РНК-вирусами была разработана схема аэрозольного применения противовирусного препарата «Тривирон». Аэрозольное применение препарата санирует носовые ходы, трахею и бронхи от возбудителей РНК-вирусных инфекций, в т. ч. и от метапневмовирусной инфекции (МПВИ), а также способствует инактивации вирусных частиц в воздухе. Так как МПВИ является «доза-зависимой» инфекцией, то даже незначительное снижение концентрации вируса в воздухе может иметь клиническое значение.
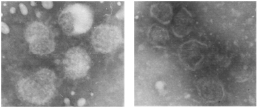
1. Результаты электронной микроскопии. Частицы вируса гриппа, не обработанные РНКазами
2. Результаты электронной микроскопии. Частицы вируса гриппа, обработанные РНКазами
Материалы и методы
Исследования проводили на базе лаборатории фармакогеномики Института химической биологии и фундаментальной медицины СО РАН и сектора молекулярной биологии Института экспериментальной ветеринарии Сибири и Дальнего Востока СФНЦА РАН.
Цыплят-бройлеров кросса Hubbard F15 в возрасте двух недель заражали вакцинным штаммом вируса инфекционного бронхита кур IB 4-91 (в составе живой аттенуированной вакцины Nobilis IB4-91, производство Intervet). Цыплятам аэрозольно была введена вакцина в расчете 1 доз на одну голову. Средний диаметр капли – 1,13 мкм, экспозиция – 3 мин.
Аэрозольная камера
Цыплята были разделены на четыре опытные (по шесть голов) и одну контрольную (семь голов) группы. Через три часа после заражения цыплят опытных групп подвергали аэрозольной обработке противовирусным препаратом «Тривирон» с экспозицией 1, 2, 4 и 6 мин. Курс лечения составил три обработки (по одной обработке в сутки).
Для контроля биодоступности аэрозоля перед завершением эксперимента (через три часа после последней обработки) цыплятам опытных групп вводили аэрозоль контрольного вещества «Aritest» с той же экспозицией, что и препарат «Тривирон».
Объем аэрозольной камеры был 111 12 см3 (с учетом объема оборудования в камере ~ 1 м3). Расход подготовленного для аэрозольного распыления рабочего раствора препарата «Тривирон» (рабочий раствор препарата «Тривирон» – это препарат «Тривирон», разведенный с водой в 1 раз) составил 3 мл/м3. Генерацию аэрозоля осуществляли с использованием компрессорного небулайзера Microlife. Средний диаметр капли – 1,13 мкм.
Компрессорный небулайзер Microlife
Результаты собственных исследований и их обсуждение
Разработка схемы аэрозольной терапии
На первом этапе исследования была разработана и оптимизирована схема подготовки противовирусного препарата «Тривирон» для его аэрозольного применения птице, т. к. для стабилизации действующего вещества и предотвращения его адсорбции на стенках емкостей в составе препарата содержится муравьиная кислота.
После разведения препарата в дистиллированной воде в соотношении 1:1 добавляют компоненты для нейтрализации муравьиной кислоты, содержащейся в препарате, и глицерин, который позволяет стабилизировать размер капли при получении аэрозоля.
При аэрозольной обработке рабочим раствором препарата «Тривирон» цыплята вели себя аналогично тому, как и при их аэрозольной обработке дистиллированной водой в смеси с глицерином (контроль). После завершения обработки поведение цыплят не отличалось от их состояния, которое было у них перед обработкой аэрозолем.
Испытание аэрозольной терапии противовирусным препаратом «Тривирон» на модели заражения двухнедельных цыплят десятикратной дозой вакцинного штамма вируса ИБК.
Цыплята в аэрозольной камере
Предварительное тестирование трахеи у цыплят в возрасте одних–трех суток методом ПЦР на наличие геномной РНК вируса инфекционного бронхита кур показало отсутствие вируса у большинства цыплят (было положительно три пробы у девяти цыплят в возрасте одних–трех суток). Это свидетельствует, что наличие трансовариальных антител в большинстве случаев препятствует вакцинации цыплят в первые дни жизни. В зарубежной литературе случаи заражения суточных цыплят, полученных от привитого родительского стада, также не были обнаружены.
Аэрозольное распыление препарата «Тривирон»
В связи с этим была предложена модель инфекции ИБК путем аэрозольного заражения цыплят десятикратной дозой вакцинного вариантного штамма ИБК. Для этого использовали живую аттенуированную вакцину Nobilis IB4-91, производство Intervet.
Размер капли аэрозоля (1,13 мкм) был оптимален для попадания вируса в бронхи и трахею, т. е. в отличие от спрей-вакцинации мы обеспечили сразу попадание значительной дозы вируса ИБК в чувствительные к заражению ткани птицы, что должно было обеспечить эффект переболевания.
Факт гибели 28,5% цыплят в контрольной группе и 16% цыплят в группе, получавшей минимальную дозу противовирусного препарата «Тривирон» (за счет меньшей экспозиции), а также наличие воспалительной реакции в легких и трахее у птиц во всех группах позволяет говорить об успешности предложенной модели инфекционного процесса.
Как следует из табл. 1, при использовании противовирусного препарата «Тривирон» удается повысить выживаемость цыплят на 28% (при экспозиции более 1 мин.) и снизить встречаемость пневмоний на 6% (при экспозиции 4 мин. и более).
По результатам ПЦР вирус инфекционного бронхита кур встречался во всех группах, что подтверждает успешность заражения вирусом ИБК. Однако вирус ИБК был обнаружен не в каждой пробе трахеи, что может быть обусловлено как разрушением эпителия трахеи, так и наличием гуморального иммунитета у части цыплят после первой вакцинации (по нашим наблюдениям, до 3–4% цыплят могут сформировать гуморальный иммунитет после вакцинации в суточном возрасте).
Легкие цыпленка из опытной группы
с экспозицией 6 мин.
Цыпленок из контрольной группы.
Легкие серого цвета, сосуды более кровенаполненные
Интересным фактом является то, что в ряде случаев в опытных группах при наличии пневмонии наблюдались абсолютно здоровые трахея и бронхи. Учитывая, что размер частиц аэрозоля позволял санировать трахею и бронхи, но не легкие, можно допустить, что в месте попадания противовирусного препарата «Тривирон» на слизистую оболочку трахеи и бронхов наблюдается защитный эффект.
Вывод
Аэрозольное применение противовирусного препарата «Тривирон» повышает выживаемость цыплят при респираторной форме инфекционного бронхита кур (на 28% при экспозиции более 1 мин.) и снижает возникновение пневмоний (на 6% при экспозиции 4 и более мин.).
Triviron forte-TRV

Triviron forte-TRV
Description:
Triviron forte-TRV is an antiviral veterinary product.
Dosage form: oral solution.
1 ml contains 30.0 mg of aRNase (1.5-bis- [N.N- 1- (4- tetradecyl) diazo1-1- abicyclo [2.2.2] octyl] pentane tetrobromide), and excipients: propylene glycol and lactic acid.
Triviron forte-TRV is used for therapeutic and prophylactic purposes in animals and poultry with infections caused by RNA viruses:
- poultry — infectious bronchitis of chickens, infectious bursal disease, avian influenza, viral arthritis in poultry, Newcastle disease, pneumovirus in poultry, paramyxoviruses in poultry, infectious encephalomyelitis in poultry, coronavirus enteritis of turkeys, astroviral infections in poultry, hepatitis of ducks, viral hepatitis of turkeys, viral nephritis of turkeys and other infections caused by RNA genomic viruses sensitive to the veterinary product;
- pigs — rotavirus diarrhea, enteroviral gastroenteritis of piglets, porcine respiratory reproductive syndrome, influenza of piglets, and other infections caused by RNA genomic viruses sensitive to the veterinary product;
- calves — rotavirus enteritis, coronavirus enteritis, parainfluenza-3, respiratory syncytial infection, and other infections caused by RNA genomic viruses sensitive to the veterinary product.
Method of administration and dosage:
The veterinary product is administered
Pigs:
- for prophylactic purposes at the dose of 0.05 ml of the veterinary product per 1 kg of body weight.
The veterinary product is introduced into the drinking system through a medicator, having previously dissolved it in a volume of water (corresponds to the volume of the medicator’s stock solution), which the pigs can drink within 6-8 hours. The course is 2-10 days.
- for therapeutic purposes at the dose of 0.1 ml of the veterinary product per 1 kg of body weight.
The veterinary product is introduced into the drinking system through a medicator, having previously dissolved it in a volume of water (corresponds to the volume of the medicator’s stock solution), which the pigs can drink within 6-8 hours. The course is 2-10 days.
Poultry:
- for prophylactic purposes at the dose of 0.00125-0.0025 ml of the veterinary product per 1 kg of body weight. The veterinary product is introduced into the drinking system through a medicator (1-2% input), having previously dissolved it in a volume of water (corresponds to the volume of the medicator’s stock solution), which the poultry can drink within 6-8 hours. The course is 2-10 days.
- for therapeutic purposes at the dose of 0.0025-0.005 ml of the veterinary product per 1 kg of body weight. The veterinary product is introduced into the drinking system through a medicator (1-2% input), having previously dissolved it in a volume of water (corresponds to the volume of the medicator’s stock solution), which the poultry can drink within 4-6 hours. The course is 2-10 days.
Cattle:
- for prophylactic purposes at the dose of 0.05 ml of the veterinary product per 1 kg of body weight. Before drinking, the veterinary product must be diluted in drinking water in a ratio of 1: 1000. The course is 2-10 days.
- for therapeutic purposes at the dose of 0.1 ml of the veterinary product per 1 kg of body weight. Before drinking, the veterinary product must be diluted in drinking water in a ratio of 1: 1000. The course is 2-10 days.
It is forbidden to drink the veterinary product in its pure form to animals and poultry!
When diluting, the veterinary product is added to water in a thin stream (to avoid the formation of a precipitate) with vigorous stirring.
Pharmaceutical properties
The veterinary product has a pronounced effect on RNA-containing viruses of the families Paramyxoviridae, Coronaviridae, Arenaviridae, Retroviridae, Picornaviridae, Birnaviridae, Orthomyxoviridae, etc.
The mechanism of action is based on the damage of RNA viral particles using a low molecular weight artificial ribonuclease. High stability to physical and chemical factors, as well as the small size of artificial RNase in comparison with protein molecules, provide high efficiency of antiviral therapy. The small molecular weight of the compound increases the efficiency of penetration of synthetic ribonuclease into the virus capsid and high chemical and temperature stability provides the possibility of oral administration of the antiviral veterinary product.
The veterinary product is not toxic, no contraindications were found.
The veterinary product, according to the degree of exposure belongs to moderate-hazard substances (hazard class 3 according to GOST 12.1.007-76).







.jpg)
.jpg)
.jpg)