Зеюла — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер: ЛП-№(002327)-(РГ-RU) от 15.05.2023
Листок-вкладыш – информация для пациента
Зеюла, 100 мг, капсулы
Действующее вещество: нирапариб
▼ Лекарственный препарат подлежит дополнительному мониторингу, который способствует быстрому выявлению новых сведений о безопасности. Это позволит в короткий срок выявить новую информацию по безопасности. Вы можете помочь, сообщая информацию о любых нежелательных реакциях, которые возникли в период применения лекарственного препарата (в том числе и о случаях его неэффективности). Способ сообщения о нежелательных реакциях описан в разделе 4 листка-вкладыша.
Перед приемом препарата полностью прочитайте листок-вкладыш, поскольку в нем содержатся важные для Вас сведения.
- Сохраните этот листок-вкладыш. Возможно, Вам потребуется прочитать его еще раз.
- Если у Вас возникли дополнительные вопросы, обратитесь к лечащему врачу.
- Препарат назначен именно Вам. Не передавайте его другим людям. Он может навредить им, даже если симптомы их заболевания совпадают с Вашими.
- Если у Вас возникли какие-либо нежелательные реакции, обратитесь к лечащему врачу. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в разделе 4 листка-вкладыша.
Содержание листка-вкладыша
- Что из себя представляет препарат Зеюла, и для чего его применяют.
- О чем следует знать перед приемом препарата Зеюла.
- Прием препарата Зеюла.
- Возможные нежелательные реакции.
- Хранение препарата Зеюла.
- Содержимое упаковки и прочие сведения.
1. Что из себя представляет препарат Зеюла, и для чего его применяют
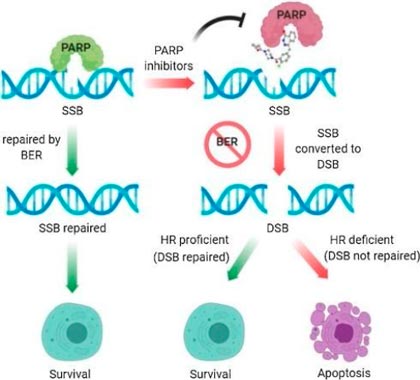
Препарат Зеюла содержит действующее вещество нирапариб. Нирапариб представляет собой разновидность противоопухолевых лекарственных препаратов, называемых ингибиторами PARP. Ингибиторы PARP блокируют фермент под названием «поли[аденозиндифосфат-рибоза] полимераза» (PARP). PARP помогает клеткам восстанавливать поврежденную ДНК, поэтому его блокировка означает, что ДНК раковых клеток не будет восстанавливаться. Это приводит к гибели раковой клетки, что помогает контролировать онкологическое заболевание.
Показания к применению
Препарат Зеюла применяется у взрослых женщин в возрасте старше 18 лет для поддерживающего лечения ракового заболевания, в случае:
- положительного эффекта (полного или частичного ответа) после первого курса химиотерапии, включавшей препараты платины;
- положительного эффекта (полного или частичного ответа) после повторного курса химиотерапии, включавшей препараты платины, после возобновления (рецидива) ракового заболевания.
Такие типы раковых заболеваний могут включать рак яичников, фаллопиевых труб (часть женской репродуктивной системы, которая связывает яичники с маткой) или брюшины (оболочка, выстилающая брюшную полость).
2. О чем следует знать перед приемом препарата Зеюла
Противопоказания
Не принимайте препарат Зеюла:
- если у Вас аллергия на нирапариб или любые другие компоненты препарата (перечисленные в разделе 6 листка-вкладыша);
- если Вы кормите ребенка грудью.
Особые указания и меры предосторожности
Проконсультируйтесь с врачом перед началом лечения или во время лечения препаратом Зеюла, если к Вам может быть применимо что-либо из нижеперечисленного:
Низкое число клеток крови
Препарат Зеюла может снижать количество клеток крови, таких как эритроциты (анемия), лейкоциты (нейтропения) или тромбоциты (тромбоцитопения). Признаки и симптомы, на которые Вам необходимо обращать внимание, включают повышенную температуру, инфекции, аномальные кровоподтеки или кровотечения (см. дополнительную информацию в разделе 4). Ваш врач будет регулярно направлять Вас на анализы крови на протяжении всего курса лечения.
Миелодиспластический синдром / острый миелоидный лейкоз
В редких случаях низкое число клеток крови может быть признаком более серьезных проблем с костным мозгом, таких как миелодиспластический синдром (МДС) или острый миелоидный лейкоз (ОМЛ). Ваш врач может направить Вас на исследование костного мозга, чтобы проверить наличие таких проблем.
Высокое артериальное давление
Препарат Зеюла может вызывать повышение артериального давления, которое в некоторых случаях может быть тяжелым. Ваш врач будет регулярно измерять Ваше артериальное давление на протяжении всего лечения. Также Ваш врач может назначить Вам препараты для лечения высокого артериального давления и при необходимости скорректировать Вашу дозу препарата Зеюла.
Синдром задней обратимой энцефалопатии (СЗОЭ)
При лечении препаратом Зеюла может развиваться редкое неврологическое нежелательное явление под названием «синдром задней обратимой энцефалопатии» (СЗОЭ). Если у Вас появились головная боль, нарушения зрения, спутанность сознания или судороги, с высоким артериальным давлением или без него, обратитесь к Вашему врачу.
Дети и подростки
Не давайте препарат Зеюла детям и подросткам в возрасте до 18 лет. Применение препарата не изучалось у детей и подростков.
Другие препараты и препарат Зеюла
Сообщите лечащему врачу о том, что Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты.
Следующие препараты могут влиять на действие препарата Зеюла и наоборот:
- препараты, подавляющие иммунную систему – иммунодепрессанты (например, циклоспорин, такролимус);
- другие препараты для лечения опухолей (например, иринотекан, метотрексат);
- препараты, применяемые для снижения уровня холестерина (например, розувастатин, симвастатин, аторвастатин);
- препараты для лечения психических расстройств (например, кветиапин, пимозид, клозапин);
- алфснтанил (обезболивающий препарат);
- эрготамин (сосудосуживающий препарат, применяется при маточных кровотечениях и мигрени);
- теофиллин (препарат для лечения бронхиальной астмы);
- галофантрин (препарат для лечения малярии);
- ропинирол (препарат для лечения болезни Паркинсона);
- метформин (препарат для лечения сахарного диабета).
Если Вы планируете вакцинацию, проконсультируйтесь с лечащим врачом.
Беременность и грудное вскармливание
Препарат Зеюла нельзя принимать во время беременности, поскольку он может нанести вред Вашему ребенку. Если Вы беременны, предполагаете, что беременны, или планируете беременность, перед началом применения препарата проконсультируйтесь с лечащим врачом.
Если Вы – женщина, способная забеременеть, Вы должны использовать высокоэффективные средства контрацепции во время лечения препаратом Зеюла, а также продолжать использовать их в течение 6 месяцев после приема последней дозы препарата. Ваш врач попросит Вас подтвердить, что Вы не беременны, сдав тест на беременность перед началом лечения. Немедленно обратитесь к Вашему врачу, если Вы забеременеете во время приема препарата Зеюла.
Препарат Зеюла не следует принимать во время грудного вскармливания, поскольку неизвестно, проникает ли он в грудное молоко. Если Вы кормите грудью, прекратите вскармливание до начала приема препарата Зеюла и не возобновляйте в течение 1 месяца после приема последней дозы препарата. Посоветуйтесь с Вашим врачом перед началом лечения данным препаратом.
Управление транспортными средствами и работа с механизмами
Во время приема препарата Зеюла Вы можете испытывать трудности с концентрацией внимания, чувствовать слабость, усталость или головокружение (см. дополнительную информацию в разделе 4), что может повлиять на Вашу способность управлять транспортными средствами и работать с механизмами. Соблюдайте осторожность во время управления транспортными средствами и работы с механизмами.
Препарат Зеюла содержит лактозу
Если у Вас непереносимость некоторых сахаров, обратитесь к лечащему врачу перед приемом данного лекарственного препарата.
Препарат Зеюла содержит тартразин (Е 102)
Тартразин может вызывать аллергические реакции.
3. Прием препарата Зеюла
Всегда принимайте препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений посоветуйтесь с лечащим врачом.
Рекомендуемая доза
Поддерживающая терапия рака яичников с положительным эффектом после первого курса химиотерапии, включающей препараты платины
Рекомендованная начальная доза составляет 200 мг (2 капсулы по 100 мг) один раз в сутки, независимо от приема пищи. Если до начала лечения Ваша масса тела составляет 77 кг и более, а число тромбоцитов составляет 150 000/мкл и более, рекомендованная начальная доза составляет 300 мг (3 капсулы по 100 мг) один раз в сутки, независимо от приема пищи.
Поддерживающая терапия при возобновлении (рецидиве) рака яичников
Рекомендованная начальная доза составляет 300 мг (3 капсулы по 100 мг) один раз в сутки, независимо от приема пищи.
Принимайте препарат Зеюла каждый день примерно в одно и то же время. Возможен прием препарата Зеюла перед сном, если в другое время после его приема Вы ощущаете тошноту.
Ваш врач может рекомендовать Вам другую дозу, если у Вас есть проблемы с печенью.
Способ применения
Проглатывайте капсулу препарата Зеюла целиком, запивая водой. Не разжевывайте и не измельчайте капсулы.
Ваш врач может рекомендовать Вам уменьшить дозу препарата при появлении у Вас нежелательных реакций (таких как тошнота, утомление, аномальные кровотечения и кровоподтеки, анемия).
Ваш врач будет регулярно контролировать Ваше состояние. Не прекращайте применение препарата Зеюла, пока он помогает Вам или пока у Вас не возникнут неприемлемые нежелательные реакции.
Если Вы приняли препарата Зеюла больше, чем следовало
Если Вы приняли большее количество препарата, чем обычно, немедленно свяжитесь с Вашим врачом.
Если Вы забыли принять препарат Зеюла
Не принимайте дополнительную дозу, если Вы пропустили прием препарата или если у Вас возникла рвота после приема препарата Зеюла. Примите Вашу следующую дозу в запланированное время. Не принимайте двойную дозу, чтобы компенсировать пропущенную дозу.
При наличии вопросов по применению препарата обратитесь к лечащему врачу.
4. Возможные нежелательные реакции
Подобно всем лекарственным препаратам, препарат Зеюла может вызывать нежелательные реакции, однако они возникают не у всех.
Немедленно обратитесь к Вашему врачу, если Вы заметите какие-либо из СЕРЬЕЗНЫХ нежелательных реакций, перечисленных ниже, – Вам может потребоваться экстренная медицинская помощь:
Очень часто (могут возникать у более чем 1 из 10 человек):
- Кровоподтеки или кровотечения, которые продолжаются дольше, чем обычно, если Вы поранитесь – это может быть признаками низкого числа тромбоцитов (тромбоцитопения).
- Одышка, чувство сильной усталости, бледная кожа или учащенное сердцебиение – это может быть признаками низкого числа эритроцитов (анемия).
- Повышенная температура или инфекция – низкое число определенного вида белых кровяных клеток – нейтрофилов (нейтропения), может повышать риск развития инфекции. Признаки могут включать повышение температуры, озноб, слабость, спутанность сознания, кашель, боль или жжение во время мочеиспускания. Некоторые инфекции могут быть серьезными и приводить к летальному исходу.
- Снижение числа лейкоцитов (лейкопения). Низкое число лейкоцитов может снижать способность Вашего организма бороться с инфекциями.
Часто (могут возникать не более чем у 1 из 10 человек):
- Низкое количество клеток крови вследствие проблем с костным мозгом или рака крови, который развивается в костном мозге (МДС или ОМЛ).
- Аллергические реакции, включая серьезные, представляющие угрозу для жизни). Признаки могут включать зудящие волдыри (крапивницу) или сыпь на коже; припухлости, иногда в области лица или рта (ангионевротический отек); затрудненное дыхание; обморок или потерю сознания.
Редко (могут возникать не более чем у 1 из 1000 человек):
- Внезапное повышение артериального давления, что может представлять собой неотложное состояние, которое может приводить к поражению органов или представлять угрозу для жизни (гипертонический криз).
- Состояние головного мозга с симптомами, включающими судороги, головную боль, спутанность сознания и нарушения зрения, которое может приводить к поражению органов или представлять угрозу для жизни (синдром задней обратимой энцефалопатии [СЗОЭ]).
При приеме препарата Зеюла могут возникать и другие нежелательные реакции (однако они возникают не у всех):
Очень часто (могут возникать у более чем 1 из 10 человек):
- боль в животе,
- нарушение пищеварения, неприятные ощущения со стороны желудка и кишечника (диспепсия),
- кашель,
- болезненное и частое мочеиспускание (инфекция мочевыводящих путей),
- головная боль,
- ощущение слабости (астения),
- упадок сил (утомляемость),
- головокружение,
- боль в суставах (артралгия),
- боль в спине,
- затрудненная дефекация (запор),
- тошнота,
- рвота,
- частый водянистый стул (диарея),
- затрудненное дыхание (одышка),
- насморк или заложенный нос (назофарингит),
- проблемы со сном (бессонница),
- снижение аппетита,
- частое или нерегулярное сердцебиение (пальпитация),
- высокое артериальное давление (артериальная гипертензия).
Часто (могут возникать не более чем у 1 из 10 человек):
- воспаление глаз (конъюнктивит);
- сухость во рту;
- отек голеней и стоп (периферический отек);
- носовое кровотечение;
- печальное, подавленное настроение (депрессия);
- боль в мышцах (миалгия);
- снижение массы тела;
- снижение уровня калия в крови (гипокалиемия), которое может приводить к нерегулярному сердцебиению;
- воспаление или отек дыхательных путей между ртом, носом и легкими (бронхит);
- болезненность, покраснение ротовой полости (мукозит/стоматит);
- сыпь на коже;
- повышение кожной чувствительности к солнечному свету (фоточувствительность);
- чувство беспокойства, нервозности или тревоги (тревожность);
- нарушение концентрации, понимания, памяти и мышления (нарушения когнитивной функции);
- учащенное сердцебиение (тахикардия), которое может вызывать головокружение, боль в груди или одышку;
- повышение уровня креатинина в крови, которое может быть признаком поражения почек;
- нетипичный вкус во рту (дисгевзия);
- вздутие живота;
- аномально высокое содержание печеночных ферментов в крови, которое может означать, что работа Вашей печени нарушена. Это может вызывать утомление, тошноту и боль в животе. Несмотря на то, что эти изменения обычно имеют легкий характер и обратимы, они также могут быть серьезными и представлять угрозу для жизни. Специфическими ферментами являются:
- аспартаттрансаминаза (ACT),
- аланинаминотрансфераза (АЛТ),
- гамма-глутамилтрансфераза (ГГТ) и/или
- щелочная фосфатаза (ЩФ).
Нечасто (могут возникать не более чем у 1 из 100 человек):
- спутанность мыслей, сложности в ориентации во времени и пространстве (спутанность сознания);
- воспаление легких, которое может приводить к одышке и затрудненному дыханию (пневмонит).
Сообщите Вашему врачу, если какая-либо из перечисленных выше нежелательных реакций приобрела тяжелый характер или причиняет беспокойство, или если Вы заметили нежелательную реакцию, которая не указана в данном листке-вкладыше.
Сообщение о нежелательных реакциях
Если у вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую через систему сообщений государств-членов Евразийского экономического союза (см. ниже). Сообщая о нежелательных реакциях, вы помогаете получить больше сведений о безопасности препарата.
Российская Федерация
Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор)
Адрес: 109012, г. Москва, Славянская площадь, д. 4, стр. 1
Сайт: roszdravnadzor.gov.ru
5. Хранение препарата Зеюла
Храните препарат в недоступном для ребенка месте так, чтобы ребенок не мог увидеть его.
Не принимайте препарат после истечения срока годности (срока хранения), указанного на блистере и картонной пачке после «Годен до».
Датой истечения срока годности является последний день месяца.
Храните при температуре не выше 25 °С.
Не принимайте препарат, если Вы заметили какое-либо повреждение или признаки нарушения целостности упаковки.
Не выбрасывайте препарат в канализацию или с бытовыми отходами. Уточните у работника аптеки, как следует утилизировать препарат, который больше не потребуется. Эти меры позволят защитить окружающую среду.
6. Содержимое упаковки и прочие сведения
Препарат Зеюла содержит:
Действующим веществом препарата Зеюла является нирапариб. Каждая капсула содержит 100 мг нирапариба (в виде тозилата моногидрата).
Прочими ингредиентами (вспомогательными веществами) являются: лактозы моногидрат, магния стеарат, твердая желатиновая капсула №0 [титана диоксид, краситель FD&C синий №1, краситель FD&C красный №3, краситель FD&C желтый №5, желатин, чернила черные SW-9049 (шеллак, дегидратированный спирт, изопропиловый спирт, бутиловый спирт, пропиленгликоль, вода очищенная, раствор аммиака концентрированный, калия гидроксид, железа оксид черный), чернила белые SB-0007P (шеллак, дегидратированный спирт, изопропиловый спирт, бутиловый спирт, пропиленгликоль, натрия гидроксид, повидон, титана диоксид)].
Внешний вид препарата Зеюла и содержимое упаковки
Препарат Зеюла представляет собой твердые желатиновые капсулы №0 с белым непрозрачным корпусом и фиолетовой непрозрачной крышечкой. На корпусе капсулы черными чернилами нанесено «100 mg», а на крышечке белыми чернилами нанесено «Niraparib». Содержимое капсулы: порошок белого или почти белого цвета.
По 14 капсул помещают в блистер из полихлортрифторэтилена (Ас1аг®)/ПВХ пленки/алюминиевой фольги. По 4 блистера вместе с листком-вкладышем в пачку картонную.
Держатель регистрационного удостоверения
АО «ГлаксоСмитКляйн Трейдинг»
Российская Федерация, 125167, г. Москва, Ленинградский пр-т, д. 37А, корпус 4, этаж 3, помещение XV, комната 1
Производитель (выпускающий контроль качества)
«ГлаксоСмитКляйн ЭлЭлСи» / GlaxoSmithKline LLC
1011 Норт Аренделл Авеню, Зебулон, Северная Каролина 27597, США /1011 North Arendell Avenue, Zebulon, North Carolina 27597, USA
За любой информацией о препарате, а также в случаях возникновения претензий следует обращаться к местному представителю держателя регистрационного удостоверения:
Российская Федерация
АО «ГлаксоСмитКляйн Трейдинг»
Адрес: 125167, г. Москва, Ленинградский пр-т, д. 37А, корпус 4, этаж 3, помещение XV, комната 1
Листок-вкладыш пересмотрен
Подробные сведения о препарате содержатся на веб-сайте Союза eec.eaeunion.org/.
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
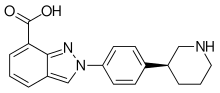
Нирапариб
Niraparib
Фармакологическое действие
Нирапариб — ингибитор фермента поли(АДФ-рибоза)полимеразы (PARP), который является высокоселективным по отношению к PARP-1 и PARP-2. PARP-1 и PARP-2, участвующих в обнаружении повреждения ДНК и способствуют восстановлению. Ингибирование ферментативной активности PARP приводит к повреждению ДНК, апоптозу и гибели клеток. Нирапариб индуцирует цитотоксичность в опухолевых клеточных линиях с дефицитом BRCA1/2 и без него.
Показания
Поддерживающее лечение рецидивирующего эпителиального яичника, маточной трубы или первичного рака брюшины у пациентов, которые полностью или частично реагируют на химиотерапию на основе платины.
Противопоказания
- Повышенная чувствительность к нирапарибу;
- отсутствие адекватных методов контрацепции;
- беременность;
- лактация.
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — N.
Адекватных и строго контролируемых исследований по безопасности применения нирапариба при беременности у человека не проведено.
Препарат может нанести вред плоду, так как он нацелен на активно делящиеся клетки. Это может вызвать тератогенность и эмбриофетальную летальность вследствие его генотоксичности.
Женщины репродуктивного возраста и мужчины, ведущие половую жизнь, во время лечения должны использовать надёжные методы контрацепции. В случае наступления беременности, отсутствия менструации или при подозрении на возможную беременность пациентка должна сообщить об этом своему лечащему врачу. Если нирапариб применяется в период беременности или беременность наступила во время лечения, пациентка должна быть предупреждена о потенциальной опасности для плода.
Применение нирапариба у беременных женщин противопоказано.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения нирапариба в период грудного вскармливания не проведено.
Неизвестно, выделяется ли нирапариб в грудное человеческое молоко. Риск для грудного ребёнка не может быть исключён.
Нирапариб противопоказан при кормлении грудью.
Фертильность
Препарат может ухудшить фертильность у мужчин с репродуктивным потенциалом.
Применение в детском возрасте
Эффективность и безопасность у детей и подростков не установлены.
Способ применения и дозы
Перорально (внутрь).
Побочные действия
Наиболее распространёнными побочными эффектами в исследованиях были: тромбоцитопения (у 61 % пациентов, тяжёлая у 29 %), анемия (у 50 %, тяжёлая у 25 %), нейтропения (у 30 %, тяжёлая у 20 %). Другие, в основном лёгкие или умеренные побочные эффекты включали тошноту, усталость, запоры . В исследовании, проводившемся более 250 дней (в среднем), 15% пациентов были вынуждены окончательно прекратить приём нирапариба из-за побочных эффектов.
Взаимодействие
Следующие препараты могут влиять на действие нирапариба и наоборот:
- препараты, подавляющие иммунную систему — иммунодепрессанты (например, циклоспорин, такролимус);
- другие препараты для лечения опухолей (например, иринотекан, метотрексат);
- препараты, применяемые для снижения уровня холестерина (например, розувастатин, симвастатин, аторвастатин);
- препараты для лечения психических расстройств (например, кветиапин, пимозид, клозапин);
- алфентанил;
- эрготамин;
- теофиллин;
- галофантрин;
- ропинирол;
- метформин.
При планируемой вакцинации необходимо получить консультацию лечащего врача.
Влияние на способность к вождению автотранспорта и управлению механизмами
Необходимо соблюдать осторожность во время управления транспортными средствами и занятий видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Классификация
-
АТХ
L01XX54, L01XK02
-
Фармакологическая группа
-
Категория при беременности по FDA
N
(не классифицировано FDA)
Информация о действующем веществе Нирапариб предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Нирапариб, содержатся в инструкции производителя, прилагаемой к упаковке.
Новости онкологии
08.11.2017
Тюляндин Сергей Алексеевич
Заслуженный деятель науки РФ, главный научный сотрудник ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, член правления RUSSCO, профессор, доктор медицинских наук, Москва
В арсенале противоопухолевых средств появился новый класс препаратов – ингибиторов PARP (поли(аденозиндтфосфат [ADP]-рибозы) полимераза). Этот фермент играет важнейшую роль в репарации однонитиевых разрывов ДНК. В случае отсутствия функции фермента PARP в результате ингибирования его функции все однонитиевые разрывы ДНК превращаются в двухнитиевые, которые наиболее трудны для восстановления. Наиболее эффективным методом восстановления структуры ДНК при разрыве двух нитей является метод гомологичной репарации.
Ключевую роль в инициации гомологичной рекомбинации играют белки BRCA 1 и 2. В случае нарушения функции белка BRCA (например, в результате мутации его гена) механизм гомологичной репарации заблокирован, клетка не может восстановить структуру ДНК, в которой накапливаются двухнитиевые разрывы, что в конечном случае должно приводить к остановке клеточного деления и включению апоптоза. Известно, что у 15-20% больных серозным раком яичников имеется герминальная (наследственная) мутация гена BRCA, в результате которой мутированный белок BRCA утрачивает способность запускать гомологичную репарацию. Еще у 5-15% больных имеется соматическая (определяемая только в опухолевых клетках) мутация гена BRCA. Однако нарушения гомологичной репарации за счет других механизмов – гораздо более часто встречаемый феномен (феномен BRCAness). Это может происходить за счет мутации генов, которые кодируют другие белки, участвующие в гомологичной репарации, или за счет гиперметилирования участков ДНК, контролирующих функцию гена BRCA.
Все это делает перспективным использование ингибиторов PARP у больных с отсутствием функции гомологичной репарации. Блокада PARP приводит к многочисленным двухнитиевым разрывам ДНК, которые клетка не может восстановить ввиду отсутствия механизма гомологичной репарации.
Первый препарат из этой группы – олапариб, который зарегистрирован в России под торговым названием «Линпарза», производства компании АстраЗенека, был изучен в качестве поддерживающей терапии у больных с платиночувствительным рецидивом и продемонстрировал достоверное увеличение времени до прогрессирования у больных серозным раком яичников с наличием герминальной мутации гена BRCA 1 и 2 [1]. Имеющийся опыт использования PARP ингибиторов не дал убедительных свидетельств о целесообразности назначения этих препаратов при наличии соматических мутаций гена BRCA или наличии феномена BRCAness. Тем важнее результаты рандомизированного исследования ингибитора PARP нирапариба в сравнении с плацебо в качестве поддерживающей терапии у больных с платиночувствительным рецидивом серозного рака яичников, которые были доложены на прошедшем в Копенгагене конгрессе ESMO и одновременно опубликованные в New England Journal of Medicine [2].
В это исследование включались больные серозным раком яичников с платиночувствительным рецидивом (6 месяцев и более от момента введения последней дозы платиновых производных до первых признаков прогрессирования), которым было проведено лечение рецидива комбинацией с включением платины с эффектом (регрессия опухоли или ее стабилизация). Согласно протоколу в исследование включалась когорта больных с наличием герминальной мутации гена BRCA (кBRCA+), в другую когорту включались больные с отсутствием герминальной мутации гена BRCA (кBRCA-). В последней когорте проводили дополнительный тест на определение дефицита функции гомологичной репарации ДНК (феномен BRCAness). Кроме того, методом секвенирования определяли наличие соматической мутации BRCA в клетках опухоли. Больные в каждой когорте были рандомизированы в соотношении 2:1 в группу нирапариба в дозе 300 мг внутрь ежедневно или в группу плацебо до признаков прогрессирования или непереносимой токсичности. Оценку противоопухолевого эффекта проводили каждые 8 недель, прогрессирование заболевания оценивали по критериям RECIST, повышение только СА-125 без клинических и радиологических симптомов не расценивалось как прогрессирование. Основным критерием эффективности считали медиану времени до прогрессирования, которую оценивали от момента рандомизации (после окончания химиотерапии рецидива) до радиологических признаков прогрессирования. Вторичными критериями были токсичность, продолжительность периода без химиотерапии, общая продолжительность жизни.
Всего в исследование было включено 553 больных: 203 больных в кBRCA+ (из них 138 в группу нирапариба и 65 в группу плацебо) и 350 больных в кBRCA- (из них 234 в группу нирапариба и 116 в группу плацебо). Средний возраст больных в кBRCA+ был 57 лет и 63 года в кBRCA-, в основном это были больные III-IV стадий, с продолжительностью безплатинового интервала более 12 мес. у 60% больных, ранее 40% пациенток получили 3 и более линий химиотерапии.
При медиане наблюдения 17 мес. медиана времени до прогрессирования была достоверно дольше в группе нирапариба во всех когортах (табл. 1). В кBRCA+ медиана составила 21 мес. и 5,5 мес. в группе нирапариба и плацебо, что соответствует достоверному относительному снижению риска прогрессирования на 73%. В группе больных с отсутствием герминальной мутации также отмечен позитивный эффект нирапариба: у этих больных относительный риск прогрессирования уменьшен на 55%. У больных с наличием нарушений гомологичной репарации в опухолевых клеток риск прогрессирования снижен на 62%. В случае, если это нарушение произошло вследствие соматической мутации гена BRCA, медиана времени до прогрессирования составила 20,9 мес. и 11 мес. соответственно. То есть нирапариб демонстрировал одинаково высокую эффективность независимо от характера мутации в гене BRCA (герминальная или соматическая). При подгрупповом анализе во всех изученных группах было показано преимущество нирипариба перед плацебо.
Таблица 1. Медиана времени до прогрессирования в группе нирапариба и плацебо.
| Когорта (число больных) |
Медиана времени до прогрессирования | ||
|---|---|---|---|
| Нирапариб | Плацебо | HR, p | |
| кBRCA+ (n=203) | 21,0 мес. | 5,5 мес. | HR=0,27; p<0,001 |
| кBRCA- (n=350) | 9,3 мес. | 3,9 мес. | HR=0,45; p<0,001 |
| кBRCA- / BRCAness+ (n=162) | 12,9 мес. | 3,8 мес. | HR=0,38; p<0,001 |
| кBRCA- / BRCAness- (n=188) | 6,9 мес. | 3,8 мес. | HR=0,58; p=0,02 |
| Соматическая мутация BRCA (n=47) | 20,9 мес. | 11,0 мес. | HR=0,27; p=0,02 |
Лечение нирапарибом сопровождалось выраженной токсичностью. Частота осложнений 3-4 степени составила 74,1% и 22,9% в группе нирапариба и плацебо. Превалирующей токсичностью 3-4 степени была гематологическая, включая тромбоцитопению (61,3% больных), анемию (50,1%) и нейтропению (30,2%). Прекращение терапии в связи с токсичностью потребовалось у 14,7% больных в группе нирапариба и у 2,2% в группе плацебо. У большинства больных в группе нирапариба потребовалось снижение дозы препарата, после чего проявления гематологической токсичности были редкими.
Таким образом, результаты исследования продемонстрировали высокую эффективность нирапариба в качестве поддерживающей терапии у больных низкодифференцированным серозным раком яичников, сохраняющим чувствительность к платине. Важным достоинством проведенного лечения была оценка эффективности нирапариба в зависимости от наличия или отсутствия герминальной мутации гена BRCA. Результаты достоверно свидетельствуют, что нирапариб увеличивает время до прогрессирования независимо от наличия герминальной мутации BRCA. Наибольший выигрыш от поддержки нирапариба получают больные с наличием герминальной и соматической мутации BRCA, а также больные с другими механизмами нарушения гомологичной репарации ДНК. Однако и больные с отсутствием нарушений гомологичной репарации в опухолевых клетках демонстрировали снижение относительного риска прогрессирования на 42% в группе нирапариба в сравнении с плацебо. Таким образом, хотя определение наличия герминальной или соматической мутации BRCA и нарушения механизма гомологичной рекомбинации в опухолевых клетках дают важную предсказывающую информацию о величине потенциального выигрыша при назначении нирапариба, эти биомаркеры не обладают достаточной точностью предсказания, кому не показано назначение этого препарата. Нирапариб обладает серьезной гематологической токсичностью, что требует редукции дозы препарата. Необходимо дополнительное время наблюдения для того, чтобы оценить влияние поддерживающей терапии нирапарибом на продолжительность жизни больных серозным раком яичников с платиночувствительным рецидивом заболевания.
Ключевые слова: серозный рак яичников, платиночувствительный рецидив, нирапариб, ингибитор PARP.
Литература:
- Ledermann J, Harter P, Gourley C, et al. Olaparib maintenance therapy in platinum-sensitive relapsed ovarian cancer. N.Engl. J.Med. 2012; 366: 1382-92.
- Mirza MR, Monk BJ, Herrstedt J, et al. Niraparib Maintenance Therapy In Platinum-sensitive, recurrent ovarian cancer. N Engl J Med 2016; 375: 2154-2164.
 |
Способ применения и дозировка Зеюла капсулы 100мгВсегда принимайте препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений посоветуйтесь с лечащим врачом.Поддерживающая терапия рака яичников с положительным эффектом после первого курса химиотерапии, включающей препараты платиныРекомендованная начальная доза составляет 200 мг (2 капсулы по 100 мг) один раз в сутки, независимо от приема пищи. Если до начала лечения Ваша масса тела составляет 77 кг и более, а число тромбоцитов составляет 150 000/мкл и более, рекомендованная начальная доза составляет 300 мг (3 капсулы по 100 мг) один раз в сутки, независимо от приема пищи.Поддерживающая терапия при возобновлении (рецидиве) рака яичниковРекомендованная начальная доза составляет 300 мг (3 капсулы по 100 мг) один раз в сутки, независимо от приема пищи.Принимайте препарат Зеюла каждый день примерно в одно и то же время. Возможен прием препарата Зеюла перед сном, если в другое время после его приема Вы ощущаете тошноту.Ваш врач может рекомендовать Вам другую дозу, если у Вас есть проблемы с печенью.Способ применения:Проглатывайте капсулу препарата Зеюла целиком, запивая водой. Не разжевывайте и не измельчайте капсулы.Ваш врач может рекомендовать Вам уменьшить дозу препарата при появлении у Вас нежелательных реакций (таких как тошнота, утомление, аномальные кровотечения и кровоподтеки, анемия).Ваш врач будет регулярно контролировать Ваше состояние. Не прекращайте применение препарата Зеюла, пока он помогает Вам или пока у Вас не возникнут неприемлемые нежелательные реакции.Не принимайте дополнительную дозу, если Вы пропустили прием препарата или если у Вас возникла рвота после приема препарата Зеюла. Примите Вашу следующую дозу в запланированное время. Не принимайте двойную дозу, чтобы компенсировать пропущенную дозу.При наличии вопросов по применению препарата обратитесь к лечащему врачу. |
 |
Побочное действие Зеюла капсулы 100мгПодобно всем лекарственным препаратам, препарат Зеюла может вызывать нежелательные реакции, однако они возникают не у всех.Немедленно обратитесь к Вашему врачу, если Вы заметите какие-либо из СЕРЬЕЗНЫХ нежелательных реакций, перечисленных ниже, — Вам может потребоваться экстренная медицинская помощь:Очень часто (могут возникать у более чем 1 из 10 человек):Кровоподтеки или кровотечения, которые продолжаются дольше, чем обычно, если Вы поранитесь — это может быть признаками низкого числа тромбоцитов (.тромбоцитопения).Одышка, чувство сильной усталости, бледная кожа или учащенное сердцебиение — это может быть признаками низкого числа эритроцитов {анемия).Повышенная температура или инфекция – низкое число определенного вида белых кровяных клеток — нейтрофилов (иейтропения), может повышать риск развития инфекции. Признаки могут включать повышение температуры, озноб, слабость, спутанность сознания, кашель, боль или жжение во время мочеиспускания. Некоторые инфекции могут быть серьезными и приводить к летальному исходу.Снижение числа лейкоцитов (лейкопения). Низкое число лейкоцитов может снижать способность Вашего организма бороться с инфекциями.Часто (могут возникать не более чем у 1 из 10 человек):Низкое количество клеток крови вследствие проблем с костным мозгом или рака крови, который развивается в костном мозге (МДС или ОМЛ).Аллергические реакции, включая серьезные, представляющие угрозу для жизни). Признаки могут включать зудящие волдыри (крапивницу) или сыпь на коже; припухлости, иногда в области лица или рта (ангионевротический отек); затрудненное дыхание; обморок или потерю сознания.Редко (могут возникать не более чем у 1 из 1000 человек):Внезапное повышение артериального давления, что может представлять собой неотложное состояние, которое может приводить к поражению органов или представлять угрозу для жизни (гипертонический криз).Состояние головного мозга с симптомами, включающими судороги, головную боль, спутанность сознания и нарушения зрения, которое может приводить к поражению органов или представлять угрозу для жизни (синдром задней обратимой энцефалопатии [СЗОЭ]).При приеме препарата Зеюла могут возникать и другие нежелательные реакции (однако они возникают не у всех):Очень часто (могут возникать у более чем 1 из 10 человек):боль в животе,нарушение пищеварения, неприятные ощущения со стороны желудка и кишечника (диспепсия),кашель,болезненное и частое мочеиспускание (инфекция мочевыводящих путей),головная боль,ощущение слабости (астения),упадок сил (утомляемость),головокружение,боль в суставах (артралгия),боль в спине,затрудненная дефекация (запор),тошнота,рвота,частый водянистый стул(диарея),затрудненное дыхание (одышка),насморк или заложенный нос (назофарингит),проблемы со сном (бессонница),снижение аппетита,частое или нерегулярное сердцебиение (пальпитация),высокое артериальное давление (артериальная гипертензия).Часто (могут возникать не более чем у 1 из 10 человек): воспаление глаз (конъюнктивит);сухость во рту;отек голеней и стоп (периферический отек);носовое кровотечение;печальное, подавленное настроение (депрессия);боль в мышцах (миалгия);снижение массы тела;снижение уровня калия в крови (гипокалиемия), которое может приводить к нерегулярному сердцебиению;воспаление или отек дыхательных путей между ртом, носом и легкими (бронхит);болезненность, покраснение ротовой полости (мукозит/стоматит);сыпь на коже;повышение кожной чувствительности к солнечному свету (фоточувствителъностъ);чувство беспокойства, нервозности или тревоги (тревожность);нарушение концентрации, понимания, памяти и мышления (нарушения когнитивной функции);учащенное сердцебиение (тахикардия), которое может вызывать головокружение, боль в груди или одышку;повышение уровня креатинина в крови, которое может быть признаком поражения почек;нетипичный вкус во рту (дисгевзия);вздутие живота;аномально высокое содержание печеночных ферментов в крови, которое может означать, что работа Вашей печени нарушена. Это может вызывать утомление, тошноту и боль в животе. Несмотря на то, что эти изменения обычно имеют легкий характер и обратимы, они также могут быть серьезными и представлять угрозу для жизни. Специфическими ферментами являются: аспартаттрансаминаза (ACT), аланинаминотрансфераза (АЛТ), гамма-глутамилтрансфераза (ГГТ) и/или щелочная фосфатаза (ЩФ).Нечасто (могут возникать не более чем у 1 из 100 человек):спутанность мыслей, сложности в ориентации во времени и пространстве (спутанность сознания);воспаление легких, которое может приводить к одышке и затрудненному дыханию (пневмонит).Сообщите Вашему врачу, если какая-либо из перечисленных выше нежелательных реакций приобрела тяжелый характер или причиняет беспокойство, или если Вы заметили нежелательную реакцию, которая не указана в данном листке-вкладыше.Если у вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую через систему сообщений государств-членов Евразийского экономического союза. Сообщая о нежелательных реакциях, вы помогаете получить больше сведений о безопасности препарата. |
 |
Взаимодействие Зеюла капсулы 100мгСообщите лечащему врачу о том, что Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты.Следующие препараты могут влиять на действие препарата Зеюла и наоборот:препараты, подавляющие иммунную систему — иммунодепрессанты (например, циклоспорин, такролимус);другие препараты для лечения опухолей (например, иринотекан, метотрексат);препараты, применяемые для снижения уровня холестерина (например, розувастатин, симвастатин, аторвастатин);препараты для лечения психических расстройств (например, кветиапин, пимозид, клозапин);алфентанил (обезболивающий препарат);эрготамин (сосудосуживающий препарат, применяется при маточных кровотечениях и мигрени);теофиллин (препарат для лечения бронхиальной астмы);галофантрин (препарат для лечения малярии);ропинирол (препарат для лечения болезни Паркинсона);мегформин (препарат для лечения сахарного диабета).Если Вы планируете вакцинацию, проконсультируйтесь с лечащим врачом. |
 |
Особые указанияПроконсультируйтесь с врачом перед началом лечения или во время лечения препаратом Зеюла, если к Вам может быть применимо что-либо из нижеперечисленного:Препарат Зеюла может снижать количество клеток крови, таких как эритроциты (анемия), лейкоциты (нейтропения) или тромбоциты (тромбоцитопения). Признаки и симптомы, на которые Вам необходимо обращать внимание, включают повышенную температуру, инфекции, аномальные кровоподтеки или кровотечения (см. дополнительную информацию в разделе 4). Ваш врач будет регулярно направлять Вас на анализы крови на протяжении всего курса лечения.В редких случаях низкое число клеток крови может быть признаком более серьезных проблем с костным мозгом, таких как миелодиспластический синдром (МДС) или острый миелоидный лейкоз (ОМЛ). Ваш врач может направить Вас на исследование костного мозга, чтобы проверить наличие таких проблем.Препарат Зеюла может вызывать повышение артериального давления, которое в некоторых случаях может быть тяжелым. Ваш врач будет регулярно измерять Ваше артериальное давление на протяжении всего лечения. Также Ваш врач может назначить Вам препараты для лечения высокого артериального давления и при необходимости скорректировать Вашу дозу препарата Зеюла.При лечении препаратом Зеюла может развиваться редкое неврологическое нежелательное явление под названием «синдром задней обратимой энцефалопатии» (СЗОЭ). Если у Вас появились головная боль, нарушения зрения, спутанность сознания или судороги, с высоким артериальным давлением или без него, обратитесь к Вашему врачу.Не давайте препарат Зеюла детям и подросткам в возрасте до 18 лет. Применение препарата не изучалось у детей и подростков.Препарат Зеюла нельзя принимать во время беременности, поскольку он может нанести вред Вашему ребенку. Если Вы беременны, предполагаете, что беременны, или планируете беременность, перед началом применения препарата проконсультируйтесь с лечащим врачом.Если Вы — женщина, способная забеременеть, Вы должны использовать высокоэффективные средства контрацепции во время лечения препаратом Зеюла, а также продолжать использовать их в течение 6 месяцев после приема последней дозы препарата. Ваш врач попросит Вас подтвердить, что Вы не беременны, сдав тест на беременность перед началом лечения. Немедленно обратитесь к Вашему врачу, если Вы забеременеете во время приема препарата Зеюла.Препарат Зеюла не следует принимать во время грудного вскармливания, поскольку неизвестно, проникает ли он в грудное молоко. Если Вы кормите грудью, прекратите вскармливание до начала приема препарата Зеюла и не возобновляйте в течение 1 месяца после приема последней дозы препарата. Посоветуйтесь с Вашим врачом перед началом лечения данным препаратом.Во время приема препарата Зеюла Вы можете испытывать трудности с концентрацией внимания, чувствовать слабость, усталость или головокружение (см. дополнительную информацию в разделе 4), что может повлиять на Вашу способность управлять транспортными средствами и работать с механизмами. Соблюдайте осторожность во время управления транспортными средствами и работы с механизмами.Если у Вас непереносимость некоторых сахаров, обратитесь к лечащему врачу перед приемом данного лекарственного препарата.Препарат Зеюла содержит тартразин (Е 102)Тартразин может вызывать аллергические реакции. |
From Wikipedia, the free encyclopedia
 |
|
| Clinical data | |
|---|---|
| Pronunciation | nih-RAP-uh-rib |
| Trade names | Zejula |
| Other names | MK-4827 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a617007 |
| License data |
|
| Pregnancy category |
|
| Routes of administration |
By mouth |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | 73% |
| Protein binding | 83% |
| Metabolism | Carboxylesterases |
| Metabolites | M1 (carboxylic acid) |
| Elimination half-life | 36 hours |
| Excretion | 48% urine, 29% feces |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.210.548 |
| Chemical and physical data | |
| Formula | C19H20N4O |
| Molar mass | 320.396 g·mol−1 |
| 3D model (JSmol) |
|
| Solubility in water | 0.7–1.1 |
|
SMILES
|
|
|
InChI
|
Niraparib, sold under the brand name Zejula, is an anti-cancer medication used for the treatment of epithelial ovarian, fallopian tube, or primary peritoneal cancer.[3][4][5] It is taken by mouth.[3][4] It is a PARP inhibitor.
The most common side effects include nausea (feeling sick), thrombocytopenia (low blood platelet counts), tiredness and weakness, anemia (low red blood cell counts), constipation, vomiting, abdominal (belly) pain, neutropenia (low levels of neutrophils, a type of white blood cell), insomnia (difficulty sleeping), headache, lack of appetite, diarrhea, dyspnea (difficulty breathing), hypertension (high blood pressure), back pain, dizziness, cough, joint pain, hot flushes and decrease in white blood cells.[4]
Niraparib was approved for medical use in the United States and in the European Union in 2017.[4][6][7]
Medical uses[edit]
Niraparib is indicated for the maintenance treatment of adults with recurrent epithelial ovarian, fallopian tube, or primary peritoneal cancer who are in complete or partial response to platinum-based chemotherapy.[5]
In October 2019, the indication for niraparib was expanded to include people with advanced ovarian, fallopian tube, or primary peritoneal cancer treated with three or more prior chemotherapy regimens and whose cancer is associated with homologous recombination deficiency (HRD)-positive status.[8] HRD is defined by either a deleterious or suspected deleterious BRCA mutation, or genomic instability in patients with disease progression greater than six months after response to the last platinum-based chemotherapy.[8]
In April 2020, the indication for niraparib was expanded to include the maintenance treatment of adults with advanced epithelial ovarian, fallopian tube, or primary peritoneal cancer who are in a complete or partial response to first-line platinum-based chemotherapy.[9]
In the European Union, niraparib is indicated: as monotherapy for the maintenance treatment of adults with advanced epithelial (FIGO Stages III and IV) high-grade ovarian, fallopian tube or primary peritoneal cancer who are in response (complete or partial) following completion of first-line platinum-based chemotherapy; and as monotherapy for the maintenance treatment of adults with platinum sensitive relapsed high grade serous epithelial ovarian, fallopian tube, or primary peritoneal cancer who are in response (complete or partial) to platinum based chemotherapy.[4]
Contraindications[edit]
No contraindications are listed in the prescribing information.[3]
Side effects[edit]
The most common side effects in studies were low blood cell counts, namely thrombocytopenia (in 61% of patients, severe in 29%), anemia (in 50%, severe in 25%) and neutropenia (in 30%, severe in 20%). Other, mostly mild to moderate side effects included nausea, fatigue, and constipation. In a study running over 250 days (median), 15% of patients had to permanently discontinue niraparib due to adverse effects.[3]
Interactions[edit]
No clinical interaction studies have been performed. The potential for interactions with other drugs is low as niraparib and its main metabolite M1 do not significantly interact with any of the important cytochrome P450 liver enzymes in vitro. Niraparib, but not M1, is transported by P-glycoprotein and BCRP, but does not significantly inhibit them. Neither niraparib nor M1 significantly interact with any of the other important transporter proteins.[3]
Pharmacology[edit]
Mechanism of action[edit]
Niraparib is an inhibitor of the enzymes PARP1 and PARP2.[10]
Pharmacokinetics[edit]
73% of ingested niraparib is absorbed in the gut,[12] and it reaches highest blood plasma concentrations after about three hours, independently of food intake. In the circulation, 83% of the substance are bound to plasma proteins. It is inactivated by carboxylesterases to the main metabolite M1, the carboxylic acid derivative,[11] which is subsequently glucuronidated.[3]
The mean biological half-life is 36 hours. 47.5% of the substance are found in the urine and 38.8% in the feces. Unmetabolised niraparib accounts for 11% in the urine and 19% in the feces.[11]
Chemistry[edit]
The drug is used in form of the salt niraparib tosylate monohydrate, which is white to off-white, non-hygroscopic crystals.[3][10]
Studies[edit]
A 2012 study in a cell line found that PARP inhibitors exhibit cytotoxic effects not based solely on their enzymatic inhibition of PARP, but by their trapping of PARP on damaged DNA, and the strength of this trapping activity was ordered niraparib >> olaparib >> veliparib.[13]
History[edit]
Niraparib was granted fast track designation by the US Food and Drug Administration (FDA), and Tesaro submitted a new drug application in 2016.[14] It was approved on 27 March 2017 in the US,[5] and approved in European Union on 16 November 2017.[15]
In a study with 553 patients, progression-free survival (PFS) for patients with a deleterious or suspected deleterious BRCA mutation in the germline was 21.0 months under niraparib therapy, as compared to 5.5 months under placebo. Patients without such a mutation had a PFS of 9.3 months under niraparib versus 3.9 months under placebo.[5][16]
The US Food and Drug Administration (FDA) granted the application for niraparib fast track, priority review, breakthrough therapy, and orphan drug designations.[5]
References[edit]
- ^ «Summary Basis of Decision (SBD) for Zejula». Health Canada. 23 October 2014. Retrieved 29 May 2022.
- ^ «Zejula 100 mg hard capsules — Summary of Product Characteristics (SmPC)». (emc). Retrieved 17 January 2021.
- ^ a b c d e f g h «Zejula- niraparib capsule». DailyMed. Retrieved 17 January 2021.
- ^ a b c d e f «Zejula EPAR». European Medicines Agency (EMA). 17 September 2018. Retrieved 17 January 2021. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ a b c d e «Niraparib (Zejula)». U.S. Food and Drug Administration (FDA). 30 March 2017.
This article incorporates text from this source, which is in the public domain.
- ^ «FDA approves maintenance treatment for recurrent epithelial ovarian, fallopian tube or primary peritoneal cancers». U.S. Food and Drug Administration (FDA) (Press release). 27 March 2017. Retrieved 17 January 2021.
This article incorporates text from this source, which is in the public domain.
- ^ «Drug Trials Snapshots: Zejula». U.S. Food and Drug Administration (FDA). 27 March 2017. Retrieved 17 January 2021.
This article incorporates text from this source, which is in the public domain.
- ^ a b «FDA approves niraparib for HRD-positive advanced ovarian cancer». U.S. Food and Drug Administration (FDA). 23 October 2019. Retrieved 17 January 2021.
This article incorporates text from this source, which is in the public domain.
- ^ «FDA approves niraparib for first-line maintenance of advanced ovarian». U.S. Food and Drug Administration (FDA). 29 April 2020. Retrieved 17 January 2021.
This article incorporates text from this source, which is in the public domain.
- ^ a b «Niraparib Monograph for Professionals». American Society of Health-System Pharmacists. 22 September 2020. Retrieved 17 January 2021.
- ^ a b c van Andel L, Zhang Z, Lu S, Kansra V, Agarwal S, Hughes L, et al. (December 2017). «14C-niraparib, a novel poly(ADP-Ribose) polymerase (PARP)-1 and PARP-2 inhibitor, in patients with advanced cancer». Investigational New Drugs. 35 (6): 751–765. doi:10.1007/s10637-017-0451-2. PMC 5694528. PMID 28303528.
- ^ van Andel L, Rosing H, Zhang Z, Hughes L, Kansra V, Sanghvi M, et al. (January 2018). «14C-microtracer and therapeutic dose in cancer patients». Cancer Chemotherapy and Pharmacology. 81 (1): 39–46. doi:10.1007/s00280-017-3455-x. PMC 5754411. PMID 29043410.
- ^ Murai J, Huang SY, Das BB, Renaud A, Zhang Y, Doroshow JH, et al. (November 2012). «Trapping of PARP1 and PARP2 by Clinical PARP Inhibitors». Cancer Research. 72 (21): 5588–99. doi:10.1158/0008-5472.CAN-12-2753. PMC 3528345. PMID 23118055.
- ^ «Niraparib Receives FDA Fast Track Designation for the Treatment of Recurrent Platinum-Sensitive Ovarian, Fallopian Tube, or Primary Peritoneal Cancer». The European Society for Medical Oncology (ESMO). 5 September 2016.
- ^ «Zejula». European Medicines Agency. 17 September 2018.
- ^ Adams B (29 June 2016). «Tesaro’s PARP ovarian cancer drug hits PhIII goal; prepares to file». Fierce Biotech.
External links[edit]
- «Niraparib». Drug Information Portal. U.S. National Library of Medicine.
- «Niraparib tosylate». Drug Information Portal. U.S. National Library of Medicine.
- «Niraparib tosylate monohydrate». NCI Drug Dictionary. National Cancer Institute.
- «Niraparib tosylate monohydrate». National Cancer Institute. 14 April 2017.
Ингибиторы PARP — современная группа таргетных противоопухолевых препаратов, которые блокируют ферменты поли(АДФ-рибоза)-полимеразы (poly(ADP-ribose) polymerase, сокращенно PARP). Эти ферменты участвуют в репарации поврежденной ДНК. Под действием ингибиторов PARP этот процесс нарушается, в генах возникают критические повреждения, и опухолевые клетки погибают.
Фактически вещества, обладающие свойствами ингибиторов PARP, были открыты еще в 1971 году. Но они оказались не очень эффективными и вызвали слишком много побочных эффектов. Первый препарат, одобренный американским управлением FDA, вошел в клиническую практику только в 2014 году. В настоящее время ингибиторы PARP применяются для лечения рака яичников и маточных труб, молочной железы, простаты, поджелудочной железы и злокачественных опухолей брюшины. Кроме того, ведутся клинические испытания, чтобы проверить, насколько эти препараты эффективны при других онкологических заболеваниях.
- Какие функции выполняет белок PARP, и почему он важен для раковых клеток?
- Как работают ингибиторы PARP?
- При каких злокачественных опухолях применяют ингибиторы PARP?
- Представители группы
- Возможные побочные эффекты
- Взгляд в будущее: перспективы применения ингибиторов PARP в онкологии
Интеллектуальная собственность https://www.euroonco.ru
Какие функции выполняет белок PARP, и почему он важен для раковых клеток?
PARP — это семейство белков-ферментов, которые выполняют в клетках различные функции. Они участвуют в регуляции преобразовании структуры хромосом, транскрипции (перенос генетической информации с ДНК на РНК, чтобы в дальнейшем синтезировался белок), репликации (удвоении ДНК), рекомбинации (обмен участками ДНК между хромосомами), репарации («починке») поврежденной ДНК. Именно последняя функция в этом списке сильнее всего интересует ученых, которые занимаются разработкой противоопухолевых препаратов.
Семейство PARP включает 18 белков. Лучше всего изучен PARP-1. Впервые упоминания о нем в научной литературе появились еще в 1963 году. В 1980 году ученые предположили, что, влияя на PARP-1, можно повысить эффективность некоторых химиопрепаратов.
Несмотря на то, что ДНК во время деления клеток в теле человека копируется с высокой точностью, периодически возникают ошибки, поломки. На этот случай природой предусмотрены специальные системы репарации поврежденного генетического материала. У человека работает шесть таких систем:
- Эксцизионная репарация оснований (base excision repair, BER) — устранение неправильных отдельных «букв» генетического кода или коротких участков ДНК, состоящих из нескольких букв.
- Эксцизионная репарация нуклеотидов (nucleotide Excision Repair, NER) — исправление более длинных поврежденных участков ДНК. Эта система «вырезает» неправильный участок в одной цепочке ДНК, а затем синтезирует его снова на матрице второй цепочки.
- Репарация однонитевых разрывов (single-strand break repair, SSBR) — «сшивание» ДНК, в одной из двух цепочек которой произошел разрыв.
- Репарация путем гомологичной рекомбинации (homologous recombination, HR) — метод починки ДНК, в которой разорвались обе цепочки. Все хромосомы в клетках человека представлены двумя копиями. Когда в одной из них происходит двухцепочечный разрыв, она использует свою «сестру» как шаблон, чтобы восстановить генетический материал.
- Негомологичное соединение концов (non-homologous end joining, NHEJ) — механизм, который просто соединяет концы ДНК при двухцепочечных разрывах, без гомологичной рекомбинации. Это менее точный метод репарации, после него могут теряться некоторые «буквы» генетического кода, возникать другие нарушения.
- Репарация ошибочно спаренных нуклеотидов (мисмэтч репарация, mismatch repair — MMR) — система, которая находит и устраняет несоответствия в генетическом коде.
Ферменты PARP-1 и PARP-2 играют важную роль в первом из перечисленных путей — эксцизионной репарации оснований. Белок PARP умеет обнаруживать разрыв одной цепочки ДНК, прикрепляется к ней в этом месте и заставляет работать другие ферменты репарации. Но этот процесс требует затрат энергии. Если PARP-1 активируется слишком сильно, например, при выраженных повреждениях ДНК и во время кислородного голодания, то энергетические ресурсы клетки истощаются, и она погибает.
Кроме того, существуют доказательства, что PARP принимают участие в восстановлении ДНК при разрыве обеих ее цепочек.
Как работают ингибиторы PARP?
При раке нередко возникают мутации в генах, которые кодируют белки, отвечающие за репарацию ДНК. Если в раковых клетках перестает работать хотя бы одна из шести систем репарации — эта особенность становится их ахиллесовой пятой. Стоит заблокировать еще один путь репарации с помощью лекарств — и повреждения ДНК достигают критического уровня, опухолевая клетка погибает. На этом и основано применение препаратов из группы ингибиторов PARP.
В 2005 году появились первые сообщения о том, что подавление функции PARP в клетках с мутациями в генах BRCA приводит к их гибели. Гены BRCA1 и BRCA2 кодируют белки, которые играют важную роль в пути репарации ДНК под номером 4 в нашем списке: репарации путем гомологичной рекомбинации. Если в этих генах возникают мутации (они бывают наследственными и приобретенными), то восстановление ДНК нарушается. С одной стороны, из-за этого в нормальной клетке накапливаются мутации, которые могут превратить ее в раковую. В то же время, если в раковых клетках заблокировать еще один путь репарации, то мутации накапливаются еще быстрее и становятся смертельными для клетки.
В настоящее время считается, что ингибиторы PARP работают против рака именно так — подавляют репарацию ДНК. В итоге одноцепочечные разрывы сохраняются, превращаются в двухцепочечные, а они тоже не устраняются, потому что не работает система гомологичной рекомбинации из-за мутации в гене BRCA.
Известны два механизма, с помощью которых могут работать ингибиторы PARP:
- связываются с ферментом PARP и блокируют его активность;
- вмешиваются, когда фермент уже соединился с ДНК, и переводят его в неактивную форму.
При каких злокачественных опухолях применяют ингибиторы PARP?
С появлением ингибиторов PARP наступила новая эра в лечении рецидивирующего и распространенного рака яичников. В первую очередь речь идет о злокачественных опухолях с наследственными и соматическими (приобретенными) мутациями в генах BRCA, так как в них уже есть одна поломка механизмов репарации ДНК.
Также ингибиторы PARP были одобрены и успешно применяются при следующих злокачественных опухолях:
- рак маточных труб;
- первичный рак брюшины;
- рак молочной железы;
- рак предстательной железы.
Представители группы
Олапариб (Линпарза) стал первым препаратом из группы ингибиторов PARP, зарегистрированным в 2014 году американским управлением FDA и Европейским агентством по лекарственным средствам (EMA). Изначально препарат был одобрен для лечения рака яичников с мутациями в генах BRCA. Со временем список показаний к его применению расширился. На данный момент он включает:
- рецидив рака яичников, маточных труб и первичных опухолей брюшины, если до этого наблюдался полный или частичный ответ на лечение химиопрепаратами из группы препаратов платины;
- распространенный рак яичников с мутациями в генах BRCA — в качестве лечения первой линии или после химиотерапии, самостоятельно или в сочетании с другими препаратами (бевацизумаб);
- HER2-отрицательный метастатический рак молочной железы с мутациями в генах BRCA, после курса химиотерапии;
- метастатический рак поджелудочной железы с мутациями в генах BRCA, если до этого как минимум в течение 16 недель заболевание не прогрессировало на фоне химиотерапии;
- кастрационно-резистентный рак предстательной железы с мутациями в генах гомологичной рекомбинации.
Рукапариб (Рубрака) во многом похож на олапариб. FDA разрешило его применение при раке яичников в рамках процедуры ускоренного одобрения лекарственных препаратов в 2016 году. В настоящее время его применяют при распространенном и рецидивирующем эпителиальном раке яичников, маточных труб и первичных злокачественных опухолях брюшины, чувствительных к препаратам платины и несущих мутации в генах BRCA. В 2020 году рукапариб был одобрен для лечения кастрационно-резистентного метастатического рака простаты с мутациями в генах BRCA.
Нирапариб (Зеджула) стал третьим препаратом из группы ингибиторов PARP, одобренных FDA. Он применяется на территории США и Европейского союза с 2017 года. Показанием к применению является лечение распространенного и рецидивирующего рака яичников, маточных труб и первичных опухолей брюшины, чувствительных к препаратам платины.
Талазопариб (Талценна) отличается от всех предыдущих препаратов тем, что он пока еще не одобрен для применения при раке яичников. Его используют при HER2-отрицательном метастатическом и местно-распространенном раке молочной железы с наследственными мутациями в генах BRCA. Талазопариб был одобрен FDA в 2018 году, регулирующими органами Европы — в 2019 году.
Возможные побочные эффекты
Таргетная терапия в целом переносится пациентами лучше, чем классическая химиотерапия. Тем не менее, таргетные препараты, в том числе ингибиторы PARP, тоже могут вызывать некоторые побочные эффекты. Наиболее распространенные из них:
- побочные эффекты, вызванные воздействием на красный костный мозг и уменьшением количества клеток крови: анемия, повышенная уязвимость к инфекциям, повышенная кровоточивость;
- тошнота;
- чувство усталости;
- диарея;
- расстройства пищеварения;
- изменение чувства вкуса;
- головные боли, головокружения;
- нарушение функции печени и почек.
Эти побочные эффекты возникают не у всех пациентов, зачастую они выражены не сильно. Чтобы вовремя обнаружить нарушения и принять необходимые меры, во время курса лечения периодически проводят контрольные обследования, пациентам назначают анализы крови.
Другая проблема — устойчивость злокачественной опухоли к ингибиторам PARP. Это явление возникает при любой противоопухолевой терапии. Препараты в первую очередь уничтожают «слабые» раковые клетки, но «сильные» выживают, в них возникают новые мутации, и со временем лекарство перестает на них действовать. Вопросы устойчивости к ингибиторам PARP в настоящее время активно изучаются. Известно, что опухолевые клетки приспосабливаются выживать в присутствии этих препаратов многими способами. Выделяют два основных механизма (хотя, есть и другие, менее изученные):
- восстановление репарации путем гомологичной рекомбинации, которая была «поломана» в результате мутаций в генах BRCA;
- стабилизация репликационной вилки — участка, в котором две цепочки ДНК рассоединяются, когда происходит ее удвоение.
Так выглядит репликационная вилка. Справа находится исходная часть ДНК. Слева она разделилась на две цепочки, и на каждой из них синтезируется новая цепочка — из них образуются две новые молекулы ДНК. Стабилизации вилки репликации является одним из механизмов устойчивости раковых клеток к ингибиторам PARP.
При запущенном раке лечение ингибиторами PARP проводят до тех пор, пока не разовьется устойчивость, либо пока они не начнут вызывать серьезные побочные эффекты. В настоящее время ученые продолжают изучать механизмы развития резистентности рака к противоопухолевым препаратам, чтобы научиться профилактировать ее и повысить эффективность лечения.
Взгляд в будущее: перспективы применения ингибиторов PARP в онкологии
В настоящее время проводятся клинические исследования, в которых изучают эффективность ингибиторов PARP при раке легкого, поджелудочной железы, головы и шеи, желудка и пищевода, шейки матки, почек, мочевого пузыря, некоторых опухолях головного мозга. Кроме того, ведутся разработки новых препаратов из этой группы, некоторые из них уже завершили тестирование на животных и перешли на стадию клинических испытаний. Изучается эффективность и безопасность применения ингибиторов PARP в сочетании с химиопрепаратами, иммунопрепаратами.
Врачи федеральной сети клиник экспертной онкологии «Евроонко» постоянно отслеживают ход клинических испытаний. Мы оперативно узнаём о регистрации в России новых противоопухолевых препаратов, расширении показаний к применению уже зарегистрированных. В наших клиниках пациенты могут получить лечение всеми оригинальными противоопухолевыми препаратами новейших поколений в соответствии с актуальными версиями международных протоколов, рекомендациями авторитетных онкологических сообществ.
Список литературы:
- Feiyue Zheng, Yi Zhang, Shuang Chenc, Xiang Weng, Yuefeng Rao, Hongmei Fang. Mechanism and current progress of Poly ADP-ribose polymerase (PARP) inhibitors in the treatment of ovarian cancer. Biomedicine & Pharmacotherapy, Volume 123, March 2020, 109661.
- Alice Chen. PARP inhibitors: its role in treatment of cancer. Chin J Cancer. 2011 Jul; 30(7): 463–471.
- Julio C. Morales, Longshan Li, Farjana J. Fattah, Ying Dong, Erik A. Bey, Malina Patel, Jinming Gao, and David A. Boothman. Review of Poly (ADP-ribose) Polymerase (PARP) Mechanisms of Action and Rationale for Targeting in Cancer and Other Diseases.
- Esha Sachdev, Roya Tabatabai, Varun Roy, B J Rimel, Monica M Mita. PARP Inhibition in Cancer: An Update on Clinical Development. Target Oncol. 2019 Dec;14(6):657-679. doi: 10.1007/s11523-019-00680-2.
- Ming Yi, Bing Dong, Shuang Qin, Qian Chu, Kongming Wu & Suxia Luo. Advances and perspectives of PARP inhibitors.
- Румянцев А. А. Эволюция ингибиторов PARP: на какой ступени мы стоим? RosOncoWeb, новости онкологии.
- PARP inhibitors. Cancer Research UK.
- Guo-Min Li. Mechanisms and functions of DNA mismatch repair. Cell Res 18, 85–98 (2008). https://doi.org/10.1038/cr.2007.115
- olaparib (Rx). Medscape.
- ИНСТРУКЦИЯ по медицинскому применению лекарственного препарата Линпарза. АстраЗенека.
- Препарат олапариб зарегистрирован в США для лечения метастатического кастрационно-резистентного рака предстательной железы с мутацией в генах гомологичной рекомбинации. AstraZeneca.
- ЛИНПАРЗА (ОЛАПАРИБ) ОДОБРЕНА ДЛЯ ЛЕЧЕНИЯ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ С МУТАЦИЕЙ BRCA1/2. Качественная клиническая практика.
- rucaparib (Rx). Medscape.
- Rucaparib. U. S. Food & Drug Administration.
- With Two FDA Approvals, Prostate Cancer Treatment Enters the PARP Era. National Cancer Institute.
- niraparib (Rx). Medscape.
- FDA approves niraparib for first-line maintenance of advanced ovarian cancer. U. S. Food & Drug Administration.
- FDA approves talazoparib for gBRCAm HER2-negative locally advanced or metastatic breast cancer. U. S. Food & Drug Administration.