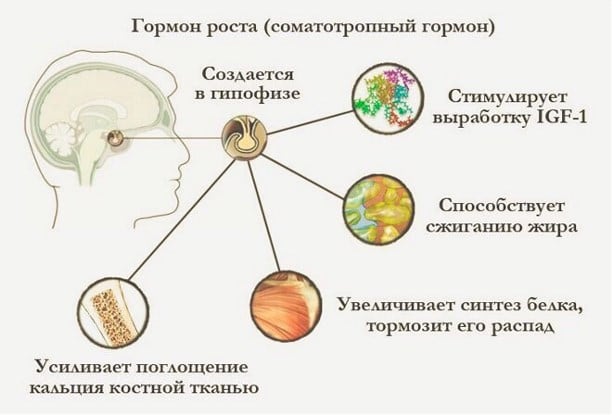
Применение препаратов гормона роста (ГР) в терапевтических алгоритмах заболеваний, сопровождающихся нарушениями динамики ростовых показателей, сегодня обусловлено широкой доступностью несмотря на высокую стоимость. Рекомбинантный человеческий ГР, полученный биосинтетическим путем, используют в педиатрической практике как средство стимуляции роста, так и как метаболический регулятор нарушенных обменных процессов начиная с 1985 г. Вместе с тем препараты соматропина (МНН препаратов гормона роста) имеют определенные показания с доказанной эффективностью. Основным показанием к назначению соматропина является гипопитуитаризм. Именно лечение недостаточности ГР при гипопитуитаризме препаратами соматропина является патогенетически обоснованным и проводится с заместительной целью.
Применение ГР при других вариантах низкорослости возможно, но прогностически непредсказуемо. К настоящему времени имеются данные об эффективности лечения ГР детей с внутриутробной задержкой роста, семейной низкорослостью, синдромами Шерешевского–Тернера, Прадера–Вилли, Рассела–Сильвера, анемией Фанкони, гликогенозом, хронической почечной недостаточностью, скелетными дисплазиями, муковисцидозом [1].
С 2003 г. в США используют биосинтетический ГР для лечения детей с идиопатической низкорослостью. Возраст в начале терапии ГР и ответ на терапию ГР в первый год лечения являются основными факторами, определяющими конечный рост при идиопатической низкорослости. Предполагалось, что дети с хорошим ростовым ответом в первый год лечения ГР при идиопатической низкорослости скорее всего будут иметь хороший конечный рост при использовании даже низких доз ГР [2]. Однако результаты наблюдения показали, что индивидуальный эффект терапии остается сложным для предсказания. Большая вариабельность ауксиологических данных, возраст, показатели роста и костного возраста на момент начала терапии, скорость роста в первый год лечения определяют многофакторный анализ, сложный для прогнозирования.
Достаточно сложно прогнозировать ответ на лечение ГР также и при заместительной терапии. Оценка эффективности лечения ГР при соматотропной недостаточности по ауксиологическим параметрам показала, что ростовой ответ является переменным и различен в каждом конкретном случае [3]. Характерной особенностью терапии соматотропной недостаточности является то, что по данным наблюдений за терапией пациентов результат первого года лечения выше, чем в последующие годы. При этом отмечено, что единственным клинически значимым предиктором ответа роста на начало лечения в первый год является возраст начала терапии. Тогда как ни пик ГР при проведении стимуляционных тестов, ни пол, ни рост на момент начала терапии, индекс массы тела (ИМТ), костный возраст, доза ГР не влияют на скорость роста в первый год терапии. Более ранняя диагностика и лечение ГР позволяют достичь лучшего конечного роста в тяжелых случаях недостаточности ГР. Показано, что лучший ответ на лечение отмечался у детей с тяжелой степенью недостаточности ГР [4]. Но, по другим данным, конечный рост не имеет существенных различий у пациентов с тяжелым дефицитом ГР и пациентов с парциальным дефицитом ГР [5].
Рядом исследований было показано, что рост родителей является одним из показателей, который позволяет прогнозировать конечный рост у пациентов с дефицитом ГР, получающих заместительную терапию ГР. Было отмечено, что лечение ГР имеет лучшую эффективность у пациентов, в семьях которых не было родственников с низкорослостью [6].
Хотя лечение препаратами ГР не всегда сопровождается достижением генетически детерминированного роста, увеличение роста в первый год лечения в возрасте до начала полового развития коррелирует с общей прибавкой в росте при терапии. Это подтверждает важность начала лечения до начала пубертата [7].
В настоящее время ведется ряд исследований, с помощью которых подбирается необходимое сочетание лекарственных препаратов, комбинация с которыми ГР улучшит результаты лечения. Так, было показано, что одновременное назначение при врожденном дефиците ГР заместительной терапии ГР и агониста гонадолиберина с целью торможения инициации полового развития не имеет преимуществ перед назначением только ГР [8].
Ростовые эффекты ГР при соматотропной недостаточности у пациентов и с изолированным дефицитом ГР, и у пациентов с множественной недостаточностью гормонов гипофиза выражены с одинаковой степенью: 89% пациентов с изолированной недостаточностью ГР и 81% пациентов при множественном дефиците гормонов гипофиза достигают прогнозируемого роста. Причем бо?льшая прибавка в росте наблюдается в возрасте до начала пубертата [9].
Многолетний опыт лечения препаратами ГР показал, что лечение детей с низкорослостью с использованием дозы соматропина, рассчитанной на массу тела ребенка, сопровождается большой вариабельностью в ростовом ответе на терапию ГР. Вопрос, почему дети с недостаточностью ГР, терапия которых направлена на простое замещение недостающего ГР, имеют такие различные клинические исходы, до настоящего времени не решен.
Ведутся исследования, направленные на поиск фармакогеномных маркеров с прогностической значимостью чувствительности клеток к ГР.
Изучено изменение уровня инсулиноподобного фактора роста 1 (ИФР-1) после 1 месяца лечения ГР у детей с недостаточностью ГР и доказано, что имеется зависимость между полиморфизмом клеточного регулятора CDK4 и степенью изменения концентрации ИФР-1. Дальнейшее изучение взаимосвязи геномных маркеров и ранних изменений уровня ИФР-1 может позволить разработать стратегию быстрого индивидуального подбора дозы ГР при врожденной соматотропной недостаточности [10].
Также на конечный рост пациентов, получающих лечение ГР, оказывает влияние наличие или отсутствие полиморфизма SOCS2 (rs3782415). Полиморфизм, выявляемый в GHR, IGFBP3 и SOCS2 локусах, влияет на результаты роста пациентов с врожденной соматотропной недостаточностью, получающих ГР. Использование этих генетических маркеров может определить пациентов, генетически предрасположенных к менее результативному лечению [11].
Конечным результатом подобных исследований должно стать признание важности индивидуального дозирования ГР для каждого пациента на основе конкретных индивидуальных геномных характеристик. Это позволит значительно улучшить терапию, которая в течение долгих лет базируется на принципе «одна дозировка подходит всем».
Насколько терапевтическая эффективность соматропина сопоставима с его безопасностью — вопрос, требующий глубокого детального анализа, решение которого возможно путем накопления опыта применения ГР при лечении различных форм низкорослости.
Безопасность во время лечения и неблагоприятные эффекты лечения ГР тщательно отслеживаются и описываются у детей с дефицитом ГР (как с изолированной, так и с множественной недостаточностью гормонов аденогипофиза) и у детей с идиопатической низкорослостью [12]. Согласно имеющейся информации, полученной в основном из постмаркетинговых исследований, поддерживаемых производителями препаратов ГР, имеется низкая частота (менее 3% пролеченных детей) побочных эффектов и увеличение благоприятного профиля безопасности ГР. Тем не менее, полный спектр потенциальных побочных эффектов ГР не точно диагностируется при помощи постмаркетинговых исследований. Это связано с достаточно длительным сроком лечения, меняющимися в динамике характеристиками больного и невозможностью отследить нежелательные явления после окончания лечения пациента [13–15].
Редко возникающим нежелательным явлением при лечении ГР является внутричерепная гипертензия. Более высокий риск ее развития отмечен в группах больных с хронической почечной недостаточностью, синдромом Шерешевского–Тернера и с органическими причинами дефицита ГР. Внутричерепная гипертензия обычно развивается в начальном периоде лечения или при увеличении дозы препаратов соматропина, прекращается с окончанием терапии ГР. Показанием для проведения фундоскопии офтальмологом являются симптомы, указывающие на внутричерепную гипертензию, такие как сильная головная боль, двоение/нечеткое зрение и рвота. Лечение часто может быть возобновлено при более низких дозах ГР без возврата симптомов.
К осложнениям терапии соматропином относят изменения в костной системе — эпифизеолиз и сколиоз. Эпифизеолиз диагностируется с частотой 73 на 100 000 лет лечения и встречается реже у больных с изолированным дефицитом ГР и идиопатической низкорослостью по сравнению с теми пациентами, у которых дефицит ГР наблюдается вследствие внутричерепных новообразований, краниофарингеомы [16]. Средняя продолжительность от начала терапии ГР до появления эпифизеолиза колеблется от 0,4 до 2,5 лет. Рекомендовано регулярное наблюдение за появлением соответствующих симптомов, таких как боли в бедре и/или боли в колене, изменения в походке, в случае положительного результата — тщательное обследование и консультация ортопеда. Эпифизеолиз требует хирургического вмешательства на эпифизе бедренной кости.
Сколиоз прогрессирует во время лечения ГР из-за быстрого роста, а не является прямым побочным эффектом ГР. Наиболее часто сколиоз развивается при лечении синдромальных форм низкорослости (например, при синдроме Шерешевского–Тернера и синдроме Прадера–Вилли) [17]. У 0,2% детей с идиопатической низкорослостью или с изолированным дефицитом ГР, получавших ГР, отмечено прогрессирование сколиоза [18]. Регулярное обследование на предмет наличия или прогрессирования сколиоза рекомендуется всем пациентам, получающим препараты ГР.
Данные научных публикаций и собственный практический клинический опыт свидетельствуют о необходимости мониторинга показателей метаболизма глюкозы у пациентов, получающих ГР. Это связано с доказанным фактом наличия резистентности к инсулину при лечении препаратами соматропина. Заболеваемость сахарным диабетом (СД) 1-го типа не увеличивается при терапии ГР. Вместе с тем известно, что больные с синдромом Шерешевского–Тернера, Прадера–Вилли имеют высокий риск развития неиммунных форм сахарного диабета. Снижение чувствительности к инсулину и компенсаторное увеличение секреции инсулина с обеспечением эугликемии сопровождается нарушением толерантности к глюкозе и требует коррекции метаболических нарушений, а в ряде случаев отмены препаратов ГР [19]. Мониторинг потенциального развития сахарного диабета с тестированием крови на уровень глюкозы и/или HbA1c должен быть включен в алгоритм наблюдения за всеми пациентами, получающими препараты ГР.
Патофизиологические и эпидемиологические наблюдения позволяют выразить опасение, что ГР может увеличить риск развития злокачественной опухоли во время или после терапии. Известно, что реализация ростового эффекта ГР опосредована соматомединами, один из которых ИФР-1. ИФР-1 и ГР относятся к веществам с митогенной и антиапоптозной активностью, и их рецепторы обнаружены в опухолях. Состояния нарушенной и избыточной секреции/действия ГР ассоциированы со снижением и повышением риска злокачественности соответственно. Снижение ИФР-1 через ограничение калорийности индуцирует апоптоз и предотвращает или замедляет рост опухоли [20–22]. Некоторые немногочисленные эпидемиологические исследования соотносят увеличение ГР и уровни ИФР-1 с опухолями толстой кишки, молочной железы, щитовидной железы и раком предстательной железы у взрослых [23]. В целом данные литературы указывают на разрешающую/факультативную, а не причинную роль ГР в онкогенезе.
Заболеваемость впервые выявленными во время лечения лейкемией или злокачественными новообразованиями в целом после лечения у детей без сопутствующих факторов риска не увеличивается по сравнению с таковой в общей популяции. Несмотря на данные об отсутствии влияния ГР на появление второго новообразования у детей, в анамнезе которых была неоплазия [24, 25], пункт о повышенном риске развития второго новообразования у пациентов, получавших ГР, в настоящее время присутствует в инструкции по применению на всех препаратах ГР в США. Отсутствуют данные относительно эффектов ГР на риск развития неоплазии у больных с заболеваниями, которые сами отнесены в группу повышенного риска возникновения новообразований. Риск новообразований у пациентов, получающих лечение ГР, был рассмотрен Комитетом по лекарственным средствам и терапии Общества детских эндокринологов, и ключевой рекомендацией является необходимость продолжающегося наблюдения всех пациентов, получавших лечение ГР, и это имеет первостепенное значение [26].
Перед началом терапии ребенка препаратами гормона роста его родители должны быть информированы о неопределенности в отношении долгосрочной безопасности (о неблагоприятных эффектах после терапии в зрелом возрасте).
Долгосрочные исследования (в среднем 17 лет) по наблюдению 6928 детей с изолированной соматотропной недостаточностью идиопатической низкорослостью, или низким гестационным возрастом, которые начали лечение ГР в период между 1985 и 1996 гг., во Франции показали 30%-й рост общей смертности по сравнению с населением в целом [27]. Все виды смертности, связанной с раком, не были увеличены, но стандартизованные показатели смертности были повышены в группах больных с опухолями костной системы, больных с нарушениями в системе кровообращения и больных с кровоизлиянием в мозг. Применение дозы препаратов ГР более 50 мкг/кг/день не рекомендовано. Полученные из той же базы данные в недавнем исследовании показали значительно более высокий риск развития инсульта (особенно геморрагического инсульта) среди пациентов, получавших ГР в детстве [28]. В противоположность этому последующее наблюдение 2543 пациентов с изолированной соматотропной недостаточностью, идиопатической низкорослостью или низким гестационным возрастом из других европейских стран не выявили никакого эффекта воздействия ГР и/или дозы на смертность или частоту развития сердечно-сосудистых событий [29].
Таким образом, имеющиеся данные относительно безопасности терапии ГР для детей с различными формами низкорослости определяют необходимость формирования персонализированного алгоритма диспансерного наблюдения пациента и должны включать информирование родителей ребенка об имеющихся сегодня сведениях о нежелательных явлениях как во время лечения, так и в отдаленные периоды жизни.
Применение высоких доз препаратов гормона роста при синдромальных формах низкорослости должно иметь взвешенный подход к сопоставлению показателей эффективности и безопасности лечения. Увеличение дозы ГР определяет рост шансов, отдаленных метаболических или злокачественных рисков, не обнаруженных в ходе проведенных на сегодняшний день исследований. Изменение характеристик пациентов, этнических особенностей и рост уровня ожирения в детстве может увеличить риск развития СД 2-го типа у получающих ГР.
Определенные побочные эффекты препаратов ГР, связанные с ускоренным ростом (прогрессирование сколиоза и эпифизеолиз) и другими неизвестными механизмами (внутричерепная гипертензия), встречаются редко, однако требуют упреждающего разъяснения и тщательного контроля.
Кроме того, следует помнить об отдаленных последствиях гормонального лечения. Поскольку исследования населения, не получающего ГР, свидетельствуют о том, что высокие нормальные уровни свободного ИФР-1 (часто выявляемые у детей, получавших ГР) могут увеличить риски онкологических заболеваний, потенциальные связи между воздействием ГР и будущими рисками возникновения неоплазии требуют постоянного контроля. И, наконец, соответствующий уровень допустимого риска для новейшей и потенциально самой большой группы пациентов, получавших ГР, — практически здоровых, но низкорослых детей — еще предстоит определить [30].
Литературы
- Петеркова В. А. Гипофизарная карликовость: диагностика и лечение // Педиатрия. 2009. № 87 (02). С. 104–110.
- Ranke M. B., Lindberg A., Price D. A. et al. KIGS International Board. Age at growth hormone therapy start and first-year responsiveness to growth hormone are major determinants of height outcome in idiopathic short stature // Horm Res. 2007. № 68 (2). Р. 53–62.
- Kelnar C. J. Growth hormone for short children — whom should we be treating and why? // J R Coll Physicians Edinb. 2012. № 42 (1). Р. 32–33.
- Ranke M. B., Lindberg A. KIGS International Board. Observed and predicted growth responses in prepubertal children with growth disorders: guidance of growth hormone treatment by empirical variables // J Clin Endocrinol Metab. 2010. № 95 (3). Р. 1229–1237.
- Cardoso D. F., Martinelli C. E. Jr, Campos V. C. et al. Comparison between the growth response to growth hormone (GH) therapy in children with partial GH insensitivity or mild GH deficiency // Arq Bras Endocrinol Metabol. 2014. № 58 (1). Р. 23–29.
- Hilczer M., Smyczynska J., Lewinski A. Parentally-adjusted deficit of height as a prognostic factor of the effectiveness of growth hormone (GH) therapy in children with GH deficiency // Neuro Endocrinol Lett. 2006. № 27 (1–2). Р. 149–152.
- Reiter E. O., Price D. A., Wilton P. et al. Effect of growth hormone (GH) treatment on the near-final height of 1258 patients with idiopathic GH deficiency: analysis of a large international database // J Clin Endocrinol Metab. 2006. № 91 (6). Р. 2047–2054.
- Colmenares A., González L., Gunczler P., Lanes R. Is the growth outcome of children with idiopathic short stature and isolated growth hormone deficiency following treatment with growth hormone and a luteinizing hormone-releasing hormone agonist superior to that obtained by GH alone? // J Pediatr Endocrinol Metab. 2012. № 25 (7–8). Р. 651–657.
- Darendeliler F., Lindberg A., Wilton P. Response to growth hormone treatment in isolated growth hormone deficiency versus multiple pituitary hormone deficiency // Horm Res Paediatr. 2011. № 76. Suppl 1. Р. 42–46.
- Stevens A., Clayton P., Tatò L. et al. Pharmacogenomics of insulin-like growth factor-I generation during GH treatment in children with GH deficiency or Turner syndrome // Pharmacogenomics J. 2014. № 14 (1). Р. 54–62.
- Braz A. F., Costalonga E. F., Trarbach E. B. Genetic predictors of long-term response to growth hormone (GH) therapy in children with GH deficiency and Turner syndrome: the influence of a SOCS2 polymorphism // J Clin Endocrinol Metab. 2014. № 99 (9). Р. 1808–1813.
- Wilson T. A., Rose S. R., Cohen P. et al. Update of guidelines for the use of growth hormone in children: The Lawson Wilkins Pediatric Endocrinology Society Drug and Therapeutics Committee // J Pediatr. 2003. № 143. Р. 415–421.
- Bell J., Parker K. L., Swinford R. D. et al. Long-term safety of recombinant human growth hormone in children // J Clin Endocrinol Metab. 2010. № 95. Р. 167–177.
- Darendeliler F., Karagiannis G., Wilton P. Headache, idiopathic intracranial hypertension and slipped capital femoral epiphysis during growth hormone treatment: a safety update from the KIGS database // Horm Res. 2007. № 68. Suppl 5. P. 41–47.
- Grimberg А., DiVall S., Polychronakos C. et al. Guidelines for Growth Hormone and Insulin-Like Growth Factor-I Treatment in Children and Adolescents: Growth Hormone Deficiency, Idiopathic Short Stature, and Primary Insulin-Like Growth Factor-I Deficiency // Horm Res Paediatr. 2016. № 86. Р. 361–397.
- Mostoufi-Moab S., Isaacoff E. J., Spiegel D. et al. Childhood cancer survivors exposed to total body irradiation are at significant risk for slipped capital femoral epiphysis during recombinant growth hormone therapy // Pediatr Blood Cancer. 2013. № 60. Р. 1766–1771.
- Kim J. Y., Rosenfeld S. R., Keyak J. H. Increased prevalence of scoliosis in Turner syndrome // J Pediatr Orthop. 2001. № 21. Р. 765–766.
- Cohen P., Bright G. M., Rogol A. D. et al. Effects of dose and gender on the growth and growth factor response to GH in GH-deficient children: implications for efficacy and safety // J Clin Endocrinol Metab. 2002. № 87. Р. 90–98.
- Bareille P., Azcona C., Matthews D. R. et al. Lipid profile, glucose tolerance and insulin sensitivity after more than four years of growth hormone therapy in non-growth hormone deficient adolescents // Clin Endocrinol (Oxf). 1999. № 51. Р. 347–353.
- Aguiar-Oliveira M., Oliveira F. T., Pereira R. M. et al. Longevity in untreated congenital growth hormone deficiency due to a homozygous mutation in the GHRH receptor gene // J Clin Endocrinol Metab. 2010. № 95. Р. 714–721.
- Orme S. M., McNally R. J. Q., Cartwright R. A., Belchetz P. E. For the United Kingdom Acromegaly Study Group: Mortality and cancer incidence in acromegaly: a retrospective cohort study // J Clin Endocrinol Metab. 1998. № 83. Р. 2730–2734.
- Speakman J. R., Mitchell S. E. Caloric restriction // Mol Aspects Med. 2011. № 32. Р. 159–221.
- Cohen P., Clemmons D. R., Rosenfeld R. G. Does the GH-IGF axis play a role in cancer pathogenesis? // Growth Horm IGF Res. 2000. № 10. Р. 297–305.
- Wilton P., Mattsson A. F., Darendeliler F. Growth hormone treatment in children is not associated with an increase in the incidence of cancer: experience from KIGS (Pfizer International Growth Database) // J Pediatr. 2010. № 157. Р. 265–270.
- Mackenzie S., Craven T., Gattamaneni H. R. et al. Longterm safety of growth hormone replacement after CNS irradiation // J Clin Endocrinol Metab. 2011. № 96. Р. 2756–2761.
- Raman S., Grimberg A., Waguespack S. G. et al. Risk of neoplasia in pediatric patients receiving growth hormone therapy — a report from the Pediatric Endocrine Society Drug and Therapeutics Committee // J Clin Endocrinol Metab. 2015. № 100. Р. 2192–2203.
- Carel J. C., Ecosse E., Landier F. et al. Long-term mortality after recombinant growth hormone treatment for isolated growth hormone deficiency or childhood short stature: preliminary report of the French SAGhE study // J Clin Endocrinol Metab. 2012. № 97. Р. 416–425.
- Poidvin A., Touze E., Ecosse E. et al. Growth hormone treatment for childhood short stature and risk of stroke in early adulthood // Neurology. 2014. № 83. Р. 780–786.
- Savendahl L., Maes M., Albertsson-Wikland K. et al. Long-term mortality and causes of death in isolated GHD, ISS, and SGA patients treated with recombinant growth hormone during childhood in Belgium, The Netherlands, and Sweden: preliminary report of 3 countries participating in the EU SAGhE study // J Clin Endocrinol Metab. 2012. № 97. Р. 213–217.
- Allen D. B. Growth hormone therapy for short stature: is the benefit worth the burden? // Pediatrics. 2006. № 118. Р. 343–348.
Е. Б. Башнина, доктор медицинских наук, профессор
О. С. Берсенева1
ФГБОУ ВО СЗГМУ им. И. И. Мечникова МЗ РФ, Санкт-Петербург
1 Контактная информация: o.berseneva@mail.ru
Рост, ростовые факторы и применение рекомбинантного человеческого гормона роста у детей с хронической почечной недостаточностью
М.В. Кварацхелия
Growth, growth factors, and the use of recombinant human growth hormone in children with chronic renal failure
M.V. Kvaratskhelia
Эндокринологический научный центр Росмедтехнологий; Детская городская больница святого Владимира, Москва
Отставание в росте с нарушением созревания скелета и задержка полового развития являются частыми и серьезными последствиями хронической почечной недостаточности у детей. Представлены сведения литературы о патогенезе нарушений роста у таких детей; основной причиной считается нарушение оси гормон роста — инсулиноподобный фактор роста-1. Лечение низкорослых детей с уремией рекомбинантным человеческим гормоном роста в супрафизиологических дозах (4 ЕД/м2 в сутки) вызывает существенное улучшение роста без ускорения костного созревания. Хотя безопасность и эффективность лечения продемонстрирована множеством клинических исследований, частота использования препарата остается низкой у данной категории больных.
Ключевые слова: дети, хроническая почечная недостаточность, задержка роста, инсулиноподобный фактор роста-1, рекомбинантный человеческий гормон роста.
Growth retardation with impaired skeletal maturation, and well as arrested sexual development are frequent and serious sequels of chronic renal failure (CRF) in children. The paper presents the data available in the literature on the pathogenesis of growth disorders in these children; their principal cause is considered to be the impaired growth hormone-insulin-like growth factor-1 axis. Treatment of short children with uremia, by using recombinant human growth hormone in supraphysiological doses (4 U/m2/day), causes a significant growth improvement, without accelerating bone maturation. Although the safety and efficiency of the treatment have been demonstrated by numerous clinical studies, the usage of the drug remains low in this group of patients.
Key words: children, chronic renal failure, growth retardation, insulin-like growth factor-1, recombinant human growth hormone.
Отставание в росте с нарушением созревания скелета и задержка полового развития являются частыми и серьезными последствиями хронической почечной недостаточности у детей. Нередко малые размеры больного ребенка могут являться препятствием при трансплантации почки. Задержка роста у ребенка может быть единственной жалобой, приводящей к диагностике хронической почечной недостаточности. Психологические последствия низкорослости оказывают негативное влияние на социальную интеграцию детей и подростков, ведут к ограничению профессионального потенциала.
Выраженность задержки роста имеет тенденцию к пропорциональной зависимости от снижения скорости клубочковой фильтрации. Ранний возраст развития хронической почечной недостаточности ассоциирован с более выраженным
© М.В. Кварацхелия, 2008
Ros Vestn Perinatal Pediat 2008; 2:84-92
Адрес для корреспонденции: 117036 Москва, ул. Дм. Ульянова, д. 11
дефицитом длины тела. При врожденной хронической почечной недостаточности заметная задержка роста может наблюдаться в течение первых 2 лет жизни. Отставание в росте у детей, нуждающихся в диализе, является более выраженным, чем на более ранних стадиях хронической почечной недостаточности или после трансплантации. По данным Европейской ассоциации по диализу и трансплантации (EDTA), уменьшение конечного роста (рост ниже 3-й перцентили) отмечено более чем у половины молодых людей в возрасте 21 года и старше с терминальной стадией хронической почечной недостаточности, получавших диализное лечение до 15-летнего возраста. Анализ данных NAPRTCS (североамериканское исследование по вопросам трансплантации почек у детей) о 2329 детях с терминальной хронической почечной недостаточностью (перед началом диализной терапии) выявил среднее стандартное отклонение роста (SDS) —2,54, —1,95 и—1,67 у детей в возрасте от 0 до 1 года, от 2 до 5 лет и от 6 до 12 лет соответственно. По данным литературы, дефицит конечного роста
МЕНЯЕТ ЖИЗНЬ К ЛУЧШЕМУ!
Нордитропин®НордиЛет®10 мг
• Единственный жидкий гормон роста в одноразовой шприц-ручке
• Не нужно смешивать
• Не нужно вставлять картридж
• Не нужно хранить в холодильнике при использовании
нордитропин нордилет
На правах рекламы
©Представительство компании Ново Нордиск А/С ж Россия, 119330, Москва,
Ломоносовский проспект 38, оф. 11 Тел. +7 (495) 95611 32, факс +7 (495) 956 5013 / IУ В ® www.novonordisk.ru
ПОУО ПОГСЛБК www.novonordisk.com
(рост меньше —2 SDS) было отмечено у 45% из 60 больных (в возрасте от 21 года до 36 лет), у которых хроническая почечная недостаточность развилась до 16-летнего возраста [1—3].
Хотя после трансплантации почки скорость роста детей увеличивается, тем не менее у большинства из них стандартное отклонение роста не увеличивается. Отрицательно влиять на рост после трансплантации может как снижение скорости клубочковой фильтрации, так и использование стероидов в комплексной иммуносупрессивной терапии [1, 2]. Недостаточная динамика роста у детей с хронической почечной недостаточностью корреляционно связана с увеличением заболеваемости и смертности. В исследовании, проводимом в группе детей, получавших заместительную почечную терапию (гемодиализ, перитонеальный диализ), отставание в росте на 1 SDS соответствовало увеличению смертности на 14% [4]. У детей на диализе или после трансплантации, имеющих умеренную или выраженную задержку роста, было отмечено увеличение риска госпитализации и смертности [5, 6].
Патогенез нарушений роста при хронической почечной недостаточности является комплексным. Степень низкорослости зависит от характера первичного поражения почек, длительности и выраженности хронической почечной недостаточности, степени белково-энергетической недостаточности, наличия ацидоза, почечной остео-дистрофии, анемии, гормональных нарушений, характера терапии (применение глюкокортикои-дов). В разные возрастные периоды у детей с хронической почечной недостаточностью в патофизиологию роста вовлечены различные гормоны: паратиреоидный гормон и кальцитриол, лютеи-низирующий, фолликулостимулирующий, половые гормоны, гормон роста и инсулиноподобный фактор роста-1. Основной причиной задержки роста при хронической почечной недостаточности считается нарушение оси гормон роста — инсули-ноподобный фактор роста-1 [7].
Нутритивные факторы оказывают особенное влияние на рост в течение первого года жизни. Часто у детей младшего возраста с почечной недостаточностью в наиболее интенсивной для них фазе роста отмечается снижение потребности в пище, а рвота, ацидоз и дегидратация осложняют проблемы, связанные с питанием. В таких ситуациях только при адекватной белково-энергетической поддержке удается избежать задержки физического развития ребенка. Неадекватная калорийность рациона у детей с хронической почечной недостаточностью, которая может приводить к истощению, заставляет прибегнуть к принудительному кормлению детей грудного возраста через назога-
стральный зонд или гастростому. Активное увеличение калорийности питания может положительно влиять на рост только у детей младшего возраста [8]. Хотя у детей с задержкой роста и рекомендуется увеличение калорийности питания, чрезмерная калорийность рациона может приводить к гипер-липидемии и гиперинсулинизму [9]. Избыточного приема белка также следует избегать, особенно у детей с терминальной стадией хронической почечной недостаточности, так как это может усугублять метаболический ацидоз и гиперфосфатемию [9].
Несмотря на достаточную калорийность питания, коррекцию ацидоза и анемии, эффективную профилактику или лечение остеодистрофии, задержка роста часто отмечается у детей с хронической почечной недостаточностью. После грудного возраста отставание в росте в основном обусловлено нарушениями в системе гормон роста-инсу-линоподобный фактор роста-1 [10]. Исследования показали исключительное значение инсулинопо-добных факторов роста-1 и -2 на всех фазах роста млекопитающих, включая внутриутробный период, детство и пубертатный период.
Эти факторы впервые были определены в 1957 г. W. Salmon и W. Daughaday как гормон роста зависимый сывороточный фактор и были названы ими «фактором сульфатации» благодаря способности стимулировать сульфатацию хряща. Позже одними авторами они были описаны как факторы с неподавляемой инсулиноподобной активностью, а другими — как соматомедин-С. В дальнейшем было показано, что аминокислотная последовательность соматомедина-С полностью идентична инсулиноподобному фактору роста-1 [11, 12]. Установлено, что основным тканевым медиатором гормона роста является инсу-линоподобный фактор роста-1. Механизмы регуляции и функции инсулиноподобного фактора роста-2 не совсем понятны, но, вероятно, он является важным для роста плода. В течение короткого периода перед рождением инсулиноподоб-ный фактор роста-1 становится исключительно значимым регулятором роста скелета.
После рождения в норме отмечаются 3 фазы соматического роста и биологического созревания, которые контролируются разными регуляторны-ми механизмами. «Доля» быстрого роста в первые 2 года жизни обеспечивает около 30% конечного роста и зависит в основном от нутритивного и метаболического профилей [13, 14]. Дальнейший пропорционально стабильный рост до достижения пубертатного возраста находится под гормональным контролем, включающим ось гормон роста — инсулиноподобный фактор роста-1 и ти-реотропный гормон. Около 20% конечного роста достигается в пубертатном периоде под влиянием
оси гормон роста — инсулиноподобный фактор роста-1 и половые гормоны [14].
Задержка наступления пубертатного периода наблюдается примерно у 2/3 всех больных с терминальной стадией хронической почечной недостаточности. У детей с уремией обычно происходит задержка наступления пубертатного периода в среднем на 2 года, иногда — на 5—6 лет, особенно у детей, длительно получающих диализное лечение. В результате отмечается значительное отставание в конечном росте [15]. В отличие от вторичных половых признаков, которые появляются с задержкой, репродуктивная функция при формировании хронической почечной недостаточности в детском возрасте может быть подавлена необратимо, несмотря на трансплантацию почки. В случае развития хронической почечной недостаточности после наступления половой зрелости нарушения фер-тильности оказываются полностью обратимыми после трансплантации [15, 16].
Синтез и секреция гормона роста (соматотроп-ного гормона, соматотропина) осуществляются соматотрофами, которые представляют собой наиболее многочисленные клетки аденогипофиза. Эти процессы контролируются двумя гипоталами-ческими нейропептидами — рилизинг-гормоном гормона роста (соматолиберин) и соматостатином. Соматолиберин стимулирует как синтез, так и секрецию гормона роста, а соматостатин ингибирует секрецию. Секреция соматолиберина и соматоста-тина гипоталамусом регулируется импульсами из вышележащих отделов ЦНС [11].
Секреция гормона роста зависит также от ну-тритивных факторов: стимулируется при белково-энергетической недостаточности, гипогликемии, ингибируется при гипергликемии. Основным эффектом соматотропного гормона у детей и подростков является стимуляция продольного роста костей. Соматотропин является анаболическим гормоном, стимулирующим синтез белка и задержку азота в организме. Соматотропный эффект гормона на уровне тканей частично реализуется путем стимуляции синтеза инсулиноподобного фактора роста-1. Циркулирующий гормон роста стимулирует синтез этого фактора во многих тканях [17].
Биологические эффекты инсулиноподобного фактора роста-1 проявляются острыми анаболическими сдвигами белкового и углеводного обмена. В биологических средах данный ростовой фактор находится практически исключительно в связанном состоянии, образуя комплексы со связывающими белками. Циркулирующий инсулиноподоб-ный фактор роста-1, синтезируемый в основном в печени, действует как классический эндокринный гормон, в то время как синтезируемый локально в других тканях (костной, мышечной, жировой) он
действует как паракринный/аутокринный фактор роста [18]. Следуя теории двойных эффекторов, оба гормона (гормон роста и инсулиноподобный фактор роста-1) действуют на различные типы клеток, стимулируя рост. Соматотропин индуцирует дифференцировку клеток-предшественников эпифизарной ростовой пластинки в хондроциты; в свою очередь, хондроциты, стимулированные гормоном роста, становятся чувствительными к ин-сулиноподобному фактору роста-1 и параллельно экспрессируют мРНК этого фактора. Стимуляция дифференцированных хондроцитов инсулинопо-добным фактором роста-1 приводит к продольному росту кости [19].
В последние годы значительное внимание было уделено роли белков, связывающих инсули-ноподобный фактор роста. Идентифицировано 6 разновидностей данных белков (IGFBP1—6; insulin-like growth factor-binding protein). Инсулиноподобный фактор роста-1 циркулирует в основном в связанном состоянии с IGFBP-3 в виде тройного комплекса массой 150 кД, в состав которого также входит кислотно-лабильная субстанция. Такой крупный комплекс, будучи не способным проникать через эндотелиальный барьер и покидать сосудистое русло, играет роль резервуара [20]. Только около 1% инсулиноподобного фактора роста-1 встречается в плазме в свободной биоактивной форме. Концентрация белков IGFBP-1 регулируется специфическими протеазами, которые, расщепляя молекулы белков, резко снижают их связывающую активность. При этом свободные молекулы инсулиноподобного фактора роста становятся доступными для рецепторов [19, 21]. Таким образом, основным назначением белков, связывающих инсулиноподобный фактор роста-1, является регуляция биоактивности этого фактора. IGFBP-1, -2, -4 и -6 ингибируют, а IGFBP-3 и -5 стимулируют функцию остеобластов путем регулирования активности инсулиноподобного фактора роста. Кроме того, недавние исследования выявили, что эти белки могут оказывать независимое от инсулиноподобного фактора роста влияние на формирование костной ткани, в частно -сти IGFBP-5 стимулирует костеобразование [18]. Задержка роста у детей с хронической почечной недостаточностью частично является результатом ингибирования биологической активности инсу-линоподобного фактора роста из-за избытка высокоаффинных IGFBP [22].
У детей и у взрослых с хронической почечной недостаточностью средний уровень гормона роста в сыворотке натощак является нормальным или повышенным в зависимости от степени недостаточности функции почек. Регуляция секреции гормона роста гипоталамо-гипофизарной осью у таких
больных нарушена. При уремии отмечается снижение почечного клиренса гормона роста, которое коррелирует с уменьшением скорости клубочковой фильтрации. Один из молекулярных механизмов периферической резистентности к соматотропному гормону у больных с уремией — снижение плотности рецепторов гормона роста в органах-мишенях [22]. Несмотря на повышенный уровень соматотро-пина в крови при уремии, концентрация инсули-ноподобного фактора роста-1 в сыворотке не увеличивается из-за снижения его синтеза в печени [18]. Кроме того, снижена биоактивность данного фактора из-за повышения уровня IGFBP-1, -2, -4 и -6, так как нарушается эффективная доставка инсу-линоподобного фактора роста-1 к рецепторам [22]. Механизм развития резистентности к гормону роста при уремии также включает нарушение постре-цепторной передачи сигнала вследствие дефекта сигнального трансдуктора и активатора транскрипции — пострецепторной Янус-киназы-2, активируемой гормоном роста [23].
Лечение низкорослых детей с уремией реком-бинантным человеческим гормоном роста в дозах, превышающих физиологическую секрецию сомато-тропина, повышает биоактивность сывороточного инсулиноподобного фактора роста-1. Таким образом, можно предположить, что одним из механизмов лечебного действия рекомбинантного гормона роста является стимулирование продукции достаточного количества инсулиноподобного фактора роста-1 для преодоления ингибиторных эффектов избытка связывающих белков IGFBP [24].
Негативное воздействие хронического метаболического ацидоза на рост также, по-видимому, хотя бы частично, опосредовано системой гормон роста — инсулиноподобный фактор роста-1. При исследовании in vitro тканевой культуры в условиях хронического метаболического ацидоза отмечается значительное снижение числа молодых хондроци-тов, что позволяет думать о дефекте эндохондраль-ной дифференциации при хронической почечной недостаточности. При этом отмечается значительное снижение экспрессии рецепторов инсулино-подобного фактора роста-1 и соматотропина. Кроме того, при хроническом метаболическом ацидозе усилена экспрессия IGFBP-2 и -4, которые служат негативными модуляторами инсулиноподобного фактора роста-1. Эти данные позволяют предположить, что хронический метаболический ацидоз оказывает антианаболическое действие на ростовые зоны кости, частично связанное с состоянием резистентности к гормону роста и инсулиноподоб-ному фактору роста-1. Этот феномен может лежать в основе нарушений линейного роста кости и обусловливать ренальную остеодистрофию у больных с хронической почечной недостаточностью [25].
Как было упомянуто выше, гормон роста проявляет свое действие через стимуляцию синтеза печеночного инсулиноподобного фактора роста-1 и путем прямого воздействия на органы-мишени, включая стимуляцию локальной продукции данного фактора. Несмотря на нормальные концентрации в плазме, при уремии отмечается снижение биологической активности инсулиноподобного фактора роста-1. Долгое время считалось, что со-матотропный гормон не играет роли в патофизиологии нарушений роста при хронической почечной недостаточности, так как его уровень в сыворотке больных не снижен. Положительное влияние на рост супрафизиологических доз соматотропина впервые продемонстрировали на моделях крыс с уремией O. Mehls и E. Ritz в 1983 г. [26]. В первых исследованиях использовался свиной гормон роста, последующие исследования показали улучшение роста в эксперименте с крысиным гормоном, а в дальнейшем с рекомбинантным человеческим гормоном роста [27, 28]. При двухлетнем плацебо-контролируемом исследовании у 125 детей препу-бертатного возраста с хронической почечной недостаточностью на фоне консервативной терапии показатели роста у группы, получающей реком-бинантный человеческий гормон роста в дозе 0,05 мг/кг в сутки (n=82), были значительно лучше, чем в группе с плацебо (n=43), но разница была более выраженной в течение первого года наблюдения. Так, средняя скорость роста в группе леченных ре-комбинантным человеческим гормоном в первый год составила 10,7±3,1 см/год против 6,5±2,6 см/ год в группе плацебо, во второй — 7,8+2,1 см/год против 5,5+1,9 см/год (р<0,00005).
Параллельно были проведены исследования эффективности рекомбинантного человеческого гормона роста у детей, получающих диализную терапию [29, 30]. У этих пациентов на фоне лечения также отмечалось улучшение роста. Но эффект был менее выраженным, чем у больных, получавших консервативную терапию хронической почечной недостаточности. Очевидной разницы в эффективности применения рекомбинантного человеческого гормона роста у детей, находящихся на гемодиализе и перитонеальном диализе, не отмечено [30, 31].
Важным вопросом является влияние рекомби-нантного человеческого гормона роста на конечный рост у детей с хронической почечной недостаточностью. Высказано предположение, что данное лекарственное средство может улучшить рост кратковременно, но за счет увеличения костного возраста ребенка, потенциально ограничивая рост в перспективе. Наблюдения за детьми с задержкой роста без хронической почечной недостаточности показали уменьшение продолжительности пубертатного периода у больных, получающих реком-
бинантный человеческий гормон роста. Однако у детей с хронической почечной недостаточностью как в кратковременных, так и в длительных рандомизированных исследованиях признаков ускорения костного возраста не отмечено [32, 33].
В нескольких работах показано, что длительное лечение рекомбинантным человеческим гормоном роста детей с хронической почечной недостаточностью приводит к ростовому скачку, и конечный рост многих пациентов достигает пределов нормы. A. Hokken-Koelega и соавт. оценили рост у 45 детей препубертатного возраста с хронической почечной недостаточностью и дефицитом роста, длительно получающих рекомбинантный человеческий гормон роста [33]. Большинство (34 из 45) больных лечились немногим менее 6 лет, и у них отмечался ростовой скачок со значительным улучшением роста по сравнению с исходным (^<0,001). Среднее стандартное отклонение роста достигало нижней границы нормы (SDS роста —2) через 3 года лечения и приближалось к целевому значению через 6 лет. Кроме того, это лечение в течение пубертатного периода привело к стойкому улучшению роста без отрицательного влияния на скорость клубоч-ковой фильтрации и созревание костей [33].
Подобные данные приведены J. Kari и L. Rees, которые описали значительное увеличение SDS роста (от —2,5+1,4 до -1,6+0,6; ^=0,001) у 21 ребенка на фоне консервативной терапии хронической почечной недостаточности, получающего реком-бинантный человеческий гормон роста в среднем в течение 3,7+2,5 года [34]. Установлена обратная корреляция между скоростью роста перед началом курса лечения и увеличением скорости роста после его окончания: у детей с более низкой скоростью роста перед началом терапии отмечен более выраженный эффект от применения рекомбинантного человеческого гормона роста [30, 35].
У значительной части детей после трансплантации почки может отмечаться плохой рост, и у них реже наблюдается ростовой скачок. Несколько исследований продемонстрировали хороший эффект от лечения рекомбинантным человеческим гормоном роста больных данной группы [36, 37]. G. Guest и соавт. [38] исследовали эффект терапии гормоном роста у 90 детей препубертатного и раннего пубертатного возраста, как минимум, через 12 мес после трансплантации с нормально функционирующим трансплантатом. У детей, леченных гормоном роста, через год отмечалось значительное увеличение скорости роста по сравнению с исходным уровнем (7,7 и 4,1 см/год соответственно, ^<0,0001), скорость роста в контрольной группе при этом не менялась. У детей, продолжавших получать рекомбинантный человеческий гормон роста, скорость роста снижалась по сравнению с
первым годом лечения, но оставалась выше исходных значений. На основании данных NAPRTCS [39, 40] показано, что конечный рост (SDS) был значимо выше у больных с трансплантацией почки, получающих длительное лечение гормоном роста (п=513), по сравнению с нелечеными (я=2263): -1,83+0,14 против -2,6+0,05 (р<0,001).
Следует подчеркнуть, что хотя пациенты, находящиеся на диализе, и реципиенты почечного трансплантата показывают хороший ответ на лечение рекомбинантным человеческим гормоном роста, большая эффективность отмечена у детей с претерминальной (консервативной) стадией хронической почечной недостаточности [41]. Это может быть связано со степенью выраженности изменений концентрации IGFBP и плотности рецепторов гормона роста по мере нарастания тяжести хронической почечной недостаточности. Следовательно, вопрос о необходимости лечения гормоном роста следует ставить как можно в более раннем возрасте и на ранних стадиях развития хронической почечной недостаточности, тем самым увеличивая возможность максимального использования ростового потенциала.
Следует рассмотреть вероятность появления побочных эффектов от применения рекомбинант-ного человеческого гормона роста у детей с хронической почечной недостаточностью. Согласно данным литературы, могут отмечаться следующие проблемы: ускоренное снижение скорости клу-бочковой фильтрации, возможное отторжение или утрата функции почечного трансплантата, костная патология, нарушения метаболизма глюкозы, внутричерепная гипертензия и малигнизация. В больших рандомизированных исследованиях по лечению гормоном роста детей после трансплантации почки разницы в частоте снижения скорости клубочковой фильтрации у детей, получающих и не получающих препарат, не было [39]. Подобные же результаты были выявлены в других рандомизированных исследованиях у пациентов, которым рекомбинантный человеческий гормон роста был назначен на фоне консервативной терапии хронической почечной недостаточности [32, 42].
В ряде источников литературы сообщается о развитии эпифизеолиза головки бедренной кости или аваскулярного некроза у детей, получающих рекомбинантный человеческий гормон роста. Некоторые из этих исследований касаются больных с хронической почечной недостаточностью [43], в остальных — данный препарат назначали детям по поводу дефицита гормона роста. При хронической почечной недостаточности такие сообщения трудно интерпретировать, учитывая, что подобные ортопедические осложнения являются нередкими последствиями почечной остеодистрофии. В дру-
гих исследованиях, посвященных применению гормона роста у детей с хронической почечной недостаточностью, о таких осложнениях не сообщается [33, 42]. В большом проспективном исследовании с охватом более чем 10 000 детей с хронической почечной недостаточностью статистически достоверных различий в развитии ортопедических осложнений у пациентов, получающих рекомби-нантный человеческий гормон роста, по сравнению с остальными не отмечено [44].
Другой проблемой, касающейся костного метаболизма у детей с хронической почечной недостаточностью, леченных гормоном роста, является возможное нарастание вторичного гиперпарати-реоза. Имеющиеся данные противоречивы. По результатам одних работ обнаруживается повышение уровня паратгормона на фоне применения реком-бинантного человеческого гормона роста [30], в других же исследованиях этого не отмечается [33]. Имеются данные, что лечение гормоном роста может оказывать положительное влияние на минеральную плотность костей у детей с хронической почечной недостаточностью [45, 46]. Исследование у 10 детей препубертатного возраста с хронической почечной недостаточностью в претерми-нальной стадии показало, что лечение гормоном роста в течение 1 года приводило к значительному увеличению минерализации костной ткани [46].
Известно, что гормон роста влияет на метаболизм глюкозы. Введение его физиологических доз приводит к кратковременному инсулиноподобному эффекту с незначительным снижением гликемии, а затем к контринсулярному действию. В связи с чем возникает вопрос о возможном развитии толерантности к углеводам при длительном применении рекомбинантного человеческого гормона роста. В нескольких исследованиях сообщалось о значительном повышении уровня инсулина в течение первого года лечения гормоном роста, однако при длительном лечении уровень инсулина возвращался к исходным значениям [37]. Хотя случаев сахарного диабета с необратимым течением у детей с хронической почечной недостаточностью не выявлено, рекомендуется тщательный мониторинг гликемии [38, 47].
В нескольких работах было отмечено развитие внутричерепной гипертензии у пациентов, получавших рекомбинантный человеческий гормон роста. Такие случаи были зарегистрированы у детей с хронической почечной недостаточностью и без таковой [44]. Интерпретация этих фактов является сложной из-за возможной связи хронической почечной недостаточности с внутричерепной гипертензией. В обширном проспективном исследовании статистически значимое нарастание данного осложнения отмечалось в предиализной когорте, хотя было обнаружено только у 3 из 1376 больных [44].
В нескольких исследованиях по применению рекомбинантного человеческого гормона роста у детей после трансплантации почки сообщалось об увеличении риска отторжения трансплантата или ухудшении его функционирования [36, 37]. В то же время по данным четырех рандомизированных исследований эффективности и безопасности гормона роста у детей после трансплантации почки [37—39] увеличения частоты отторжения трансплантата у реципиентов, получающих этот препарат, не выявлено. Также не наблюдалось ухудшения функции трансплантата по сравнению с контрольной группой. Согласно результатам двух из этих работ [38, 39], более чем 1 эпизод отторжения трансплантата в анамнезе до назначения гормона роста увеличивает риск последующего отторжения. Подобное же отмечалось и в контрольной группе. R. Fine и D. Stablein на основании длительного (более 5 лет) наблюдения и анализа данных NAPRTCS о 513 детях-реципиентах почечного трансплантата не выявили разницы в частоте отторжения или утрате функции трансплантата по сравнению с контрольной группой. Использование рекомбинантного человеческого гормона роста признано эффективным и безопасным для лечения реципиентов почечного трансплантата с задержкой роста [40].
Описаны случаи малигнизации и панкреатита в качестве побочных эффектов лечения детей гормоном роста. Однако длительные наблюдения не подтвердили наличие причинной связи между данными побочными явлениями и применением рекомби-нантного человеческого гормона роста у детей с хронической почечной недостаточностью [44].
Проблемы, связанные с использованием гормона роста у детей, требуют дополнительного изучения. Одной из них является то обстоятельство, что большое количество детей с хронической почечной недостаточностью, нуждающихся в лечении рекомбинантным человеческим гормоном роста, не получают его. По данным NAPRTCS, только 22% детей с предиализной хронической почечной недостаточностью и ростом ниже 3-й перцентили получают указанную терапию спустя 1 год после постановки на учет (данные 2003 г.). Факторами, влияющими отрицательно на частоту лечения, могут быть высокая стоимость препарата и необходимость в ежедневных подкожных инъекциях [48].
В руководствах Национального почечного фонда США K/DOQI по питанию (2000 г.) и по костному метаболизму у детей (2005 г.) представлены рекомендации по срокам начала и окончания терапии гормоном роста [49, 50]. Одной из рекомендаций является прекращение применения препарата при достижении либо 50-й перцентили по возрасту либо целевого среднего роста родителей. Некоторые дети сохраняют нормальную скорость роста
даже после перерыва в лечении гормоном роста [30, 51]. Однако все же у многих из них после прекращения терапии отмечается снижение скорости роста и SDS роста [51]. В такой ситуации возникает вопрос, когда следует возобновлять лечение гормоном роста и нужно ли при этом использовать более низкую дозу.
Известно также, что некоторые дети недостаточно отвечают на назначение гормона роста в дозе 0,05 мг/кг в сутки, несмотря на соответствующую коррекцию других факторов, отрицательно влияющих на рост. P. Park и P. Cohen предлагают следующую стратегию коррекции дозировки гормона роста, основанную на диагнозе заболевания, массе тела, уровне инсулиноподобного фактора роста-1 в сыворотке и скорости роста: 1) исходная доза рассчитывается по массе тела в общепринятых дозировках для данной нозологии; 2) корректировка дозы осуществляется в зависимости от уровня инсулино-подобного фактора роста-1 (у больных с более высоким уровнем этого фактора скорость роста была выше); 3) регулярно мониторируется скорость роста и соответственно регулируется доза гормона с целью достижения оптимального конечного роста [52].
В группу кандидатов по лечению гормоном роста предлагается включать детей с хронической почечной недостаточностью (скорость клубочковой фильтрации <75 мл/мин на 1,73 м2 площади поверхности тела) и задержкой роста ниже 3-й перцентили (SDS роста <—1,88) [53]. В подавляющем большинстве исследований рекомендуемой дозой препарата у детей с хронической почечной недостаточностью является 0,05 мг/кг в сутки (0,35 мг/кг в неделю или
28—30 ЕД/м2 в неделю), назначаемой ежедневно в виде подкожных инъекций [53]. В процессе лечения гормоном роста необходимо наблюдение за больными каждые 3—4 мес для антропометрии, определения степени пубертатного созревания, оценки нутритивного статуса, исследования глазного дна и биохимических показателей крови, а также уровня паратиреоидного гормона. Лечение гормоном роста должно быть прекращено при закрытии эпифи-зарных зон роста, при достижении целевого роста (средний рост родителей или 50-я перцентиль по возрасту). Лечение, хотя бы временно, должно быть прервано при обнаружении признаков неоплазии, эпифизеолиза головки бедренной кости, доброкачественной внутричерепной гипертензии, выраженного гиперпаратиреоза (содержание паратгор-мона в крови >900 пг/мл при терминальной стадии или >400 пг/мл при более ранних стадиях хронической почечной недостаточности) [53].
В заключение следует подчеркнуть, что хотя безопасность и эффективность применения ре-комбинантного человеческого гормона роста для лечения задержки роста у детей с хронической почечной недостаточностью продемонстрированы множеством клинических исследований, частота использования препарата остается низкой у данной категории больных. Это, по-видимому, можно объяснить отсутствием четких клинических рекомендаций, касающихся сроков начала терапии и мониторинга лечения, высокой стоимостью препарата и недооценкой проблемы низкорослости и ассоциированных с ней вопросов у детей с хронической почечной недостаточностью.
ЛИТЕРАТУРА
1. North American Pediatric Renal Transplant Cooperative Study (2006) Annual report. Renal transplantation, dialysis, chronic renal insufficiency. Available at: http://web. emmes.com/study/ped/annlrept 2006.pdf
2. Andre J.L., Bourquard R., Guillemin F. Final height in children who have not received growth hormone. Pediatr Nephrol 2003; 18: 685—691.
3. Schaefer F., Wingen A.M., Hennicke M. European Study Group for Nutritional Treatment of Chronic Renal Failure in Childhood. Growth charts for prepubertal children with chronic renal failure due to congenital renal disorders. Pediat Nephrol 1996; 10: 288—293.
4. WongC.S., Gipson D.S., Gillen D.L. Anthropometric measures and risk of death in children with end-stage renal disease. Am J Kidney Dis 2000; 36: 811—819.
5. Furth S.L., Hwang W., Yang C. Growth failure, risk of hospitalization and death for children with end-stage renal disease. Pediat Nephrol 2002; 17: 450—455.
6. Furth S.L., Stablein D., Fine R.N. Adverse clinical outcomes associated with short stature at dialysis initiation: A report of the North American Pediatric Renal Transplant Cooperative Study. Pediatrics 2002; 109: 909—913.
7. Mehls O. Treatment with growth hormone of growth impairment in renal disorders. In: M.B.Ranke, R.Gunnarsson
(ed): Progress in growth hormone therapy—5 years of KIGS. J&J Verlag, Mannheim 1994; 267—277.
8. Sedman A., Friedman A, Boineau F. Nutritional management of the child with mild to moderate chronic renal failure. J Pediat 1996; 129: S13—S18.
9. Wingen A.M., Mehls O. Nutrition in children with preterminal chronic renal failure. Pediat Nephrol 2002; 17: 111—120.
10. Kaskel F. Chronic renal disease: A growing problem. Kidney Int 2003; 64: 1141—1151.
11. Дедов И.И., Тюльпаков А.Н., Петеркова В.А. Соматотропная недостаточность. М: Изд-во «ИндексПринт» 1998; 25—28.
12. Laron Z. Insulin-like growth factor-1 (IGF-1): a growth hormone. J Clin Pathol: Mol Pathol 2001; 54: 311—316.
13. Schaefer F., Mehls O. Endocrine and growth disturbances. Pediatric Nephrology (ed 4). Lippincott Williams and Wilkins 1999; 1197—1230.
14. Van Dyck M., Bilem N., Proesmans W. Conservative treatment for chronic renal failure from birth: A 3-year follow-up study. Pediat Nephrol 1999; 13: 865—869.
15. Schaefer F., Seidel C., Binding A. Pubertal growth in chronic renal failure. Pediat Res 1990; 28: 5—10.
16. Mehls O., Ritz E., Hunziker E.B. Role of growth hormone in growth failure of uraemia—perspectives for application
of recombinant growth hormone. Acta Pediat Scand 1988; 343: 118—126.
17. Roelfsema V., ClarkR.G. The growth hormone and insulinlike growth factor axis: Its manipulation for the benefit of growth disorders in renal failure. J Am Soc Nephrol 2001; 12: 1297—1306.
18. Govoni K..E, Baylink D.J., Mohan S. The multi-functional role of insulin-like growth factor binding proteins in bone. Pediat Nephrol 2004; 20: 261—268.
19. Tonshoff B., Kiepe D, Ciarmatori S. Growth hormone/insulin-like growth factor system in children with chronic renal failure. Pediat Nephrol 2005; 20: 279—289.
20. Powell D.R., Durham S.K., Liu F. The insulin-like growth factor axis and growth in children with chronic renal failure: A report of the Southwest Pediatric Nephrology Study Group. J Clin Endocrinol Metab 1998; 83: 1654—1661.
21. Feld S, Hirschberg R. Growth hormone, the insulin-like growth factor system, and the kidney. Endocr Rev 1996; 17: 423—480.
22. Powell D.R., Liu F., Baker B.K. Effect of chronic renal failure and growth hormone therapy on the insulin-like growth factors and their binding proteins. Pediat Nephrol 2000; 14: 579—583.
23. Schaefer F., Chen Y., Tsao T. Impaired JAK-STAT signal transduction contributes to growth hormone resistance in chronic uremia. J Clin Invest 2001; 108: 467—475.
24. Yakar S., Liu J.L., Le Roith D. The growth hormone/insulin-like growth factor-I system: implications for organ growth and development. Pediat Nephrol 2000; 14: 544— 549.
25. Green J., Maor G. Effect of metabolic acidosis on the growth hormone/IGF-I endocrine axis in skeletal growth centers. Kidney Int 2000; 57: 2258—2267.
26. Mehls O., Ritz E. Skeletal growth in experimental uremia. Kidney Int 1983; 15: S53—S62.
27. Nakano M., Kainer G., Foreman J.W. The effects of exogenous rat growth hormone therapy on growth of uremic rats fed an 8% protein diet. Pediat Res 1989; 26: 204—207.
28. Mehls O., Ritz E., Hunziker E.B. Improvement of growth and food utilization by human recombinant growth hormone in uremia. Kidney Int 1988; 33: 45—52.
29. Haffner D., Schaefer F., NisselR. German Study Group for Growth Hormone Treatment in Chronic Renal Failure. Effect of growth hormone treatment on the adult height of children with chronic renal failure. N Engl J Med 2000; 343: 923—930.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
30. Berard E., Crosnier H., Six-Beneton A. French Society of Pediatric Nephrology. Recombinant human growth hormone treatment of children on hemodialysis. Pediat Nephrol 1998; 12: 304—310.
31. Wuhl E., Haffner D., Nissel R. German Study Group for Growth Hormone Treatment in Chronic Renal Failure. Short dialyzed children respond less to growth hormone than patients prior to dialysis. Pediat Nephrol 1996; 10: 294—298.
32. Fine R.N., Kohaut E.C., Brown D. Growth after recombinant human growth hormone treatment in children with chronic renal failure: Report of a multicenter randomized double-blind placebo-controlled study. J Pediat 1994; 124: 374—382.
33. Hokken-Koelega A, Mulder P., De Jong R. et al. Long-term effects of growth hormone treatment on growth and puberty in patients with chronic renal insufficiency. Pediat Nephrol 2000; 14: 701—706.
34. Kari J.A., Rees L. Growth hormone for children with chronic renal failure and on dialysis. Pediat Nephrol 2005; 20: 618—621.
35. WuhlE., Haffner D., Tonshoff B. German Study Group for Growth Hormone Treatment in Chronic Renal Failure.
Predictors of growth response to rhGH in short children before and after renal transplantation. Kidney Int 1993; 43: S76—S82.
36. Broyer M., Pharmacia & Upjohn Study Group. Results and side-effects of treating children with growth hormone after kidney transplantation—a preliminary report. Acta Paedi-atrica 1996; 417: 76—79.
37. Maxwell H., Rees L. British Association for Pediatric Ne-phrology. Randomised controlled trial of recombinant human growth hormone in prepubertal and pubertal renal transplant recipients. Arch Dis Child 1998; 79: 481—487.
38. Guest G., BerardE., Crosnier H. French Society of Pediatric Nephrology. Effects of growth hormone in short children after renal transplantation. Pediat Nephrol 1998; 12: 437—446.
39. Fine R.N., Stablein D., Cohen A.H. et al. Recombinant human growth hormone post-renal transplantation in children: a randomised controlled study of the NAPRTCS. Kidney Int 2002; 62: 688—696.
40. Fine R.N., Stablein D. Long-term use of recombinant human growth hormone in pediatric allograft recipients: a report of the NAPRTCS Transplant Registry. Pediat Nephrol 2005; 20: 404—408.
41. Seikaly M.G., Salhab N, Warady B.A., Stablein D. Use of rhGH in children with chronic kidney disease: lessons from NAPRTCS. Pediat Nephrol 2007; 22: 1195—1204.
42. Hokken-Koelega A.C., Stijnen T., de Muinck Keizer-Schra-ma S.M. Placebo-controlled, double-blind, cross-over trial of growth hormone treatment in prepubertal children with chronic renal failure. Lancet 1991; 338: 585—590.
43. Boechat M.I., Winters W.D., Hogg R.J. Avascular necrosis of the femoral head in children with chronic renal disease. Radiology 2001; 218: 411—413.
44. Fine R.N., Ho M., Tejani A. Adverse events with rhGH treatment of patients with chronic renal insufficiency and end-stage renal disease. J Pediat 2003; 142: 539—545.
45. Van Dyck M., Gyssels A, Proesmans W. Growth hormone treatment enhances bone mineralisation in children with chronic renal failure. Eur J Pediat 2001; 160: 359—363.
46. Van der Sluis I.M., Boot A.M., Nauta J. Bone density and body composition in chronic renal failure: Effects of growth hormone treatment. Pediat Nephrol 2000; 15: 221—228.
47. Haffner D., Nissel R., Wuhl E. Metabolic effects of long-term growth hormone treatment in prepubertal children with chronic renal failure and after kidney transplantation. Pediat Res 1998; 43: 209—215.
48. Ho M., Stablein D.M. North American Pediatric Renal Transplant Cooperative Study (NAPRTCS) Annual Report. Rockville, Maryland 2003; 28.
49. National Kidney Foundation. K/DOQI clinical practice guidelines for nutrition in chronic renal failure. Am J Kidney Dis 2000; 35: S1—S140.
50. National Kidney Foundation. K/DOQI Clinical Practice Guidelines for Bone Metabolism and Disease in Children With Chronic Kidney Disease 2005. http:// www.kidney. org/professionals/KDOQI/guidelines_pedbone/index. htm
51. Fine R.N., Kohaut E., Brown D. Long-term treatment of growth retarded children with chronic renal insufficiency, with recombinant human growth hormone. Kidney Int 1996; 49: 781—785.
52. Park P., Cohen P. The role of insulin-like growth factor I monitoring in growth hormone treated children. Horm Res 2004; 62: 59—65.
53. Mahan J.D., Warady B.A. Assesment and treatment of short stature in pediatric patients with chronic kidney disease: a consensus statement. Pediat Nephrol 2006; 21: 917—930.
Поступила 11.12.07
Содержание
- 1 О гормоне
- 2 Функции
- 2.1 Расщепление жиров
- 2.2 Поддержание упругости кожи
- 2.3 Увеличение силы мышц и прочности костей
- 2.4 Регулировка жирового обмена
- 3 Нормативные показатели
- 4 Повышенные и пониженные значения: как с ними бороться
- 5 Советы от врачей
Ни один человек не может нормально жить без нормального уровня соматотропного гормона. Чаще всего его называют гормоном роста. Это активный белок, который занимает в организме важное место по части обмена вещества и выработки новых клеток. Синтез его происходит в гипофизе, благодаря чему воздействуют на процессы непосредственно из мозга.
О гормоне
В организме человек формируется огромное количество химических соединений, которые управляют процессами развития организма, регулируют работу важных для жизнедеятельности желёз, контролируют обмен веществ. Соматотропный гормон роста формируется в гипофизе под непосредственным контролем гипоталамуса. Он отвечает за рост организма, регулирование обменных процессов, в том числе расщеплении белков, жиров и углеводов, а также работу желез внутренней секреции.
Самые большие концентрации соматотропина наблюдаются в детском возрасте, когда малыш активно растёт. Дефицит гормона роста влечёт за собой отставание ребёнка в процессе роста от сверстников. В запущенных случаях это может повлечь задержки общего развития, что чревато опасными последствиями.
Важно отметить, что переизбыток соматотропина также приводит к нежелательным последствиям. В данном случае ребёнок обгоняет сверстников по всем параметрам и рост не прекращается даже после завершения периода полового созревания. Это может перерасти в гигантизм или акромегалию.
Максимальные дозы синтеза гормона роста происходят в период с рождения малыша до окончания пубертатного возраста. Однако за его концентрацией важно следить и во взрослом периоде. Он отвечает за многие важные процессы в организме, в том числе выработку клеток, формирование тканей и правильный обмен веществ.
Функции
Соматотропин выполняет ряд важных функций для поддержания здоровья человека. Это процессы, без которых невозможна нормальная жизнедеятельность человека, а также восстановление после стрессов, физических нагрузок и других неприятных последствий.
Расщепление жиров
Гормон роста вырабатывается в ночное время, когда организм отдыхает. Происходит так потому, что в дневные часы человеку хватает потребляемых с пищей углеводов. Они дают энергию. В ночные часы активно вырабатывается соматотропин, расщепляя отложения жиров. Именно поэтому после пробуждения мы выглядим несколько худее, чем в течение дня.
Но данные процессы не работают, если человек предпочитает плотно поесть перед сном или лечь спать позже обычного. Чтобы соматотропин вырабатывался в соответствии с природной функцией, важно соблюдать ряд правил:
- не наедаться на ночь;
- исключить мучные, солёные и сладкие кулинарные изыски в вечерние часы;
- ложиться спать вовремя;
- не употреблять пищу хотя бы за пару часов до отхода ко сну.
Расщепляя жиры, гормон вырабатывает нужную нам энергию. При этом в переработку идут даже отложившиеся давно жиры, застоявшиеся в организме. Человек «худеет» не прилагая к этому особых усилий.
Поддержание упругости кожи
Участие в регенерации тканей, а также усиленная выработка белка помогает поддерживать кожу в тонусе и активно поддерживать кожу в тонусе. Она подтягивается, становится более упругой и ровной, замедляется процесс появления морщин.
Увеличение силы мышц и прочности костей
Под воздействием гормона роста и при достаточном количестве его выработки гипофизом происходит укрепление мышц и костей, они становятся более упругими и эластичными, дольше сохраняют «молодость». Существенно уменьшается риск развития остеопороза, в результате которого минеральные вещества вымываются из костей. Также сокращается риск переломов.
Благодаря спортивным тренировкам можно усилить процесс укрепления, так как при физических нагрузках соматотропин вырабатывается сильнее и быстрее.
Чтобы походить с помощью выработки гормона роста и занятий в фитнес-центре, обязательно отказаться от употребления перед тренировкой шоколада, а также сладких напитков, кофе и чая. Они являются источниками поступления в организм углеводов, которых будет достаточно на взятие нагрузок. Выработка соматотропина будет приостановлена.
Регулировка жирового обмена
Гормон роста регулирует и снижает выработку вредного холестерина, который способен оседать на стенках сосудов и провоцировать развитие атеросклероза, инфарктов, инсультов, нарушений сосудистой системы.
Функции гормона роста достаточно обширны. Он расщепляет поступающие в организм вещества и энергетически подпитывает органы и ткани. В результате нормальной работы синтеза гормонов происходит укрепление организма в целом, появляется упругость костей, тканей, нормализация метаболизма.
Нормативные показатели
Пациенты любого возраста могут быть исследованы на количественное содержание гормона в сыворотке крови. Для этого достаточно посетить ближайшую лабораторию для забора биоматериала. Анализ назначается в следующих случаях:
- замедление или ускорение роста у пациентов детского возраста;
- слабость мышц у взрослых;
- диагностика гипоактивности железы;
- порфирия;
- вымывание минеральных веществ из костей;
- патологическое потоотделение;
- гипотериоз первичного типа;
- гипогликемия.
Чтобы показатели секреции гормона роста были качественными, важно правильно подготовиться к посещению лаборатории. Для этого соблюдают режим голодания от 8 до 12 часов, без употребления кофе, чая, сладких соков и газировки. Можно пить только чистую питьевую воду без газа.
Обязательно воздержаться от физических и эмоциональных перегрузов хотя бы за сутки до исследования, а также от курения не менее чем за три часа до сдачи крови. Перед забором венозной крови рекомендуется посидеть в состоянии покоя не менее получаса перед кабинетом лаборантов.
Существуют таблицы, которые определяют референсные значения гормона роста. Стоит ориентироваться на них при оценке результата, но заниматься самолечением категорически запрещено. Диагностику и назначение соответствующей терапии проводит только врач.
Уровень инсулиносвязанного гормона изменяется в зависимости от пола и возраста пациента. Здесь даются подробные таблицы с усреднёнными значениями:
| Возраст и пол пациента | Концентрация (нг/мл) |
| женщины от 16 до 19 лет | 176–249 |
| мужчины от 16 до 19 лет | 57–425 |
| пациенты в возрасте от 19 до 22 лет | 105–345 |
| граждане в возрасте от 23 до 25 лет | 107–367 |
| люди от 26 до 30 лет | 88–537 |
| пациенты от 31 до 35 лет | 41–246 |
| пациенты 36 – 40 лет | 57–241 |
| пациенты 41 – 45 лет | 43–210 |
| граждане от 46 до 50 лет | 75–196 |
| от 51 до 55 лет | 55–250 |
| пациенты от 56 до 60 лет | 35–200 |
| пациенты от 61 до 65 лет | 50–187 |
| пациенты от 66 до 70 лет | 37–220 |
| пожилые люди от 71 до 80 лет | 25–200 |
| люди старше 80 лет | 17–325 |
В целом у взрослого населения показатель выработки соматотропина у женщин должен быть ниже 8 мкг/л, у мужчин – до 3 мкг/л.
Повышенные и пониженные значения: как с ними бороться
Если гормон роста вырабатывается некорректно, в этом случае идёт речь о понижении или повышении количественных значений. Увеличение показателей соматотропина наблюдается в случае алкоголизма или соблюдения диеты пациентом. Показатели меняются также при активных физических нагрузках.
Речь может идти о гигантизме и акромегалии, если количественные значения сильно превышают норму выработки гормона. Чрезмерный синтез соматотропного гормона приводит к усиленному росту в детском и подростковом возрасте. При этом пропорции тела сохраняются.
Акромегалия представляет собой рост, но только уже не костей и тканей, как у подростков, а внутренних органов, так как наблюдается у взрослых пациентов. Увеличивается их размеры и вес, что создаёт существенные проблемы для нормальной жизнедеятельности. Всё это указывает на то, что гормон роста в крови повышен.
Также повышение уровня вырабатываемого железой гормона роста происходит после перенесённых травм и операций. В этот момент организму нужна активная стимуляция клеток и рост новых для поддержания здоровья организма и его восстановления. Самототропин вырабатывается в усиленном режиме, наблюдается избыток гормона роста.
Недостаток вещества характеризуется задержкой в росте и общем развитии. Нужна срочная помощь, чтобы не спровоцировать отклонения у ребёнка. У взрослых сниженные показатели также опасны, так как могут спровоцировать развитие различных заболеваний, к примеру, остеопороз.
Чтобы восполнить недостаток гормона роста, следует наладить режим сна и отдыха. Действительность такова, что наибольшая концентрация соматотропина наблюдается в ночной период. Поэтому ложиться спать нужно не позднее 22 часов, предварительно подготовившись и отложив гаджеты.
Важно правильно и сбалансированно питаться. Нельзя отказывать себе в потреблении белка, содержащегося в мясе и рыбе. Повысить уровень гормона можно также за счёт умеренных физических перегрузов.
После консультации с доктором можно перейти на приём лекарственных препаратов и аминокислот. Важно не заниматься самостоятельным, бесконтрольным приёмом, чтобы не навредить организму.
Советы от врачей
Железа, вырабатывающая гормон роста, должна работать как часы, в противном случае качество жизни будет существенно снижено. Чтобы этого не произошло, обязательно наладить режим дня. Следует вовремя ложиться спать и высыпаться положенное время, качественно отдыхать и заниматься спортом. Умеренные физические нагрузки способствуют питанию мышц и формированию правильного мышечного каркаса.
Режим питания и сбалансированность продуктов – один из ключевых моментов. В организм пациента должно поступать достаточное количество белков, жиров и углеводов. Не стоит есть перед сном или переедать в течение дня, рекомендуется придерживаться «правильного» питания с полезными продуктами.
При подозрении на отклонения в нормативах содержания соматотропного гормона рекомендуется незамедлительно обратиться к доктору и получить назначение на анализ крови. Лабораторное исследование покажет, необходима ли человеку восстановительная терапия.
Справиться с патологическим недостатком или переизбытком соматотропина можно только с помощью отслеживания лечащего доктора. Самостоятельное лечение или бесконтрольный приём аминокислот способен привести к обратному результату. Не стоит заниматься самолечением, даже если уже сданы все анализы и по протоколу исследования видны нарушения нормативного содержания гормона роста.
Клиническое использование ДНК-рекомбинантного гормона роста человека
https://doi.org/10.14341/probl11996
Полный текст:
- Статья
- Об авторе
Аннотация
Статья посвящена вопросу клинического использования ДНК-рекомбинантного гормона роста человека.
Ключевые слова
Гормон роста, или соматотропный гормон гипофиза (СТГ), является одним из ключевых гормональных факторов в развитии организма, обладающих чрезвычайно широким спектром физиологических эффектов в тканях, главным из которых является мощное анаболическое действие, определяющее рост организма в широком понимании: это — линейный рост и прежде всего развитие костной, мышечной, сердечно-сосудистой, нервной и других систем, внутренних органов и т. д.; инсулиноподобное действие, липолитический, диабетогенный и лактогенный эффекты. Хорошо изучен механизм реализации действия СТГ в периферических тканях различной локализации, иначе называемых органами-мишенями. Эффекты СТГ опосредуются главным образом через вторичные факторы роста — инсулиноподобные факторы роста (ИФР, в основном через ИФР1) — соматомедины. Последние синтезируются главным образом печенью и почками в ответ на СТГ. Итак, нисходящая, эффекторная гормональная вертикаль сложной системы, регулирующей развитие организма, включает СТГ (гипофиз) — ростовые факторы, ИФР1 (печень) — ткани-мишени с рецепторами в клетках к СТГ и ИФРГ СТГ стимулирует, скажем, линейный рост костей как прямо, активизируя дифференцировку клеток-предшественников в эпифизарной зоне роста, так и опосредованно, индуцируя ответ клеток хряща на ИФР1 и одновременно стимулируя локальный синтез ИФР1 в зонах роста. Последний в зонах роста костей стимулирует строго лимитированный пролиферативный пул клеток хряща, которые позднее трансформируются в костные клетки. Функциональная система, регулирующая биосинтез и секрецию в кровь СТГ соматотропными клетками передней доли гипофиза, имеет сложную инфраструктуру. Ведущую роль в этой системе играет гипоталамус, где вырабатываются два нейропептида с противоположным на СТГ действием: СТГ-ингибирующий фактор, или соматостатин, и СТГ-стимулирующий фактор, или соматолиберин. Оптимальный пул этих гипоталамических рили- зинг-гормонов контролируется широким спектром нейротрансмиттеров, продуцируемых в серотонин-, норадреналин- и дофаминергических нейроцитах гипоталамуса, а также в вышерасположенных нервных образованиях ЦНС. Поэтому сон, психический стресс и особенно дистресс, физические перегрузки, множество лекарственных средств изменяют оптимальную и синхронизированную активность нейротрансмиттеров гипоталамуса, имеющую следствием нарушение секреции соматостатина и соматолиберина и как результат — нарушение секреции СТГ. Между тем для СТГ характерен четкий циркадианный ритм с максимальным уровнем ночью, причем пик СТГ регистрируется через 1 ч после наступления фазы глубокого сна. Секреция СТГ продолжается на протяжении всей жизни человека: с младенческого возраста до глубокой старости. При нарушении секреции СТГ возникает системный дефект в развитии организма и диагностируется тяжелая патология. Длительная повышенная секреция приводит к гигантизму и акромегалии, а дефицит гормона роста является главной причиной гипофизарной карликовости (гипофизарного нанизма). Настоящая статья включает краткие комментарии к использованию в клинической практике генно-инженерного гормона роста. Идеальным объектом для использования СТГ, естественно, является гипофизарный нанизм. В 70-е годы СТГ был получен путем экстракции из передней доли гипофиза трупов человека. В СССР использовался препарат «Соматотропин» производства Каунасского завода. При лечении больных гипофизарным нанизмом отмечен положительный эффект, однако быстрое нарастание титра антител к СТГ приводило к резкому снижению СТГ-подобного ростового действия препарата. Позднее было установлено, что полученные подобным образом препараты с СТГ-дей- ствием дают серьезнейшие побочные реакции, вызывая такое тяжелое, с летальным исходом неврологическое осложнение, как синдром Крейтцфельда — Якоба, что послужило основанием повсеместно запретить использование препаратов СТГ, получаемых из трупного материала. Драматическая развязка в истории с трупным гипофизарным СТГ и острая социальная потребность в гормоне роста, особенно в детской эндокринологии, стимулировали разработку технологии получения генно-инженерного СТГ различными фирмами. Первой получила ДНК-рекомби- нантный СТГ фирма «Каби Фармация» (Швеция) с трейдмаркой «Генотропин». Чуть позже успешно опробовали свои аналогичные препараты СТГ фирмы «Элай Лилли» (США) — «Хума- троп», «Арес-Сероно» (Италия) — «Сайзен», «Ново Нордиск» (Дания) — «Нордитропин». В настоящее время в нашем центре проводятся клинические испытания отечественного препарата «Соматоген» — генно-инженерного СТГ, разработанного центром «Биоинженерия» РАН. Все эти препараты СТГ обладают высокой эффективностью и безопасностью. Наш собственный опыт использования СТГ базируется на клиническом испытании генно-инженерного СТГ «Сайзен» (фирма «Арес-Сероно»). Это референтное исследование было проведено по международному протоколу при лечении детей, страдающих гипофизарным нанизмом. Эта болезнь включает различные по этиологии и патогенезу группы пациентов, поэтому уместно привести краткую характеристику нанизма. Nanos (греч.) — карлик, синонимы: карликовость, наносомия, микросомия. Нанизм — резкое отставание в росте и физическом развитии, обусловленное абсолютным или относительным дефицитом гормона роста, которое встречается при патологии собственно гипофиза (нарушение чувствительности соматотро- фов к действию СТГ-рилизинг-гормонов, нарушение биосинтеза СТГ внутри клеток), при дефиците в тканях соматомединов, прежде всего ИФР1, при дефекте в тканях-мишенях рецепторов к СТГ [1]. Следовательно, нанизм, связанный с нарушением системы СТГ — соматомедины — рецепторы, является неоднородным по этиологии и патогенезу заболеванием. У большей части таких больных диагностируется нарушение секреции большинства гипофизарных гормонов (ФСГ, ЛГ, ТТГ, пролактин). Этот синдром характеризуется сложной симптоматикой эндокринных и соматических нарушений. Гипофизарный нанизм встречается с частотой 1:30 000. Кроме истинного гипосоматотропного гипофизарного нанизма встречаются клинические формы, обусловленные генетически детерминированным дефектом продукции соматомединов или рецепторов к СТГ в тканях. Так, известны варианты псевдогипофизарного нанизма с высоким уровнем СТГ и ИФРГ Генез его связывают с дефектом рецепторов к ИФР1, что косвенно доказано резким снижением связывания кожных фибробластов с ИФРГ Наш опыт лечения в течение 12 мес детей разного возраста, страдающих гипофизарным нанизмом, показал чрезвычайно высокую эффективность генно-инженерного СТГ. Как и другие авторы, мы отмечали прибавку роста до 12 см в год. Причем чем раньше установлен диагноз и начато лечение, тем значительнее клинический результат. Международный опыт свидетельствует о том, что при истинном гипофизарном нанизме эффект, близкий к действию СТГ, можно получить с помощью инъекций ИФР1 [9]. Эти работы подчеркивают особую важность проведения диагностического поиска по протоколу, практически исключающему ошибку, поскольку, например, при дефиците ИФР1 или дефекте продукции рецепторов к СТГ, при сходной клинической картине с истинным гипофизарным нанизмом, лечение таких больных, независимо от дозы и продолжительности курсов, обречено на неуспех. Следовательно, крайне важна верификация диагноза истинного гипофизарного нанизма. В различных странах накоплен солидный клинический опыт по использованию генно-инженерного СТГ при лечении гипофизарного нанизма и синдрома Тернера. При этом, разумеется, всегда остается сфера деятельности для исследователей, в частности в области оптимизации доз гормона. курсов лечения, выбора продолжительности перерывов между курсами лечения и т. д. Эра использования генно-инженерного СТГ в эндокринологии и клинике внутренних и других болезней только начинается, ожидаются фантастические результаты. В самом деле, СТГ и ИФР1 повышают кровоток и клубочковую фильтрацию у больных с различной почечной патологией [3, 5]. Обнаружено нарушение секреции СТГ и ИФР1 у женщин с первичным бесплодием, ановуляторными циклами [7], сочетанное введение человеческого СТГ и человеческого гонадотропного гормона способствует повышенной продукции прогестерона лютеиновыми клетками [6]. СТГ усиливает овуляцию у женщин со слабым овариальным ответом на изолированное введение гонадотропина [4]. Выраженный позитивный результат — похудание — отмечен при лечении СТГ женщин с экзогенным ожирением [8]. Получены данные о роли СТГ в регуляции метаболизма миокарда при инфаркте миокарда, что открывает новые подходы к лечению и профилактике этой грозной патологии. В последнее время все чаще появляются работы, в которых показано благотворное влияние СТГ при назначении его лицам пожилого возраста. Известно, что с возрастом уровень СТГ снижается, а у пожилых лиц и людей преклонных лет он достигает минимальных показателей. Синхронно со снижением уровня СТГ атрофируется мышечная масса, уменьшается физическая сила, а следовательно, и толерантность к физическим нагрузкам, резко изменяется инфраструктура костей, как правило, повышается масса жировой ткани, снижается фильтрационная и экскреторная функция почек, частота сердечно-сосудистой патологии значительно выше у лиц с гипофункцией гипофиза. Короткий курс введения человеческого СТГ у пожилых улучшает психосоциальную адаптацию, улучшает или нормализует структуру тела, увеличивает мышечную массу и физическую силу, улучшает функцию сердца и нормализует функции почек [2]. Конечно, такие интригующие результаты благотворного действия СТГ на организм пожилых лиц открывают исключительные перспективы в области геронтологии. Разумеется, следует быть предельно осторожным в выборе доз СТГ, продолжительности курсов лечения и т. д. Необходим строго индивидуальный подход при выборе лиц для использования СТГ. Последний не может быть панацеей для восстановления функций в организме пожилых людей. Первые результаты обнадеживают, соблазнительны, но требуется архиосторожность, чтобы не повредить пожилому человеку, хотя бы и страстно, любой ценой желающему омоложения. Да и важно не скомпрометировать такой препарат, как гормон роста. Так что необходимо осторожно, терпеливо изучать оптимальные показания к применению СТГ с учетом многих хронических болезней у пожилых людей. Данный краткий обзор, думаю, убедил читателя в перспективности использования человеческого СТГ в медицине. Мы планируем организацию на базе детского отделения ЭНЦ РАМН Центра по диагностике и лечению СТГ-дефицит- ных состояний. Возможно, мы организуем такой центр совместно с одной из фирм-производителей генно-инженерного СТГ, куда мы сможем госпитализировать пациентов независимо от территориальной принадлежности и где мы будем располагать всем необходимым для быстрого диагностического поиска и выбора оптимальных комбинаций лечения больных с различной эндокринной патологией.
Список литературы
1. Amselem S. et al. // International Symposium on Growth and Growth Disorders, 11-th.- Stockholm, 1991.- P. 81-86.
2. Christiansen J. S., Jorgensen J. 0. L. // Acta endocr. (Kbh.).- 1991.- Vol. 125.- P. 7-13.
3. Hirschberg R., Rabb H., Bergamo R., Kopple J. D. // Kidney int.- 1989.- Vol. 35.- P. 865-870.
4. Ibrahim Z. H. Z., Matson P. L., Buck P., Lieberman B. A. // Fertil. and Steril.- 1991.- Vol. 55, N 1.- P. 202-204.
5. Kopple J. D., Hirschberg R. // Miner. Electrolyte Metab.- 1990.- Vol. 16.- P. 82-88.
6. Lanzone A., Simone N. D., Castellani R. et al. // Fertil. and Steril.- 1992.- Vol. 57, N 1.- P. 92-96.
7. Ovesen P., Moller J., Moller N. et al. // Ibid.- P. 97-101.
8. Skaggs S. R., Crist D. M. // Horm. Res.- 1991.- Vol. 35.- P. 19-24.
9. Wilton P., Sietnieks A. et al. // International Symposium on Growth Disorders, 11-th.- Stockholm, 1991.- P. Ill — 115.
Об авторе
И. И. Дедов
Эндокринологический научный центр РАМН
Россия
Рецензия
Просмотров: 1789
Описание препарата
Marten воздействует на эндогенный человеческий гормон роста.
Гормон роста Marten поможет вам залечить давние и текущие травмы, сжечь подкожный жир.
Marten может:
- ускорять синтез протеина во всем организме;
- стимулировать синтез иммунного глобина;
- увеличивает способность к сопротивлению инфекциям;
- стимулирует разрастание коллагеноцита, ускоряет заживление ран;
- ускорять синтез кардиоцитов, улучшать сократительную способность сердца и снижает потребление медицинского кислорода сердца;
- подавляет холестерин сыворотки крови и снижает уровень плотности протеина;
- восполняет недостаток или отсутствие гормона роста, регулирует жировой обмен, остеометаболизм, сердечную функцию и почечную функцию у взрослых.
Применение гормона роста MARTEN МАРТЕН:
Применения гормона роста Marten в совокупности с иными препаратами, поможет вам перейти тот максимум ваших способностей в силовых тренировках, а в частности увеличить силовые показатели, придать рельефную структуру вашего тела, создать рельефность, набрать качественную мышечную массу и т.д.!
Гормон Роста получил широкое применение во всем мире за свои уникальные свойства, в бодибилдинге, пауэрлифтинге, фитнесе, в различных единоборствах! Многие девушки желая преобразиться, сбросить лишние килограммы, сжечь жир, омолодиться, применяют гормон роста! Для профилактических и лечебных действий, достаточно небольшого количества применения гормона роста, чтобы почувствовать прилив сил, энергии, омолаживающий эффект и качественный результат.
Форма выпуска:
2 флакона 5 мл по 50МЕ (16,5мг) соматотропного гормона роста в стабильной жидкой форме в буферном, антибактериальном растворе со стабилизаторами
Условия хранения:
В защищенном от света месте при температуре от 2 °С до 8 °С. Не замораживать. Биологическая активность при хранении соматропина при комнатной температуре (15-25С) в течение до 4-х недель не снижается, и все же следует предпочесть прохладное место (2-8С). Хранить в недоступном для детей месте.
{{ isErrorSetToBasket === false ? ‘Товар добавлен вкорзину’ : ‘Не удалось добавить товар в корзину’}}
Перейти в корзину
{{Object.keys(error)[0]}}:
{{Object.values(error)[0]}}
Продолжить покупки
{{isErrorSetToBasket === true && countBasket != 0 ? » : `(${countBasket})`}}

Цена По запросу
Количество
Вы уже добавили максимально доступное на складе кол-во товара
Достигнуто максимально доступное кол-во
Под заказ
{{!!storageProduct ? ‘На складе’ : ‘Под заказ’}}
Ожидается поставка
Скачать каталог «ХИММЕД» в формате pdf

Химические реактивы

Лабораторное оборудование

Аналитическое оборудование
Биохимия

Проектирование лабораторий
Материалы для микроэлектроники
Для уточнения данных о стоимости и наличии товаров, пожалуйста, обращайтесь к
менеджерам по продажам.
Похоже, что-то пошло не так.
Попробуйте перезагрузить страницу.
×
Авторизация прошла успешно.