Со стороны органов кроветворения: тромбоцитопения развивается спустя 4 недели, лейкопения спустя 5-6 недель после применения препарата и может продолжаться 1-2 недели. Обычно тромбоцитопения имеет более тяжелый характер, чем лейкопения. Реже наблюдается анемия и гранулоцитопения.
Ломустин может вызывать кумулятивную миелосупрессию, причем после приема повторных доз может отмечаться более выраженное подавление костного мозга, или же продолжительность миелосупрессии может быть большей.
Со стороны органов пищеварения: тошнота и рвота (через 3-6 часов после приема ломустина, обычно продолжаются до 24 ч), анорексия. Частота и продолжительность этих побочных эффектов могут быть снижены за счет профилактического применения противорвотных препаратов, а также путем назначения ломустина больным натощак. Редко — диарея, стоматит, повышение активности печеночных ферментов и концентрации билирубина.
Со стороны органов дыхания: редко — кашель, дыхательная недостаточность, сопутствующие появлению инфильтратов и/или фиброза легких (отмечалось через 6 мес или через более длительные сроки после начала лечения при суммарных дозах препарата более 1100 мг/м2. Сообщалось об одном случае легочной токсичности при кумулятивной дозе 600 мг/м2).
Со стороны нервной системы: дезориентация, летаргия, атаксия, расстройство артикуляции речи, повышенная утомляемость.
Со стороны мочевыделительной системы: задержка мочи, отеки стоп или нижних конечностей, азотемия, уменьшение размеров почек (обычно при высоких кумулятивных дозах препарата в условиях продолжительного лечения ломустином и другими препаратами нитрозомочевины).
Со стороны репродуктивной системы: азооспермия (в некоторых случаях необратимая), аменорея.
Прочие: редко — алопеция, необратимое поражение зрительных нервов, приводящее к слепоте (при сочетании с лучевой терапией головного мозга). Сообщалось об острых лейкемиях и дисплазиях костного мозга в результате лечения препаратами нитрозомочевины.
Ломустин медак — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
П N016023/01
Торговое наименование препарата
Ломустин медак
Международное непатентованное наименование
Ломустин
Лекарственная форма
капсулы
Состав
Каждая капсула содержит
Активное вещество: Ломустин — 40 мг.
Вспомогательные вещества: лактозы моногидрат 100 мг, крахмал пшеничный 40 мг, тальк 16 мг, магния стеарат 4 мг.
Оболочка капсулы: желатин 49 мг, титана диоксид (Е171) 0,5 мг, индигокармин (Е132) 0,06 мг.
Описание
Твердые желатиновые капсулы № 3 с корпусом и крышечкой голубого цвета. Содержимое капсулы — порошок от белого до светло-желтого цвета, возможно наличие вкраплений желтого цвета.
Фармакотерапевтическая группа
Противоопухолевое средство — алкилирующее соединение
Код АТХ
L01AD
Фармакодинамика:
Ломустин — противоопухолевый препарат алкилирующего действия из группы нитрозомочевины. Механизм действия заключается в алкилировании ДНК и РНК, а также ингибировании отдельных этапов синтеза нуклеиновых кислот и репарации отдельных разрывов цепи ДНК. Ингибирование синтеза ДНК обусловлено карбамоилированием ДНК-полимеразы и других ферментов репарации ДНК, и повреждением ДНК-матрицы. Препарат также может тормозить ключевые ферментативные процессы путем изменения структуры и функции многих белков и ферментов. Ломустин действует в поздней фазе G1 и ранней S-фазе клеточного цикла. Наиболее высокая чувствительность к ломустину у клеток в стационарной фазе роста (фактор, определяющий активность при солидных опухолях с низким пролиферативным пулом).
Фармакокинетика:
После приема внутрь быстро и практически полностью всасывается из желудочно-кишечного тракта. Максимальная концентрация в плазме крови (0,5-2 нг/мл) достигается в среднем через 3 часа после перорального приема дозы препарата 30-100 мг/м2.
Связь с белками плазмы — 50 %. Проникает через гематоэнцефалический барьер. После перорального введения ломустина, меченого радиоизотопной меткой, радиоактивность в спинномозговой жидкости составляет от 15 до 30 % радиоактивности, измеренной в плазме.
Быстро метаболизируется в печени с образованием активных метаболитов (оксиметилдиазония и изоцианата). Оксиметилдиазоний ионизируется и превращается в ион метилдиазония, который трансформируется в более устойчивую таутомерную форму (диазометан), либо распадается на метилкарбониевый ион и азот.
Хлорэтильная группа выводится из плазмы однофазно с периодом полувыведения 72 часа. Выведение циклогексильной группы является двухфазным с периодом полувыведения T1/2α= 4 часа и Т1/2β = 50 часов. Выводится преимущественно почками в виде метаболитов, менее 5 % — через кишечник. Активная форма ломустина в моче не обнаруживается.
Показания:
Ломустин применяется в ионотерапии и в комбинированной терапии (в том числе в комбинации с лучевой терапией и хирургическим лечением) следующих заболеваний:
— первичные и метастатические опухоли мозга,
— рак легкого (особенно мелкоклеточный),
— лимфогранулематоз (болезнь Ходжкина), резистентный к стандартной химиотерапии,
— злокачественная метастатическая меланома.
Ломустин медак может также применяться в терапии множественной миеломы, рака желудка и кишечника, рака почки.
Противопоказания:
— Повышенная чувствительность к ломустину и другим компонентам препарата, другим производным нитрозомочевины, в том числе в анамнезе;
— Ранее выявленная резистентность опухоли к производным нитрозомочевины;
— Выраженное подавление функции костного мозга;
— Тяжелая почечная недостаточность;
— Целиакия или аллергия на пшеницу;
— Совместное применение с вакциной желтой лихорадки или другими живыми вакцинами у пациентов со сниженным иммунным статусом;
— Беременность и период кормления грудью.
С осторожностью:
У пациентов с миелосупрессией и пониженной концентрацией тромбоцитов, лейкоцитов, эритроцитов в крови; ветряная оспа (в т.ч. недавно перенесенная или после контакта с заболевшими), опоясывающий герпес и другие острые инфекционные заболевания вирусной, грибковой или бактериальной природы; кахексия, интоксикации, почечная и/или печеночная недостаточность, дыхательная недостаточность, лечение цитостатиками и лучевая терапия в анамнезе, непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция (т.к. препарат содержит лактозу).
Беременность и лактация:
Беременность
Препарат противопоказан при беременности. В доклинических исследованиях ломустин проявлял эмбриотоксическое и тератогенное действие. Пациентки, применяющие препарат, должны быть осведомлены о потенциальной опасности для плода в случае, если беременность наступает во время лечения препаратом Ломустин медак. Женщинам детородного возраста необходимо избегать наступления беременности. В случае наступления беременности на фоне приема препарата пациентке следует проинформировать об этом своего лечащего врача.
Период грудного вскармливания
Так как ломустин обладает липофильными свойствами, есть основания полагать, что он проникает в грудное молоко. Учитывая риск негативного воздействия на ребенка, следует тщательно взвесить ожидаемую пользу лечения для матери и потенциальный риск для ребенка и принять решение о прекращении грудного вскармливания или о прекращении лечения ломустином.
Способ применения и дозы:
Ломустин следует принимать внутрь вечером, перед сном или через 3 часа после приема пищи.
В профилактических целях рекомендуется применение совместно с ломустином антиэметиков.
Рекомендуемая доза ломустина у взрослых и детей с нормальной функцией костного мозга составляет 120-130 мг/м2 при однократном приеме внутрь каждые 6-8 недель. Данную дозу можно разделить на три приема в течение трех последовательных дней.
У пациентов со сниженной функцией костного мозга дозу можно снизить до 100 мг/м2 при сохранении шестинедельного интервала между приемами.
Кумулятивная миелосупрессия может потребовать более продолжительного интервала между приемом препарата.
Перед каждым очередным приемом ломустина следует проводить общий анализ крови и при необходимости корректировать дозу препарата.
Дозу необходимо уменьшить в случае, если:
— препарат применяется в составе схемы терапии, в которую входят другие препараты с миелосупрессивными свойствами:
— при лейкопении ниже 3000/мкл или тромбоцитопении ниже 75000/мкл.
R случае комбинированной терапии препарат применяют в дозе 70-100 мг/м2.
При применении ломустина подавление функции костного мозга является более продолжительным, чем после воздействия соединений трихлортриэтиламина, восстановление содержания лейкоцитов и тромбоцитов может происходить в течение 6 недель и более. Повторные курсы не следует назначать при количестве тромбоцитов менее 100000/мкл и лейкоцитов менее 4000/мкл. Дальнейшие дозы препарата должны подбираться в зависимости от гематологического ответа пациента на предыдущую дозу. При подборе доз можно ориентироваться на следующую схему:
|
Минимальные показатели после приема предыдущей дозы |
Рекомендуемая следующая доза (% от предыдущей дозы) |
|
|
Лейкоциты/мкл |
Тромбоциты/мкл |
|
|
3000-4000 |
75000-100000 |
100% |
|
2000-2999 |
25000-74999 |
70% |
|
Менее 2000 |
Менее 25000 |
50% |
Применение у детей
Применение препарата для лечения детей с онкологическими заболеваниями должно проводиться только в специализированных центрах и только после оценки соотношения ожидаемой пользы лечения к потенциальному риску.
Побочные эффекты:
Частота побочных реакций, приведенных ниже, изложена в соответствии со следующей градацией: очень часто (≥ 1/10), часто (≥1/100, < 1/10); нечасто (≥1/1000, < 1/100); редко (≥1/10000, < 1/1000); очень редко (< 1/10000), частота неизвестна (не может быть определена на основании имеющихся данных).
Нарушения со стороны крови и лимфатической системы
Очень часто: угнетение костномозгового кроветворения, тромбоцитопения, лейкопения, анемия.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы)
Частота неизвестна: сообщалось о развитии острого лейкоза и дисплазии костного мозга у пациентов, в течение длительного времени получавших препараты нитрозомочевины.
Нарушения со стороны желудочно-кишечного тракта
Очень часто: тошнота, рвота, анорексия.
Редко: диарея, стоматит.
Нарушения со стороны печени и желчевыводящих путей
Часто: нарушение функции печени (в большинстве случаев легкой степени выраженности).
Редко: холестатическая желтуха, печеночная недостаточность.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Редко: интерстициальная пневмония, инфильтративные процессы, фиброз легких.
Нарушения со стороны нервной системы
Редко: нарушение координации, спутанность сознания, сонливость, апатия, расстройство артикуляции речи, заикание (сообщалось о развитии этих симптомов при проведении комбинированной терапии с применением других противоопухолевых средств и лучевой терапии).
Нарушения со стороны ночек и мочевыводящих путей
Частота неизвестна: почечная недостаточность, прогрессирующая азотемия, уменьшение размеров (атрофия) почек.
Нарушения со стороны колеи и подкожных тканей
Редко: алопеция.
Нарушения со стороны органа зрения
Очень редко: поражение зрительных нервов (при сочетании с лучевой терапией опухолей головного мозга), необратимая потеря зрения.
Влияние на результаты лабораторных и инструментальных исследований
Частота неизвестна: повышение активности печеночных ферментов (аспартатаминотрансферазы (ACT), аланинаминотрансферазы (АЛТ), лактатдегидрогеназы (ЛДГ), щелочной фосфатазы), повышение концентрации билирубина в сыворотке крови.
Основным нежелательным побочным эффектом ломустина является отсроченная или пролонгированная миелотоксичность, которая обычно проявляется через 4-6 недель после приема препарата и носит дозозависимый характер. Тромбоцитопения наблюдается приблизительно через 4 недели после приема дозы ломустина и обычно сохраняется на уровне 80000 — 100000/мкл в течение 1-2 недель. Через 5-6 недель появляется лейкопения (около 4000 — 5000/мкл), которая сохраняется в течение одной или двух недель. Реже наблюдается анемия, однако, по сравнению с тромбоцитопенией и лейкопенией, она наблюдается реже и протекает в менее тяжёлой форме.
Гематологическая токсичность может иметь кумулятивный характер, причем после приема повторных доз может отмечаться более выраженное подавление функции костного мозга. Приблизительно у 65 % пациентов, получающих препарат в дозе 130 мг/м2, концентрация лейкоцитов снижалась до уровней менее 5000/мкл. У 36 % пациентов этот показатель составил менее 3000/мкл. Как правило, тромбоцитопения носит более тяжелый характер, чем лейкопения; однако, оба вида токсичности могут оказаться дозолимитирующими.
Тошнота и рвота обычно проявляются через 4-6 ч после введения полной разовой дозы ломустина и продолжаются 24-48 ч, анорексия обычно продолжается в течение 2-3 дней. Выраженность этих побочных явлений может быть уменьшена путем разделения разовой дозы, рассчитанной на 6 недель, натри приема в первые три дня каждого 6-недельного цикла. Обычно препарат хорошо переносится, если его применение сопровождается профилактическим приемом противорвотных средств (например, метоклопрамида или хлорпромазина).
В единичных случаях после продолжительного лечения ломустином и другими препаратами нитрозомочевины при достижении высокой кумулятивной дозы наблюдались почечная недостаточность, прогрессирующая азотемия, уменьшение размеров (атрофия) почек. В связи с этим рекомендуется не превышать максимальную общую кумулятивную дозу ломустина 1000 мг/м2. Однако, необходимо учитывать, что поражение почек возможно также у пациентов, получавших более низкие кумулятивные дозы препарата.
Передозировка:
Сообщалось о случаях передозировки ломустином, включая смертельные исходы.
Возможные симптомы при передозировке: миелотоксичность. гематологическая токсичность, боль в абдоминальной области, тошнота, рвота, диарея, анорексия, сонливость, головокружение, нарушение функции печени, кашель, одышка. Антидот не известен. При передозировке следует немедленно провести промывание желудка. Лечение симптоматическое. При наличии клинических показаний следует предпринять меры для восполнения потери форменных элементов крови.
Взаимодействие:
Миелотоксичность ломустина может усиливаться при его совместном использовании с теофиллином или циметидином, являющимся анатагонистом Н2-рецепторов. Для ломустина характерна перекрестная резистентность с другими производными нитрозомочевины, которая не наблюдается в отношении других алкилирующих средств.
Фенобарбитал, активирующий микросомальные ферменты печени, может усиливать метаболизм ломустина и ускорять его выведение из организма, поэтому применение фенобарбитала перед ломустином может снизить противоопухолевую активность последнего.
Применение вакцины против желтой лихорадки повышает риск системных поствакцинальных осложнений, в том числе с летальным исходом. Пациентам, проходящим иммуносупрессивную терапию, противопоказано применение живых вакцин.
Совместное применение противоэпилептических и химиотерапевтических препаратов, включая ломустин, может вызвать осложнения, вызванные фармакокинетическим взаимодействием между препаратами.
Одновременное применение ломустина с другими цитостатическими препаратами и радиотерапией может усиливать миелотоксичность ломустина. Ломустин при совместном применении с амфотерицином В может усиливать токсичность последнего.
Особые указания:
Лечение Ломустином медак должен проводить врач-онколог, имеющий опыт проведения противоопухолевой терапии.
Пациентов необходимо обязательно проинформировать о том, что разовую дозу препарата следует принимать внутрь один раз в 6 недель, в течение которых нельзя принимать повторные дозы, а также о недопустимости приема препарата в дозах, превышающих назначенные врачом.
Наиболее распространенный и тяжелый токсический эффект ломустина — отсроченное подавление функции костного мозга, проявляющееся в первую очередь тромбоцитопенией и лейкопенией, которые могут привести к развитию кровотечений и инфекций у ослабленных пациентов. Поэтому до начала приема препарата и в течение всего курса лечения (раз в неделю как минимум в течение 6 недель после приема препарата) необходимо проводить развернутый клинический анализ крови.
При назначении терапии ломустином и определении дозы следует руководствоваться главным образом значениями концентрации гемоглобина, лейкоцитов и тромбоцитов в сыворотке крови. Миелосупрессия, вызываемая ломустином, является кумулятивной, поэтому очередную дозу следует подбирать с учетом минимального значения концентрации форменных элементов крови, наблюдавшегося после последнего приема препарата. Применение ломустина потенциально может привести к нарушению функции печени, почек. Необходимо периодически контролировать функцию печени и почек.
Легочная токсичность ломустина носит дозозависимый характер. До начала и в процессе лечения необходимо регулярно контролировать функцию легких. Пациенты со сниженными менее 70 % исходными значениями форсированной жизненной емкости легких, а также диффузионной способности легких по поглощению оксида углерода (DLco), входят в группу особого риска.
Сообщалось о возможной взаимосвязи развития вторичных злокачественных новообразований с длительным применением препаратов нитрозомочевины.
Фертильность
Мужчинам и женщинам детородного возраста во время лечения и, как минимум, в течение 6 месяцев после его окончания необходимо применять надежные методы контрацепции.
Пациенты мужского пола должны быть проинформированы о риске необратимого наступления бесплодия в результате лечения ломустином.
При обращении с ломустином, как и с любыми другими противоопухолевыми препаратами, необходимо соблюдать осторожность. Не вскрывать капсулы. Следует избегать контакта содержимого капсул с кожей и слизистыми оболочками. При контакте с порошком препарата необходимо использовать специально выделенные для этого материалы, пользоваться перчатками, после контакта следует утилизировать использованные материалы и вымыть руки водой с мылом.
Влияние на способность управлять транспортными средствами и механизмами:
Препарат может оказывать влияние на способность управлять автомобилем и использовать механизмы ввиду риска развития тошноты и рвоты. При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Форма выпуска/дозировка:
Капсулы 40 мг.
Упаковка:
По 20 капсул в пластиковой банке с контролем первого вскрытия. 1 банка вместе с инструкцией по применению в картонной пачке.
Условия хранения:
В защищенном от света месте при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Срок годности:
3 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
медак ГмбХ, Theaterstrasse 6, 22880 Wedel, Germany, Германия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
медак ГмбХ
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Introduction
Glioblastoma is the most aggressive glioma (WHO Grade IV) and is associated with a uniformly poor prognosis (1). The current standard treatment for glioblastoma (GBM) consists of a multimodality approach which includes maximal surgical resection and radiotherapy with concurrent temozolomide, followed by cycles of adjuvant chemotherapy (2). Despite multimodality treatments, recent clinical trials have reported a median survival of only 14–16 months with a 2-year survival rate of 26–33% (2, 3). There is therefore an urgent need to explore new therapeutic strategies to improve patient prognosis.
Glioblastoma multiforme is a highly vascularized tumor where the vascular endothelial growth factor (VEGF) pathway is up-regulated, and it has been hypothesized that GBM would respond well to antiangiogenic treatments (4). Bevacizumab (BEV) is an antibody against the vascular endothelial growth factor receptor (VEGF) and a common therapy used for colorectal, lung, breast, kidney, and ovarian cancers (5–7). In 2009, bevacizumab was approved by the Food and Drug Administration for use as a treatment of recurrent glioblastoma (8). Despite obvious radiographic responses and an observed increase in progression-free survival (PFS), some clinical studies which investigated BEV reported that treatment has not resulted in a durable overall survival (OS) benefit in either recurrent or newly diagnosed GBM (9–12).
In a phase III study, enzastaurin was compared with lomustine, an alkylating agent of the nitrosourea family that is widely used as a salvage treatment drug, and lomustine was found to be more effective in treating GBM, suggesting that nitrosourea plays an important role in the treatment of recurrent GBM (13). A previous meta-analysis (14) study explored the efficacy of bevacizumab plus lomustine treatment in progressive glioblastoma, but the studies included were so few that the results were controversial, and the correlation subgroup analysis was incomplete. Thus, a further statistical analysis is needed to increase the credibility of this treatment combination.
Materials and Methods
This meta-analysis was performed according to the Cochrane Handbook for Systematic Reviews of Interventions and is presented based on the Preferred Reporting Items for Systematic Reviews and Meta-analyses guidelines. The protocol for this meta-analysis is available in PROSPERO (CRD42020190739).
Inclusion Criteria
Studies that met the following criteria were included in the meta-analysis: Population: recurrent GBM adult patients (≥18 years old), with a Karnofsky Performance Status score ≥50 or a WHO Performance Status score between 0 and 2, were used. Intervention: lomustine plus bevacizumab; Comparison: monotherapy of bevacizumab, lomustine, or bevacizumab plus irinotecan. Outcome: the outcomes of interest were OS and PFS or 6-month PFS, and their corresponding 95% confidence intervals (CIs) were provided; Non-English language literature was excluded. In addition, when we found duplicated or overlapping data in multiple reports, we included the one with the most complete information.
Search Strategy
Two investigators independently searched the electronic databases PubMed, EMBASE, and the Cochrane Library for relevant literature published up until June 2020. The search syntax included the following text words: “glioblastoma,” “bevacizumab,” “lomustine,” and “CCNU.” The detailed search strategy is available in the Supplementary Material.
Data Extraction
All data were reviewed and separately computed by two independent investigators. The following information was extracted from each trial: median OS, median PFS, 6-month PFS, study design, control group measures, isocitrate dehydrogenase (IDH) status, promoter of O6-methylguanine-DNA-methyltransferase (MGMT) status, Karnofsky Performance Status or WHO Performance Status score, drug dose, and the number and age of the patients in the experimental and control arms.
Quality Assessment
Two investigators separately rated the quality of the retrieved studies. We chose the risk-of-bias items recommended by The Cochrane Handbook for Systematic Reviews of Interventions for randomized controlled trials (RCTs). Items were evaluated in three categories: low risk of bias, unclear bias, and high risk of bias. In addition, we used the Methodological Index for Non-Randomized Studies (MINORS) for other clinically controlled trials.
Statistical Analysis
The statistical analyses were performed using the Review Manager Version 5.3 software (RevMan; The Cochrane Collaboration, Oxford, UK). The end points of interest in the pooled analysis were OS, PFS, and 6-month PFS. Because the outcome index is a continuous variable, the mean difference (MD) was used as the effect index. Heterogeneity across studies was examined using the I2 statistic (15). Studies with an I2 of 25–50%, 50–75%, or >75% were considered to have low, moderate, or high heterogeneity, respectively (16). We used the random-effects model of statistical analysis and a value of p < 0.05 indicated statistical significance. In addition, we did a subgroup analysis based on dose and measures in the control groups in order to analyze the factors that influence disease response and a sensitivity analysis to find the sources of heterogeneity.
Results
Overview of the Literature Search
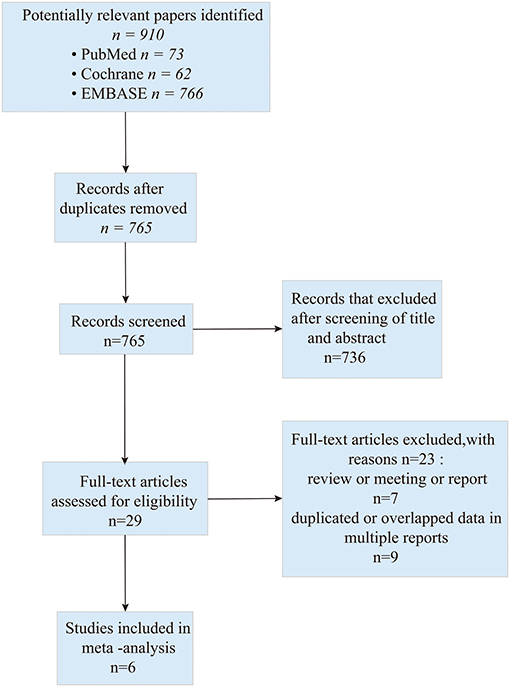
A total of 901 studies were retrieved initially for the evaluation. We did the initial screening based on the title and abstract, and 29 publications were chosen for further analysis. Eventually, six studies (one of the studies was split into two groups) (17–22) which addressed the combination of bevacizumab and lomustine in treating GBM were included in this study. The search process is described in Figure 1.
Figure 1. Flow diagram of study selection based on the PRISMA statement.
Study Characteristics and Bias Risk Assessment Results
All included studies in this study were based on moderate to high-quality evidence. The primary characteristics of the six studies are detailed in Table 1. Of the six studies included, four were RCTs and two were non-RCTs. According to the type of study, we used The Cochrane Handbook for Systematic Reviews of Interventions and MINORS to assess the risk of bias, respectively. The results of the quality assessment results are shown in the Supplementary Tables 1, 2.
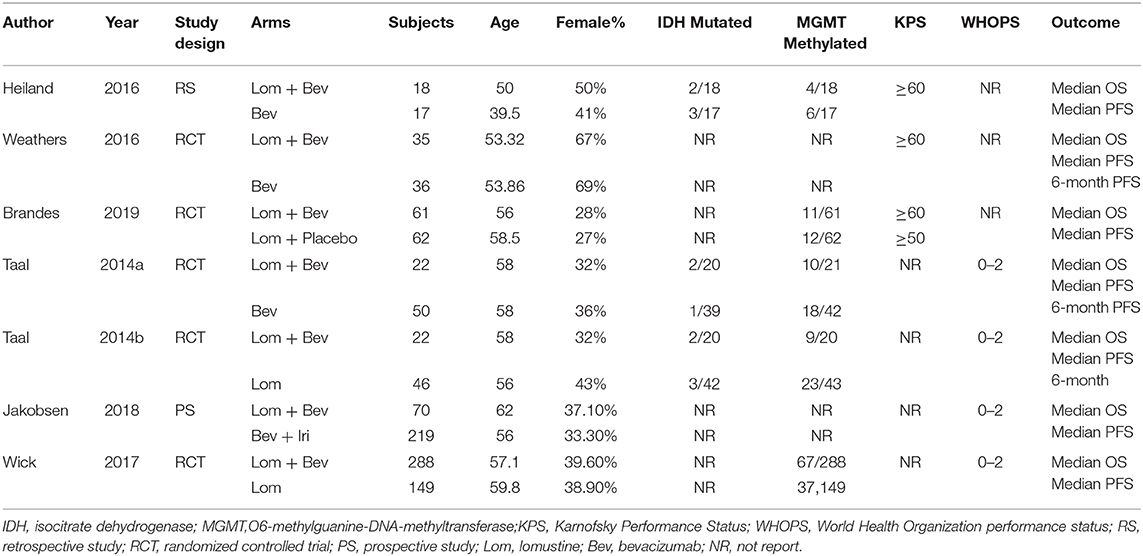
Table 1. Basic characteristics of patients in the included studies.
Clinical Effect With the Combination of Bevacizumab and Lomustine in GBM
Pooled Analysis of OS
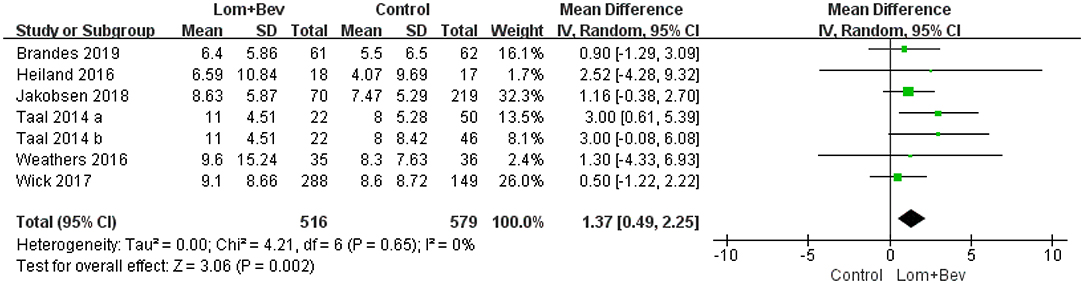
Pooling the OS data from the six studies (17–22) showed that bevacizumab combined with lomustine did prolong OS (MD =1.37; 95% CI, 0.49–2.25; p = 0.002) when compared to OS in the bevacizumab or lomustine monotherapy groups and the bevacizumab plus irinotecan group (Figure 2).
Figure 2. Forest plot of OS in glioblastoma between lomustine plus bevacizumab and control groups. OS, overall survival; Lom, lomustine; Bev, bevacizumab.
Pooled Analysis of PFS and Sensitivity Analysis
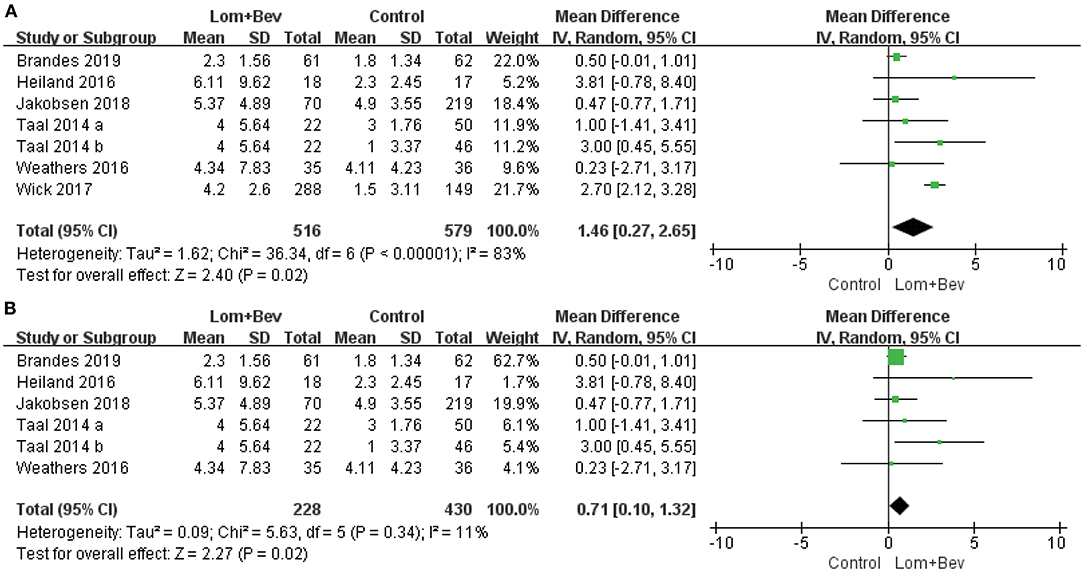
A random effects model was used to pool the PFS data (17–22). Despite the high degree of heterogeneity (I2 = 83%), the pooled data showed that the combination of bevacizumab and lomustine resulted in longer PFS (MD = 1.46; 95% CI, 0.27–2.65; p = 0.02) than in the control groups. We then looked for heterogeneous sources based on the sensitivity analysis. The results showed a significant decrease in heterogeneity (I2 = 11%) when the study of Wick (20) was removed and still had statistical significance (p = 0.02). This data indicates the results were robust (Figure 3).
Figure 3. Forest plot of PFS in glioblastoma between lomustine plus bevacizumab and control groups. (A) All of the studies were included. (B) The study of Wick was removed. PFS, progression-free survival; Lom, lomustine; Bev, bevacizumab.
Pooled Analysis of 6-Month PFS
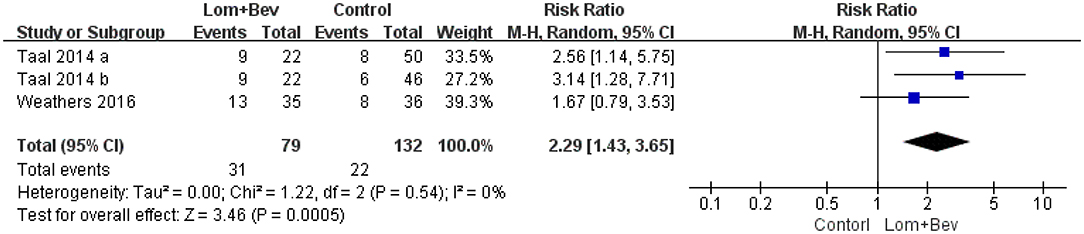
Pooling the 6-month PFS data from two of the studies (17, 19) showed that bevacizumab plus lomustine did improve the 6-month PFS (RR = 2.29; 95% CI, 1.43–3.65; p < 0.0005) compared with that in the bevacizumab or lomustine monotherapy groups (Figure 4).
Figure 4. Forest plot of 6-month PFS in glioblastoma between lomustine plus bevacizumab and control groups. Six-month PFS, the percentage of patients who could progression-free survival for 6 months; Lom, lomustine; Bev, bevacizumab.
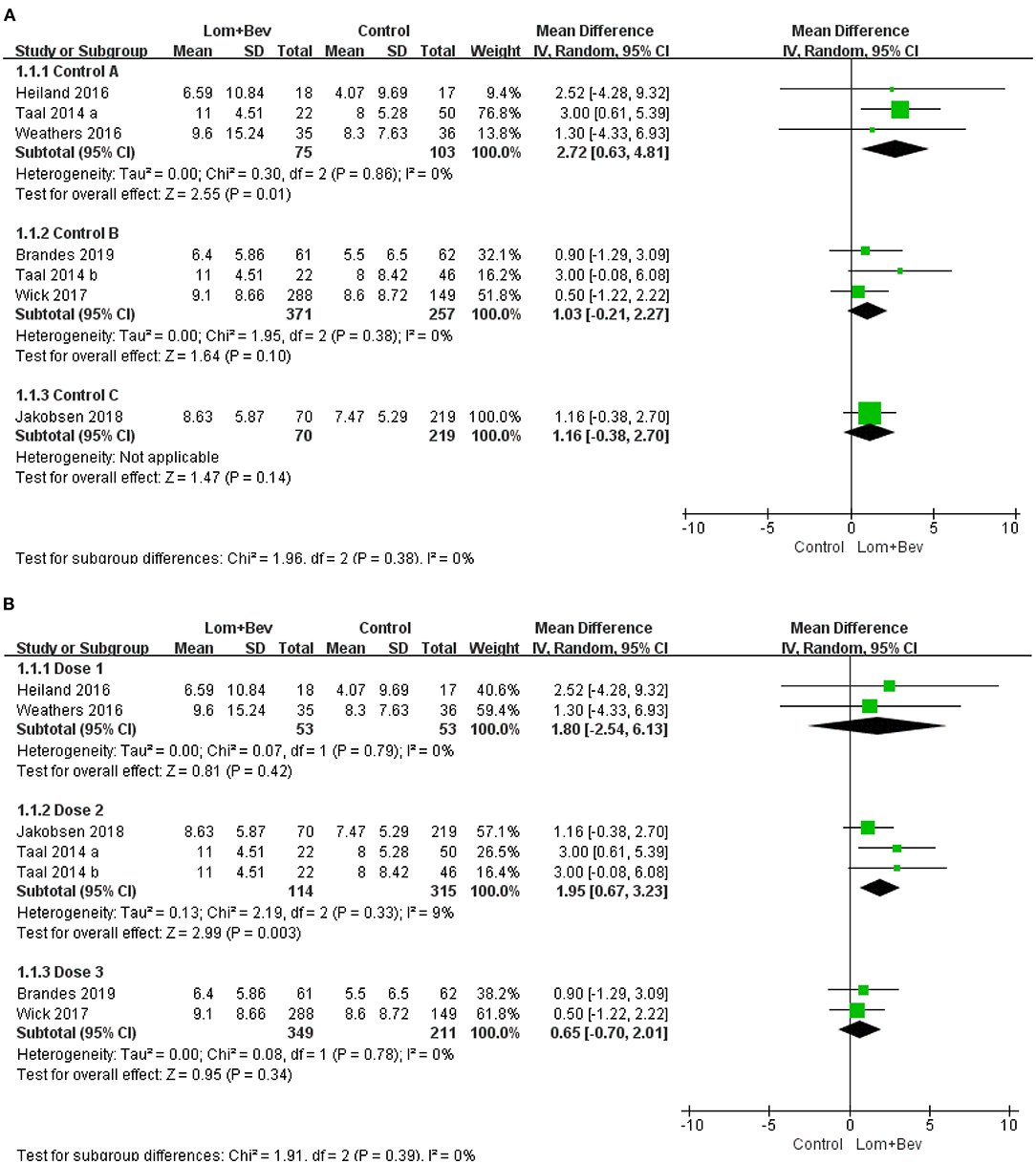
Subgroup Analysis of OS
First, we divided the patient data into Control group A (bevacizumab monotherapy; MD = 2.72; 95% CI, 0.63–4.81; p = 0.01), Control group B (lomustine monotherapy or lomustine plus placebo; MD = 1.03; 95% CI, −0.21 to 2.27; p = 0.10), and Control group C (bevacizumab plus irinotecan; MD = 1.16; 95% CI, −0.38 to 2.7; p = 0.14). Only Control group A showed statistical significance. Based on the different doses used in each study, we then divided the patients into Dose group 1 [Bev (5 mg/kg every 3 weeks) + Lom (90 mg/m2 every 6 weeks)]; MD = 1.80; 95% CI, −2.54 to 6.13; p = 0.42, Dose group 2 [Bev (10 mg/kg every 2 weeks) + Lom (90 mg/m2 every 6 weeks)]; MD = 1.95; 95% CI, 0.67−3.23; p = 0.003, and Dose group 3 [Bev (10 mg/kg every 2 weeks) + Lom (90–200 mg/m2 every 6 weeks)]; MD = 0.65; 95% CI, −0.70 to 2.01; p = 0.34. The results show that only the results of Dose group 2 had statistical significance. A forest plot of all subgroup analyses is shown in Figure 5.
Figure 5. Subgroup analysis of OS in glioblastoma according to (A) different control groups, (B) different dose groups. Control group A, bevacizumab monotherapy; Control group B, lomustine monotherapy or lomustine plus placebo; Control group C, bevacizumab plus irinotecan; Dose1, Bev(5 mg/kg every 3 weeks) + Lom(90 mg/m2 every 6 weeks); Dose2, Bev (10 mg/kg every 2 weeks) + Lom (90 mg/m2 every 6 weeks); Dose3, Bev(10 mg/kg every 2 weeks) + Lom (90–200mg/m2 every 6 weeks).
Discussion
Glioblastoma (GBM) is one of the most aggressive brain cancers in adults (2). Despite surgical treatment and chemotherapy options, the prognosis for patients remains poor (23). Bevacizumab, a monoclonal antibody against VEGF-A, used alone or in combination with cytotoxic drugs, showed interesting results in terms of radiographic response rates and PFS in initial phase 2 studies of GBM (11, 24). However, these studies lacked a non-bevacizumab control group and OS did not increase with the experimental group compared to the control group. Another study showed that early treatment with bevacizumab improved PFS, but not OS, again suggesting that the treatment with bevacizumab alone might not be sufficient in improving GBM patient prognosis (25). Thus, we looked for another drug to combine with bevacizumab to improve OS and chose lomustine, a DNA alkylating agent. Lomustine is an approved treatment option for recurrent GBM and has also been frequently administered in clinical trials as the standard treatment (26).
In our study, lomustine plus bevacizumab showed a positive effect not only on PFS but also on OS in GBM patients. In addition, we found that the combination significantly improved 6-month PFS in GBM patients. These results are different to a previous meta-analysis (14) study which had explored the efficacy of lomustine plus bevacizumab in progressive GBM and which showed that treating patients with bevacizumab and lomustine could improve PFS significantly compared to control groups. However, there was no significant difference on OS. Because the previous study (14) did not provide a subgroup analysis, we performed some subgroup analyses based on the different control groups and drug doses to determine whether the results from the six studies included in our study, were comparable.
It is a remarkable fact that the dose selection we obtained through the subgroup analysis is different from previous study (27) results. The previous study (27) emphasized that the potential negative consequences of higher doses of bevacizumab are related to the promotion of tumor hypoxia, a well-known therapeutic tolerant medium, and the promotion of the aggressive phenotype of GBM. Furthermore, in a retrospective analysis, bevacizumab at low dose strength (<5 mg/kg/week) can improve PFS and OS better than bevacizumab at normal dose strength, and for patients with high-grade glioma, there was an inverse relationship between the dose intensity of bevacizumab and OS (r = 0.48, p > 0.00001) (28). It was hypothesized that lower doses of anti-angiogenic therapy may potentially improve the delivery of chemotherapeutic drugs and ultimately improve the prognosis of patients. However, in our study, the improvement in survival outcomes was more pronounced in Dose group 2 than in Dose group 1, which suggests that the bevacizumab dose may not be inversely related to OS. Moreover, based on the results of Dose group 3, we concluded that at the same dose of bevacizumab, an excessive dose of lomustine may be detrimental to OS. Although this study shows that Dose group 2 resulted in the best outcomes, the grouping is still not detailed enough. In future trials, more doses should be tested to determine the best dose combination, and the corresponding adverse reactions.
The mechanism behind the observed increase in OS, PFS, and 6-month PFS, when patients are treated with both lomustine and bevacizumab, is still not completely clear. It has been proposed that the normalization of vessels around the tumor, improvement of regional cerebral blood flow, augmentation of the antitumor effects of chemotherapy and radiotherapy are key components of the antiangiogenic activity (29–31), but more studies are needed.
Since there are not enough clinical studies on lomustine combined with bevacizumab in the treatment of GBM, only six studies were included. There may be some bias in these conclusions and a more systematic and theoretical analysis is required to determine the effectiveness of this drug combination in GBM. At present, the results of lomustine combined with bevacizumab are still encouraging for clinical treatment of GBM, and Dose group 2 is a potential option that provides a good starting point for discussions and further clinical trials.
Data Availability Statement
The original contributions presented in the study are included in the article/Supplementary Material, further inquiries can be directed to the corresponding author/s.
Author Contributions
XR: the main author of this article and the thought provider of this meta-analysis. DA: provided technical guidance for the meta-analysis. TL: assisting in writing articles, searching literature, and proofreading. LX: mainly responsible for the editing of figures and tables. LS: responsible for overall supervision. All authors contributed to the article and approved the submitted version.
Conflict of Interest
The authors declare that the research was conducted in the absence of any commercial or financial relationships that could be construed as a potential conflict of interest.
Supplementary Material
The Supplementary Material for this article can be found online at: https://www.frontiersin.org/articles/10.3389/fneur.2020.603947/full#supplementary-material
References
1. Louis DN, Perry A, Reifenberger G, von Deimling A, Figarella-Branger D, Cavenee WK, et al. The 2016 World Health Organization classification of tumors of the central nervous system: a summary. Acta Neuropathol. (2016) 131:803–20. doi: 10.1007/s00401-016-1545-1
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Stupp R, Mason WP, van den Bent MJ, Weller M, Fisher B, Taphoorn MJ, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. New Engl J Med. (2005) 352:987–96. doi: 10.1056/NEJMoa043330
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Gilbert MR, Wang M, Aldape KD, Stupp R, Hegi ME, Jaeckle KA, et al. Dose-dense temozolomide for newly diagnosed glioblastoma: a randomized phase III clinical trial. J Clin Oncol. (2013) 31:4085–91. doi: 10.1200/JCO.2013.49.6968
CrossRef Full Text | Google Scholar
4. Erdem-Eraslan L, van den Bent MJ, Hoogstrate Y, Naz-Khan H, Stubbs A, van der Spek P, et al. Identification of patients with recurrent glioblastoma who may benefit from combined bevacizumab and CCNU therapy: a report from the BELOB trial. Cancer Res. (2016) 76:525–34. doi: 10.1158/0008-5472.CAN-15-0776
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Komiyama S, Kugimiya T, Takeya C, Takahashi R, Kubushiro K. Platinum-resistant recurrent ovarian cancer with long survival on bevacizumab and gemcitabine. J Obstetr Gynaecol Res. (2018) 44:1330–4. doi: 10.1111/jog.13664
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Lu KV, Chang JP, Parachoniak CA, Pandika MM, Aghi MK, Meyronet D, et al. VEGF inhibits tumor cell invasion and mesenchymal transition through a MET/VEGFR2 complex. Cancer Cell. (2012) 22:21–35. doi: 10.1016/j.ccr.2012.05.037
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Cohen MH, Shen YL, Keegan P, Pazdur R. FDA drug approval summary: bevacizumab (Avastin) as treatment of recurrent glioblastoma multiforme. Oncologist. (2009) 14:1131–8. doi: 10.1634/theoncologist.2009-0121
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Chinot OL, Wick W, Mason W, Henriksson R, Saran F, Nishikawa R, et al. Bevacizumab plus radiotherapy-temozolomide for newly diagnosed glioblastoma. New Engl J Med. (2014) 370:709–22. doi: 10.1056/NEJMoa1308345
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Gilbert MR, Dignam JJ, Armstrong TS, Wefel JS, Blumenthal DT, Vogelbaum MA, et al. A randomized trial of bevacizumab for newly diagnosed glioblastoma. New Engl J Med. (2014) 370:699–708. doi: 10.1056/NEJMoa1308573
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Friedman HS, Prados MD, Wen PY, Mikkelsen T, Schiff D, Abrey LE, et al. Bevacizumab alone and in combination with irinotecan in recurrent glioblastoma. J Clin Oncol. (2009) 27:4733–40. doi: 10.1200/JCO.2008.19.8721
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Vredenburgh JJ, Desjardins A, Herndon JE, 2nd, Marcello J, Reardon DA, Quinn JA, et al. Bevacizumab plus irinotecan in recurrent glioblastoma multiforme. J Clin Oncol. (2007) 25:4722–9. doi: 10.1200/JCO.2007.12.2440
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Wick W, Puduvalli VK, Chamberlain MC, van den Bent MJ, Carpentier AF, Cher LM, et al. Phase III study of enzastaurin compared with lomustine in the treatment of recurrent intracranial glioblastoma. J Clin Oncol. (2010) 28:1168–74. doi: 10.1200/JCO.2009.23.2595
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Song J, Xue YQ, Zhao MM, Xu P. Effectiveness of lomustine and bevacizumab in progressive glioblastoma: a meta-analysis. OncoTargets Therapy. (2018) 11:3435–9. doi: 10.2147/OTT.S160685
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Taal W, Oosterkamp HM, Walenkamp AME, Dubbink HJ, Beerepoot LV, Hanse MCJ, et al. Single-agent bevacizumab or lomustine versus a combination of bevacizumab plus lomustine in patients with recurrent glioblastoma (BELOB trial): a randomised controlled phase 2 trial. Lancet Oncol. (2014) 15:943–53. doi: 10.1016/S1470-2045(14)70314-6
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Heiland DH, Masalha W, Franco P, Machein MR, Weyerbrock A. Progression-free and overall survival in patients with recurrent Glioblastoma multiforme treated with last-line bevacizumab versus bevacizumab/lomustine. J Neurooncol. (2016) 126:567–75. doi: 10.1007/s11060-015-2002-z
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Weathers SP, Han X, Liu DD, Conrad CA, Gilbert MR, Loghin ME, et al. A randomized phase II trial of standard dose bevacizumab versus low dose bevacizumab plus lomustine (CCNU) in adults with recurrent glioblastoma. J Neuro Oncol. (2016) 129:487–94. doi: 10.1007/s11060-016-2195-9
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Wick W, Gorlia T, Bendszus M, Taphoorn M, Sahm F, Harting I, et al. Lomustine and bevacizumab in progressive glioblastoma. New Engl J Med. (2017) 377:1954–63. doi: 10.1056/NEJMoa1707358
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Jakobsen JN, Urup T, Grunnet K, Toft A, Johansen MD, Poulsen SH, et al. Toxicity and efficacy of lomustine and bevacizumab in recurrent glioblastoma patients. J Neurooncol. (2018) 137:439–46. doi: 10.1007/s11060-017-2736-x
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Brandes AA, Gil-Gil M, Saran F, Carpentier AF, Nowak AK, Mason W, et al. A randomized phase II trial (TAMIGA) evaluating the efficacy and safety of continuous bevacizumab through multiple lines of treatment for recurrent glioblastoma. Oncologist. (2019) 24:521–8. doi: 10.1634/theoncologist.2018-0290
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Lombardi G, Pambuku A, Bellu L, Farina M, Della Puppa A, Denaro L, et al. Effectiveness of antiangiogenic drugs in glioblastoma patients: a systematic review and meta-analysis of randomized clinical trials. Crit Rev Oncol Hematol. (2017) 111:94–102. doi: 10.1016/j.critrevonc.2017.01.018
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Kreisl TN, Kim L, Moore K, Duic P, Royce C, Stroud I, et al. Phase II trial of single-agent bevacizumab followed by bevacizumab plus irinotecan at tumor progression in recurrent glioblastoma. J Clin Oncol. (2009) 27:740–5. doi: 10.1200/JCO.2008.16.3055
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Schaub C, Schäfer N, Mack F, Stuplich M, Kebir S, Niessen M, et al. The earlier the better? Bevacizumab in the treatment of recurrent MGMT-non-methylated glioblastoma. J Cancer Res Clin Oncol. (2016) 142:1825–9. doi: 10.1007/s00432-016-2187-3
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Batchelor TT, Mulholland P, Neyns B, Nabors LB, Campone M, Wick A, et al. Phase III randomized trial comparing the efficacy of cediranib as monotherapy, and in combination with lomustine, versus lomustine alone in patients with recurrent glioblastoma. J Clin Oncol. (2013) 31:3212–8. doi: 10.1200/JCO.2012.47.2464
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Lorgis V, Maura G, Coppa G, Hassani K, Taillandier L, Chauffert B, et al. Relation between bevacizumab dose intensity and high-grade glioma survival: a retrospective study in two large cohorts. J Neurooncol. (2012) 107:351–8. doi: 10.1007/s11060-011-0748-5
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Batchelor TT, Sorensen AG, di Tomaso E, Zhang WT, Duda DG, Cohen KS, et al. AZD2171, a pan-VEGF receptor tyrosine kinase inhibitor, normalizes tumor vasculature and alleviates edema in glioblastoma patients. Cancer Cell. (2007) 11:83–95. doi: 10.1016/j.ccr.2006.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Field KM, Jordan JT, Wen PY, Rosenthal MA, Reardon DA. Bevacizumab and glioblastoma: scientific review, newly reported updates, and ongoing controversies. Cancer. (2015) 121:997–1007. doi: 10.1002/cncr.28935
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Jahnke K, Muldoon LL, Varallyay CG, Lewin SJ, Kraemer DF, Neuwelt EA. Bevacizumab and carboplatin increase survival and asymptomatic tumor volume in a glioma model. Neuro Oncol. (2009) 11:142–50. doi: 10.1215/15228517-2008-077
PubMed Abstract | CrossRef Full Text | Google Scholar
 |
Международное непатентованное название? Ломустин |
 |
Действующее вещество: Ломустин — 40 мг. Вспомогательные вещества: лактозы моногидрат (сахар молочный) — 100,0 мг, крахмал пшеничный — 40,0 мг, тальк — 16,0 мг, магния стеарат — 4,0 мг. |
 |
Противоопухолевое средство — алкилирующее соединение |
 |
ПроизводителиМедак(Германия), Хаупт Фарма Амарег/Медак(Германия) |
 |
Показания к применению Ломустин Медак капсулы 40мгЛомустин применяется в монотерапии и в комбинированной терапии (в том числе в комбинации с лучевой терапией и хирургическим лечением) следующих заболеваний: первичные и метастатические опухоли мозга; рак легкого (особенно мелкоклеточный); лимфогранулематоз (болезнь Ходжкина) резистентный к стандартной химиотерапии; злокачественная метастатическая меланома.Ломустин медак может также применяться в терапии множественной миеломы, рака желудка и кишечника, рака почки. |
 |
Способ применения и дозировка Ломустин Медак капсулы 40мгЛомустин следует принимать внутрь вечером, перед сном или через 3 часа после приема пищи. В профилактических целях рекомендуется применение совместно с ломустином антиэметиков. Рекомендуемая доза ломустина у взрослых и детей с нормальной функцией костного мозга составляет 120-130 мг/кв.м при однократном приеме внутрь каждые 6-8 недель. Данную дозу можно разделить на три приема в течение трех последовательных дней. У пациентов со сниженной функцией костного мозга дозу можно снизить до 100 мг/кв.м при сохранении шестинедельного интервала между приемами. Кумулятивная миелосупрессия может потребовать более продолжительного интервала между приемом препарата. Перед каждым очередным приемом ломустина следует проводить общий анализ крови и при необходимости корректировать дозу препарата. Дозу необходимо уменьшить в случае, если: препарат применяется в составе схемы терапии, в которую входят другие препараты с миелосупрессивными свойствами; при лейкопении ниже 3000/мкл или тромбоцитопении ниже 75000/мкл.В случае комбинированной терапии препарат применяют в дозе 70-100 мг/кв.м. При применении ломустина подавление функции костного мозга является более продолжительным, чем после воздействия соединений трихлортриэтиламина, восстановление содержания лейкоцитов и тромбоцитов может происходить в течение 6 недель и более. Повторные курсы не следует назначать при количестве тромбоцитов менее 100000/мкл и лейкоцитов менее 4000/мкл. Дальнейшие дозы препарата должны подбираться в зависимости от гемато-логического ответа пациента на предыдущую дозу. При подборе доз можно ориентироваться на следующую схему: Минимальные показатели после приема предыдущей дозы: лейкоциты 3000-4000/мкл; тромбоциты 75 000- 100 000/мкл. Рекомендуемая следующая доза (% от предыдущей дозы) — 100%. Минимальные показатели после приема предыдущей дозы: лейкоциты 2000-2999/мкл; тромбоциты 25 000 — 74 999/мкл. Рекомендуемая следующая доза (% от предыдущей дозы) -70%. Минимальные показатели после приема предыдущей дозы: лейкоциты менее 2000/мкл; тромбоциты менее 25 000/мкл. Рекомендуемая следующая доза (% от предыдущей дозы) — 50%. Применение у детей. Применение препарата для лечения детей с онкологическими заболеваниями должно проводиться только в специализированных центрах и только после соотношения ожидаемой пользы лечения к потенциальному риску. |
 |
Противопоказания Ломустин Медак капсулы 40мгПовышенная чувствительность к ломустину и другим компонентам препарата, другим производным нитрозомочевины, в том числе в анамнезе. Ранее выявление резистентность опухоли к производным нитрозомочевины. Выраженное подавление функции костного мозга. Тяжелая почечная недостаточность. Совместное применение с вакциной желтой лихорадки или другими живыми вакцинами у пациентов со сниженным иммунным статусом. Беременность и период грудного вскармливания. С осторожностью: у пациентов с миелосупрессией и пониженной концентрацией тромбоцитов, лейкоцитов, эритроцитов в крови; ветряная оспа (в т.ч. недавно перенесенная или после контакта с заболевшими);опоясывающий герпес и другие острые инфекционные заболевания вирусной, грибковой или бактериальной природы; кахексия; интоксикации; почечная и/или печеночная недостаточность; дыхательная недостаточность; лечение цитостатиками и лучевая терапия в анамнезе; непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция (т.к. препарат содержит лактозу).Применение при беременности и в период грудного вскармливания. Беременность. Препарат противопоказан при беременности. В доклинических исследованиях ломустин проявлял эмбриотоксическое и тератогенное действие. Пациентки, применяющие препарат, должны быть осведомлены о потенциальной опасности для плода в случае, если беременность наступает во время лечения препаратом Ломустин медак. Женщинам детородного возраста необходимо избегать наступления беременности. В случае наступления беременности на фоне приема препарата пациентке следует проинформировать своего врача.Период грудного вскармливания. Так как ломустин обладает липофильными свойствами, есть основания полагать, что он проникает в грудное молоко. Учитывая риск негативного воздействия на ребенка, следует тщательно взвесить ожидаемую пользу лечения для матери и потенциальный риск для ребенка и принять решение о прекращении грудного вскармливания или о прекращении лечения ломустином. |
 |
Фармакологическое действиеФармакодинамика. Ломустин — противоопухолевый препарат алкилирующего действия из группы нитрозомочевины. Механизм действия заключается в алкилировании ДНК и РНК, а также ингибировании отдельных этапов синтеза нуклеиновых кислот и репарации отдельных разрывов цепи ДНК. Ингибирование синтеза ДНК обусловлено карбамоилированием ДНК-полимеразы и других ферментов репарации ДНК и повреждением ДНК-матрицы. Препарат может также тормозить ключевые ферментативные процессы путем изменения структуры и функции многих белков и ферментов. Ломустин действует в поздней фазе G1 и ранней S-фазе клеточного цикла. Наиболее высокая чувствительность к ломустину у клеток в стационарной фазе роста (фактор, определяющий активность при солидных опухолях с низким пролиферативным пулом). Фармакокинетика. После приема внутрь быстро и практически полностью всасывается из желу-дочно-кишечного тракта. Максимальная концентрация в плазме крови (0,5- 2 нг/мл) достигаются в среднем через 3 часа после перорального приема дозы препарата 30-100 мг/кв.м. Связь с белками плазмы — 50 %. Проникает через гематоэнцефалический барьер. После перорального введения ломустина, меченого радиоизотопной меткой, радиоактивность в спинномозговой жидкости составляет от 15 до 30 % радиоактивности, измеренной в плазме. Быстро метаболизируется в печени с образованием активных метаболитов (оксиметилдиазония и изоцианата). Оксиметилдиазоний ионизируется и превращается в ион метилдиазония, который трансформируется в более устойчивую таутомерную форму (диазометан), либо распадается на метилкарбониевый ион и азот. Хлорэтильная группа выводится из плазмы однофазно с периодом полувыведения 72 часа. Выведение циклогексильной группы является двухвазным с периодом полувыведения Т1/2альфа = 4 часа и Т1/2бета = 50 часов. Выводится преимущественно почками в виде метаболитов, менее 5 % — через кишечник. Активная форма ломустина в моче не обнаруживается. |
 |
Побочное действие Ломустин Медак капсулы 40мгЧастота побочных реакций изложена в соответствии со следующей градацией: очень часто (>1/10), часто (>1/100, <1/10), нечасто (>1/1000, <1/100), редко (>1/10000, <1/1000), очень редко (<1/10000), частота неизвестна (не может быть определена на основании имеющихся данных). Нарушения со стороны крови и лимфатической системы: очень часто — угнетение костномозгового кроветворения, тромбоцитопения, лейкопения, анемия. Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): частота неизвестна — сообщалось о развитии острого лейкоза и дисплазии костного мозга у пациентов, в течение длительного времени получавших препараты нитрозомочевины. Нарушения со стороны желудочно-кишечного тракта: очень часто — тошнота, рвота, анорексия; редко: диарея, стоматит. Нарушения со стороны печени и желчевыводящих путей: часто — нарушение функции печени (в большинстве случаев легкой степени выраженности); редко — холестатическая желтуха, печеночная недостаточность. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: редко — интерстициальная пневмония, инфильтративные процессы, фиброз легких. Нарушения со стороны нервной системы: редко — нарушение координации, спутанность сознания, сонливость, апатия, расстройство артикуляции речи, заикание (сообщалось о развитии этих симптомов при проведении комбинированной терапии с применением других противоопухолевых средств и лучевой терапии). Нарушения со стороны почек и мочевыводящих путей: частота неизвестна — почечная недостаточность, прогрессирующая азотемия, уменьшение размеров (атрофия) почек. Нарушение со стороны кожи и подкожных тканей: редко — алопеция. Нарушение со стороны органа зрения: очень редко — поражение зрительных нервов (при сочетании с лучевой терапией опухолей головного мозга), необратимая потеря зрения. Влияние на результаты лабораторных и инструментальных исследований: частота неизвестна — повышение активности печеночных ферментов(аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), лактатдегидрогеназы (ЛДГ), щелочной фосфатазы), повышение концентрации билирубина в сыворотке крови.Основным нежелательным побочным эффектом ломустина является отсроченная или пролонгированная миелотоксичность, которая обычно проявляется через 4-6 недель после приема препарата и носит дозозависимый характер. Тромбоцитопения наблюдается приблизительно через 4 недели после приема дозы ломустина и обычно сохраняется на уровне 80000 — 100000/мкл в течение 1-2 недель. Через 5-6 недель появляется лейкопения (около 4000- 5000/мкл), которая сохраняется в течение одной или двух недель. Реже наблюдается анемия, однако, по сравнению с тромбоцитопенией и лейкопенией, она наблюдается реже и протекает в менее тяжелой форме. Гематологическая токсичность может иметь кумулятивный характер, причем после приема повторных доз может отмечаться более выраженное подавление функции костного мозга. Приблизительно у 65 % пациентов, получающих препарат в дозе 130 мг/м2, концентрация лейкоцитов снижалась до уровней менее 5000/мкл. У 36 % пациентов этот показатель составил менее 3000/мкл. Как правило, тромбоцитопения носит более тяжелый характер, чем лейкопения; однако, оба вида токсичности могут оказаться дозолимитирующими. Тошнота и рвота обычно проявляются через 4-6 ч после введения полной разовой дозы ломустина и продолжаются 24-48 ч, анорексия обычно продолжается в течение 2-3 дней. Выраженность этих побочных явлений может быть уменьшена путем разделения разовой дозы, рассчитанной на 6 недель, на три приема в первые три дня каждого 6-недельного цикла. Обычно препарат хорошо переносится, если его применение сопровождается профилактическим приемом противорвотных средств (например, метоклопрамида или хлорпромазина). В единичных случаях после продолжительного лечения ломустином и другими препаратами нитрозомочевины при достижении высокой кумулятивной дозы наблюдались почечная недостаточность, прогрессирующая азотемия, уменьшение размеров (атрофия) почек. В связи с этим рекомендуется не превышать максимальную общую кумулятивную дозу ломустина 1000 мг/кв.м. Однако, необходимо учитывать, что поражение почек возможно также у пациентов, получивших более низкие кумулятивные дозы препарата. |
 |
ПередозировкаСообщалось о случаях передозировки ломустином, включая смертельные исходы. Возможные симптомы при передозировке: миелотоксичность, гематологическая токсичность, боль в абдоминальной области, тошнота, рвота, диарея, анорексия, сонливость, головокружение, нарушение функции печени, кашель, одышка. Антидот не известен. При передозировке следует немедленно провести промывание желудка. Лечение симптоматическое. При наличии клинических показаний следует предпринять меры для восполнения потери форменных элементов крови. |
 |
Взаимодействие Ломустин Медак капсулы 40мгМиелотоксичность ломустина может усиливаться при его совместном использовании с теофиллином или циметидином, являющимся анатагонистом Н2-рецепторов. Для ломустина характерна перекрестная резистентность с другими производными нитрозомочевины, которая не наблюдается в отношении других алкилирующих средств. Фенобарбитал, активирующий микросомальные ферменты печени, может усиливать метаболизм ломустина и ускорять его выведение из организма, поэтому применение фенобарбитала перед ломустином может снизить противоопухолевую активность последнего. Применение вакцины против желтой лихорадки повышает риск системных поствакцинальных осложнений, в том числе с летальным исходом. Пациентам, проходящим иммуносупрессивную терапию, противопоказано применение живых вакцин. Совместное применение противоэпилептических и химиотерапевтических препаратов, включая ломустин, может вызвать осложнения, вызванные фармакокинетическим взаимодействием между препаратами. Одновременное применение ломустина с другими цитостатическими препаратами и радиотерапией может усиливать миелотоксичность ломустина. Ломустин при совместном применении с амфотерицином В может усиливать токсичность последнего. |
 |
Особые указанияЛечение Ломустином медак должен проводить врач-онколог, имеющий опыт проведения противоопухолевой терапии.Пациентов необходимо обязательно проинформировать о том, что разовую дозу препарата следует принимать внутрь один раз в 6 недель, в течение которых нельзя принимать повторные дозы, а также о недопустимости приема препарата в дозах, превышающих назначенные врачом. Наиболее распространенный и тяжелый токсический эффект ломустина — отсроченное подавление функции костного мозга, проявляющееся в первую очередь тромбоцитопенией и лейкопенией, которые могут привести к развитию кровотечений и инфекций у ослабленных пациентов. Поэтому до начала приема препарата и в течение всего курса лечения (раз в неделю как минимум в течение 6 недель после приема препарата) необходимо проводить развернутый клинический анализ крови.При назначении терапии ломустином и определении дозы следует руководствоваться главным образом значениями концентрации гемоглобина, лейкоцитов и тромбоцитов в сыворотке крови. Миелосупрессия, вызываемая ломустином, является кумулятивной, поэтому очередную дозу следует подбирать с учетом минимального значения концентрации форменных элементов крови, наблюдавшегося после последнего приема препарата. Применение ломустина потенциально может привести к нарушению функции печени, почек. Необходимо периодически контролировать функцию печени и почек. Легочная токсичность ломустина носит дозозависимый характер. До начала и в процессе лечения необходимо регулярно контролировать функцию легких. Пациенты со сниженными менее 70 % исходными значениями форсированной жизненной емкости легких, а также диффузной способности легких по поглощению оксида углерода (DLсо), входят в группу особого риска. Сообщалось о возможности взаимосвязи развития вторичных злокачественных новообразований с длительным применением препаратов нитрозомочевины. Фертильность. Мужчинам и женщинам детородного возраста во время лечения и, как минимум, в течение 6 месяцев после его окончания необходимо применять надежные методы контрацепции. Пациенты мужского пола должны быть проинформированы и риске необратимого наступления бесплодия в результате лечения ломустином. При обращении с ломустином, как и с любыми другими противоопухолевыми препаратами, необходимо соблюдать осторожность. Не вскрывать капсулы. Следует избегать контакта содержимого капсул с кожей и слизистыми оболочками. При контакте с порошком препарата необходимо использовать специально выделенные для этого материалы, пользоваться перчатками, после контакта следует утилизировать использованные материалы и вымыть руки водой с мылом. Влияние на способность управлять транспортными средствами и механизмами. Препарат может оказывать влияние на способность управлять автомобилем и использовать механизмы ввиду риска развития тошноты и рвоты. При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности. |
 |
Условия храненияХранить в защищенном от света, недоступном для детей месте при температуре не выше 25 °С. |