Козэнтикс — инструкция по применению
Синонимы, аналоги
Статьи
Внимательно прочитайте эту инструкцию перед тем, как начать прием/применение этого лекарства.
Сохраните инструкцию, она может потребоваться вновь.
Если у Вас возникли вопросы, обратитесь к врачу.
Это лекарство назначено лично Вам, и его не следует передавать другим лицам, поскольку оно может причинить им вред даже при наличии тех же симптомов, что и у Вас.
Регистрационный номер:
ЛП-003780
Торговое наименование:
Козэнтикс
МНН или группировочное наименование:
секукинумаб
Лекарственная форма:
раствор для подкожного введения.
Состав
Действующее вещество: секукинумаб 150,00 мг;
вспомогательные вещества: трегалозы дигидрат 75,67 мг, гистидин/гистидина гидрохлорида моногидрат 3,103 мг, метионин 0,746 мг, полисорбат-80 0,200 мг, вода для инъекций 1069 мг.
Описание:
от бесцветного до светло-желтого цвета прозрачный или опалесцирующий раствор.
Фармакотерапевтическая группа:
ингибиторы интерлейкина.
Код ATX:
L04AC10.
Фармакологические свойства
Механизм действия
Секукинумаб представляет собой полностью человеческое антитело (иммуноглобулин G1, IgGl), которое селективно связывается и нейтрализует провоспалительный цитокин -интерлейкин-17А (ИЛ-17А). Секукинумаб оказывает направленное действие на ИЛ-17 и ингибирует его взаимодействие с рецептором ИЛ-17, который экспрессируется разными типами клеток, включая кератиноциты и синовиоциты. В результате этого секукинумаб ингибирует высвобождение провоспалительных цитокинов, хемокинов и медиаторов повреждения тканей, снижает вклад ИЛ-17А в аутоиммунные и воспалительные заболевания. Секукинумаб в клинически значимых концентрациях достигает кожи и снижает концентрацию воспалительных маркеров. Прямым следствием лечения секукинумабом является уменьшение выраженности покраснения, уплотнения и шелушения кожи, что наблюдается в очагах поражения при бляшечном псориазе.
ИЛ-17А является естественным цитокином, который участвует в нормально протекающих реакциях воспаления и иммунного ответа. ИЛ-17А играет ключевую роль в патогенезе бляшечного псориаза, псориатического артрита и анкилозирующего спондилита. В крови у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом, а также в клетках пораженных участков кожи у пациентов с бляшечным псориазом обнаружено увеличение концентрации ИЛ-17А, а также увеличение количества лимфоцитов и клеток врожденного иммунитета, продуцирующих ИЛ-17А. Продукция ИЛ-17А существенно повышена в пораженных участках по сравнению со здоровыми участками кожи у пациентов с бляшечным псориазом. Кроме того, у пациентов с псориатическим артритом в синовиальной жидкости отмечается увеличение количества клеток, продуцирующих ИЛ-17А. У пациентов с анкилозирующим спондилитом значительное увеличение количества клеток, продуцирующих ИЛ-17А, отмечается в субхондральном костном мозге фасеточных суставов. ИЛ-17А также способствует развитию воспаления тканей, инфильтрации нейтрофилами, деструкции костей и тканей, а также ремоделированию тканей, включая ангиогенез и фиброз.
Применение секукинумаба у пациентов с бляшечным псориазом в дозе 300 мг обеспечивает более выраженное очищение кожных покровов по сравнению с применением в дозе 150 мг, с максимальным эффектом на 16 неделе. Секукинумаб демонстрирует эффективность как у пациентов, ранее не получавших терапию генно-инженерными биологическими препаратами (ГИБП), так и у пациентов с недостаточным ответом на терапию ГИБП-ингибиторами ФНОа (фактор некроза опухоли а), при этом несколько более выраженный ответ отмечен у пациентов, ранее не получавших терапию вышеуказанными препаратами. При применении секукинумаба отмечено улучшение симптомов и признаков заболевания, улучшение качества жизни, связанное с функциональным статусом и состоянием здоровья, а также замедление прогрессирования поражения периферических суставов.
У пациентов с псориатическим артритом на фоне терапии секукинумабом отмечается схожий ответ на лечение вне зависимости от применения его в монотерапии или в комбинации с метотрексатом. При применении секукинумаба к 16 и 24 неделям отмечено улучшение периферических симптомов псориатического артрита (например, уменьшение количества болезненных/припухших суставов, разрешение дактилитов, энтезитов, уменьшение степени выраженности поражения ногтей). Применение секукинумаба в дозе 150 мг к 24 неделе значительно подавляло степень прогрессирования поражения периферических суставов (относительного исходного показателя модифицированного общего счета Шарпа). Рентгенологические признаки подавления прогрессии отмечены как у пациентов, ранее не получавших терапию ингибиторами ФНОа, так и у пациентов с недостаточным ответом на предшествующую терапию указанными препаратами. Схожее подавление структурного поражения отмечалось вне зависимости от комбинированного применения метотрексата.
Применение секукинумаба у пациентов с анкилозирующим спондилитом приводило к улучшению подвижности позвоночника и его функции, уменьшению активности заболевания (в том числе снижению концентрации высокочувствительного СРБ). У пациентов, получавших секукинумаб без предшествующей терапии ингибиторами ФНОа, при магниторезонансной томографии к 16 неделе отмечено уменьшение признаков воспаления крестцово-подвздошных сочленений и позвоночника относительно исходных показателей.
Фармакодинамика
Концентрация общего ИЛ-17А (свободного и связанного с секукинумабом) в сыворотке крови увеличивается в пределах 2-7 дней вследствие замедления клиренса, связанного с секукинумабом ИЛ-17А, свидетельствуя, что секукинумаб селективно связывается со свободным ИЛ-17А, который играет ключевую роль в патогенезе бляшечного псориаза.
В исследовании у пациентов с бляшечным псориазом после одной-двух недель лечения секукинумабом значительно снижались инфильтрация эпидермиса нейтрофилами и количество различных ассоциированных с ними маркеров, которое часто повышено в пораженных участках кожи у данных пациентов.
На фоне терапии секукинумабом у пациентов с псориатическим артритом и анкилозирующим спондилитом в течение 1-2 недель отмечалось снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
Всасывание
После однократного подкожного (п/к) введения в дозе 150 мг или 300 мг при бляшечном псориазе максимальная концентрация секукинумаба в сыворотке крови составляла соответственно 13,7±4,8 мкг/мл или 27,3±9,5 мкг/мл в интервале между 5 и 6 днем после введения.
После первоначального еженедельного введения во время первого месяца максимальная концентрация достигалась между 31 и 34 днем.
Максимальная концентрация в равновесном состоянии (Cmax,ss) после п/к введения 150 мг или 300 мг составила 27,6 мкг/мл и 55,2 мкг/мл соответственно. Равновесная концентрация достигается после 20 недель при ежемесячном режиме введения.
По сравнению с экспозицией после однократной дозы отмечено двукратное повышение максимальной концентрации и площади под фармакокинетической кривой «концентрация-время» (AUC) после многократного ежемесячного введения во время поддерживающей терапии.
Секукинумаб всасывается со средним показателем абсолютной биодоступности 73%.
Распределение
Средний объем распределения в терминальной фазе (Vz) после однократного внутривенного введения варьировал между 7,10 и 8,60 л у пациентов с бляшечным псориазом, что позволяет предположить, что секукинумаб ограниченно распределяется на периферии.
Концентрации секукинумаба в межклеточной жидкости кожи у пациентов с бляшечным псориазом варьировали от 28% до 39% от таковой в сыворотке крови на 1-2 неделе после однократного п/к введения в дозе 300 мг.
Выведение
Средний системный клиренс (CL) у пациентов с бляшечным псориазом составил 0,19л/сутки. Клиренс был дозо- и время-зависимым, как и предполагалось для терапевтического IgGl моноклонального антитела, взаимодействующего с растворимой цитокиновой мишенью, такой как ИЛ-17А.
Средний период полувыведения у пациентов с бляшечным псориазом составлял 27 дней. Расчетный период полувыведения у отдельных пациентов с псориазом варьировал от 17 до 41 дня.
Линейность / нелинейность
Фармакокинетические параметры при однократном и многократном введении секукинумаба у пациентов с бляшечным псориазом были определены в нескольких исследованиях с внутривенным введением в дозах от 1×0,3 мг/кг до 3×10 мг/кг и с п/к введением в дозах, от 1 х25 мг до многократной дозы 300 мг. При всех режимах дозирования экспозиция была пропорциональна дозе.
Фармакокинетические параметры секукинумаба у пациентов с псориатическим артритом, анкилозирующим спондилитом и бляшечным псориазом одинаковы.
Фармакокинетика в особых клинических случаях
Пациенты старше 65 лет
По данным популяционного фармакокинетического анализа клиренс у пациентов старше 65 лет и пациентов моложе данной возрастной группы был сходным.
Пациенты с нарушениями функции печени или почек
Нет данных по фармакокинетике секукинумаба у пациентов с нарушениями функции печени или почек.
Показания к применению
- Лечение псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия.
- Лечение активного псориатического артрита в монотерапии или в комбинации с метотрексатом у взрослых пациентов при недостаточном ответе на предшествующую терапию базисными препаратами.
- Лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
Противопоказания
- Тяжелые реакции гиперчувствительности к секукинумабу или к другим вспомогательным веществам препарата.
- Клинически значимые инфекции в стадии обострения (например, активный туберкулез).
- Возраст до 18 лет в связи с отсутствием данных по эффективности и безопасности.
- Беременность и период грудного вскармливания.
С осторожностью
- Хронические рецидивирующие инфекции в анамнезе;
- риск развития реакции гиперчувствительности к латексу;
- болезнь Крона в активной фазе;
- вакцинация.
Применение при беременности и в период грудного вскармливания
Беременность
Резюме рисков
Нет достаточных данных по применению препарата у беременных женщин.
Исследования у животных не показали прямого или косвенного негативного влияния секукинумаба на беременность, эмбриональное/фетальное развитие, роды или постнатальное развитие. Поскольку результаты исследований у животных не всегда позволяют предположить ответ у человека, препарат противопоказан к применению во время беременности.
Данные исследований у животных
В исследовании эмбриофетального развития при применении секукинумаба у яванских макак во время органогенеза и на поздних стадиях гестации не выявлено явлений материнской токсичности, эмбриотоксичности или тератогенных свойств.
Грудное вскармливание
Неизвестно, проникает ли секукинумаб в грудное молоко у человека. Поскольку иммуноглобулины проникают в грудное молоко человека, не рекомендуется применять препарат Козэнтикс в период грудного вскармливания.
Влияние на фертильность
Данные о влиянии секукинумаба на мужскую и женскую фертильность отсутствуют. В исследованиях у животных не отмечено прямого или непрямого негативного влияния секукинумаба на фертильность.
Способ применения и дозы
Препарат Козэнтикс вводят путем п/к инъекции. По возможности следует избегать для инъекции пораженных участков кожи при бляшечном псориазе.
Лечение псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия: рекомендуемая доза составляет 300 мг в виде п/к инъекции в качестве начальной дозы на 0, 1, 2, 3 неделе с последующим ежемесячным введением в качестве поддерживающей дозы, начиная с 4 недели. Каждую дозу 300 мг вводят в виде двух отдельных п/к инъекций по 150 мг.
Лечение активного псориатического артрита в монотерапии или в комбинации с метотрексатом у взрослых пациентов при недостаточном ответе на предшествующую терапию базисными препаратами: рекомендуемая доза составляет 150 мг в виде п/к инъекции в качестве начальной дозы на 0, 1, 2, 3 неделе с последующим ежемесячным введением в качестве поддерживающей дозы, начиная с 4 недели. В зависимости от клинического ответа, дозу препарата можно увеличить до 300 мг.
Для пациентов с неадекватным ответом на терапию препаратами ингибиторами ФНОа или для пациентов с сопутствующим псориазом средней и тяжелой степени тяжести рекомендуемая доза составляет 300 мг в виде п/к инъекции в качестве начальной дозы на 0, 1, 2, 3 неделе с последующим ежемесячным введением в качестве поддерживающей дозы, начиная с 4 недели.
Каждую дозу 300 мг вводят в виде двух отдельных п/к инъекций по 150 мг.
Лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию: рекомендуемая доза составляет 150 мг в виде п/к инъекции в качестве начальной дозы на 0, 1, 2, 3 неделе с последующим ежемесячным введением в качестве поддерживающей дозы, начиная с 4 недели.
Особые группы пациентов
Пациенты с нарушением функции печени или почек
Отсутствуют данные по применению препарата Козэнтикс у пациентов данной группы.
Пациенты моложе 18 лет
Эффективность и безопасность препарата у детей до 18 лет не установлена.
Пациенты старше 65 лет
Коррекция дозы не требуется.
На усмотрение лечащего врача после соответствующего обучения технике подкожной инъекции пациент может самостоятельно вводить препарат Козэнтикс, однако врач должен обеспечить соответствующее наблюдение пациента. Следует проинструктировать пациента о необходимости в полной мере соблюдать инструкцию по введению препарата Козэнтикс в соответствии с Указаниями по применению.
Указания по применению
Инструкция по применению препарата Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы
Прочтите инструкцию полностью перед инъекцией. Не пытайтесь самостоятельно вводить препарат, пока Вы не прошли подготовку с Вашим врачом. В пачке находятся 1 или 2 предварительно заполненных шприца в блистере.
Описание препарата Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы
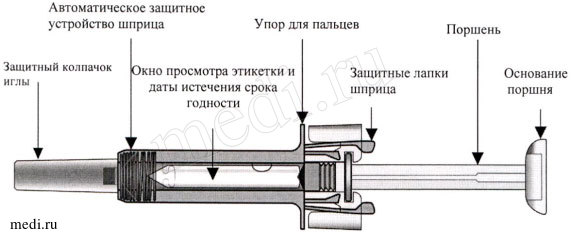
После того, как препарат был введен, автоматическое защитное устройство шприца активируется и скрывает иглу. Предварительно заполненный шприц с устройством для пассивной защиты иглы обеспечивает дополнительную защиту от случайных уколов иглой для медицинских работников, пациентов, которые самостоятельно вводят препарат по предписанию врача, а также ухаживающих за пациентом лиц.
Что нужно дополнительно для проведения инъекции:

- Спиртовой тампон.
- Ватный или марлевый тампон.
- Контейнер для утилизации острых предметов.
Важная информация по безопасности
Внимание: храните препарат в недоступном для детей месте.
Колпачок иглы шприца может содержать сухой каучук (латекс), который не рекомендовано использовать лицам с гиперчувствительностью к этому веществу.
Не открывайте запечатанную пачку, пока Вы не будете готовы использовать препарат.
Не используйте препарат при нарушении целостности пачки или блистера, поскольку применение в этом случае небезопасно.
Никогда не оставляйте препарат в местах, доступных для других лиц.
Не встряхивайте предварительно заполненный шприц.
Будьте осторожны и не прикасайтесь к защитным лапкам шприца до использования.
Прикосновение к ним может вызвать преждевременную активацию автоматического защитного устройства шприца.
Не снимайте колпачок с иглы до непосредственного момента введения препарата.
Недопустимо повторное использование предварительно заполненного шприца. Утилизируйте использованный предварительно заполненный шприц с устройством для пассивной защиты иглы сразу после использования в контейнер для острых предметов.
Хранение препарата Козэнтикс
Храните препарат Козэнтикс в закрытой оригинальной упаковке для защиты от света. Храните в холодильнике при температуре от 2° С до 8° С. Не замораживать!
Перед инъекцией достаньте предварительно заполненный шприц из холодильника и дайте ему согреться до комнатной температуры (от 15 до 30 минут).
При необходимости, препарат может храниться до 4 дней вне холодильника, при комнатной температуре, не превышающей 30°С.
Не используйте с препарат после истечения срока годности, указанного на упаковке или этикетке шприца.
Места для инъекций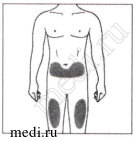
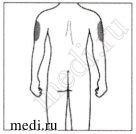
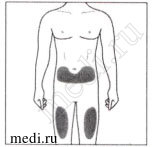
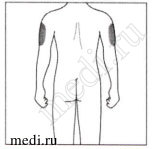
Рекомендуемые зоны для инъекций располагаются на передней поверхности бедер. Вы также можете вводить препарат в нижнюю треть живота, избегая пятисантиметровой области вокруг пупка. Если инъекцию проводит лицо, осуществляющее уход за пациентом, инъекция может быть проведена в наружную поверхность плеча.
Каждый раз меняйте места инъекции.
Не следует проводить инъекции в места с поражением кожных покровов (истончение, покраснение, раздражение, уплотнение, шелушение). Избегайте введения в места с наличием рубцов и растяжек.
Подготовка к использованию препарата Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы
Достаньте упаковку с препаратом из холодильника, и оставьте его, не вскрывая, на 15-30 минут, чтобы он согрелся до комнатной температуры.
Вымойте тщательно руки водой с мылом перед использованием.
Протрите место инъекции спиртовым тампоном.
Извлеките предварительно заполненный шприц с устройством для пассивной защиты иглы из пачки, а затем из блистера.
Осмотрите предварительно заполненный шприц. Жидкость в нем должна быть прозрачной. Ее цвет может варьировать от бесцветного до слегка желтоватого. Вы можете увидеть небольшой пузырек воздуха. НЕ ИСПОЛЬЗУЙТЕ препарат, если жидкость содержит видимые частицы, мутная или очевидно коричневая. НЕ ИСПОЛЬЗУЙТЕ препарат, если целостность предварительно заполненного шприца нарушена. Во всех случаях обратитесь к врачу.
Как использовать препарат Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы
Осторожно снимите колпачок иглы с предварительно заполненного шприца и выбросьте его. Вы можете увидеть каплю жидкости на конце иглы. Это нормально.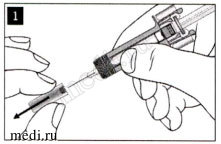
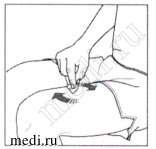
Аккуратно соберите кожную складку между пальцами в месте инъекции и введите иглу, как показано на рисунке. Введите иглу на всю длину, чтобы обеспечить полное введение препарата.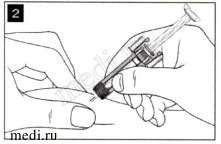
Придерживая шприц, как указано на рисунке, медленно нажимайте на поршень до тех пор, пока основание поршня не окажется между защитными боковыми лапками.
Удерживайте нажатый до упора поршень вместе со шприцем в течение 5 секунд.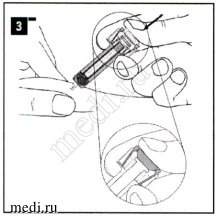
Удерживайте нажатый до упора поршень, пока Вы извлекаете иглу из места инъекции.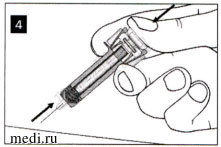
Медленно отпустите поршень и позвольте автоматическому защитному устройству скрыть иглу.
В месте инъекции может появиться небольшое количество крови. Вы можете приложить ватный или марлевый тампон к месту инъекции и удерживать его в течение 10 секунд. Не растирайте место инъекции. При необходимости можно закрыть место инъекции небольшим пластырем.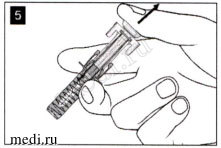
Инструкции по утилизации
Поместите использованный предварительно заполненный шприц в контейнер для острых предметов (закрывающийся, устойчивый к проколам контейнер). В целях Вашей безопасности и здоровья других, иглы и использованные шприцы недопустимо использовать повторно.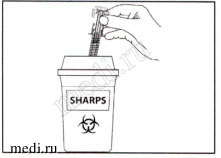
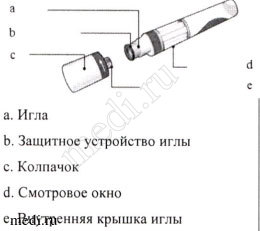
Инструкция по применению препарата Козэнтикс в предварительно заполненном шприце в автоинжекторе
Препарат Козэнтикс в предварительно заполненном шприце в автоинжекторе
Предварительно заполненный шприц в автоинжекторе изображен со снятым колпачком.
Не снимайте колпачок до тех пор, пока Вы не будете готовы ввести препарат. Храните упаковку в холодильнике при температуре от 2°С до 8°С, в местах, не доступных для детей.
При необходимости, препарат может храниться до 4 дней вне холодильника, при комнатной температуре, не превышающей 30°С.
Не замораживать.
Не встряхивать.
Не используйте препарат если автоинжектор упал без колпачка.
Во избежание дискомфорта при введении, предварительно достаньте препарат из холодильника и оставьте при комнатной температуре в течение 15-30 минут перед введением.
Что Вам необходимо для инъекции:
Включено в упаковку:
Препарат Козэнтикс в предварительно заполненном шприце в автоинжекторе.
Не включено в упаковку:
- Спиртовой тампон.
- Ватный или марлевый тампон.
- Контейнер для утилизации острых предметов.

Перед инъекцией:
1. Что необходимо проверить для безопасного проведения инъекции:
Жидкость должна быть прозрачной. Ее цвет может варьировать от бесцветного до слегка желтоватого.
Не используйте препарат, если жидкость содержит легко видимые частицы, мутная или очевидно коричневая. Вы можете увидеть небольшой пузырек воздуха, что является нормальным.
Не используйте препарат Козэнтикс, если срок годности истек.
Не используйте, если целостность контроля первичного вскрытия нарушена.
2а. Выберите место для инъекции:
Рекомендуемые места располагаются на передней поверхности бедер. Вы также можете вводить препарат в нижнюю треть живота, избегая пятисантиметровой области вокруг пупка.
Каждый раз меняйте места инъекции.
Не следует проводить инъекции в места с поражением кожных покровов (истончение, покраснение, раздражение, уплотнение, шелушение). Избегайте введения в места с наличием рубцов и растяжек.
2b. Только для лиц, осуществляющих уход за пациентом, и медицинских работников:
Если инъекцию проводит медицинский работник или лицо, осуществляющее уход за пациентом, инъекция может быть проведена в наружную поверхность плеча.
3. Обработка места инъекции:
Вымойте руки горячей водой с мылом.
Круговыми движениями протрите место инъекции спиртовым тампоном. Дождитесь пока поверхность кожи высохнет.
Не касайтесь предварительно обработанной области до инъекции.
Инъекция:
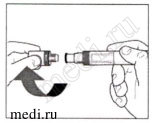
4. Снятие колпачка:
Снимите колпачок с автоинжектора только когда будете готовы ввести препарат.
Отверните колпачок в направлении, указанном стрелкой.
После снятия выбросьте колпачок. Не пытайтесь повторно надеть колпачок.
Используйте препарат в течение 5 минут после удаления колпачка.
5. Положение предварительно автоинжектора:
Держите предварительно заполненный шприц в автоинжекторе под углом 90 градусов к обработанному месту инъекции.
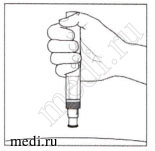
ОБЯЗАТЕЛЬНО ПРОЧТИТЕ ДАННУЮ ИНФОРМАЦИЮ ПЕРЕД ИНЪЕКЦИЕЙ 
Во время инъекции Вы услышите 2 громких щелчка.
1-й щелчок означает начало инъекции. Через несколько секунд 2-й щелчок укажет на то, что инъекция почти закончилась.
Удерживайте автоинжектор плотно прилегающим к коже, пока зеленый индикатор полностью заполнит смотровое окошко.
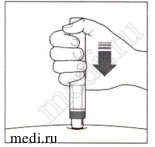
6. Начало инъекции:
Прижмите автоинжектор плотно к коже, чтобы начать введение.
1-й щелчок означает, что инъекция началась.
Удерживайте автоинжектор, плотно прилегающим к коже.
Зеленый индикатор показывает ход выполнения инъекции.
7. Завершение инъекции:
Прислушивайтесь ко 2-му щелчку. Он указывает на то, что инъекция почти завершена.
Убедитесь, что зеленый индикатор заполнил окно и перестал двигаться.
Теперь автоинжектор можно извлечь.
После инъекции:
8. Убедитесь, что зеленый индикатор заполнил окно:
Это означает, что лекарство было введено. Обратитесь к врачу, если зеленый индикатор не виден.
В месте инъекции может выступить небольшое количество крови. Вы можете приложить ватный или марлевый тампон к месту инъекции и удерживать его в течение 10 секунд. Не растирайте место инъекции. При необходимости можно закрыть место инъекции небольшим пластырем.
9. Утилизация:
Поместите использованный автоинжектор в контейнер для острых предметов (закрывающийся устойчивый к проколам контейнер).
Недопустимо использовать автоинжектор повторно.
Побочное действие
В клинических исследованиях секукинумаб получали более 11900 пациентов по различным показаниям, при этом 7100 пациент получал препарат на протяжении минимум 1 года.
Наиболее часто встречающимися нежелательными лекарственными реакциями (НЛР) на фоне применения препарата Козэнтикс были инфекции верхних дыхательных путей (наиболее часто назофарингит, ринит). Большинство из них были легкой или средней степени тяжести. В клинических исследованиях прекращение терапии препаратом в связи с развитием НЛР потребовалось около 1,2% пациентов, получавших секукинумаб, и около 1,2% пациентов, получавших плацебо.
НЛР, выявленные в клинических исследованиях у пациентов с псориазом, перечислены ниже в соответствии с системно-органным классом медицинского словаря для нормативноправовой деятельности MedDRA. В пределах каждого системно-органного класса НРЛ распределены по частоте возникновения в порядке уменьшения их важности. Для оценки частоты использованы следующие критерии: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000), включая отдельные сообщения; частота неизвестна* — по имеющимся данным установить частоту возникновения не представляется возможным.
Инфекционные и паразитарные заболевания: очень часто — инфекции верхних дыхательных путей (в том числе: очень часто — назофарингит, часто — инфекция верхних отделов дыхательных путей, ринит, фарингит, нечасто — синусит, тонзиллит); часто — герпетическая инфекция слизистой оболочки полости рта; нечасто — кандидозная инфекция полости рта, грибковое поражение кожи стоп, наружный отит; частота неизвестна — кандидозная инфекция кожи и слизистых оболочек.
Нарушения со стороны крови и лимфатической системы: нечасто — нейтропения.
Нарушения со стороны иммунной системы: редко — анафилактические реакции.
Нарушения со стороны органа зрения: нечасто — конъюнктивит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: часто — ринорея.
Нарушения со стороны желудочно-кишечного тракта: часто — диарея.
Нарушения со стороны кожи и подкожных тканей: часто — крапивница.
* — поскольку информация о данных НЛР получена методом спонтанных сообщений и точное число пациентов, принимавших препарат, не определено, оценить частоту возникновения данных реакций не представляется возможным, в связи с чем для них указано «частота неизвестна».
Инфекции
В плацебо-контролируемых клинических исследованиях у пациентов с бляшечным псориазом отмечено развитие инфекционных заболеваний у 28,7% и 18,9% пациентов, получавших секукинумаб и плацебо соответственно. Большинство случаев были легкой или средней степени тяжести. Серьезные инфекционные заболевания отмечены у 0,14% пациентов, получавших секукинумаб, и 0,3%, пациентов, получавших плацебо. При долгосрочной терапии препаратом в клинических исследованиях (до 52 недель терапии у большинства пациентов) инфекции отмечены у 47,5% пациентов, получавших секукинумаб, при этом серьезные инфекции зарегистрированы у 1,2% пациентов.
Частота инфекционных заболеваний была схожей в клинических исследованиях у пациентов с псориазом, псориатическим артритом и анкилозирующим спондилитом.
Реакции гиперчувствительности
В клинических исследованиях зарегистрированы случаи крапивницы и в очень редких случаях — анафилактических реакций на введение препарата.
Иммуногенность
По данным клинических исследований препарата Козэнтикс в <1% случаев наблюдалось образование антител к секукинумабу к 52 неделе терапии. Около половины антител, образовавшихся на фоне терапии, являлись нейтрализующими, что не ассоциировалось с потерей эффективности терапии или влиянием на фармакокинетические параметры препарата.
Профиль безопасности секукинумаба у пациентов с псориатическим артритом и анкилозирующим спондилитом соответствовал профилю безопасности у пациентов с псориазом по данным клинических исследований.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка
В ходе клинических исследований препарата Козэнтикс сообщений о случаях передозировки не было.
В ходе клинических исследований внутривенное введение дозы до 30 мг/кг (т.е. приблизительно 2000-3000 мг) не сопровождалось развитием дозолимитирующей токсичности. В случае передозировки рекомендуется наблюдение пациента для выявления признаков и симптомов нежелательных реакций. При необходимости следует незамедлительно провести симптоматическое лечение.
Взаимодействие с другими лекарственными средствами
Препарат Козэнтикс нельзя применять одновременно с живыми вакцинами.
В клинических исследованиях у пациентов с псориазом не отмечено лекарственного взаимодействия между секукинумабом и мидазоламом (субстратом изофермента CYP ЗА4). Нет прямых данных, свидетельствующих об участии ИЛ-17А в экспрессии изоферментов системы цитохрома CYP450. Повышенная концентрация цитокинов в условиях хронического воспалительного процесса подавляет образование некоторых изоферментов системы цитохрома. Таким образом, противовоспалительная терапия, в т.ч. секукинумабом, ингибитором ИЛ-17А, может привести к нормализации активности изоферментов цитохрома CYP450, сопровождающейся уменьшением экспозиции одновременно применяемых препаратов, метаболизм которых осуществляется с участием указанных изоферментов. Таким образом, нельзя исключить клинически значимого влияния на препараты — субстраты изоферментов системы цитохрома с узким терапевтическим индексом, доза которых подбирается индивидуально (например, варфарин). Следует рассмотреть возможность терапевтического контроля при начале терапии секукинумабом у пациентов, получающих лечение препаратами вышеуказанных групп.
Не выявлено лекарственного взаимодействия секукинумаба с метотрексатом и/или глюкокортикостероидами при их одновременном применении у пациентов с псориатическим артритом и анкилозирующим спондилитом.
Особые указания
Инфекции
Препарат Козэнтикс может увеличивать риск развития инфекций. В клинических исследованиях у пациентов, получавших препарат Козэнтикс, наблюдались случаи развития инфекции, большинство которых были легкой или средней степени тяжести. Следует соблюдать осторожность при решении вопроса о применении препарата Козэнтикс у пациентов с хронической инфекцией или с рецидивирующей инфекцией в анамнезе.
Следует информировать пациента о необходимости обращения к врачу в случае появления признаков и симптомов, позволяющих заподозрить развитие инфекции. При развитии тяжелой инфекции необходимо тщательно наблюдать пациента, терапию препаратом следует отложить вплоть до разрешения инфекционного процесса.
В клинических исследованиях не получено сообщений об увеличении восприимчивости к туберкулезу, однако препарат Козэнтикс не следует применять у пациентов с активной формой туберкулеза. Перед началом лечения препаратом у пациентов с латентной формой туберкулеза следует рассмотреть возможность проведения противотуберкулезной терапии.
Болезнь Крона
Следует соблюдать осторожность при применении препарата у пациентов с болезнью Крона в активной фазе, поскольку в клинических исследованиях отмечены случаи обострения болезни Крона, в некоторых случаях тяжелые, у пациентов, получавших как препарат, так и плацебо. Следует тщательно наблюдать пациента с болезнью Крона в активной фазе, получающего терапию препаратом.
Реакции гиперчувствительности
В клинических исследованиях у пациентов, получавших препарат, отмечались редкие случаи развития анафилактических реакций. При возникновении анафилактических или других серьезных аллергических реакций применение препарата Козэнтикс следует немедленно прекратить и немедленно начать соответствующую терапию.
Пациенты с гиперчувствительностью к латексу
Съемный колпачок предварительно заполненного шприца с устройством для пассивной защиты иглы/предварительно заполненного шприца в автоинжекторе содержит производные натурального каучукового латекса. Хотя натуральный каучуковый латекс не обнаруживается в колпачке, безопасность применения препарата Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы/предварительно заполненном шприце в автоинжекторе у пациентов с гиперчувствительностью к латексу не изучалась.
Вакцинация
На фоне терапии препаратом не следует проводить вакцинацию живыми вакцинами. Для пациента, получающего терапию препаратом, следует применять инактивированные или убитые вакцины. В клиническом исследовании у схожего количества пациентов, получавших препарат Козэнтикс, и получавших плацебо, отмечался адекватный иммунный ответ после вакцинации менингококковой и инактивированной гриппозной вакцинами, что проявлялось в виде 4-кратного увеличения титра антител к указанным вакцинам. Эти данные свидетельствуют, что препарат не подавляет гуморальный иммунный ответ к менингококковой и инактивированной гриппозной вакцинам.
Влияние на фертильность
Женщинам с сохраненным репродуктивным потенциалом следует использовать надежные методы контрацепции во время лечения препаратом и как минимум в течение 20 недель после прекращения терапии.
Влияние на способность управлять транспортными средствами и/или механизмами
Отсутствуют данные о влиянии препарата на способность управлять транспортными средствами и/или механизмами.
Форма выпуска
По 1 мл в стеклянный шприц с закрепленной иглой с защитным колпачком (предварительно заполненный шприц).
По 1 или 2 предварительно заполненных шприца с устройством для пассивной защиты иглы в блистер, заклеенный этикеткой, вместе с инструкцией по медицинскому применению в пачку картонную с контролем первичного вскрытия.
По 1 или 2 предварительно заполненных шприца в автоинжекторах (ручках) с контролем первичного вскрытия, вместе с инструкцией по медицинскому применению в пачку картонную с контролем первичного вскрытия.
Условия хранения
В защищенном от света месте при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Препарат не следует применять после истечения срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
Новартис Фарма АГ; Лихтштрассе 35, 4056 Базель, Швейцария / Novartis Pharma AG; Lichtstrasse 35, 4056 Basel, Switzerland
Производитель
Новартис Фарма Штейн АГ; Шаффхаузерштрассе, 4332 Штейн, Швейцария / Novartis Pharma Stein AG; Schaffhauserstrasse, 4332 Stein, Switzerland
Получить дополнительную информацию о препарате, а также направитьпретензии и информацию о нежелательных явлениях можно по следующему адресу в России:
ООО «Новартис Фарма»
125315, г. Москва, Ленинградский проспект, дом 72, корпус 3
Купить Козэнтикс в Планета Здоровья
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Форма выпуска, упаковка и состав
препарата Козэнтикс
Лиофилизат для приготовления раствора для п/к введения в виде белого порошка или аморфной массы.
Вспомогательные вещества: сахароза — 92.43 мг, гистидина гидрохлорида моногидрат /гистидин — 4.656 мг, полисорбат 80 — 0.6 мг.
150 мг — флаконы бесцветного стекла (тип I) вместимостью 6 мл (1) — пачки.
Фармакологическое действие
Секукинумаб представляет собой полностью человеческое антитело (иммуноглобулин G1, IgG1), которое селективно связывается и нейтрализует провоспалительный цитокин — интерлейкин-17А (ИЛ-17А). Секукинумаб оказывает направленное действие на ИЛ-17 и ингибирует его взаимодействие с рецептором ИЛ-17, который экспрессируется разными типами клеток, включая кератиноциты и синовиоциты. В результате этого секукинумаб ингибирует высвобождение провоспалительных цитокинов, хемокинов и медиаторов повреждения тканей, снижает вклад ИЛ-17А в аутоиммунные и воспалительные заболевания. Секукинумаб в клинически значимых концентрациях достигает кожи и снижает концентрацию воспалительных маркеров. Прямым следствием лечения секукинумабом является уменьшение выраженности покраснения, уплотнения и шелушения кожи, что наблюдается в очагах поражения при бляшечном псориазе.
Применение секукинумаба у пациентов с бляшечным псориазом в дозе 300 мг обеспечивает более выраженное очищение кожных покровов по сравнению с применением в дозе 150 мг, с максимальным эффектом на 16 неделе. Секукинумаб демонстрирует эффективность как у пациентов, ранее не получавших терапию генно-инженерными биологическими препаратами (ГИБП), так и у пациентов с недостаточным ответом на терапию ГИБП-ингибиторами ФНОα, при этом несколько более выраженный ответ отмечен у пациентов, ранее не получавших терапию вышеуказанными препаратами. При применении секукинумаба отмечено улучшение симптомов и признаков заболевания, улучшение качества жизни, связанное с функциональным статусом и состоянием здоровья, а также замедление прогрессирования поражения периферических суставов.
У пациентов с псориатическим артритом на фоне терапии секукинумабом отмечается схожий ответ на лечение вне зависимости от применения его в монотерапии или в комбинации с метотрексатом. При применении секукинумаба к 16 и 24 неделям отмечено улучшение периферических симптомов псориатического артрита (например, уменьшение количества болезненных/припухших суставов, разрешение дактилитов, энтезитов, уменьшение степени выраженности поражения ногтей). Применение секукинумаба в дозе 150 мг к 24 неделе значительно подавляло степень прогрессирования поражения периферических суставов (относительного исходного показателя модифицированного общего счета Шарпа).
Рентгенологические признаки подавления прогрессии отмечены как у пациентов, ранее не получавших терапию ингибиторами ФНОα, так и у пациентов с недостаточным ответом на предшествующую терапию указанными препаратами. Схожее подавление структурного поражения отмечалось вне зависимости от комбинированного применения метотрексата. Применение секукинумаба у пациентов с анкилозирующим спондилитом приводило к улучшению подвижности позвоночника и его функции, уменьшению активности заболевания (в том числе снижению концентрации высокочувствительного СРБ). У пациентов, получавших секукинумаб без предшествующей терапии ингибиторами ФНОα, при магниторезонансной томографии к 16 неделе отмечено уменьшение признаков воспаления крестцово-подвздошных сочленений и позвоночника относительно исходных показателей.
Концентрация общего ИЛ-17А (свободного и связанного с секукинумабом) в сыворотке крови увеличивается в пределах 2-7 дней вследствие замедления клиренса, связанного с секукинумабом ИЛ-17А, свидетельствуя, что секукинумаб селективно связывается со свободным ИЛ-17А, который играет ключевую роль в патогенезе бляшечного псориаза.
В исследовании у пациентов с бляшечным псориазом после 1-2 недель лечения секукинумабом значительно снижались инфильтрация эпидермиса нейтрофилами и количество различных ассоциированных с ними маркеров, которое часто повышено в пораженных участках кожи у данных пациентов.
На фоне терапии секукинумабом у пациентов с псориатическим артритом и анкилозирующим спондилитом в течение 1-2 недель отмечалось снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
После однократного п/к введения в дозе 150 мг или 300 мг при бляшечном псориазе Cmax секукинумаба в сыворотке крови составляла соответственно 13.7±4.8 мкг/мл или 27.3±9.5 мкг/мл в интервале между 5 и 6 днем после введения.
После первоначального еженедельного введения во время первого месяца Cmax достигалась между 31 и 34 днем.
Cmax в равновесном состоянии после п/к введения 150 мг или 300 мг составила 27.6 мкг/мл и 55.2 мкг/мл соответственно. Css достигается после 20 недель при ежемесячном режиме введения.
По сравнению с экспозицией после однократной дозы отмечено двукратное увеличение Cmax и AUC после многократного ежемесячного введения во время поддерживающей терапии.
Секукинумаб всасывается со средним показателем абсолютной биодоступности 73%.
Средний объем распределения в терминальной фазе (Vz) после однократного в/в введения варьировал между 7.10 и 8.60 л у пациентов с бляшечным псориазом, что позволяет предположить, что секукинумаб ограниченно распределяется на периферии.
Концентрации секукинумаба в межклеточной жидкости кожи у пациентов с бляшечным псориазом варьировали от 28% до 39% от таковой в сыворотке крови на 1-2 неделе после однократного п/к введения в дозе 300 мг.
Средний системный клиренс (CL) у пациентов с бляшечным псориазом составил 0.19 л/сут. Клиренс был дозо- и времязависимым, как и предполагалось для терапевтического IgG1-моноклонального антитела, взаимодействующего с растворимой цитокиновой мишенью, такой как ИЛ-17А.
Средний T1/2 у пациентов с бляшечным псориазом составлял 27 дней. Расчетный T1/2 у отдельных пациентов с псориазом варьировал от 17 до 41 дня.
При всех режимах дозирования экспозиция была пропорциональна дозе.
Фармакокинетические параметры секукинумаба у пациентов с псориатическим артритом, анкилозирующим спондилитом и бляшечным псориазом одинаковы.
Показания активных веществ препарата
Козэнтикс
Лечение псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия; лечение активного псориатического артрита в монотерапии или в комбинации с метотрексатом у взрослых пациентов при недостаточном ответе на предшествующую терапию базисными препаратами; лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Для п/к введения.
Начальная доза — 300 мг в виде двух отдельных п/к инъекций по 150 мг.
Схема лечения зависит от показаний и клинического ответа.
Побочное действие
Со стороны системы кроветворения: нечасто — нейтропения.
Аллергические реакции: часто — крапивница; редко — анафилактические реакции.
Со стороны органа зрения: нечасто — конъюнктивит.
Со стороны дыхательной системы: очень часто — инфекции верхних дыхательных путей (в т.ч. очень часто — назофарингит, часто — инфекция верхних отделов дыхательных путей, ринит, фарингит, нечасто — синусит, тонзиллит); часто — ринорея.
Со стороны пищеварительной системы: часто — герпетическая инфекция слизистой оболочки полости рта; часто — диарея.
Со стороны кожи и подкожных тканей: нечасто — кандидозная инфекция полости рта, грибковое поражение кожи стоп, наружный отит; частота неизвестна — кандидозная инфекция кожи и слизистых оболочек
Противопоказания к применению
Повышенная чувствительность к секукинумабу; клинически значимые инфекции в фазе обострения (например, активный туберкулез); возраст до 18 лет; беременность, период грудного вскармливания.
С осторожностью: хронические рецидивирующие инфекции в анамнезе; болезнь Крона в активной фазе; вакцинация.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Женщинам с сохраненным репродуктивным потенциалом следует использовать надежные методы контрацепции во время лечения препаратом и как минимум в течение 20 недель после прекращения терапии
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Применение у пожилых пациентов
Препарат разрешен для применения у пожилых пациентов
Особые указания
Секукинумаб может увеличивать риск развития инфекций. Следует соблюдать осторожность при решении вопроса о применении секукинумаба у пациентов с хронической инфекцией или с рецидивирующей инфекцией в анамнезе.
Следует информировать пациента о необходимости обращения к врачу в случае появления признаков и симптомов, позволяющих заподозрить развитие инфекции. При развитии тяжелой инфекции необходимо тщательно наблюдать пациента, терапию секукинумабом следует отложить вплоть до разрешения инфекционного процесса.
Не следует применять у пациентов с активной формой туберкулеза. Перед началом лечения у пациентов с латентной формой туберкулеза следует рассмотреть возможность проведения противотуберкулезной терапии.
Следует соблюдать осторожность при применении препарата у пациентов с болезнью Крона в активной фазе, поскольку в клинических исследованиях отмечены случаи обострения болезни Крона. Следует тщательно наблюдать пациента с болезнью Крона в активной фазе, получающего терапию секукинумабом.
При возникновении анафилактических или других серьезных аллергических реакций применение секукинумаба следует немедленно прекратить и немедленно начать соответствующую терапию.
На фоне терапии секукинумабом не следует проводить вакцинацию живыми вакцинами. Для пациента, получающего секукинумаб, следует применять инактивированные или убитые вакцины. В клиническом исследовании у схожего количества пациентов, получавших секукинумаб, и получавших плацебо, отмечался адекватный иммунный ответ после вакцинации менингококковой и инактивированной гриппозной вакцинами, что проявлялось в виде 4-кратного увеличения титра антител к указанным вакцинам. Эти данные свидетельствуют, что секукинумаб не подавляет гуморальный иммунный ответ к менингококковой и инактивированной гриппозной вакцинам.
Лекарственное взаимодействие
Не применять одновременно с живыми вакцинами.
Повышенная концентрация цитокинов в условиях хронического воспалительного процесса подавляет образование некоторых изоферментов системы цитохрома. Таким образом, противовоспалительная терапия, в т.ч. секукинумабом, ингибитором ИЛ-17А, может привести к нормализации активности изоферментов цитохрома CYP450, сопровождающейся уменьшением экспозиции одновременно применяемых препаратов, метаболизм которых осуществляется с участием указанных изоферментов. Таким образом, нельзя исключить клинически значимого влияния на препараты — субстраты изоферментов системы цитохрома с узким терапевтическим индексом, доза которых подбирается индивидуально (например, варфарин). Следует рассмотреть возможность терапевтического контроля при начале терапии секукинумабом у пациентов, получающих лечение препаратами вышеуказанных групп.
Инструкции по приготовлению раствора препарата Козэнтикс
- Доведите флакон с препаратом Козэнтикс, лиофилизат для приготовления раствора для инъекций, 150 мг, и стерильную воду для инъекций до комнатной температуры.
- Наберите чуть более 1,0 мл стерильной воды для инъекций в одноразовый шприц с градуировкой 1 мл и выровняйте на отметке 1,0 мл.
- Снимите пластиковый колпачок с флакона.
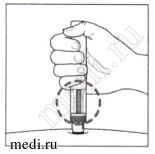
- Вставьте иглу шприца во флакон, содержащий лиофилизат препарата Козэнтикс, через центр резиновой пробки и восстановите лиофилизат медленным введением 1,0 мл стерильной воды для инъекций во флакон. Струя стерильной воды для инъекций должна быть направлена на лиофилизат.
Наклоните флакон под углом около 45° и, удерживая кончиками пальцев, аккуратно вращайте приблизительно в течение 1 минуты. Не встряхивайте и не переворачивайте флакон.
Оставьте флакон стоять при комнатной температуре не менее, чем на 10 минут для достижения полного растворения. Может наблюдаться вспенивание раствора.
Наклоните флакон под углом около 45° и, удерживая кончиками пальцев, аккуратно вращайте приблизительно в течение 1 минуты. Не встряхивайте и не переворачивайте флакон.
Оставьте флакон в вертикальном положении при комнатной температуре приблизительно на 5 минут. Полученный раствор должен быть прозрачным или опалесцирующим. Его цвет может варьировать от бесцветного до светло-желтого.
Не используйте препарат, если лиофилизат полностью не растворяется, или если жидкость содержит легко заметные частицы, а также, если она мутная или коричневого цвета. Подготовьте необходимое количество флаконов (1 флакон для дозы 150 мг, 2 флакона для дозы 300 мг).
После приготовления раствор для подкожных инъекций может быть введен незамедлительно или может храниться при температуре от 2°С до 8°С не более 24 ч. Не замораживать. После хранения при температуре от 2°С до 8°С раствор перед введением следует выдержать при комнатной температуре около 20 минут. Раствор должен быть использован в течение 1 ч после изъятия из условий хранения при температуре от 2°С до 8°С.
Инструкция по введению раствора препарата Козэнтикс
Наклоните флакон под углом приблизительно 45° и поместите кончик иглы на дно флакона с раствором при наборе в шприц. Не переворачивайте флакон.
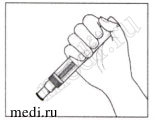
Осторожно отберите чуть более 1,0 мл раствора для подкожного введения из флакона в одноразовый шприц с градуировкой 1 мл и с иглой подходящего размера (например, «21G х 2»). Данная игла будет использована только для забора препарата Козэнтикс в одноразовый шприц. Подготовьте необходимое количество шприцев (1 шприц для дозы 150 мг, 2 шприца для дозы 300 мг).
Удерживая шприц иглой вверх, слегка постучите по шприцу для перемещения пузырьков воздуха кверху.
Замените иглу, использованную для забора препарата, на другую, размером «27 G х /г».
Замените иглу, использованную для забора препарата, на другую, размером «27 G х /г».
Замените иглу, использованную для забора препарата, на другую, размером «27G х ».
Удалите пузырьки воздуха и продвиньте поршень до отметки 1,0 мл.
Продезинфицируйте место инъекции спиртовым тампоном.
Введите раствор препарата Козэнтикс подкожно в переднебоковую поверхность бедра или нижнюю часть живота (за исключением пятисантиметровой области вокруг пупка) или наружную поверхность плеча. Места инъекции следует каждый раз менять. Не следует вводить в область поврежденной кожи (истончение, покраснение, раздражение, уплотнение, шелушение). Избегайте введения в места с наличием шрамов и растяжек.
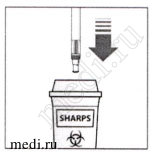
Оставшийся раствор во флаконе не должен использоваться и должен быть утилизирован. Флаконы предназначены только для одноразового использования. Утилизируйте использованный шприц в контейнер для острых предметов (закрывающийся, устойчивый к проколам контейнер). В целях Вашей безопасности и здоровья других, иглы и использованные шприцы ни в коем случае не должны использоваться повторно.
Действующее вещество
— секукинумаб (secukinumab)
Состав и форма выпуска препарата
Раствор для п/к введения от бесцветного до светло-желтого цвета, прозрачный или опалесцирующий.
Вспомогательные вещества: трегалозы дигидрат — 75.67 мг, гистидина гидрохлорида моногидрат /гистидин — 3.103 мг, метионин — 0.746 мг, полисорбат 80 — 0.2 мг, вода д/и — 1069 мг.
1 мл — шприцы стеклянные (1) с закреп. иглой с защит. колп..
1 мл — шприцы стеклянные (1) с устройством иглы в блистер — пачки картонные.
1 мл — шприцы стеклянные (2) с устройством иглы в блистер — пачки картонные.
1 мл — шприц-ручки (1) с устройством иглы в блистер — пачки картонные.
1 мл — шприц-ручки (2) с устройством иглы в блистер — пачки картонные.
Фармакологическое действие
Секукинумаб представляет собой полностью человеческое антитело (иммуноглобулин G1, IgG1), которое селективно связывается и нейтрализует провоспалительный цитокин — интерлейкин-17А (ИЛ-17А). Секукинумаб оказывает направленное действие на ИЛ-17 и ингибирует его взаимодействие с рецептором ИЛ-17, который экспрессируется разными типами клеток, включая кератиноциты и синовиоциты. В результате этого секукинумаб ингибирует высвобождение провоспалительных цитокинов, хемокинов и медиаторов повреждения тканей, снижает вклад ИЛ-17А в аутоиммунные и воспалительные заболевания. Секукинумаб в клинически значимых концентрациях достигает кожи и снижает концентрацию воспалительных маркеров. Прямым следствием лечения секукинумабом является уменьшение выраженности покраснения, уплотнения и шелушения кожи, что наблюдается в очагах поражения при бляшечном псориазе.
Применение секукинумаба у пациентов с бляшечным псориазом в дозе 300 мг обеспечивает более выраженное очищение кожных покровов по сравнению с применением в дозе 150 мг, с максимальным эффектом на 16 неделе. Секукинумаб демонстрирует эффективность как у пациентов, ранее не получавших терапию генно-инженерными биологическими препаратами (ГИБП), так и у пациентов с недостаточным ответом на терапию ГИБП-ингибиторами ФНОα, при этом несколько более выраженный ответ отмечен у пациентов, ранее не получавших терапию вышеуказанными препаратами. При применении секукинумаба отмечено улучшение симптомов и признаков заболевания, улучшение качества жизни, связанное с функциональным статусом и состоянием здоровья, а также замедление прогрессирования поражения периферических суставов.
У пациентов с псориатическим артритом на фоне терапии секукинумабом отмечается схожий ответ на лечение вне зависимости от применения его в монотерапии или в комбинации с метотрексатом. При применении секукинумаба к 16 и 24 неделям отмечено улучшение периферических симптомов псориатического артрита (например, уменьшение количества болезненных/припухших суставов, разрешение дактилитов, энтезитов, уменьшение степени выраженности поражения ногтей). Применение секукинумаба в дозе 150 мг к 24 неделе значительно подавляло степень прогрессирования поражения периферических суставов (относительного исходного показателя модифицированного общего счета Шарпа).
Рентгенологические признаки подавления прогрессии отмечены как у пациентов, ранее не получавших терапию ингибиторами ФНОα, так и у пациентов с недостаточным ответом на предшествующую терапию указанными препаратами. Схожее подавление структурного поражения отмечалось вне зависимости от комбинированного применения метотрексата. Применение секукинумаба у пациентов с анкилозирующим спондилитом приводило к улучшению подвижности позвоночника и его функции, уменьшению активности заболевания (в том числе снижению концентрации высокочувствительного СРБ). У пациентов, получавших секукинумаб без предшествующей терапии ингибиторами ФНОα, при магниторезонансной томографии к 16 неделе отмечено уменьшение признаков воспаления крестцово-подвздошных сочленений и позвоночника относительно исходных показателей.
Концентрация общего ИЛ-17А (свободного и связанного с секукинумабом) в сыворотке крови увеличивается в пределах 2-7 дней вследствие замедления клиренса, связанного с секукинумабом ИЛ-17А, свидетельствуя, что секукинумаб селективно связывается со свободным ИЛ-17А, который играет ключевую роль в патогенезе бляшечного псориаза.
В исследовании у пациентов с бляшечным псориазом после 1-2 недель лечения секукинумабом значительно снижались инфильтрация эпидермиса нейтрофилами и количество различных ассоциированных с ними маркеров, которое часто повышено в пораженных участках кожи у данных пациентов.
На фоне терапии секукинумабом у пациентов с псориатическим артритом и анкилозирующим спондилитом в течение 1-2 недель отмечалось снижение концентрации С-реактивного белка, являющегося маркером воспаления.
Фармакокинетика
После однократного п/к введения в дозе 150 мг или 300 мг при бляшечном псориазе Cmax секукинумаба в сыворотке крови составляла соответственно 13.7±4.8 мкг/мл или 27.3±9.5 мкг/мл в интервале между 5 и 6 днем после введения.
После первоначального еженедельного введения во время первого месяца Cmax достигалась между 31 и 34 днем.
Cmax в равновесном состоянии после п/к введения 150 мг или 300 мг составила 27.6 мкг/мл и 55.2 мкг/мл соответственно. Css достигается после 20 недель при ежемесячном режиме введения.
По сравнению с экспозицией после однократной дозы отмечено двукратное увеличение Cmax и AUC после многократного ежемесячного введения во время поддерживающей терапии.
Секукинумаб всасывается со средним показателем абсолютной биодоступности 73%.
Средний объем распределения в терминальной фазе (Vz) после однократного в/в введения варьировал между 7.10 и 8.60 л у пациентов с бляшечным псориазом, что позволяет предположить, что секукинумаб ограниченно распределяется на периферии.
Концентрации секукинумаба в межклеточной жидкости кожи у пациентов с бляшечным псориазом варьировали от 28% до 39% от таковой в сыворотке крови на 1-2 неделе после однократного п/к введения в дозе 300 мг.
Средний системный клиренс (CL) у пациентов с бляшечным псориазом составил 0.19 л/сут. Клиренс был дозо- и времязависимым, как и предполагалось для терапевтического IgG1-моноклонального антитела, взаимодействующего с растворимой цитокиновой мишенью, такой как ИЛ-17А.
Средний T1/2 у пациентов с бляшечным псориазом составлял 27 дней. Расчетный T1/2 у отдельных пациентов с псориазом варьировал от 17 до 41 дня.
При всех режимах дозирования экспозиция была пропорциональна дозе.
Фармакокинетические параметры секукинумаба у пациентов с псориатическим артритом, анкилозирующим спондилитом и бляшечным псориазом одинаковы.
Показания
Лечение псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия; лечение активного псориатического артрита в монотерапии или в комбинации с метотрексатом у взрослых пациентов при недостаточном ответе на предшествующую терапию базисными препаратами; лечение активного анкилозирующего спондилита у взрослых пациентов при недостаточном ответе на стандартную терапию.
Противопоказания
Повышенная чувствительность к секукинумабу; клинически значимые инфекции в фазе обострения (например, активный туберкулез); возраст до 18 лет; беременность, период грудного вскармливания.
С осторожностью: хронические рецидивирующие инфекции в анамнезе; болезнь Крона в активной фазе; вакцинация.
Дозировка
Для п/к введения.
Начальная доза — 300 мг в виде двух отдельных п/к инъекций по 150 мг.
Схема лечения зависит от показаний и клинического ответа.
Побочные действия
Со стороны системы кроветворения: нечасто — нейтропения.
Аллергические реакции: часто — крапивница; редко — анафилактические реакции.
Со стороны органа зрения: нечасто — конъюнктивит.
Со стороны дыхательной системы: очень часто — инфекции верхних дыхательных путей (в т.ч. очень часто — назофарингит, часто — инфекция верхних отделов дыхательных путей, ринит, фарингит, нечасто — синусит, тонзиллит); часто — ринорея.
Со стороны пищеварительной системы: часто — герпетическая инфекция слизистой оболочки полости рта; часто — диарея.
Со стороны кожи и подкожных тканей: нечасто — кандидозная инфекция полости рта, грибковое поражение кожи стоп, наружный отит; частота неизвестна — кандидозная инфекция кожи и слизистых оболочек
Лекарственное взаимодействие
Не применять одновременно с живыми вакцинами.
Повышенная концентрация цитокинов в условиях хронического воспалительного процесса подавляет образование некоторых изоферментов системы цитохрома. Таким образом, противовоспалительная терапия, в т.ч. секукинумабом, ингибитором ИЛ-17А, может привести к нормализации активности изоферментов цитохрома CYP450, сопровождающейся уменьшением экспозиции одновременно применяемых препаратов, метаболизм которых осуществляется с участием указанных изоферментов. Таким образом, нельзя исключить клинически значимого влияния на препараты — субстраты изоферментов системы цитохрома с узким терапевтическим индексом, доза которых подбирается индивидуально (например, варфарин). Следует рассмотреть возможность терапевтического контроля при начале терапии секукинумабом у пациентов, получающих лечение препаратами вышеуказанных групп.
Особые указания
Секукинумаб может увеличивать риск развития инфекций. Следует соблюдать осторожность при решении вопроса о применении секукинумаба у пациентов с хронической инфекцией или с рецидивирующей инфекцией в анамнезе.
Следует информировать пациента о необходимости обращения к врачу в случае появления признаков и симптомов, позволяющих заподозрить развитие инфекции. При развитии тяжелой инфекции необходимо тщательно наблюдать пациента, терапию секукинумабом следует отложить вплоть до разрешения инфекционного процесса.
Не следует применять у пациентов с активной формой туберкулеза. Перед началом лечения у пациентов с латентной формой туберкулеза следует рассмотреть возможность проведения противотуберкулезной терапии.
Следует соблюдать осторожность при применении препарата у пациентов с болезнью Крона в активной фазе, поскольку в клинических исследованиях отмечены случаи обострения болезни Крона. Следует тщательно наблюдать пациента с болезнью Крона в активной фазе, получающего терапию секукинумабом.
При возникновении анафилактических или других серьезных аллергических реакций применение секукинумаба следует немедленно прекратить и немедленно начать соответствующую терапию.
На фоне терапии секукинумабом не следует проводить вакцинацию живыми вакцинами. Для пациента, получающего секукинумаб, следует применять инактивированные или убитые вакцины. В клиническом исследовании у схожего количества пациентов, получавших секукинумаб, и получавших плацебо, отмечался адекватный иммунный ответ после вакцинации менингококковой и инактивированной гриппозной вакцинами, что проявлялось в виде 4-кратного увеличения титра антител к указанным вакцинам. Эти данные свидетельствуют, что секукинумаб не подавляет гуморальный иммунный ответ к менингококковой и инактивированной гриппозной вакцинам.
Беременность и лактация
Противопоказано применение при беременности и в период грудного вскармливания.
Женщинам с сохраненным репродуктивным потенциалом следует использовать надежные методы контрацепции во время лечения препаратом и как минимум в течение 20 недель после прекращения терапии
Применение в детском возрасте
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Применение в пожилом возрасте
Препарат разрешен для применения у пожилых пациентов
Описание препарата КОЗЭНТИКС основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Вспомогательные вещества: сахароза 92,43 мг, гистидин/гистидина гидрохлорида моногидрат 4,656 мг, полисорбат-80 0,60 мг.
- Клинически значимые инфекции в стадии обострения (например, активный туберкулез).
- Возраст до 18 лет в связи с отсутствием данных по эффективности и безопасности.
- Беременность и период грудного вскармливания.
C осторожностью
Следует соблюдать осторожность при назначении препарата Козэнтикс пациентам с хроническими инфекциями или с анамнестическими указаниями на них из-за повышенного риска развития инфекции, а также пациентам с активной стадией болезни Крона.
Так как съемный колпачок предварительно заполненного шприца с устройством для пассивной защиты иглы/предварительно заполненного шприца в автоинжекторе содержит производные натурального каучукового латекса, необходимо соблюдать осторожность при применении препарата Козэнтикс у пациентов с индивидуальной непереносимостью латекса. Пациенты, получающие препарат Козэнтикс, могут быть вакцинированы инактивированными или убитыми вакцинами, введение живых вакцин не должно проводиться.
Если у Вас одно из перечисленных заболеваний, перед приемом препарата обязательно проконсультируйтесь с врачом.
Рекомендации по применению
Препарат Козэнтикс вводится путем подкожной инъекции. По возможности следует избегать в качестве места для инъекции участки кожи, пораженные псориазом.
Лечение псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия: рекомендуемая доза составляет 300 мг в качестве начальной дозы на 0, 1, 2 и 3 неделе путем подкожной инъекции, которая в последующем вводится ежемесячно в качестве поддерживающей дозы, начиная с 4-й недели. Каждая доза 300 мг вводится в виде двух отдельных подкожных инъекций по 150 мг.
Лечение активного псориатического артрита в режиме монотерапии или в комбинации с метотрексатом у взрослых пациентов при недостаточном ответе на предшествующую терапию базисными препаратами: рекомендуемая доза составляет 150 мг в качестве начальной дозы на 0, 1, 2 и 3 неделе путем подкожной инъекции, которая в последующем вводится ежемесячно в качестве поддерживающей дозы, начиная с 4-й недели. Для пациентов с неадекватным ответом на терапию анти-ФНОα (фактор некроза опухоли α) препаратами или для пациентов с псориазом средней и тяжелой степени тяжести рекомендуемая доза составляет 300 мг в качестве начальной дозы на 0, 1, 2 и 3 неделе путем подкожной инъекции, которая в последующем вводится ежемесячно в качестве поддерживающей дозы, начиная с 4-й недели. Каждая доза 300 мг вводится в виде двух отдельных подкожных инъекций по 150 мг.
Лечение активного анкилозирующего спондилита у взрослых пациентов, при недостаточном ответе на стандартную терапию: рекомендуемая доза составляет 150 мг в качестве начальной дозы на 0, 1, 2 и 3 неделе путем подкожной инъекции, которая в последующем вводится ежемесячно в качестве поддерживающей дозы, начиная с 4-й недели.
Особые группы пациентов
Пациенты с нарушением функции печени или почек
Отсутствуют данные по применению препарата Козэнтикс у данной группы пациентов.
Пациенты моложе 18 лет
Эффективность и безопасность препарата у детей до 18 лет не установлена.
Пациенты старше 65 лет
Коррекция дозы не требуется.
Применение Козэнтикс при беременности и кормлении грудью
Исследования у лабораторных животных не показали прямого или косвенного негативного влияния на беременность, эмбриональное/фетальное развитие, роды или постнатальное развитие. Так как отсутствуют адекватные данные применения препарата Козэнтикс у беременных женщин, его применение у данной категории пациентов не рекомендовано. Неизвестно, проникает ли секукинумаб в грудное молоко у человека. Поскольку иммуноглобулины экскретируются с грудным молоком человека, не рекомендуется применять препарат Козэнтикс в период грудного вскармливания. Данных о влиянии препарата Козэнтикс на фертильность мужчин и женщин нет. В исследованиях препарата Козэнтикс у животных снижения фертильности отмечено не было.
Фармакологическое действие
Секукинумаб представляет собой полностью человеческое антитело (иммуноглобулин G1 (IgG1), которое селективно связывается и нейтрализует провоспалительный цитокин — интерлейкин-17А (ИЛ-17А). Секукинумаб оказывает направленное действие на ИЛ-17 и ингибирование его взаимодействия с рецептором ИЛ-17, который экспрессируется разными типами клеток, включая кератиноциты и синовиоциты. В результате этого секукинумаб ингибирует высвобождение провоспалительных цитокинов, хемокинов и медиаторов повреждения тканей, и снижает вклад ИЛ-17А в аутоиммунные и воспалительные заболевания. В клинически значимых концентрациях секукинумаб достигает кожи и снижает концентрацию местных воспалительных маркеров. Прямым следствием лечения секукинумабом является снижение выраженности покраснения, уплотнения и шелушения, являющихся результатом псориатического поражения.
ИЛ-17A является естественным цитокином, который участвует в нормально протекающих реакциях воспаления и иммунного ответа. ИЛ-17А играет ключевую роль в патогенезе развития бляшечного псориаза, псориатического артрита и анкилозирующего спондилита. Повышение концентрации ИЛ-17А, продуцируемого лимфоцитами и врожденными иммунными клетками, было обнаружено в крови и пораженных участках кожи у пациентов с бляшечным псориазом, псориатическим артритом и анкилозирующим спондилитом. Продукция ИЛ-17А является высокой в пораженной коже по сравнению с неповрежденной кожей у пациентов с бляшечным псориазом. В синовиальной жидкости у пациентов с псориатическим артритом и в субхондральном костном мозге костей фасеточных суставов у пациентов с анкилозирующим спондилитом обнаруживается высокая концентрация клеток, продуцирующих ИЛ-17А.
ИЛ-17А также способствует развитию воспаления тканей, инфильтрации нейтрофилами, деструкции костей и тканей, а также ремоделированию тканей, включая ангиогенез и фиброз.
Концентрация общего ИЛ-17А (свободного и связанного с секукинумабом ИЛ-17А) повышается вследствие снижения клиренса, связанного с секукинумабом ИЛ-17А в течение 2-7 дней у пациентов, получающих секукинумаб, указывая на то, что секукинумаб селективно захватывает свободный ИЛ-17А, играющий ключевую роль в патогенезе бляшечного псориаза.
После однократного подкожного введения дозы 150 мг или 300 мг при бляшечном псориазе, максимальная концентрация секукинумаба в сыворотке крови составляла, соответственно, 13,7±4,8 мкг/мл или 27,3±9,5 мкг/мл в интервале между 5 и 6 днем после введения.
После первоначального еженедельного введения во время первого месяца, время достижения максимальной концентрации было между 31 и 34 днем.
Максимальная концентрация в равновесном состоянии (Cmax, s s ) после подкожного введения 150 мг или 300 мг составила 27,6 мкг/мл и 55,2 мкг/мл, соответственно. Равновесное состояние достигается после 20 недель при ежемесячном режиме введения.
По сравнению с экспозицией после однократной дозы, отмечено двукратное повышение максимальной концентрации и площади под кривой зависимости концентрации от времени (AUC) после многократного ежемесячного введения во время поддерживающей терапии. Секукинумаб абсорбируется со средним показателем абсолютной биодоступности 73%.
Распределение
Средний объем распределения в терминальной фазе (Vz) после однократного внутривенного введения варьировал между 7,10 и 8,60 л у пациентов с бляшечным псориазом, вероятно, что секукинумаб ограниченно распределяется на периферии.
Концентрации секукинумаба в межклеточной жидкости кожи у пациентов с бляшечным псориазом варьировали от 28% до 39% от таковой в сыворотке крови на 1-2 неделе после однократного подкожного введения секукинумаба в дозе 300 мг.
Выведение
Средний системный клиренс (CL) у пациентов с бляшечным псориазом составил 0,19 л/сутки. Клиренс был дозо- и времязависимым, как и предполагалось для терапевтического IgGl моноклонального антитела, взаимодействующего с растворимой цитокиновой мишенью, такой как ИЛ-17А.
Средний период полувыведения у пациентов с бляшечным псориазом составлял 27 дней. Период полувыведения у отдельных пациентов с псориазом варьировал от 17 до 41 дня.
Линейность / нелинейность
Фармакокинетические параметры при однократном и многократном введении секукинумаба у пациентов с бляшечным псориазом были определены в отдельных исследованиях с внутривенным введением доз, варьировавших от 1 x 0,3 мг/кг до 3х10 мг/кг и с подкожным введением доз, варьировавших от 1х25 мг до многократной дозы 300 мг. При всех режимах дозирования экспозиция была пропорциональна дозе.
Фармакокинетические параметры секукинумаба у пациентов с псориатическим артритом, анкилозирующим артритом и бляшечным псориазом одинаковы.
Фармакокинетика в особых клинических случаях
Пациенты старше 65 лет
Основываясь на популяционном анализе фармакокинетических параметров, клиренс у пациентов старше 65 лет и пациентов младше данной возрастной группы был сходным.
Пациенты с нарушениями функции печени или почек
Доступные данные по фармакокинетике у пациентов с нарушениями функции печени или почек отсутствуют.
Побочные действия Козэнтикс
Наиболее часто встречаемыми нежелательными явлениями (НЯ) на фоне применения препарата Козэнтикс были инфекции верхних дыхательных путей (наиболее часто назофарингит, ринит). Большинство из них были слабо или умеренно выражены.
НЯ перечислены в соответствии с системно-органным классом медицинского словаря для нормативно-правовой деятельности MedDRA. В пределах каждого системно-органного класса НЯ распределены по частоте возникновения в порядке уменьшения их важности. Для оценки частоты использованы следующие критерии: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000), включая отдельные сообщения.
Инфекционные и паразитарные заболевания : очень часто — назофарингит, инфекция верхних отделов дыхательных путей; часто — ринит, фарингит, герпетическая инфекция слизистой оболочки полости рта; нечасто — синусит, тонзиллит, кандидозная инфекция полости рта, грибковое поражение кожи, воспаление наружного уха.
Нарушения со стороны крови и лимфатической системы: нечасто — нейтропения.
Нарушения со стороны органов зрения: нечасто — конъюнктивит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: часто — ринорея.
Нарушения со стороны желудочно-кишечного тракта: часто — диарея.
Нарушения со стороны кожи и подкожных тканей: часто — крапивница; редко — анафилактические реакции.
Иммуногенность
По данным клинических исследований препарата Козэнтикс в <1% случаев наблюдалось образование антител к секукинумабу, что не отразилось на эффективности терапии и фармакокинетических параметрах.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Особые указания
Инфекции
Препарат Козэнтикс может повышать риск развития инфекций. В клинических исследованиях у пациентов, получавших препарат Козэнтикс, наблюдались случаи развития инфекции, большинство которых были легкой или средней степени тяжести. Следует соблюдать осторожность при решении вопроса о применении препарата Козэнтикс у пациентов с хроническими инфекциями или с наличием в анамнезе рецидивирующей инфекции.
Пациенты должны быть проинформированы о необходимости обращения к врачу в случае появления признаков и симптомов, предполагающих развитие инфекции. В случае развития тяжелой инфекции пациент должен находиться под наблюдением, препарат Козэнтикс не должен вводиться до разрешения инфекции.
В клинических исследованиях не сообщалось о повышенной восприимчивости к туберкулезу, тем не менее, препарат Козэнтикс не следует назначать пациентам с активной формой туберкулеза. До начала лечения препаратом Козэнтикс должно быть принято решение о проведении противотуберкулезной терапии у пациентов с латентными формами туберкулеза.
Болезнь Крона
Следует соблюдать осторожность при назначении препарата Козэнтикс пациентам с обострением болезни Крона, поскольку в клинических исследованиях наблюдалось усугубление течения болезни Крона, в некоторых случаях тяжелое. Пациенты с обострением болезни Крона на фоне лечения препаратом Козэнтикс должны тщательно наблюдаться.
Реакции гиперчувствительности
При возникновении анафилактических или других серьезных аллергических реакций, применение препарата Козэнтикс следует немедленно прекратить, необходимо немедленно начать соответствующую симптоматическую терапию.
Пациенты с гиперчувствительностью к латексу
Съемный колпачок предварительно заполненного шприца с устройством для пассивной защиты иглы/предварительно заполненного шприца в автоинжекторе содержит производные натурального каучукового латекса. Хотя натуральный каучуковый латекс не обнаруживается в колпачке, безопасность применения препарата Козэнтикс в предварительно заполненном шприце с устройством для пассивной защиты иглы/предварительно заполненном шприце в автоинжекторе у пациентов с гиперчувствительностью к латексу не изучалась.
Вакцинация
Вакцинация живыми вакцинами не должна проводиться на фоне лечения препаратом Козэнтикс.
Пациенты, получающие препарат Козэнтикс, могут быть вакцинированы инактивированными или убитыми вакцинами. После вакцинации инактивированной менингококковой и гриппозной вакциной, у пациентов, получавших препарат Козэнтикс, отмечался адекватный иммунный ответ в виде как минимум четырехкратного повышения титра антител к менингококковой и гриппозной вакцине. Эти данные свидетельствуют о том, что препарат Козэнтикс не подавляет развитие иммунного ответа на введение менингококковой и гриппозной вакцины.
Влияние на фертильность
Женщинам с сохраненным детородным потенциалом следует использовать надежные методы контрацепции во время лечения препаратом и как минимум в течение 20 недель после прекращения терапии.
Влияние на способность управлять транспортными средствами и/или механизмами
Отсутствуют данные о влиянии препарата на способность управлять транспортными средствами и/или механизмами.
Передозировка
В ходе клинических исследований препарата Козэнтикс сообщений о случаях передозировки не было.
В ходе клинических исследований дозы до 30 мг/кг (т.е. приблизительно 2000-3000 мг) вводились внутривенно без развития дозолимитирующей токсичности. В случае передозировки рекомендуется наблюдение за пациентами для выявления признаков и симптомов НЯ. При необходимости следует незамедлительно провести симптоматическое лечение.
Лекарственное взаимодействие
Препарат Козэнтикс нельзя назначать вместе с живыми вакцинами. Данных о взаимодействии препарата Козэнтикс с другими лекарственными средствами у человека нет. Нет прямых данных, свидетельствующих об участии ИЛ-17А в экспрессии изоферментов системы цитохрома CYP450. Повышенная концентрация цитокинов в условиях хронического воспалительного процесса подавляет образование некоторых изоферментов системы цитохрома. Таким образом, противовоспалительная терапия, в т. ч. секукинумабом, ингибитором ИЛ-17А, может привести к нормализации активности изоферментов цитохрома CYP450, сопровождающейся уменьшением экспозиции одновременно применяемых препаратов, метаболизм которых осуществляется с участием указанных изоферментов. Т. о. не может быть исключено клинически значимое влияние на препараты, являющиеся субстратами изоферментов системы цитохрома с узким терапевтическим индексом, доза которых подбирается индивидуально (например, варфарин). Следует рассмотреть возможность проведения терапевтического контроля при начале терапии секукинумабом у пациентов, получающих лечение препаратами вышеуказанных групп.
При назначении препарата Козэнтикс одновременно с метотрексатом и/или глюкокортикостероидами у пациентов с псориатическим артритом и анкилозирующим спондилитом лекарственных взаимодействий выявлено не было.
Препарат Козэнтикс не должен смешиваться с какими-либо лекарственными препаратами.
Условия хранения
Хранить в недоступном для детей месте при температуре от 2 до 8 °С. Срок годности — 3 года.
Условия отпуска
Без рецепта
Козэнтикс
Козэнтикс: инструкция по применению и отзывы
- 1. Форма выпуска и состав
- 2. Фармакологические свойства
- 3. Показания к применению
- 4. Противопоказания
- 5. Способ применения и дозировка
- 6. Побочные действия
- 7. Передозировка
- 8. Особые указания
- 9. Применение при беременности и лактации
- 10. Применение в детском возрасте
- 11. При нарушениях функции почек
- 12. При нарушениях функции печени
- 13. Применение в пожилом возрасте
- 14. Лекарственное взаимодействие
- 15. Аналоги
- 16. Сроки и условия хранения
- 17. Условия отпуска из аптек
- 18. Отзывы
- 19. Цена в аптеках
Латинское название: Cosentyx
Код ATX: L04AC10
Действующее вещество: секукинумаб (Secukinumab)
Производитель: Новартис Фарма, АГ (Novartis Pharma, AG) (Швейцария)
Актуализация описания и фото: 28.10.2021
Цены в аптеках: от 14522 руб.
Козэнтикс – ингибитор интерлейкина.
Форма выпуска и состав
Лекарственные формы Козэнтикса:
- раствор для подкожного (п/к) введения: прозрачный или опалесцирующий, от бесцветного до светло-желтого цвета [по 1 мл в предварительно заполненных шприцах в автоинжекторах (шприц-ручках) или предварительно заполненных шприцах с устройством для пассивной защиты иглы, в картонной пачке 1–2 шприц-ручки или 1 блистер, содержащий 1–2 шприца с устройством для пассивной защиты иглы];
- лиофилизат для приготовления раствора для п/к введения: порошок или аморфная масса белого цвета (по 150 мг в бесцветных стеклянных флаконах объемом 6 мл, в картонной пачке 1 флакон).
В каждой пачке также содержится инструкция по применению Козэнтикса.
Состав 1 мл раствора:
- активное вещество: секукинумаб – 150 мг;
- вспомогательные компоненты: полисорбат-80, метионин, вода для инъекций, трегалозы дигидрат, гистидин или гистидина гидрохлорида моногидрат.
Состав 1 флакона лиофилизата:
- активное вещество: секукинумаб – 150 мг;
- вспомогательные компоненты: полисорбат-80, сахароза, гистидин или гистидина гидрохлорида моногидрат.
Фармакологические свойства
Фармакодинамика
Секукинумаб является полностью человеческим антителом, иммуноглобулином G1 (IgGl). Избирательно связывается и нейтрализует провоспалительный цитокин – интерлейкин-17А (ИЛ-17А), который экспрессируется разными типами клеток, включая синовиоциты и кератиноциты. ИЛ-17А участвует в нормально протекающих реакциях воспаления и иммунного ответа, играет ключевую роль в патогенезе развития бляшечного псориаза, анкилозирующего спондилита и псориатического артрита. При этих заболеваниях у пациентов в крови и пораженных участках кожи выявлена повышенная концентрация ИЛ-17А, вырабатываемого врожденными иммунными клетками и лимфоцитами.
В пораженной бляшечным псориазом коже продукция ИЛ-17А выше, чем в неповрежденной коже. В синовиальной жидкости у пациентов с псориатическим артритом, в субхондральном костном мозге костей фасеточных суставов у больных с анкилозирующим спондилитом обнаруживается высокая концентрация клеток, которые продуцируют ИЛ-17А.
ИЛ-17А также способствует развитию воспалительных процессов в тканях, инфильтрации нейтрофилами, деструкции тканей и костей. Содействует ремоделированию тканей, включая фиброз и ангиогенез.
Секукинумаб оказывает направленное действие на ИЛ-17 и ингибирует его взаимодействие с рецептором ИЛ-17, вследствие чего подавляет высвобождение провоспалительных цитокинов, медиаторов повреждения тканей и хемокинов, уменьшает вклад ИЛ-17А в развитие воспалительных и аутоиммунных заболеваний.
В клинически значимых концентрациях препарат достигает кожи, где уменьшает содержание местных воспалительных маркеров, в результате снижается выраженность покраснений, шелушения и уплотнения псориатических поражений.
На фоне применения Козэнтикса в течение 2–7 дней концентрация общего ИЛ-17А (свободного и связанного с секукинумабом) возрастает по причине снижения клиренса ИЛ-17А, связанного с секукинумабом. Это указывает на то, что секукинумаб избирательно захватывает свободный ИЛ-17А.
Согласно результатам исследования, повышенная инфильтрация эпидермальными нейтрофилами и различными нейтрофил-связанными маркерами в поврежденной бляшечным псориазом коже после 1–2 недель лечения препаратом значительно снижается.
У пациентов с псориатическим артритом и анкилозирующим спондилитом через 1–2 недели применения секукинумаба отмечается уменьшение концентрации С-реактивного белка (маркера воспаления).
Фармакокинетика
После однократного п/к введения Козэнтикса в дозе 150 или 300 мг пациентам с бляшечным псориазом максимальная плазменная концентрация (Cmax) достигается в течение 5–6 дней и составляет 13,7 ± 4,8 или 27,3 ± 9,5 мкг/мл соответственно.
После первоначального введения препарата 1 раз в неделю в течение 1 месяца время достижения Cmax составляло 31–34 дня.
В равновесном состоянии, которое при ежемесячном режиме введения достигается через 20 недель, Cmax после п/к введения дозы 150 или 300 мг составляла соответственно 27,6 или 55,2 мкг/мл.
При продолжительной поддерживающей терапии при ежемесячном режиме введения Козэнтикса отмечено 2-кратное повышение Cmax и AUC (площади под кривой «концентрация – время») по сравнению с экспозицией после однократного введения секукинумаба.
После однократного внутривенного (в/в) введения средний объем распределения в терминальной фазе (Vz) у пациентов с бляшечным псориазом варьировал между 7,1 и 8,6 л. Это, вероятно, свидетельствует об ограниченном распределении препарата на периферии.
У больных с бляшечным псориазом средний системный клиренс (CL) составлял 0,19 л/сутки. Клиренс характеризовался зависимостью от дозы и интервалов между введениями, как и ожидалось для терапевтического IgGl моноклонального антитела, которое взаимодействует с растворимой цитокиновой мишенью, такой как ИЛ-17А.
Период полувыведения (Т½) у пациентов с бляшечным псориазом в среднем составлял 27 дней, у отдельных пациентов варьировал от 17 до 41 дня.
При однократном и многократном применении Козэнтикса у пациентов с бляшечным псориазом фармакокинетические параметры определялись в отдельных исследованиях с в/в введением от одной дозы 0,3 мг/кг до трех доз по 10 мг/кг и с п/к введением от одной дозы 25 мг до многократных доз по 300 мг. При всех режимах дозирования экспозиция секукинумаба была пропорциональна дозе.
При псориатическом артрите, анкилозирующем артрите и бляшечном псориазе фармакокинетические характеристики секукинумаба одинаковы.
Нет доступных данных о фармакокинетике Козэнтикса у пациентов с нарушениями функции почек и печени.
Согласно данным популяционного анализа фармакокинетики секукинумаба, у лиц старше 65 лет клиренс препарата схож с таковым у пациентов более молодого возраста.
Показания к применению
- псориаз среднетяжелой и тяжелой степени при необходимости проведения системной терапии или фототерапии;
- активный псориатический артрит при недостаточном ответе на предшествующую терапию базисными лекарственными средствами (в качестве монопрепарата или в сочетании с метотрексатом);
- активный анкилозирующий спондилит при недостаточном ответе на стандартную терапию.
Противопоказания
Абсолютные:
- клинически значимые инфекции в стадии обострения (например, активный туберкулез);
- беременность и период грудного вскармливания;
- вакцинация живыми вакцинами;
- возраст до 18 лет;
- тяжелые реакции гиперчувствительности к любому компоненту препарата.
С осторожностью Козэнтикс должен применяться при активной стадии болезни Крона, хронических инфекциях в настоящее время или в анамнезе.
На предварительно заполненных шприцах и шприцах в автоинжекторах съемный колпачок содержит производные натурального каучукового латекса, что следует учитывать пациентам с индивидуальной непереносимостью латекса.
Козэнтикс, инструкция по применению: способ и дозировка
Препарат Козэнтикс предназначен для п/к введения. Для инъекций рекомендуется выбирать место в области передней поверхности бедер. Также можно вводить раствор в нижнюю треть живота, избегая пятисантиметровой области вокруг пупка. Если пациенту препарат вводит кто-то другой, допускается делать инъекции в наружную поверхность плеча. Места инъекции каждый раз следует менять.
Нельзя вводить Козэнтикс в участки, на которых поражены кожные покровы: присутствует уплотнение или истончение, шелушение, раздражение, покраснение. Также необходимо избегать введения в места, где имеются растяжки или шрамы, и в участки кожи, пораженные псориазом.
Рекомендуемые режимы дозирования:
- псориаз среднетяжелой и тяжелой степени: по 300 мг (в виде двух инъекций по 150 мг) на 0, 1, 2 и 3 неделе. Далее, начиная с 4-й недели, проводят поддерживающую терапию с введением Козэнтикса в аналогичной дозе 1 раз в месяц;
- активный псориатический артрит: по 150 мг на 0, 1, 2 и 3 неделе; начиная с 4-й недели – по 150 мг 1 раз в месяц. Пациентам с неадекватным ответом на терапию анти-ФНОα (фактор некроза опухоли альфа) рекомендуется повышение дозы до 300 мг (в виде двух инъекций по 150 мг), введение осуществляют по аналогичной схеме;
- активный анкилозирующий спондилит: по 150 мг на 0, 1, 2 и 3 неделе; начиная с 4-й недели – по 150 мг 1 раз в месяц.
После обучения технике введения препарата врач может доверить пациенту самостоятельное введение Козэнтикса, однако должен обеспечить соответствующее наблюдение во время всего лечения.
Для проведения инъекции потребуются:
- препарат;
- спиртовой тампон;
- марлевый или ватный тампон;
- контейнер для утилизации острых предметов.
Важная информация по безопасности и хранению:
- хранить в недоступном для детей месте;
- никогда не оставлять в местах, доступных для других лиц;
- не открывать запечатанную пачку до момента использования препарата;
- не использовать в случае нарушения целостности пачки или блистера, поскольку это может быть опасно;
- не встряхивать шприцы с раствором;
- до введения не прикасаться к защитным лапкам шприца, поскольку так можно преждевременно активировать автоматическое защитное устройство шприца;
- не снимать с иглы колпачок непосредственно до момента инъекции;
- всегда осматривать препарат на предмет соответствия цвета и прозрачности. Не использовать раствор в случае помутнения, изменения цвета или наличия видимых включений, а также при нарушении целостности шприца. Присутствие в растворе небольшого пузырька воздуха является нормальным;
- не применять шприцы повторно, использованные шприцы утилизировать в специальный контейнер для острых предметов;
- хранить препарат в холодильнике при температуре 2–8 °С, не замораживать;
- не использовать Козэнтикс после истечения срока годности, указанного на этикетке шприца или на картонной упаковке.
Применение Козэнтикса в предварительно заполненном шприце с устройством для пассивной защиты иглы
- Достать препарат из холодильника и оставить на 15–30 минут, чтобы раствор нагрелся до комнатной температуры.
- Тщательно вымыть руки с мылом.
- Спиртовым раствором протереть место будущей инъекции.
- Извлечь шприц из пачки и блистера.
- Осмотреть препарат на предмет соответствия цвета и прозрачности.
- Осторожно снять с иглы колпачок. На конце иглы может присутствовать капля раствора, это является нормой.
- Аккуратно собрать кожную складку между пальцами и под углом 45 ° ввести иглу на всю длину.
- Придерживая шприц, медленно нажать на поршень, пока его основание не окажется между боковыми защитными лапками.
- Удерживать шприц с нажатым поршнем в течение 5 секунд.
- Не отпуская поршень, извлечь иглу, затем медленно отпустить поршень и подождать, пока автоматическое защитное устройство скроет иглу.
- В случае кровоточивости приложить к месту инъекции марлевый/ватный тампон на 10 секунд. Не растирать область укола. При необходимости заклеить пластырем.
- Поместить использованный шприц в специальный контейнер.
Применение Козэнтикса в предварительно заполненном шприце в автоинжекторе
- Достать препарат из холодильника и оставить на 15–30 минут, чтобы раствор нагрелся до комнатной температуры.
- Тщательно вымыть руки с мылом.
- Спиртовым раствором протереть место будущей инъекции и оставить просохнуть.
- Снять со шприца колпачок и выбросить его.
- Взять шприц под углом 90 ° к месту инъекции.
- Прижать шприц плотно к коже. Во время введения препарата прозвучит два щелчка: первый означает начало инъекции, второй (раздастся через несколько секунд) указывает, что введение почти окончено. Необходимо удерживать шприц плотно прилегающим к коже, ожидая, пока зеленый индикатор заполнит смотровое окно и перестанет двигаться.
- Удалить шприц.
- В случае кровоточивости приложить к месту инъекции марлевый/ватный тампон на 10 секунд. Не растирать область укола. При необходимости заклеить пластырем.
- Поместить использованный шприц в специальный контейнер.
Применение Козэнтикса в форме лиофилизата для приготовления раствора для инъекций
- Согреть флакон с препаратом и стерильную инъекционную воду до комнатной температуры.
- Набрать 1 мл инъекционной воды в одноразовый шприц.
- Снять с флакона, содержащего лиофилизат, пластиковый колпачок.
- Вставить иглу в центр резиновой пробки флакона и медленно ввести инъекционную воду, направляя струю на лиофилизат.
- Наклонить флакон под углом примерно 45 °. Удерживая его кончиками пальцев, осторожно вращать в течение примерно 1 минуты. Не встряхивать и не переворачивать флакон.
- Оставить флакон в вертикальном положении хотя бы на 10 минут для полного растворения лиофилизата.
- Снова взять флакон под углом 45 ° и еще в течение 1 минуты вращать, не встряхивая и не переворачивая.
- Оставить флакон минут на 5 в вертикальном положении. Готовый раствор должен быть от бесцветного до светло-желтого цвета, прозрачным или опалесцирующим. Нельзя использовать препарат, если лиофилизат не растворился полностью, либо раствор содержит видимые включения, помутнел или изменил цвет.
- При назначении дозы 300 мг подготовить указанным выше способом второй флакон.
- Наклонить флакон под углом примерно 45° и поместить кончик иглы на дно флакона. Не переворачивать флакон.
- В одноразовый шприц с иглой подходящего размера (например, «21G × 2») осторожно отобрать чуть больше 1 мл раствора. При назначении дозы 300 мг подготовить второй шприц.
- Поднять шприц иглой вверх и слегка постучать по нему, чтобы пузырьки воздуха переместились вверх.
- Заменить иглу на другую, размером «27G × 1/2». Удалить из шприца пузырьки воздуха и подвинуть поршень до отметки 1 мл.
- Спиртовым тампоном продезинфицировать место инъекции.
- Ввести препарат.
- Утилизировать шприц, иглы и оставшийся во флаконе раствор.
Побочные действия
- инфекционные и паразитарные заболевания: очень часто (≥ 1/10) – назофарингит, инфекция верхних отделов дыхательных путей; часто (от ≥ 1/100 до < 1/10) – герпетическая инфекция слизистой оболочки полости рта, фарингит, ринит; нечасто (от ≥ 1/1000 до < 1/100) – кандидозная инфекция полости рта, тонзиллит, синусит, воспаление наружного уха, грибковое поражение кожи;
- со стороны кожи и подкожных тканей: часто – крапивница; редко (от ≥ 1/10 000 до < 1/1000) – анафилактические реакции;
- со стороны желудочно-кишечного тракта: часто – диарея;
- со стороны дыхательной системы: часто – ринорея;
- со стороны крови и лимфатической системы: нечасто – нейтропения;
- со стороны органов зрения: нечасто – конъюнктивит.
Согласно данным клинических исследований Козэнтикса, менее чем у 1% пациентов выявлялось образование антител к секукинумабу, однако на фармакокинетических параметрах и эффективности лечения это не отразилось.
Передозировка
Отсутствуют сообщения о случаях передозировки препарата. В клинических исследованиях в/в вводились дозы до 30 мг/кг (примерно 2000–3000 мг), дозолимитирующая токсичность не отмечена.
В случае введения чрезмерной дозы Козэнтикса показано тщательное наблюдение за состоянием пациента, при необходимости – проведение симптоматической терапии.
Особые указания
Отсутствует информация о влиянии Козэнтикса на фертильность. У животных снижение репродуктивной функции не отмечено. Тем не менее женщинам репродуктивного возраста во время лечения данным лекарственным средством и минимум в течение 20 недель после его окончания рекомендовано использовать надежные методы контрацепции.
На фоне терапии секукинумабом отмечено повышение риска развития инфекций. В клинических исследованиях наблюдались случаи инфекционных заболеваний, в большинстве случаев носящих легкий и умеренный характер. Пациентам с хроническими инфекциями и рецидивирующими инфекциями в анамнезе Козэнтикс должен назначаться после тщательной оценки соотношения пользы и потенциальных рисков.
Пациентов следует предупреждать о возможных симптомах, дающих основание подозревать развитие инфекции, при которых следует незамедлительно обращаться к врачу. При тяжелых инфекционных процессах требуется тщательный контроль. Применение Козэнтикса должно быть отменено до полного выздоровления.
В клинических исследованиях не отмечена повышенная восприимчивость к туберкулезу, однако при активной форме назначение Козэнтикса противопоказано. До назначения препарата пациентам с латентными формами заболевания рекомендуется проведение противотуберкулезной терапии.
Известны случаи усугубления болезни Крона у пациентов, получавших секукинумаб. В случае обострения заболевания требуется тщательное врачебное наблюдение.
Препарат Козэнтикс противопоказано применять совместно с живыми вакцинами. Если возникает необходимость, вакцинировать пациентов в период терапии следует инактивированными/убитыми вакцинами. У больных, получавших секукинумаб, после иммунизации инактивированной менингококковой и гриппозной вакциной был отмечен адекватный иммунный ответ в виде как минимум 4-кратного увеличения титра антител, что свидетельствует об отсутствии у Козэнтикса подавляющего действия в отношении указанных видов вакцин.
В случае развития серьезных аллергических или анафилактических реакций следует срочно отменить Козэнтикс и начать проведение соответствующей терапии.
В состав съемного колпачка предварительно заполненного шприца входят производные натурального каучукового латекса. И хотя сам натуральный латекс не содержится в колпачке, безопасность применения препарата в этой упаковке у пациентов с повышенной чувствительностью к латексу не установлена.
Влияние на способность к управлению автотранспортом и сложными механизмами
Данных о негативном влиянии Козэнтикса на способность к концентрации внимания и скорость реакций нет.
Применение при беременности и лактации
В исследованиях на животных не выявлено прямого или опосредованного негативного влияния на течение беременности, эмбриональное и фетальное развитие, а также на роды и постнатальное развитие. Однако опыта применения секукинумаба у беременных нет, поэтому женщинам, вынашивающим ребенка, противопоказано назначать Козэнтикс.
Экскретируется ли секукинумаб с грудным молоком, неизвестно (однако установлено, что иммуноглобулины выделяются с молоком матери), в связи с чем в период лактации Козэнтикс противопоказан.
Применение в детском возрасте
В связи с отсутствием данных о безопасности и эффективности лечения секукинумабом детей и подростков до 18 лет Козэнтикс не применяют в педиатрии.
При нарушениях функции почек
Нет доступных данных о фармакокинетике препарата у пациентов с нарушениями функции почек.
При нарушениях функции печени
Нет доступных данных о фармакокинетике Козэнтикса у пациентов с нарушениями функции печени.
Применение в пожилом возрасте
Коррекция дозы пациентам пожилого возраста не требуется.
Лекарственное взаимодействие
Козэнтикс противопоказано применять совместно с живыми вакцинами. Пациентам в период терапии можно вакцинироваться инактивированными вакцинами.
Козэнтикс нельзя смешивать ни с какими другими лекарственными препаратами. Лиофилизат можно разводить только водой для инъекций.
У пациентов с псориатическим артритом и анкилозирующим спондилитом не выявлены взаимодействия при одновременном применении метотрексата и/или глюкокортикостероидов.
Отсутствуют прямые данные об участии ИЛ-17А в экспрессии изоферментов системы цитохрома CYP450. Повышенный уровень цитокинов при хроническом воспалительном процессе подавляет образование некоторых изоферментов системы цитохрома. В связи с этим секукинумаб может нормализовать активность изоферментов цитохрома CYP450, что сопровождается снижением экспозиции одновременно применяемых лекарственных средств, которые метаболизируются при участии указанных изоферментов. Таким образом, нельзя исключить, что секукинумаб будет оказывать клинически значимое влияние на препараты, являющиеся субстратами изоферментов системы цитохрома, обладающие узким терапевтическим индексом, дозу которых подбирают индивидуально (например, варфарин). В таких ситуациях рекомендуется осуществлять тщательный контроль проводимой комбинированной терапии.
Аналоги
Информация об аналогах Козэнтикса отсутствует.
Сроки и условия хранения
Хранить в недоступном для детей, защищенном от света месте при температуре 2–8 °С. Не замораживать.
Срок годности раствора для инъекций – 2 года, лиофилизата для приготовления инъекционного раствора – 3 года.
После изъятия из холодильника использовать препарат следует в течение 1 ч.
Приготовленный из лиофилизата раствор можно хранить не более 24 ч при температуре 2–8 °С.
Условия отпуска из аптек
Отпускается по рецепту.
Отзывы о Козэнтиксе
На отечественном фармацевтическом рынке препарат появился сравнительно недавно, поэтому отзывов о Козэнтиксе немного. Пациенты отмечают, что уже после нескольких инъекций состояние значительно улучшается: мелкие псориатические высыпания исчезают, а крупные – существенно уменьшаются. К недостаткам относят высокую стоимость препарата.
Цена на Козэнтикс в аптеках
Примерная цена на Козэнтикс составляет: 1 шприц-ручка (1 мл раствора для инъекций) – 46 800 руб., 1 флакон с лиофилизатом для приготовления инъекционного раствора (150 мг) – 44 000 руб.
Информация о препарате является обобщенной, предоставляется в ознакомительных целях и не заменяет официальную инструкцию. Самолечение опасно для здоровья!