Добавил:
mrPutin
Я с Вами навсегда!
Опубликованный материал нарушает ваши авторские права? Сообщите нам.
Вуз:
Предмет:
Файл:
Скачиваний:
330
Добавлен:
11.05.2017
Размер:
476.16 Кб
Скачать
Принцип метода
основан на измерении поглощения света,
проходящего через исследуемый раствор.
|
№ |
Манипуляции |
Операции |
|
Подготовка |
||
|
1 |
|
Открыть крышку |
|
2 |
Тумблер «сеть» |
Включить на |
|
3 |
пуск |
Нажать красную |
|
4 |
Ø светофильтр |
Установить |
|
5 |
Ø фотоприемник |
Установить Правило
индикация
переключателя
светофильтра
(черная) →
красная → |
|
Измерение |
||
|
6 |
Ш0 |
Нажать клавишу |
|
7 |
|
Закрыть крышку |
|
8 |
К |
Нажать клавишу |
|
9 |
Еоп |
Ввести в световой |
|
10 |
Ест |
Ввести в световой |
|
Расчет |
||
|
9 |
Соп(х)=Еоп/Ест·Сст |
Пример: Еоп
Ест |
Инструкция по работе с фотокалориметром кфк-2
Принцип метода
основан на измерении поглощения света,
проходящего через исследуемый раствор.
|
№ |
Манипуляции |
Операции |
|
Подготовка |
||
|
1 |
|
Открыть крышку |
|
2 |
Тумблер «сеть» |
Включить на |
|
3 |
Ø |
Установить |
|
4 |
1 Ø |
Установить Правило
индикация
переключателя
светофильтра
(черная) →
красная → |
|
Измерение |
||
|
5 |
|
Закрыть крышку |
|
6 |
«0» |
Установить «0» |
|
7 |
Еоп |
Ввести в световой |
|
8 |
Ест |
Ввести в световой |
|
Расчет |
||
|
9 |
Соп(х)=Еоп/Ест·Сст |
Пример: Еоп
Ест |
46
Инструкция по эксплуатации прибора КФК-2 ИОТ — 024 — 10
1. Методика работы
1. Проверить заземление прибора.
2. Прибор прогреть 15 минут (кюветное отделение должно быть открыто).
3. Установить исследуемую пробу и контроль в кюветное отделение.
4. Рукояткой установить длину волны.
При измерении со светофильтрами 315, 364, 400, 440, 490, 540 нм, отмеченными на лицевой панели колориметра черным цветом, ручку «чувствительность» устанавливать в одно из положений «1» («2», «3»), отмеченных на лицевой панели также черным цветом.
При измерении со светофильтрами 590, 670, 750, 870, 980 нм, отмеченными на лицевой панели красным цветом, ручку «чувствительность» установить в положение «1» («2», «3»), отмеченное также красным цветом.
Установить ручку «точно» и ручку «установка 100 грубо» в крайне левое положение.
5. В световой пучок поместить кювету с контрольным раствором.
6. Закрыть крышку кюветного отделения.
7. Ручкой «чувствительность» и «установка 100 грубо» и «точно» установить отсчет 100 по шкале колориметра. Ручка «чувствительность» может находиться в одном из трех положений.
8. Затем поворотом ручки кювету с контрольным раствором заменить кювету с исследуемым раствором.
9. Снять отсчет по шкале колориметра, соответствующий коэффициенту пропускания исследуемого раствора в процентах.
10. Измерение проводить 3-5 раз и взять среднее значение из полученных значений.
11. Кюветы вынуть, прибор выключить.
12. Кюветы сполоснуть дистиллированной водой и этиловым спиртом, высушить. Протереть кюветное отделение.
2. Общие требования безопасности
2.1. К работе с прибором допускаются лица, изучившие настоящую инструкцию и паспорт к прибору, действующие правила эксплуатации и правила работы с химическими растворами.
2.2. Прибор должен быть заземлен.
2.3. Во время профилактических работ прибор должен быть отключен от сети.
2.4. Запрещается вскрывать прибор, работать на неисправном приборе, оставлять прибор включенным без присмотра.
2.5. Знать и выполнять инструкцию по охране труда в химической лаборатории.
|
ОПРЕДЕЛЕНИЕ Цель работы: Приборы и принадлежности: колориметр фотоэлектрический концентрационный КФК-2МП, набор 1.
|
|||||||||||
|
Зависимость коэффициента поглощения от длины волны называется спектром |
|||||||||||
|
Поэтому в случае слабых растворов, где взаимодействие молекул
где α0 – коэффициент поглощения, характерный для Соотношение (2) носит название закона Бера Учитывая (2), получим обобщенный закон Бугера–Бера:
При прохождении световых лучей через Изменение интенсивности света с учетом его поглощения и рассеяния
где γ – коэффициент рассеяния. В соответствии с законом Рэлея
Согласно закону |
|||||||||||
|
2. В данной работе измеряется оптическая плотность растворов. Оптическая плотность – это физическая величина, равная логарифму
Из формулы (3) следует
Тогда
и с учетом (6)
Между С0 и концентрацией С, выраженной в %, Для измерения оптической плотности Колориметр позволяет производить измерения коэффициентов пропускания Колориметр может применяться на предприятиях водоснабжения, в Внешний вид колориметра представлен на рис. 2. Колориметр состоит из колориметрического блока 1, вычислительного блока 2 В колориметрический блок входят осветитель, узел оптический, В узел оптический встроены конденсор, диафрагма и объектив (см. рис. Светофильтры |
|||||||||||
|
|
|||||||||||
Рис. 2 |
|||||||||||
|
Кюветы с растворителем или контрольным раствором устанавливаются в |
|||||||||||
|
|||||||||||
|
В фотометрическое В вычислительный блок 2 На передней панели МПС расположены клавиатура, цифровое табло и два Клавиша «Ц/Р» предназначена для перевода МПС в режим одиночных В блок питания входят стабилизаторы напряжений с выпрямителями и Оптическая схема колориметра изображена на рис. 3. Нить лампы 1 (см. рис. 3) Пластина 14 делит световой Принцип действия колориметра основан на поочередном измерении Световые потоки Ф0 и Ф фотоприемниками преобразуются |
|||||||||||
|
3. 3.1. Подсоедините колориметр к сети 220 В 3.2. Нажмите клавишу «пуск» – на цифровом табло появляется мигающая 3.3. Поворотом ручки 6 (см. 3.4. В кюветное отделение установите кюветы (l = 1 см) с растворителем и исследуемым раствором С1 3.5. Закройте крышку кюветного отделения, 3.6. Затем ручку 4 (см. рис. 3.7. Нажмите клавишу «Д(5)». На цифровом табло слева от мигающей 3.8. Операции по п. 3.4-3.7 проведите 3 раза. Оптическую плотность 3.9. Измерение оптической плотности проведите для ряда растворов 3.10. Полученные данные занесите в 3.11. По полученным экспериментальным данным постройте зависимость D 3.12. По диаграмме D = f (С) определите |
|||||||||||
|
Форма таблицы |
|||||||||||
|
|||||||||||
|
ВОПРОСЫ 1. Какова цель работы? 2. Поясните принцип действия колориметра. 3. Объясните механизм поглощения света веществом. 4. Опишите ход работы. 5. Дайте понятие оптической плотности. ВОПРОСЫ 1. Выведите закон Бугера–Бера. 2. Поясните границы применения закона Бугера–Бера. 3. Опишите практическое использование колориметра. ЛИТЕРАТУРА1. Кортнев А.В., 2. Годжаев Н.М. 3. Колориметр фотоэлектрический |
План урока производственного обучения
Раздел: Инструментальные методы анализа.
Цели урока:
- Обучающая: Интегрировать знания обучающихся по приёмам
последовательности работы на концентрационном фотоэлектроколориметре КФК-2. - Развивающая: формировать профессиональные компетенции
навыков и умений по определению оптических плотностей растворов и расчета
концентраций с использованием данных экспериментальной работы. Развивать
творческое мышление, память, трудолюбие. - Воспитывающая: прививать чувство ответственности, умения
грамотно использовать профессиональную лексику и самостоятельного овладения
дополнительными знаниями в области профессиональной деятельности. - Экологическое воспитание; раскрыть роль лаборанта-аналитика
в охране окружающей среды, водных ресурсов. - Здоровьесберегающая: профилактика умственного перенапряжения
путем смены видов деятельности.
Дидактические принципы
Научность обучения, связь теории и
практики, сознательность и добросовестность выполнения экспериментальной работы,
доступность овладения знаниями, активность обучения
Межпредметные связи
Аналитическая химия «Оптические методы анализа», технический
анализ «Анализ воды»,технический анализ производства СК «Определение иона
аммония с реактивом Несслера», физика «Спектральный анализ»,электротехника
«Определение цены деления прибора»,химия «Комплексные
соединения»,природопользование и охрана окружающей среды, охрана труда
Особые правила техники безопасности
Урок производственного обучения
проводится в лаборатории химического анализа ГОУ НПО ПУ-54 с соблюдением
основных параметров микроклимата согласно Роспотребнадзора
ХОД УРОКА
1. Организационная часть урока — 5 минут
Приветствие обучающихся,
Проверить посещаемость и внешний вид (наличие спецодежды).
2. Вводный инструктаж — 45 минут
Тема сегодняшнего урока производственного обучения:
«Фотоэлектрический колориметр КФК-2»
Цель: научиться работать на приборе – фотоэлектрическом
колориметре, снимать показания, определять оптическую плотность раствора и
концентрацию анализируемого вещества.
Прежде чем начать объяснение, хотела бы задать вопросы:
- Какими методами анализа можно определить состав вещества?
- Какие методы физико-химического анализа вы можете перечислить?
- Какие оптические методы анализа вы знаете?
За правильные подробные ответы, внимательность,
аккуратность, точность вы, будущие аналитики, будете получать баллы в течение
всех этапов урока производственного обучения, которые будут суммироваться в
конце занятия.
Объяснение нового материала
Для аналитических целей в исследовательских и
производственных лабораториях наряду с химическими методами широко применяют
физико-химические и физические методы анализа. Для выполнения таких анализов
применяют приборы со сложными электронными и оптическими схемами. Оптические
методы используют связь между составом анализируемого вещества и его
оптическими свойствами.
В зависимости от типа приборов различают
фотоколориметрический и спектрофотометрический методы.
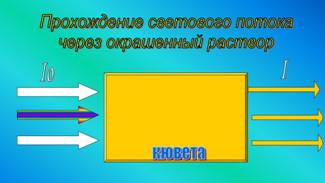
Если окрашенный раствор поместить в стеклянный сосуд с
плоскими стенками (кювету) и направить на него световой поток, то часть
светового потока отразится от кюветы, часть поглотится раствором и часть
пройдёт через раствор.
Когда световой поток проходит через окрашенный раствор,
поглощение света зависит от двух факторов – концентрации раствора и толщины
слоя, через который проходит световой поток. Эту зависимость выражает закон
Бугера-Ламберта–Бера, называемый также объединенным законом светопоглощения
Таким образом, оптическая плотность раствора прямо
пропорциональна концентрации раствора и толщине поглощающего слоя.
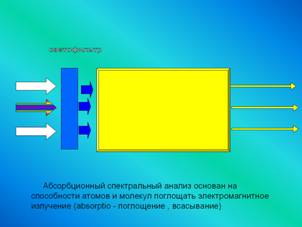
Окраска растворов связана с их способностью поглощать лучи
определенной длины волны. Для аналитических определений выделяют определенную
полосу спектра. Для этого используют светофильтры, которые обладают
избирательным поглощением лучистой энергии.
В приборах – фотоэлектроколориметрах – используется набор
цветных светофильтров, повышающих точность и чувствительность количественных
определений.
При колориметрическом методе анализа широко применяется
метод калибровочной кривой. Для этого предварительно готовят серию стандартных
растворов с известным содержанием определяемого вещества. Измеряют оптическую
плотность каждого раствора и строят график зависимости оптической плотности
раствора от концентрации – калибровочную кривую.
По калибровочной кривой находят содержание определяемого
вещества в анализируемом растворе.
Назначение и работа фотоэлектроколориметра КФК-2
Колориметр применяется на предприятиях водоснабжения, в
металлургической, химической, пищевой промышленности, в сельском хозяйстве, в
медицине и в других областях народного хозяйства.
Нормальными условиями работы колориметра являются:
температура окружающей среды (20 + 5)º С, относительная влажность воздуха
45- 80%, напряжение питания сети (220+ 4,4) В, 50 Гц.
Внешний вид колориметра КФК-2
Порядок измерений на
фотоэлектроколориметре КФК-2
1. Колориметр включить в сеть за
15 минут до начала измерений. Во время прогрева кюветное отделение должно быть
открыто (при этом шторка перед фотоприемниками перекрывает световой пучок).
2. Ввести необходимый по роду
измерения цветной светофильтр.
3. Установить минимальную
чувствительность колориметра. Для этого ручку ЧУВСТВИТЕЛЬНОСТЬ установить в
положение «1», ручку УСТАНОВКА 100 ГРУБО — в крайнее левое положение.
4. Перед измерениями и при
переключении фотоприемников проверить установку стрелки колориметра на «О».
5. В световой пучок поместить
кювету с растворителем или контрольным раствором, по отношению к которому
производятся измерения.
6. Закрыть крышку кюветного
отделения.
7 Ручками ЧУВСТВИТЕЛЬНОСТЬ и
УСТАНОВКА 100 ГРУБО и ТОЧНО установить отсчет 100 по шкале колориметра. Ручка
ЧУВСТВИТЕЛЬНОСТЬ может находиться в одном из трех положений: «1», «2» или «3».
8. Затем, поворотом ручки 4 кювету
с растворителем или контрольным раствором заменить кюветой с исследуемым
раствором.
9 Снять отсчет по шкале
колориметра, соответствующий коэффициенту пропускания исследуемого раствора в процентах
или по шкале Д в единицах оптической плотности.
10 Измерение проводить 2-3 раза
и окончательное значение измеренной величины определить как среднее
арифметическое из полученных значений.
Указания мер безопасности
Методика выполнения анализа «Определение
ионов аммония»
Состав и свойства воды для
хозяйственно-питьевых целей должны, прежде всего, отвечать санитарным требованиям.
Вода, поступающая из водоисточника, должна быть подвергнута анализу до и после
водоподготовки.
Ионы аммония и аммиак появляются в
грунтовых водах в результате жизнедеятельности микроорганизмов. Повышенное
содержание аммиака в поверхностных водах объясняется спуском в них бытовых
сточных вод и некоторых промышленных вод, содержащих значительные количества
аммиака или солей аммония, являющихся отходами производства.
Методика предназначена для
измерения содержания массовой концентрации ионов аммония от 0,05-4,0 мг/дм3
в природных и очищенных сточных водах фотометрическим методом с реактивом
Несслера.
Сущность метода
Фотометрический метод определения
массовой концентрации ионов аммония основан на взаимодействии NН4+-ионов
с тетраиодомеркуратом калия в щелочной среде (реактив Несслера) с образованием
коричневой, не растворимой в воде соли основания Миллона, переходящей в
коллоидную форму при малых содержаниях NH4 –
иона.
Светопоглощение раствора измеряют
при λ =440 нм в кюветах с длиной поглощающего слоя 50 мм. Интенсивность
окраски прямо пропорциональна концентрации NH4
+— ионов в растворе пробы.
Средства измерений, вспомогательные
устройства, реактивы и материалы
- Фотоэлектроколориметр КФК-2,
измеряющий светопоглощение при λ =440 нм. - Кюветы с длиной поглощающего слоя
50 мм. - Колбы мерные, наливные на 50
см³ - Пипетки на 1 см³
- Колбы с притёртыми пробками
вместимостью 250 см3 для хранения проб
Реактивы
- Стандартный образец с
аттестованным содержанием ионов аммония или аммоний хлористый ГОСТ 3773. - Реактив Несслера ТУ 6-09-2089.
- Калий-натрий виннокислый -4-х водный
(сегнетова соль) - Вода дистиллированная
- Все реактивы должны быть
квалификации х.ч. или ч.д.а.
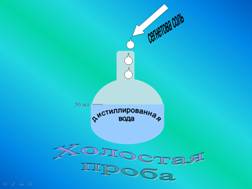
Приготовление основного раствора
хлористого аммония
Раствор готовят в день проведения
анализа, разбавлением основного стандартного раствора безаммиачной водой.
1 см3
раствора содержит 0,005 мг NH4+.
Выполнение измерений
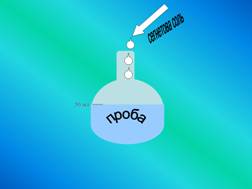
К 50 см3 первоначальной
пробы прибавляют 1-2 капли раствора сегнетовой соли и смесь тщательно
перемешивают. Затем добавляют 1 см3 реактива Несслера и снова
перемешивают. Через 10 мин измеряют оптическую плотность. Окраска смеси
устойчива в течение 30 мин.
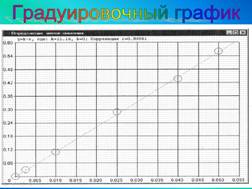
Построение градуировочного
графика
В мерные колбы вместимостью 50 см3
вносят 0,0; 0,5; 1,0; 2,0; 4,0; 6,0; 8,0; 10,0 см3 рабочего стандартного
раствора хлористого аммония, доводят до метки безаммиачной водой. Полученную
шкалу растворов с содержанием 0,0; 0,0025; 0,005; 0,01; 0,02; 0,03; 0,04; 0,05
мг NН4+ обрабатывают описанным
выше способом.
График строят методом наименьших
квадратов в координатах «оптическая плотность-содержание ионов аммония (мг)»
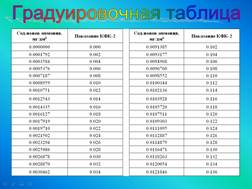
Обработка результатов измерения
Содержание ионов аммония NH4+ в мг/дм3 вычисляют по
градуировочному графику: КФК-2 кювета-50 мм, с/ф-440 нм.
Проверка усвоения учащимися материала
- Назначение фотоэлектроколориметра
КФК-2 - Внешний вид прибора
- Какой параметр снимают со шкалы
прибора? - Порядок работы на
фотоэлектроколориметре - Методика определения иона аммония
в сточных водах - Безопасным приемы труда на
рабочем месте в химической лаборатории. Запись в журнале инструктажей
охраны труда в лаборатории химического анализа ГОУ НПО ПУ-54.
3. Текущий инструктаж – 300 мин
Учебно-тренировочные упражнения
Формирование навыков и приемов
работы на КФК.
1. Группа разбивается на 2 бригады.
2. Выдается задание и инструкционная карта каждому учащемуся.
3. Решение производственной задачи. Видеосюжет проблемной ситуации «Оценить
работу лаборанта при выполнении анализа в производственных условиях».
4. Бригада №1 работает на КФК №1, бригада №2 Работает на КФК №2
5. Учащиеся проводят фотометрические измерения.
6. Результаты анализов корректируются и обобщаются в оценочном листе
профессиональной подготовленности обучающихся
Целевые обходы рабочих мест
Проверить содержание рабочих мест.
Особое внимание уделить проверке соблюдения безопасности
труда, требований безопасности при работе с электроприбором КФК-2, химическими
реактивами, стеклянной посудой
Правильность трудовых приемов:
- работа с пипетками,
- точность отбора проб воды,
- последовательность приливания
реактивов - подготовка и заполнение кювет,
- выбор светофильтра,
чувствительности, установка на ноль «грубо», «точно» - правильность отсчета по шкале
фотоэлектроколориметра.
Проверить правильность и точность расчета по
градуировочному графику.
- соблюдение технических условий
- ведение самоконтроля.
Провести приемку и оценку работ.
Выдать дополнительные работы наиболее успевающим учащимся.
4. Заключительный инструктаж – 10 мин
- Подвести итоги за день.
- Сообщить оценку качества каждого
учащегося. - Отметить, кто из учащихся добился
отличного качества работы. - Разобрать наиболее характерные
недочеты, их причины и способы устранения в работе. - Уборка рабочих мест.
- Домашнее задание:
1) Выполнить творческую работу по фотоколориметрическому
методу анализа в форме 10 тестов или вопросов (на выбор).
В.П.Васильев Аналитическая химия, с155-161;
2) составить алгоритмы работы на КФК-2.
Список использованной литературы
1. Аналитическая химия. Лабораторный практикум: учебное пособие для вузов/
под. ред. В.П.Васильева – М.: Дрофа, 2006. — 414с.
2. Гурвич Я.А. Химический анализ: Учебник для средних ПТУ. – М.: — Высшая
школа, 1985. – 295 с.
3. Инструкция ИОТ-10 Охрана труда при выполнении лабораторных работ,
Стерлитамак 2006 – 15с.
4. Методика лаборатории службы воздуха ОАО «Синтез-Каучук» Определение иона
аммония в сточных водах фотометрическим методом
5. Паспорт. Колориметр фотоэлектрический концентрационный КФК-2
Приложения
1. Вопросы проверки уровня усвоения знаний (Приложение 1)
2. Мониторинг результатов знаний и трудовых приемов, обучающихся
при выполнении фотометрического определения ионов аммония в сточных водах
(Приложение 2)
3. Структурные элементы занятия (Приложение 3)
4. Оценочный лист профессиональной подготовленности обучающихся
на уроке п/о (Приложение 4)
5. Инструкционная карта практической работы № 1 (Приложение
5)
6. Презентация «Фотоэлектрической колориметр КФК-2» (Приложение
6)