Fluorouracil Cream Prescribing Information
Package insert / product label
Dosage form: cream
Drug class: Topical antineoplastics
Medically reviewed by Drugs.com. Last updated on Dec 19, 2021.
On This Page
- Description
- Clinical Pharmacology
- Indications and Usage
- Contraindications
- Warnings
- Precautions
- Patient Counseling Information
- Adverse Reactions/Side Effects
- Overdosage
- Dosage and Administration
- How Supplied/Storage and Handling
- Storage and Handling
Rx only
FOR TOPICAL USE ONLY
NOT FOR OPHTHALMIC, ORAL, OR INTRAVAGINAL USE
Fluorouracil Cream Description
Fluorouracil Topical Cream is a topical preparation containing the fluorinated pyrimidine 5-fluorouracil, an antineoplastic antimetabolite.
Fluorouracil Topical Cream contains 5% w/w of fluorouracil USP in a cream base consisting of methylparaben, polysorbate 60, propylene glycol, propylparaben, purified water, stearyl alcohol and white petrolatum.
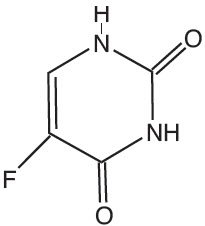
Chemically, fluorouracil is 5-fluoro-2,4(1H,3H)-pyrimidinedione. It is a white to practically white crystalline powder which is sparingly soluble in water and slightly soluble in alcohol. One gram of fluorouracil is soluble in 100 mL of propylene glycol. The molecular weight of 5-fluorouracil is 130.08 and the structural formula is:
Fluorouracil Cream — Clinical Pharmacology
There is evidence that the metabolism of fluorouracil in the anabolic pathway blocks the methylation reaction of deoxyuridylic acid to thymidylic acid. In this manner fluorouracil interferes with the synthesis of deoxyribonucleic acid (DNA) and to a lesser extent inhibits the formation of ribonucleic acid (RNA). Since DNA and RNA are essential for cell division and growth, the effect of fluorouracil may be to create a thymine deficiency which provokes unbalanced growth and death of the cell. The effects of DNA and RNA deprivation are most marked on those cells which grow more rapidly and take up fluorouracil at a more rapid rate. The catabolic metabolism of fluorouracil results in degradation products (e.g., CO2, urea, α-fluoro-β-alanine) which are inactive.
Systemic absorption studies of topically applied fluorouracil have been performed on patients with actinic keratoses using tracer amounts of 14C-labeled fluorouracil added to a 5% preparation. All patients had been receiving nonlabeled fluorouracil until the peak of the inflammatory reaction occurred (2 to 3 weeks), ensuring that the time of maximum absorption was used for measurement. One gram of labeled preparation was applied to the entire face and neck and left in place for 12 hours. Urine samples were collected. At the end of 3 days, the total recovery ranged between 0.48% and 0.94% with an average of 0.76%, indicating that approximately 5.98% of the topical dose was absorbed systemically. If applied twice daily, this would indicate systemic absorption of topical fluorouracil to be in the range of 5 to 6 mg per daily dose of 100 mg. In an additional study, negligible amounts of labeled material were found in plasma, urine and expired CO2 after 3 days of treatment with topically applied 14C-labeled fluorouracil.
Indications and Usage for Fluorouracil Cream
Fluorouracil is recommended for the topical treatment of multiple actinic or solar keratoses. In the 5% strength, it is also useful in the treatment of superficial basal cell carcinomas when conventional methods are impractical, such as with multiple lesions or difficult treatment sites. Safety and efficacy in other indications have not been established.
The diagnosis should be established prior to treatment, since this method has not been proven effective in other types of basal cell carcinomas. With isolated, easily accessible basal cell carcinomas, surgery is preferred since success with such lesions is almost 100%. The success rate with fluorouracil cream and solution is approximately 93%, based on 113 lesions in 54 patients. Twenty-five lesions treated with the solution produced 1 failure and 88 lesions treated with the cream produced 7 failures.
Contraindications
Fluorouracil may cause fetal harm when administered to a pregnant woman.
There are no adequate and well-controlled studies in pregnant women with either the topical or the parenteral forms of fluorouracil. One birth defect (cleft lip and palate) has been reported in the newborn of a patient using fluorouracil as recommended. One birth defect (ventricular septal defect) and cases of miscarriage have been reported when fluorouracil was applied to mucous membrane areas. Multiple birth defects have been reported in a fetus of a patient treated with intravenous fluorouracil.
Animal reproduction studies have not been conducted with fluorouracil. Fluorouracil administered parenterally has been shown to be teratogenic in mice, rats, and hamsters when given at doses equivalent to the usual human intravenous dose; however, the amount of fluorouracil absorbed systemically after topical administration to actinic keratoses is minimal (see CLINICAL PHARMACOLOGY). Fluorouracil exhibited maximum teratogenicity when given to mice as single intraperitoneal injections of 10 to 40 mg/kg on Day 10 or 12 of gestation. Similarly, intraperitoneal doses of 12 to 37 mg/kg given to rats between Days 9 and 12 of gestation and intramuscular doses of 3 to 9 mg/kg given to hamsters between Days 8 and 11 of gestation were teratogenic and/or embryotoxic (i.e., resulted in increased resorptions or embryolethality). In monkeys, divided doses of 40 mg/kg given between Days 20 and 24 of gestation were not teratogenic. Doses higher than 40 mg/kg resulted in abortion.
Fluorouracil should not be used in patients with dihydropyrimidine dehydrogenase (DPD) enzyme deficiency. A large percentage of fluorouracil is catabolized by the DPD enzyme. DPD enzyme deficiency can result in shunting of fluorouracil to the anabolic pathway, leading to cytotoxic activity and potential toxicities.
Fluorouracil is contraindicated in women who are or may become pregnant during therapy. If this drug is used during pregnancy, or if the patient becomes pregnant while using this drug, the patient should be apprised of the potential hazard to the fetus.
Fluorouracil is also contraindicated in patients with known hypersensitivity to any of its components.
Warnings
Application to mucous membranes should be avoided due to the possibility of local inflammation and ulceration. Additionally, cases of miscarriage and a birth defect (ventricular septal defect) have been reported when fluorouracil was applied to mucous membrane areas during pregnancy.
Occlusion of the skin with resultant hydration has been shown to increase percutaneous penetration of several topical preparations. If any occlusive dressing is used in treatment of basal cell carcinoma, there may be an increase in the severity of inflammatory reactions in the adjacent normal skin. A porous gauze dressing may be applied for cosmetic reasons without increase in reaction.
Exposure to ultraviolet rays should be minimized during and immediately following treatment with fluorouracil because the intensity of the reaction may be increased.
Patients should discontinue therapy with fluorouracil if symptoms of DPD enzyme deficiency develop (see CONTRAINDICATIONS section).
Rarely, life-threatening toxicities such as stomatitis, diarrhea, neutropenia, and neurotoxicity have been reported with intravenous administration of fluorouracil in patients with DPD enzyme deficiency. One case of life-threatening systemic toxicity has been reported with the topical use of fluorouracil in a patient with DPD enzyme deficiency. Symptoms included severe abdominal pain, bloody diarrhea, vomiting, fever, and chills. Physical examination revealed stomatitis, erythematous skin rash, neutropenia, thrombocytopenia, inflammation of the esophagus, stomach, and small bowel. Although this case was observed with 5% fluorouracil cream, it is unknown whether patients with profound DPD enzyme deficiency would develop systemic toxicity with lower concentrations of topically applied fluorouracil.
Precautions
General
There is a possibility of increased absorption through ulcerated or inflamed skin.
Information for Patients
Patients should be forewarned that the reaction in the treated areas may be unsightly during therapy and, usually, for several weeks following cessation of therapy. Patients should be instructed to avoid exposure to ultraviolet rays during and immediately following treatment with fluorouracil because the intensity of the reaction may be increased. If fluorouracil is applied with the fingers, the hands should be washed immediately afterward. Fluorouracil should not be applied on the eyelids or directly into the eyes, nose or mouth because irritation may occur.
Fluorouracil, including fluorouracil cream, may be fatal if ingested by pets. Avoid allowing pets to contact the fluorouracil cream container or the skin where fluorouracil cream has been applied. Store fluorouracil cream out of reach of pets. Safely discard or clean any cloth or applicator that may retain fluorouracil cream and avoid leaving any residues of fluorouracil cream on your hands, clothing, carpeting or furniture.
Laboratory Tests
Solar keratoses which do not respond should be biopsied to confirm the diagnosis. Follow-up biopsies should be performed as indicated in the management of superficial basal cell carcinoma.
Carcinogenesis, Mutagenesis, Impairment of Fertility
Adequate long-term studies in animals to evaluate carcinogenic potential have not been conducted with fluorouracil. Studies with the active ingredient of fluorouracil, 5-fluorouracil, have shown positive effects in in vitro tests for mutagenicity and on impairment of fertility.
5-Fluorouracil was positive in three in vitro cell neoplastic transformation assays. In the C3H/10T½ clone 8 mouse embryo cell system, the resulting morphologically transformed cells formed tumors when inoculated into immunosuppressed syngeneic mice.
While no evidence for mutagenic activity was observed in the Ames test (three studies), fluorouracil has been shown to be mutagenic in the survival count rec-assay with Bacillus subtilis and in the Drosophila wing-hair spot test. Fluorouracil produced petite mutations in Saccharomyces cerevisiae and was positive in the micronucleus test (bone marrow cells of male mice).
Fluorouracil was clastogenic in vitro (i.e., chromatid gaps, breaks and exchanges) in Chinese hamster fibroblasts at concentrations of 1.0 and 2.0 mcg/mL and has been shown to increase sister chromatid exchange in vitro in human lymphocytes. In addition, 5-fluorouracil has been reported to produce an increase in numerical and structural chromosome aberrations in peripheral lymphocytes of patients treated with this product.
Doses of 125 to 250 mg/kg, administered intraperitoneally, have been shown to induce chromosomal aberrations and changes in chromosome organization of spermatogonia in rats. Spermatogonial differentiation was also inhibited by fluorouracil, resulting in transient infertility. However, in studies with a strain of mouse which is sensitive to the induction of sperm head abnormalities after exposure to a range of chemical mutagens and carcinogens, fluorouracil was inactive at oral doses of 5 to 80 mg/kg/day. In female rats, fluorouracil administered intraperitoneally at doses of 25 and 50 mg/kg during the preovulatory phase of oogenesis significantly reduced the incidence of fertile matings, delayed the development of preimplantation and postimplantation embryos, increased the incidence of preimplantation lethality and induced chromosomal anomalies in these embryos. Single-dose intravenous and intraperitoneal injections of 5-fluorouracil have been reported to kill differentiated spermatogonia and spermatocytes (at 500 mg/kg) and to produce abnormalities in spermatids (at 50 mg/kg) in mice.
Pregnancy
See CONTRAINDICATIONS.
Nursing Mothers
It is not known whether fluorouracil is excreted in human milk. Because there is some systemic absorption of fluorouracil after topical administration (see CLINICAL PHARMACOLOGY), because many drugs are excreted in human milk, and because of the potential for serious adverse reactions in nursing infants, a decision should be made whether to discontinue nursing or to discontinue use of the drug, taking into account the importance of the drug to the mother.
Pediatric Use
Safety and effectiveness in children have not been established.
Adverse Reactions/Side Effects
The most frequent adverse reactions to fluorouracil occur locally and are often related to an extension of the pharmacological activity of the drug. These include burning, crusting, allergic contact dermatitis, pruritus, scarring, rash, soreness and ulceration. Ulcerations, other local reactions, cases of miscarriage and a birth defect (ventricular septal defect) have been reported when fluorouracil was applied to mucous membrane areas. Leukocytosis is the most frequent hematological side effect.
Although a causal relationship is remote, other adverse reactions which have been reported infrequently are:
Central Nervous System: Emotional upset, insomnia, irritability.
Gastrointestinal: Medicinal taste, stomatitis.
Hematological: Eosinophilia, thrombocytopenia, toxic granulation.
Integumentary: Alopecia, blistering, bullous pemphigoid, discomfort, ichthyosis, scaling, suppuration, swelling, telangiectasia, tenderness, urticaria, skin rash.
Special Senses: Conjunctival reaction, corneal reaction, lacrimation, nasal irritation.
Miscellaneous: Herpes simplex.
To report SUSPECTED ADVERSE REACTIONS, contact Northstar RxLLC at 1-800-206-7821 and/or FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
Overdosage
There have been no reports of overdosage with fluorouracil.
The oral LD50 for the 5% topical cream was 234 mg/kg in rats and 39 mg/kg in dogs. These doses represented 11.7 and 1.95 mg/kg of fluorouracil, respectively. Studies with a 5% topical solution yielded an oral LD50 of 214 mg/kg in rats and 28.5 mg/kg in dogs, corresponding to 10.7 and 1.43 mg/kg of fluorouracil, respectively. The topical application of the 5% cream to rats yielded an LD50 of greater than 500 mg/kg.
Fluorouracil Cream Dosage and Administration
When fluorouracil is applied to a lesion, a response occurs with the following sequence: erythema, usually followed by vesiculation, desquamation, erosion and re-epithelialization.
Fluorouracil should be applied preferably with a nonmetal applicator or suitable glove. If fluorouracil is applied with the fingers, the hands should be washed immediately afterward.
Actinic or Solar Keratosis
Apply cream twice daily in an amount sufficient to cover the lesions. Medication should be continued until the inflammatory response reaches the erosion stage, at which time use of the drug should be terminated. The usual duration of therapy is from 2 to 4 weeks. Complete healing of the lesions may not be evident for 1 to 2 months following cessation of fluorouracil therapy.
Superficial Basal Cell Carcinomas
Only the 5% strength is recommended. Apply cream twice daily in an amount sufficient to cover the lesions. Treatment should be continued for at least 3 to 6 weeks. Therapy may be required for as long as 10 to 12 weeks before the lesions are obliterated. As in any neoplastic condition, the patient should be followed for a reasonable period of time to determine if a cure has been obtained.
How is Fluorouracil Cream supplied
Fluorouracil Topical Cream USP, 5% is supplied in a 40 g tube (NDC 16714-178-01).
Store at 20° to 25°C (68° to 77°F) [see USP Controlled Room Temperature].
Manufactured for: Northstar RxLLC
Memphis, TN 38141.
Manufactured by: Taro Pharmaceutical Industries Ltd.
Haifa Bay, Israel, 2624761
Issued: November 2021
5223743-1121-00 29
PRINCIPAL DISPLAY PANEL — 40 g Tube Carton
NDC 16714-178-01
Rx only
Fluorouracil Topical Cream USP
5%
FOR TOPICAL USE ONLY. NOT FOR OPHTHALMIC, ORAL, OR INTRAVAGINAL USE.
NORTHSTARx®
40 g
| FLUOROURACIL fluorouracil cream |
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
Labeler — NORTHSTAR RX LLC
(830546433)
Medical Disclaimer
Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Фторурацил
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Фторурацил
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Фторурацил
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Фторурацил
Структурная формула
Русское название
Фторурацил
Английское название
Fluorouracil
Латинское название
Phthoruracilum (род. Phthoruracili)
Химическое название
5-Фтор-2,4-(1Н,3Н)-пиримидиндион (и в виде натриевой соли)
Брутто формула
C4H3FN2O2
Фармакологическая группа вещества Фторурацил
Нозологическая классификация
Список кодов МКБ-10
-
C15 Злокачественное новообразование пищевода
-
C16 Злокачественное новообразование желудка
-
C18 Злокачественное новообразование ободочной кишки
-
C19 Злокачественное новообразование ректосигмоидного соединения
-
C20 Злокачественное новообразование прямой кишки
-
C22.0 Печеночноклеточный рак
-
C25 Злокачественное новообразование поджелудочной железы
-
C26 Злокачественное новообразование других и неточно обозначенных органов пищеварения
-
C50 Злокачественные новообразования молочной железы
-
C51 Злокачественное новообразование вульвы
-
C53 Злокачественное новообразование шейки матки
-
C56 Злокачественное новообразование яичника
-
C60 Злокачественное новообразование полового члена
-
C61 Злокачественное новообразование предстательной железы
-
C67 Злокачественное новообразование мочевого пузыря
-
C74 Злокачественное новообразование надпочечника
-
C76.0 Головы, лица и шеи
Код CAS
51-21-8
Фармакологическое действие
—
противоопухолевое, цитостатическое.
Характеристика
Кристаллический порошок от белого до практически белого цвета, практически без запаха. Разлагается при температуре около 282 °C. Слабо растворим в воде и спирте и практически нерастворим в хлороформе и эфире. Молекулярная масса 130,08 г/моль.
Фармакология
Механизм действия
По-видимому, существует два механизма действия фторурацила, которые приводят к цитотоксическим эффектам. Одним из них является конкурентное ингибирование тимидилатсинтетазы, фермента, катализирующего метилирование дезоксиуридиловой кислоты, приводящее к образованию тимидиловой кислоты. Последующий дефицит тимидина приводит к ингибированию синтеза ДНК, вызывая таким образом гибель клеток. О втором механизме действия свидетельствует умеренное ингибирование РНК и включение фторурацила в РНК. Преобладающий механизм противоопухолевого действия, по-видимому, зависит, по крайней мере частично, от индивидуального внутриклеточного метаболизма опухоли.
Последствия угнетения образования ДНК и РНК наиболее значительны для тех клеток, которые наиболее быстро размножаются.
Фармакокинетика
После в/в введения фторурацил быстро выводится из плазмы (T1/2 около 10–20 мин) и распределяется по тканям организма, включая спинномозговую жидкость и злокачественные выпоты, демонстрируя Vd, эквивалентный общему объему жидкости в организме. Концентрация фторурацила в плазме крови снижается до величин, которые ниже измеримых уровней, в течение 3 ч. Пероральное применение фторурацила показало заметную вариабельность его биодоступности — от 28 до 100%. При непрерывной в/в инфузии в течение 96 ч наблюдался постоянный уровень фторурацила в плазме крови и значительно меньшее его количество (от 50 до 1000 раз) обнаруживалось в костном мозге.
Фторурацил превращается в активные нуклеотидные метаболиты, 5-фторуридинмонофосфат и 5-фтордезоксиуридилат внутри самой клетки-мишени. Примерно 20% в/в дозы выводится в неизмененном виде с мочой в течение 6 ч. Остальная часть метаболизируется главным образом в печени, где при ферментативном расщеплении образуются альфа-фтор-бета-аланин, диоксид углерода, мочевина и аммиак. Нелинейность фармакокинетики фторурацила связана с насыщаемостью ферментов, ответственных за его деградацию.
Исследования на клеточных культурах
Механизм цитотоксичности, вызываемой фторурацилом, связан с прямым действием как на РНК, так и на ДНК, в зависимости от линии опухолевых клеток. Предварительная обработка лимфоцитов мыши фторурацилом предотвращала переход этих клеток из фазы G1 в фазу S клеточного цикла, тем самым ингибируя репликацию их ДНК и вызывая многочисленные обрывы цепи ДНК. В нетоксичных концентрациях фторурацил проявлял способность синхронизировать и увеличивать долю клеток в чувствительной к нему S-фазе. Усиление цитотоксичности фторурацила было продемонстрировано в клетках Hela, синхронизированных методом двойного тимидинового блока и обработанных препаратом во время фазы синтеза ДНК. Противоопухолевая активность возрастала при увеличении времени воздействия. Метаболическое фосфорилирование фторурацила происходило быстрее в опухолевой ткани, чем в нормальной.
Исследования на животных
У крыс с пересаженной опухолью толстой кишки семидневная в/в инфузия фторурацила (от 25 до 35 мг/кг/сут) приводила к излечению от опухоли на 30–70%, в то время как ежедневные в/в болюсные инъекции (25 мг/кг/день) в течение 7 дней давали от 80 до 100% излечечения без видимой лекарственной токсичности. Зависимость эффекта от концентрации наблюдалась при 7-дневной инфузии фторурацила, где скорость излечения увеличилась с 30 до 80%, когда Css возрастала с 136 нг/мл при дозе 25 мг/кг/сут до 240 нг/мл при дозе 35 мг/кг/сут. Дальнейшее увеличение Css до 331 нг/мл при дозе 50 мг/кг/сут приводило к тяжелым токсическим реакциям. При используемых дозировках распределение фторурацила описывалось нелинейной кинетикой, выведение из крови зависело от способа введения, а также скорости инфузии, при этом клиренс увеличивался при более медленных скоростях введения.
Доклинические исследования
Острая токсичность
| Вид | Количество | Путь введения | Среднее значение LD50, мг/кг | Пол |
| Мышь | 3–6 | Внутрибрюшинно | 340 | Женский |
| Морская свинка | 5 | В/в | 25,5 | Мужской |
Подострая токсичность
Мышам вводили фторурацил путем в/в инъекции в дозах 33, 66, 134 и 200 мг/кг ежедневно в течение 1, 2, 3 или 4 дней подряд. У групп по 5 мышей оценивали гематологические, гистологические и биохимические параметры в дни 1, 3, 6, 10, 14 и 21 после введения. Значения LD10 для 1, 2, 3 и 4 последовательных суточных доз составляли 200, 162, 61 и 39 мг/кг/доза соответственно. Подсчет ретикулоцитов выявил подавление функции костного мозга в течение 2 дней после начальной дозы, за которым последовала дозозависимая задержка возврата к нормальному количеству ретикулоцитов. На 10-й день после введения произошло максимальное снижение уровня эритроцитов. Периферическая лейкопения характеризовалась как гранулоцитопенией, так и лимфопенией. Тяжесть и время восстановления зависели от дозы.
Введение фторурацила влияло на соотношение миелоидных и эритроидных клеток-предшественниц. Соотношение миелоидных и эритроидных клеток было выше нормы на 1-й день введения, но восстанавливалось примерно на 6-й день, что указывает на возобновление эритроидной и миелоидной пролиферации. Дозозависимая потеря массы тела от 6 до 22% достигала максимального снижения на 3-й день и не зависела от дозы. Все выжившие восстановили свой потерянный вес к 21-му дню.
Клинические эффекты химиотерапии ничем не проявлялись. Повреждение ЖКТ было наиболее распространенным, вызванным ЛС поражением, выявленным при гистологическом исследовании. Однократная доза фторурацила вызвала кратковременный эпизод легкого изменения эпителия кишечника на 3-й день. После 3 последовательных доз токсичность явно зависела от дозы, что проявлялось степенью и тяжестью эпителиальной гиперплазии и атрофии ворсинок в тонкой кишке. Поражения наблюдались у 0, 20, 40, 80 и 100% животных, получавших 0, 33, 66, 134 и 200 мг/кг фторурацила соответственно в трех последовательных ежедневных дозах.
Кардиологические исследования
У анестезированных морских свинок с открытой грудной клеткой после в/в введения фторурацила наблюдались изменения ЭКГ, свидетельствующие об ишемии. Частота аномалий ЭКГ через 3 ч у семи животных, получавших дозу 60 мг/кг, составила 100%, в то время как у животных, получавших 30 мг/кг, — 44% (4 из 10 животных). При дозе от 10 до 20 мг/кг изменений ЭКГ не наблюдалось. Истощение высокоэнергетических фосфатных соединений миокарда желудочков, наблюдаемое в результате исследований биохимии тканей, отражает действие фторурацила на цикл трикарбоновых кислот.
Репродуктивная токсичность
Тератогенный эффект фторурацила изучали на куриных эмбрионах в течение первых четырех дней развития. Инъекция фторурацила в желточный мешок приводила к специфическим и воспроизводимым аномалиям развития, которые менялись в зависимости от продолжительности инъекции.
Тератологические эффекты наблюдались у плодов хомяка, когда самка получала однократную в/м инъекцию фторурацила (от 3 до 9 мг) между 8-м и 11-м днями беременности. Частота пороков развития была связана с дозой и продолжительностью введения. По мере развития органогенеза появление эмбрионов с уродствами наблюдалось при более высоких дозах фторурацила. Общая частота пороков развития была самой высокой на 9-й день (78%). Фторурацил был высокотоксичен для эмбриона между 8-м и 11-м днями беременности с высокой скоростью резорбции на 9–11-й день.
В/в введение фторурацила в дозе 40 мг/кг беременным мышам-альбиносам на 10-й день беременности приводило к летальности эмбрионов в 96,3% случаев и порокам развития у выживших плодов в 100% случаев.
Клинические исследования
Не выявлено определенного влияния фторурацила на иммунные функции у 12 пациентов, страдавших диссеминированным раком, о чем свидетельствовали количество Т- или В-клеток, функция В-клеток, уровни Ig в сыворотке крови или титры ABO-антител. Однако фторурацил, по-видимому, влиял на функцию Т-клеток.
Применение вещества Фторурацил
Паллиативное лечение колоректального рака и рака молочной железы; лечение рака желудка, поджелудочной железы, предстательной железы, яичников, мочевого пузыря, головы и шеи — либо в качестве монотерапии, либо в комбинации с лучевой терапией и/или другими химиотерапевтическими средствами.
Ниже перечислены основные схемы химиотерапии с применением фторурацила.
Рак молочной железы
Фторурацил + циклофосфамид + доксорубицин, циклофосфамид + эпирубицин, циклофосфамид + доксорубицин + винкристин + преднизон, циклофосфамид + метотрексат + фторурацил (при запущенных заболеваниях, а также в качестве вспомогательного средства).
Несколько исследований адъювантной химиотерапии продемонстрировали умеренное снижение риска рецидива у пациентов с первичным операбельным раком молочной железы.
Наиболее распространенным режимом химиотерапии является комбинация циклофосфамид + метотрексат + фторурацил у пациентов, отрицательных по рецепторам эстрогенов, с добавлением тамоксифена у пациентов, положительных по рецепторам эстрогенов. Режим, включающий комбинацию фторурацил + доксорубицин + циклофосфамид в качестве адъювантной химиотерапии, также оказался эффективным, хотя и с риском развития кардиотоксичности со стороны доксорубицина.
Рак желудка
Фторурацил + доксорубицин + митомицин.
Рак поджелудочной железы
Фторурацил + доксорубицин + митомицин, фторурацил + митомицин + стрептозотоцин.
Рак мочевого пузыря
Фторурацил в виде монотерапии, фторурацил + доксорубицин, фторурацил + доксорубицин + цисплатин, фторурацил + доксорубицин + циклофосфамид, фторурацил + метотрексат + циклофосфамид + винкристин.
Рак предстательной железы
Фторурацил в виде монотерапии, фторурацил + доксорубицин + циклофосфамид.
Рак головы и шеи
Фторурацил + цисплатин, фторурацил + карбоплатин.
Рак яичника
Фторурацил + гексаметилмеламин + циклофосфамид + доксорубицин.
Колоректальный рак
Сравнение, проведенное у пациентов, получавших послеоперационную адъювантную химиотерапию и только лечебную хирургическую резекцию, показало улучшение показателей ответа и общее улучшение безрецидивной выживаемости в пользу адъювантной химиотерапии. Эффективные методы лечения включали комбинацию фторурацила и других химиотерапевтических средств (например, семустин и винкристин) и применение фторурацила с модуляцией кальция фолинатом у пациентов с раком толстой кишки стадии В и С по Дьюку.
Отсутствуют исследования, показывающие, что злокачественная меланома, карцинома почек, лейкозы и лимфомы, саркомы мягких тканей и костей, бронхогенная карцинома, опухоли головного мозга и метастазы в ЦНС в значительной степени отвечают на терапию фторурацилом.
Инъекция фторурацила не предназначена для профилактического применения.
Противопоказания
Ослабленные пациенты или пациенты с плохим питанием, угнетенной функцией костного мозга после лучевой терапии или терапии другими противоопухолевыми ЛС, или потенциально серьезными инфекциями, или с известной гиперчувствительностью к фторурацилу; проведение инъекции в течение 4 нед после лечения бривудином, соривудином или их химически родственными аналогами (бривудин, соривудин и их аналоги являются сильными ингибиторами дигидропиримидиндегидрогеназы, разрушающей фторурацил); пациенты с известным полным отсутствием активности дигидропиримидиндегидрогеназы (тестирование на дефицит дигидропиримидиндегидрогеназы следует рассмотреть до начала лечения, основываясь на местной доступности и действующих рекомендациях).
Применение при беременности и кормлении грудью
Фторурацил обладает тератогенным действием на животных, и его не следует применять во время беременности, особенно в I триместре, если только потенциальная польза для пациентки не перевешивает риски.
Поскольку мутагенность фторурацила не оценивалась, необходимо учитывать ее возможные последствия для мужчин и женщин.
Неизвестно, выделяется ли фторурацил с грудным молоком. Поскольку фторурацил ингибирует синтез ДНК, РНК и белка, противопоказано кормление грудью во время его применения.
Побочные действия вещества Фторурацил
Основные токсические эффекты фторурацила проявляются на нормальных, быстро пролиферирующих тканях, особенно в костном мозге и слизистой оболочке ЖКТ. Часто отмечаются стоматит и эзофагофарингит (может привести к шелушению и изъязвлению), диарея, анорексия и рвота.
Сообщалось о случаях развития синдрома Стивенса-Джонсона и токсического эпидермального некролиза, некоторые из которых заканчивались летальным исходом, у пациентов, получавших фторурацил в комбинации с другими ЛС, которые, как известно, ассоциируются с этими побочными реакциями.
Инфекции и инвазии: инфекции, сепсис, септический шок, нейтропенический сепсис, пневмония, суперинфекция, инфекция мочевыводящих путей, флегмона. Сообщалось о некоторых случаях летального исхода в результате сепсиса и септического шока.
Гематологические эффекты: миелосупрессия почти постоянно сопровождает курс адекватной терапии фторурацилом. Снижение числа лейкоцитов обычно впервые наблюдается между 9-м и 14-м днем после первого курса лечения, причем максимальное снижение наблюдается в течение третьей недели, хотя иногда задерживается как минимум на 25 дней. К 30-му дню число лейкоцитов обычно находится в пределах нормы. Также могут возникать тромбоцитопения, гранулоцитопения и панцитопения. Сообщалось о некоторых случаях летального исхода в случае гранулоцитопении и панцитопении.
Гемолитико-уремическое состояние низкой степени тяжести, усугубляемое переливаниями крови, было связано с длительной терапией комбинацией фторурацил + митомицин.
Со стороны иммунной системы: анафилактическая реакция и повышенная чувствительность. Сообщалось о некоторых случаях летального исхода у пациентов, получавших несколько режимов химиотерапии.
Со стороны обмена веществ и питания: обезвоживание.
Нарушения психики: спутанность сознания, дезориентация, эйфорическое настроение.
Со стороны сосудов: кровотечение, тромбофлебит. Сообщалось о некоторых смертельных случаях кровотечения.
Со стороны ЖКТ: анорексия и тошнота являются одними из самых ранних побочных эффектов во время курса терапии и обычно возникают в течение первой недели. За этими реакциями быстро следуют стоматит и диарея, которые являются надежными предупреждающими сигналами о том, что была введена достаточная доза. Также сообщалось о случаях развития эзофагита. Отмечался синдром Мэллори-Вейсса после в/в введения фторурацила в составе комбинированной химиотерапии. Сообщалось о развитии желудочно-кишечных кровотечений, язвы ЖКТ, мелены. Имеются случаи смертельного исхода в случае желудочно-кишечного кровотечения.
Дерматологические эффекты: алопеция и дерматит наблюдаются в значительном числе случаев, и пациенты должны быть проинформированы об этом последствии лечения. Алопеция обратима. Дерматит часто представляет собой зудящую пятнисто-папулезную сыпь, обычно появляющуюся на конечностях и реже на туловище. Обычно она обратима и поддается симптоматическому лечению. Также были отмечены сухость кожи и образование трещин.
Введение фторурацила было связано с возникновением синдрома ладонно-подошвенной эритродизестезии. Непрерывная инфузия фторурацила может увеличить частоту и тяжесть ладонно-подошвенной эритродизестезии. Этот синдром характеризуется ощущением покалывания в руках и ногах, которое может прогрессировать в течение следующих нескольких дней до боли при удержании предметов или ходьбе. Ладони и подошвы становятся симметрично опухшими и эритематозными с болезненностью дистальных фаланг, возможно, сопровождающейся шелушением. За прерыванием терапии следует постепенное разрешение в течение 5–7 дней. Сообщалось, что дополнительное пероральное применение пиридоксина предотвращает или устраняет такие симптомы.
Иногда может возникать реакция светочувствительности, проявляющаяся эритемой или повышенной пигментацией кожи, а также изменениями ногтей, включая исчерченность или выпадение ногтей и изменение цвета вен вблизи мест инъекций.
Неврологические эффекты: сообщалось о некоторых спорадических случаях развития лейкоэнцефалопатии с появлением различных неврологических симптомов, таких как снижение внимания, возбуждение и дезориентация, снижение памяти. Обычно лейкоэнцефалопатия разрешается благополучно в течение нескольких дней после прекращения применения фторурацила. Сообщалось о головной боли и нистагме.
Со стороны органа зрения: сообщалось о случаях светобоязни, нарушения зрения и приобретенного дакриостеноза.
Со стороны ССС: кардиогенный шок, сердечная недостаточность, кардиомиопатия, миокардит, перикардит, стенокардия, нарушения ЭКГ, инфаркт миокарда. Следует уделять внимание пациентам, которые испытывают боль в груди во время лечения и с заболеваниями сердца в анамнезе.
Другие побочные реакции: боли в груди, которые варьируют от легкой стенокардии до очень сильной боли, неотличимой от боли при инфаркте миокарда. Это может повториться при последующих дозах фторурацила. Сообщалось о развитии лихорадки.
Менее чем у 1% пациентов, получающих фторурацил, может наблюдаться атаксия или другие проявления острого мозжечкового синдрома из-за нейротоксичности препарата, хотя частота увеличивается, когда используются высокие дозы или интенсивные ежедневные режимы. Дисфункция полностью обратима и может не возникнуть при повторном введении. Были отмечены глазодвигательные нарушения, связанные с нейротоксичностью и выражающиеся в первую очередь в виде слабости конвергенции и дивергенции.
Сообщалось о чрезмерном слезотечении, которое постепенно появляется после лечения фторурацилом и сохраняется на протяжении всего курса лечения.
Взаимодействие
Бривудин, соривудин или их химически родственные аналоги необратимо ингибируют дигидропиримидиндегидрогеназу, что приводит к значительному увеличению экспозиции фторурацила. Это может привести к усилению токсичности, связанной с фторпиримидином, с потенциально смертельным исходом. Поэтому следует использовать другую противовирусную терапию либо сделать интервал не менее 4 нед между применением бривудина, соривудина или их аналогов и началом лечения фторурацилом. В случае случайного введения аналогов нуклеозидов, которые ингибируют активность дигидропиримидиндегидрогеназы, пациентам, получающим фторурацил, следует принять эффективные меры для снижения токсичности фторурацила. Рекомендуется немедленная госпитализация.
Различные пурины, пиримидины и антиметаболиты показали биохимическую модуляцию фторурацила в тест-системах in vitro. Пурины включают инозин, гуанозин, гуанозин-5′-фосфат и дезоксиинозин. Пиримидины включают тимидин, уридин и цитидин. Антиметаболиты включают метотрексат, тамоксифен, интерферон, L-аспартат, аллопуринол, гидроксикарбамид, дипиридамол и кальция фолинат. Синергические цитотоксические взаимодействия, такие как взаимодействие фторурацила с лейковорином, показали благоприятные терапевтические эффекты, особенно при раке толстой кишки. Однако комбинация ЛС может привести к усилению клинической токсичности фторурацила.
Фторурацил вызывает изменение спектрофотометрического спектра цитарабина, что, возможно, снижает его эффективность. Фторурацил в сочетании с метотрексатом изменяет спектры обоих веществ. Фторурацил физически несовместим с доксорубицином, эпирубицином и диазепамом. При смешивании фторурацила с этими ЛС образуется осадок. Рекомендуется проводить полную промывку в/в линии между инъекциями фторурацила и цитарабина, метотрексата, доксорубицина, эпирубицина или диазепама.
Лечение циметидином в течение нескольких недель до начала введения фторурацила может привести к повышению концентрации последнего в плазме крови. Этот эффект, вероятно, обусловлен как ингибированием печеночных ферментов, так и уменьшением печеночного кровотока. Следует соблюдать осторожность, если пациент одновременно получает фторурацил и циметидин, в некоторых случаях сообщалось о летальном исходе.
Метронидазол может усиливать токсичность фторурацила. Предполагается, что механизм взаимодействия заключается в снижении клиренса фторурацила при одновременном применении метронидазола. Следует избегать их одновременного применения, имеются сообщения о случаях летальных исходов.
У пациентов, получающих фторурацил, следует регулярно контролировать уровень фенитоина. В возможно, потребуется снизить дозу фенитоина. Сообщалось о токсичности, связанной с повышением концентрации фенитоина в плазме крови, при одновременном применении фенитоина и фторурацила или его аналогов. Официальные исследования лекарственного взаимодействия с фенитоином не проводились, но предполагается, что механизм взаимодействия заключается в ингибировании изофермента CYP2C9 фторурацилом.
Сообщалось о повышении уровня МНО и эпизодах кровотечения при одновременном применении варфарина и фторурацила или его аналогов. В этих случаях фторурацил обычно назначался в качестве одного из компонентов противоопухолевой комбинированной схемы. У пациентов, получающих фторурацил, следует регулярно контролировать адекватный антикоагулянтный ответ на терапию варфарином и другими производными кумарина; имеются сообщения о случаях летальных исходов.
Влияние на результаты лабораторных исследований. Сообщалось о повышении уровней общего T4 и T3 в сыворотке крови у пациентов с эутиреозом и прогрессирующей карциномой молочной железы, получавших фторурацил в рамках одной схемы применения. Эти уровни вовращались к значениям до лечения в течение 4 нед после окончания применения фторурацила.
Передозировка
Симптомы: суточные дозы фторурацила 30 мг/кг/сут (1,1–1,2 г/м2/сут) при 5-дневной непрерывной инфузии были переносимыми. При дозе 35 мг/кг/сут у семи из восьми пациентов развился тяжелый стоматит.
Лечение: применение фторурацила следует немедленно прекратить при появлении стоматита или эзофарингита, лейкопении или быстром снижении количества лейкоцитов, тромбоцитопении, непреодолимой рвоты, диареи, изъязвления ЖКТ и кровотечения или кровоизлияния.
Тошноту и рвоту можно облегчить с помощью противорвотных средств. Хроническая передозировка может привести к серьезной миелосупрессии. Для предотвращения передозировки следует проводить ежедневное гематологическое обследование. Триацетат уридина является специфическим антидотом для лечения передозировки фторурацила или лечения тяжелых ранних токсических состояний. Его следует вводить в течение 96 ч после окончания инфузии фторурацила. В случае, если триацетат уридина недоступен, лечение должно быть симптоматическим и поддерживающим. Переливание крови или тромбоцитов следует проводить при любых признаках кровотечения. Пациенты должны находиться под тщательным наблюдением на предмет интеркуррентной инфекции, и при ее наличии следует незамедлительно назначить соответствующую антибактериальную терапию.
Способ применения и дозы
В/в, в/а, путем в/в инфузии или инъекции, соблюдая осторожность, чтобы избежать экстравазации. Дозировка обычно зависит от веса пациента, для получения оптимального терапевтического результата с минимальными побочными эффектами дозировка должна основываться на клинической и гематологической реакции и переносимости пациента.
Меры предосторожности
Фторурацил должен назначаться только врачом или применяться под наблюдением врача, который хорошо знаком с применением сильных антиметаболитов.
Фторурацил необходимо применять с особой осторожностью у пациентов групп высокого риска, которые недавно перенесли операцию, имели в анамнезе облучение в высоких дозах областей, содержащих костный мозг (в т.ч. таз, позвоночник, ребра), или ранее применяли другое химиотерапевтическое средство, вызывающее миелосупрессию, имеют широко распространенное поражение костного мозга метастазами опухолей, или у которых нарушена функция печени или почек. Клинические последствия тяжелой миелосупрессии включают инфекции. Вирусные, бактериальные, грибковые и/или паразитарные инфекции, как локализованные, так и системные, могут быть связаны с применением фторурацила в монотерапии или в комбинации с другими иммуносупрессивными ЛС. Эти инфекции могут протекать в легкой форме, но могут быть тяжелыми, а иногда и смертельными.
Лечение фторурацилом может усилить некроз, вызванный радиацией.
Тяжелая токсичность (например, стоматит, диарея, нейтропения и нейротоксичность), связанная с применением фторурацила, объясняется дефицитом активности дигидропиримидиндегидрогеназы. В некоторых случаях сообщалось о летальном исходе. Отсутствие этого катаболического фермента, по-видимому, приводит к длительному выведению фторурацила. Особое внимание следует уделять статусу дигидропиримидиндегидрогеназы при оценке пациентов, испытывающих токсичность, связанную с фторурацилом. Ни одна доза не была доказана безопасной для пациентов с полным отсутствием активности дигидропиримидиндегидрогеназы.
Пациенты, получающие фенитоин одновременно с фторурацилом, должны регулярно проходить тестирование из-за возможности повышения уровня фенитоина в плазме крови.
Тяжелая токсичность и летальный исход более вероятны у пациентов групп высокого риска, но иногда отмечаются у пациентов, находящихся в относительно хорошем состоянии. Любая форма терапии, которая усиливает стресс пациента, нарушает усвоение питательных веществ или угнетает функцию костного мозга, увеличит токсичность фторурацила.
Фторурацил — цитотоксический препарат с небольшим запасом безопасности. Пациент должен быть проинформирован, что терапевтический ответ вряд ли наступит без каких-либо признаков токсичности.
Перед каждой дозой рекомендуется проводить дифференциальный подсчет лейкоцитов и тромбоцитов, а также контролировать гематологический статус во время терапии.
Следует рассмотреть вопрос о немедленной приостановке терапии фторурацилом при появлении любого из следующих признаков:
— стоматит или эзофагофарингит (при первых видимых признаках небольших изъязвлений на внутреннем краю губ);
— непреодолимая рвота;
— диарея (жидкий стул или частые дефекации);
— изъязвление ЖКТ;
— кровотечение любой локализации;
— лейкопения (число лейкоцитов <3500/мм3) или быстрое снижение количества лейкоцитов;
— гранулоцитопения (<1500 мм3);
— тромбоцитопения (число тромбоцитов <100000/мм3).
Применение фторурацила следует возобновить только тогда, когда у пациента исчезнут вышеуказанные признаки.
Фторурацил следует применять с осторожностью у пациентов с нарушением функции печени и желтухой.
У некоторых пациентов могут возникнуть реакции светочувствительности после применения фторурацила, поэтому рекомендуется предупредить пациентов о необходимости избегать длительного воздействия солнечного света.
Сообщалось о случаях развития синдрома Стивенса-Джонсона и токсического эпидермального некролиза, некоторые из которых заканчивались летальным исходом, у пациентов, получавших фторурацил в составе комбинированной терапии.
Иммунодепрессия/повышенная восприимчивость к инфекциям. Введение живых или живых ослабленных вакцин пациентам с ослабленным иммунитетом, получающим химиотерапевтические ЛС, включая фторурацил, может привести к развитию серьезных или смертельных инфекций. У пациентов, получающих фторурацил, необходимо избегать применения живых вакцин. Могут вводиться убитые или инактивированные вакцины, однако реакция на такие вакцины может быть снижена.
ССС. Сообщалось о развитии кардиогенного шока, сердечной недостаточности, кардиомиопатии, миокардита, стенокардии, нарушениях ЭКГ, инфаркте миокарда и перикардите после применения фторурацила. Поэтому следует уделять внимание пациентам, которые испытывают боль в груди во время лечения, и с заболеваниями сердца в анамнезе.
Источники информации
Product monograph, 2022.
Торговые названия с действующим веществом Фторурацил
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Фторурацил-ЛЭНС® |
от 1835.60 до 1835.60 |
Фторурацил (Fluorouracil)
💊 Состав препарата Фторурацил
✅ Применение препарата Фторурацил
Описание активных компонентов препарата
Фторурацил
(Fluorouracil)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2021.12.01
Владелец регистрационного удостоверения:
Код ATX:
L01BC02
(Фторурацил)
Лекарственная форма
| Фторурацил |
Р-р для в/сосудистого и в/полостного введения 50 мг/1 мл: фл. 5 мл, 10 мл, 20 мл или 100 мл рег. №: ЛП-(000665)-(РГ-RU) Предыдущий рег. №: ЛП-004943 |
Форма выпуска, упаковка и состав
препарата Фторурацил
Раствор для внутрисосудистого и внутриполостного введения прозрачный, от бесцветного до светло-желтого цвета.
Вспомогательные вещества: натрия гидроксид — около 13.7 мг, вода д/и — до 1 мл.
5 мл — флаконы темного стекла типа I (EP/USP) (1) — пачки картонные.
10 мл — флаконы темного стекла типа I (EP/USP) (1) — пачки картонные.
20 мл — флаконы темного стекла типа I (EP/USP) (1) — пачки картонные.
100 мл — флаконы темного стекла типа I (EP/USP) (1) — пачки картонные.
Фармакологическое действие
Противоопухолевое средство из группы антиметаболитов. Ингибирует процесс деления клеток путем блокирования синтеза ДНК (вследствие угнетения активности фермента тимидилатсинтетазы) и образования структурно несовершенной РНК (вследствие внедрения фторурацила в ее структуру).
Фармакокинетика
После в/в или в/а введения фторурацил биотрансформируется и распределяется в быстро пролиферирующих тканях, таких как костный мозг, слизистая оболочка ЖКТ и опухолевых тканях. Vd составляет 0.12 л/кг массы тела, связывание с белками плазмы крови — около 10%. Легко проникает через ГЭБ, попадая в спинномозговую жидкость и ткани головного мозга. Метаболизируется в основном в печени. T1/2 фторурацила зависит от вводимой дозы и составляет 8-22 мин. Около 7-20% фторурацила выводится через почки в неизмененном виде в течение 6 ч (90% выводится в течение первого часа), 60-80% — через дыхательные пути в форме СО2, незначительное количество выводится с желчью. Почечный клиренс фторурацила составляет 170-180 мл/мин.
Показания активных веществ препарата
Фторурацил
Рак толстой и прямой кишки, рак молочной железы, рак пищевода, рак желудка, рак поджелудочной железы, первичный рак печени, рак яичников, рак шейки матки, рак мочевого пузыря, злокачественные опухоли головы и шеи, рак предстательной железы, рак надпочечников, рак вульвы, рак полового члена, карциноид.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Применяют в/в (струйно или путем медленной инфузии), в/а, внутриполостно. Режим дозирования устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Побочное действие
Со стороны системы кроветворения: очень часто — дозолимитирующая лейкопения, нейтропения, тромбоцитопения, анемия, носовое кровотечение; часто — фебрильная нейтропения; очень редко — агранулоцитоз, панцитопения.
Со стороны иммунной системы: очень часто — иммуносупрессия с увеличением частоты возникновения инфекционных заболеваний; редко — генерализованные аллергические реакции, анафилактический шок; частота неизвестна — развитие вторичных инфекций, сепсис.
Со стороны эндокринной системы: частота неизвестна — повышение общего тироксина и трийодтиронина в плазме крови, без повышения содержания свободного общего тироксина и ТТГ и без клинических признаков гипертиреоза.
Со стороны обмена веществ: очень часто — гиперурикемия.
Со стороны нервной системы: нечасто — нистагм, головная боль, вертиго, паркинсонизм, пирамидные симптомы, транзиторный обратимый церебральный синдром, сонливость, эйфория, ретробульбарный неврит; редко — периферическая невропатия (при применении в сочетании с лучевой терапией); очень редко — дисгевзия, атаксия, нарушение речи, спутанность сознания, нарушение ориентации, миастения, афазия, судороги, кома, инфаркт головного мозга (при комбинированной терапии с митомицином или цисплатином); частота неизвестна — печеночная энцефалопатия.
Со стороны органа зрения: нечасто — конъюнктивит, избыточное слезотечение, нечеткость зрения, снижение остроты зрения, блефарит, выворот века, светобоязнь, неврит зрительного нерва, диплопия, ограничение подвижности глаз, нарушение зрения, корковая слепота (при высоких дозах).
Со стороны сердечно-сосудистой системы: очень часто — ишемические изменения на ЭКГ; часто — боли в области сердца; нечасто — снижение АД, аритмии, ишемия, инфаркт миокарда, миокардит, дилатационная кардиомиопатия, кардиогенный шок, сердечная недостаточность; редко — тромбофлебит; очень редко — стенокардия, остановка сердца, внезапная сердечная смерть; частота неизвестна — перикардит, нарушение периферического, церебрального и интестинального кровообращения, синдром Рейно, тромбоэмболия.
Со стороны дыхательной системы: очень часто — бронхоспазм.
Со стороны пищеварительной системы: очень часто — снижение аппетита, эрозивно-язвенные поражения ЖКТ, диарея, тошнота, рвота, анорексия; нечасто — обезвоживание, сепсис, кровотечения из ЖКТ, отслойка некротизированного эпителия слизистых оболочек; частота неизвестна — изжога.
Со стороны печени и желчевыводящих путей: нечасто — повреждение клеток печени, некалькулезный холецистит; очень редко — некроз печени (в т.ч. с летальным исходом).
Со стороны мочевыделительной системы: нечасто — почечная недостаточность.
Со стороны репродуктивной системы: нечасто — обратимое угнетение функции половых желез, приводящее к аменорее или азооспермии.
Со стороны кожи и подкожных тканей: очень часто — обратимая алопеция, удлинение сроков заживления ран, синдром ладонно-подошвенной эритродизестезии; нечасто — экзантемы, гиперпигментация или депигментация кожи в виде полос вблизи вен, сухость кожи, трещины кожи, эритема, зуд кожных покровов, макуло-папулезная сыпь, телеангиоэктазии, изменение и схождение ногтевых пластинок, фотосенсибилизация, дерматит, крапивница.
Прочие: очень часто — повышенная утомляемость, астения, лихорадка, слабость, снижение мотивации; частота неизвестна — тромбофлебит в месте введения.
Противопоказания к применению
Повышенная чувствительность к фторурацилу; выраженная лейкопения, нейтропения, тромбоцитопения, угнетение костномозгового кроветворения, активное кровотечение, стоматит, изъязвления слизистой оболочки полости рта и ЖКТ, псевдомембранозный энтероколит, тяжелые инфекции, тяжелые нарушения функции печени, тяжелые нарушения функции почек; беременность, период грудного вскармливания (в ходе терапии и в течение 2 недель после последнего введения фторурацила); детский возраст; комбинация с ингибиторами дигидропиримидиндегидрогеназы (бривудин, соривудин); установленный полный дефицит активности дигидропиримидиндегидрогеназы (ДПД); ослабленные пациенты.
С осторожностью
У пациентов с почечной недостаточностью легкой и средней степени тяжести; с печеночной недостаточностью легкой и средней степени тяжести; острыми инфекционными заболеваниями вирусной, грибковой или бактериальной природы (в т.ч. туберкулез, ветряная оспа, опоясывающий лишай); сердечно-сосудистыми заболеваниями в анамнезе; инфильтрацией костного мозга опухолевыми клетками, ранее проводившейся лучевой терапией или химиотерапией; у пациентов с частичным дефицитом ДПД.
Применение при беременности и кормлении грудью
Фторурацил противопоказан к применению при беременности. При необходимости применения в период лактации следует прекратить грудное вскармливание.
Женщины репродуктивного возраста должны применять надежные методы контрацепции во время лечения фторурацилом и как минимум в течение 6 мес после окончания терапии. В том случае, если пациентка забеременеет во время лечения фторурацилом, следует рассмотреть вопрос о генетическом консультировании.
Применение при нарушениях функции печени
Противопоказано применение при тяжелых нарушениях функции печени. С осторожностью следует применять у пациентов с печеночной недостаточностью легкой и средней степени тяжести.
Применение при нарушениях функции почек
Противопоказано применение при тяжелых нарушениях функции почек. С осторожностью следует применять у пациентов с печеночной недостаточностью легкой и средней степени тяжести.
Применение у детей
Противопоказано применение у детей.
Особые указания
Лечение фторурацилом должно осуществляться под наблюдением врача-онколога, имеющего опыт применения антиметаболитов. Принимая во внимание риск развития тяжелых токсических реакций, в т.ч. с летальным исходом, врач обязан подробно проинформировать пациента о возможном риске и необходимых мерах безопасности. Начинать лечение необходимо в условиях стационара.
Перед началом и в процессе терапии фторурацилом следует контролировать картину периферической крови, лабораторные показатели функции печени и почек.
Следует соблюдать осторожность при лечении пациентов, испытывающих боли в сердце во время курсов лечения, или у пациентов с заболеваниями сердца в анамнезе. Необходимо регулярно контролировать функцию сердца. В случае развития выраженной кардиотоксичности лечение должно быть прекращено.
При развитии симптомов энцефалопатии следует немедленно приостановить лечение и определить уровень аммиака в плазме крови. При повышенной концентрации аммиака в плазме крови следует начать терапию с целью его снижения.
Необходимо соблюдать осторожность при применении фторурацила у пациентов с почечной и/или печеночной недостаточностью легкой и средней степени тяжести. У пациентов со сниженной функцией почек/печени возрастает риск развития гипераммониемии и печеночной энцефалопатии.
У пациентов, у которых активность ДПД, фермента, участвующего в катаболизме фторурацила, снижена или отсутствует, существует повышенный риск развития тяжелых, жизнеугрожающих или летальных нежелательных реакций, вызванных применением фторурацила.
При одновременном применении фторурацила и пероральных антикоагулянтов необходимо тщательно контролировать свертываемость крови (например, протромбиновый индекс).
Фторурацил может снижать иммунологический ответ на вакцинацию. Применение живых вакцин в период лечения фторурацилом может привести к усиленной репликации вируса. В период применения фторурацила противопоказано применение живых вакцин, также следует избегать контакта с людьми, недавно вакцинированными против полиомиелита.
Мужчинам и женщинам репродуктивного возраста во время лечения фторурацилом и как минимум в течение 6 мес после окончания терапии следует применять надежные методы контрацепции. Мужчинам следует проконсультироваться с врачом о возможности криоконсервации спермы до начала лечения из-за возможного необратимого бесплодия вследствие применения фторурацила.
Необходимо принимать все меры для предотвращения попадания раствора фторурацила на кожу и слизистые оболочки. При попадании фторурацила на кожу или слизистые оболочки необходимо тщательно промыть их мылом и водой, при попадании на слизистую оболочку глаз — большим количеством воды.
Влияние на способность к управлению транспортными средствами и механизмами
В период применения фторурацила пациентам следует соблюдать осторожность при управлении транспортными средствами и механизмами, а также при занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Лекарственное взаимодействие
При одновременном применении кальция фолинат усиливает терапевтический и токсический эффекты фторурацила. Выраженная диарея, иногда с летальным исходом может возникнуть как клиническое проявление данного взаимодействия.
При применении фторурацила в комбинации с другими цитостатиками и интерфероном-альфа может наблюдаться усиление как противоопухолевого эффекта, так и токсичности фторурацила.
При применении фторурацила в комбинации с лучевой терапией возможно усиление кожной токсичности последней.
При длительном совместном применении с митомицином наблюдалось появление гемолитического уремического синдрома.
При одновременном применении фторурацила и антрациклинов может усиливаться кардиотоксический эффект последних.
При одновременном применении с ингибиторами фермента дигидропиримидиндегидрогеназы, ответственного за катаболизм эндогенных и фторированных пиримидинов (бривудин, соривудин), значительно увеличивается токсичность фторурацила. Интервал между применением фторурацила и бривудина, соривудина или их аналогов должен составлять не менее 4 недель.
При одновременном применении фенитоина и фторурацила, повышается плазменная концентрация фенитоина, что может привести к появлению симптомов интоксикации.
При одновременном применении хлордиазепоксид, дисульфирам, гризеофульвин и изониазид могут усиливать активность фторурацила.
При одновременном применении левамизол может усиливать гепатотоксичность фторурацила.
Имеются сообщения о снижении времени свертывания крови по Квику при одновременном применении варфарина и фторурацила, а также в комбинации с левамизолом.
При одновременном применении метронидазол, циметидин, интерфероны и аллопуринол могут повышать концентрацию фторурацила в плазме крови, тем самым повышая его токсические эффекты.
У пациенток, принимающих тиазидные диуретики совместно с циклофосфамидом, метотрексатом и фторурацилом, отмечалось более выраженное снижение числа гранулоцитов по сравнению с такой же цитостатической терапией без применения тиазидных диуретиков.
При одновременном применении винорелбина и фторурацила/фолиновой кислоты возможно развитие выраженного воспаления слизистых оболочек полости рта и ЖКТ, в т.ч. с летальным исходом.
У пациентов с раком молочной железы, получающих комбинированную терапию с циклофосфамидом, метотрексатом, фторурацилом и тамоксифеном, увеличивается риск развития тромбоэмболических осложнений.
При применении фторурацила возможны ложноположительные результаты при определении билирубина и 5-гидроксииндолуксусной кислоты в моче.
Фторурацил не следует смешивать с растворами, содержащими другие химиотерапевтические вещества.
Фторурацил несовместим со следующими средствами: цисплатин, цитарабин, диазепам, доксорубицин, дроперидол, филграстим, галлия нитрат, лейковорин, метотрексат, метоклопрамид, морфин, ондансетрон, растворы для парентерального питания, винорелбин.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Efudix®5% крем (Эфудикс) — Флуороурацил (Fluorouracil) — топический (применяемый местно) цитостатический препарат. Действующее вещество Efudix® Флуороурацил, препятствует клеточному росту и используется исключительно для местного лечения определенных изменений кожи.
Инструкция по применению EFUDIX® Флуороурацил (Fluorouracil)
Действующее вещество: Флуороурацил.
1. ЧТО ТАКОЕ EFUDIX® Флуороурацил (Fluorouracil) и для чего применяется данный препарат?
Цитостатик представляет собой химическое вещество, препятствующее клеточному росту или замедляющее его. Поскольку опухолевые клетки, в отличие от здоровых, делятся с повышенной скоростью, цитостатик прежде всего воздействует на них.
EFUDIX® Флуороурацил (Fluorouracil) применяется при предопухолевых изменениях кожи, таких как актинический кератоз или болезнь Боуэна (чечевицеобразный дискоидный дискератоз).
В качестве пробного лечения Efudix® Флуороурацил (Fluorouracil) можно применять вместо предпочтительной хирургической терапии, а также для лечения поверхностной базалиомы, если хирургические либо рентгенохирургические методы не принесли результата или были неприменимы, например, при множественных поражениях или в труднодоступных для обработки местах. Перед применением препарата необходимо гистологически подтвердить диагноз, поскольку Efudix® Флуороурацил (Fluorouracil) недостаточно эффективен при лечении определенных разновидностей базалиом. Также необходимо контролировать персистенцию (дальнейшее существование) опухоли под излеченным на поверхности кожным участком.
2. НА ЧТО НЕОБХОДИМО ОБРАТИТЬ ВНИМАНИЕ ПЕРЕД НАЧАЛОМ ПРИЕМА EFUDIX®?
Применение Efudix® Флуороурацил (Fluorouracil) запрещается в следующих случаях:
- При повышенной чувствительности (аллергии) к Флуороурацил у, метил-4-гидроксибензоату, пропил-4-гидроксибензоату или иным компонентам Efudix®.
- На слизистых оболочках и переходах кожи в слизистую оболочку, таких как анально-генитальная зона, ноздри, губы, а также ладони без повязки.
- При беременности и кормлении грудью.
- При текущем или имевшем место в течение последних 4-х недель лечении бривудином, соривудином или аналогичными препаратами (антивирусными нуклеозидами). Данные медикаменты обычно применяются для лечения опоясывающего герпеса. Сочетание Флуороурацил а с бривудином, соривудином или их производными может значительно усилить побочное действие Efudix®.
При аллергии на латекс (повышенной чувствительности к каучуку) запрещается наносить Efudix® при помощи прилагаемого к препарату напальчника.
Меры особой предосторожности при применении Efudix® Флуороурацил (Fluorouracil):
- При лечении одного из партнеров при помощи Efudix® следует пользоваться противозачаточными средствами.
- При лечении мужчин при помощи Efudix® Флуороурацил (Fluorouracil) рекомендуется во время лечения и в течение 6 месяцев после его окончания воздерживаться от зачатия ребенка, поскольку Efudix® может оказывать повреждающее воздействие на наследственный материал. В связи с этим при желании зачать ребенка после курса лечения при помощи Efudix® рекомендуется обратиться за медико-генетической консультацией.
- В случае применения препарата на большой площади (на участках кожи свыше 500 см2, ок. 23х23 см) существует возможность системного токсического воздействия и тем самым повышенный риск возникновения нежелательных реакций. В связи с этим следует применять Efudix® только под контролем врача.
Запрещается применять Efudix® Флуороурацил (Fluorouracil):
- На открытых ранах, поскольку это может привести к попаданию крема в кровеносную систему и в единичных случаях к тяжелым побочным эффектам.
- В случае если у Вас понижена активность энзима дигидропиримидиндегидрогеназы (ДПД), существует повышенный риск возникновения серьезных побочных эффектов, таких как диарея, воспаление слизистых оболочек, поражение костного мозга и нервов. При возникновении тяжелых побочных эффектов во время применения Efudix® необходимо сделать анализ на активность энзима ДПД.
Поставьте Вашего врача в известность, если Вы в течение последних 4-х недель принимали препараты для лечения герпесных инфекций, поскольку при одновременном приеме данных препаратов существует риск значительного усиления побочного действия препарата.
Не рекомендуется использовать Efudix® Флуороурацил (Fluorouracil) для лечения детей.
Совместимость Efudix® с другими лекарственными препаратами: поставьте Вашего врача в известность, если Вы принимаете /используете или недавно принимали/использовали другие лекарственные препараты, в том числе продающиеся без рецепта.
При одновременном использовании метотрексата и местном применении 5-Флуороурацил а в единичных случаях возможно возникновение тяжелых кожных реакций. При лечении метотрексатом использование Efudix® Флуороурацил (Fluorouracil) запрещается.
Запрещается применять Efudix® Флуороурацил (Fluorouracil) в сочетании с бривудином, соривудином или аналогичными препаратами. Данные медикаменты необратимо угнетают энзим дигидропиримидиндегидрогеназу (ДПД), одновременное применение может привести к накоплению и повышению токсичности Флуороурацил а. Между лечением с использованием бривудина и началом лечения при помощи Efudix® должно пройти не менее 4-х недель. Пациентам, недавно принимавшим бривудин, соривудин или аналогичные препараты, перед началом применения в качестве меры дополнительной предосторожности необходимо сделать анализ на активность энзима ДПД.
Период беременности и кормления грудью: перед приемом/использованием любых лекарственных препаратов проконсультируйтесь у врача или фармацевта. Efudix® может оказывать повреждающее воздействие на наследственный материал и влиять на внутриутробное развитие плода. В связи с этим запрещается использовать Efudix® Флуороурацил (Fluorouracil) во время беременности. При наступлении беременности во время лечения при помощи Efudix® Флуороурацил (Fluorouracil) сразу же поставьте в известность врача и по возможности получите медико-генетическую консультацию. Применение Efudix® Флуороурацил (Fluorouracil) в течение периода кормления грудью в общем случае не разрешается. Если врач сочтет необходимым применение препарата в течение периода кормления грудью, ребенка будет необходимо отнять от груди.
Влияние препарата на способность управления автомобилем и работы с машинами и механизмами: не требуется никаких особых мер предосторожности.
Важная информация о компонентах Efudix® Флуороурацил (Fluorouracil):
- Пропиленгликоль может вызывать раздражение кожи.
- Стеариловый спирт может вызывать местное раздражение кожи (напр., контактный дерматит).
3. КАК ПРИМЕНЯТЬ EFUDIX® ФЛУОРОУРАЦИЛ (FLUOROURACIL)?
При использовании Efudix® Флуороурацил (Fluorouracil) всегда в точности следуйте указаниям врача. При наличии вопросов консультируйтесь у врача или фармацевта.
Стандартная дозировка (если врачом не будет предписано иное):
Наносить Efudix® Флуороурацил (Fluorouracil) два раза в день в достаточном количестве, чтобы полностью покрыть пораженные участки. Лечение следует продолжать до тех пор, пока не будет достигнута воспалительная реакция в эрозионной стадии (поверхностные повреждения ткани, заживающие без рубцов), после чего применение следует прекратить. Обычный срок лечения при актиническом кератозе составляет 2-4 недели, полное заживление поражений в зависимости от конкретных обстоятельств может проявиться только спустя 1-2 месяца.
Неоперабельную или не подлежащую облучению поверхностную базалиому следует обрабатывать минимум 3-6 недель до проявления изъязвления. В некоторых случаях для полного устранения поражений требуется лечение длительностью 10-12 недель. Как и при любых неопластических заболеваниях, пациенту после курса лечения необходимо проверяться в течение достаточного срока, чтобы удостовериться в излечении.
Окончание курса лечения при помощи Efudix® Флуороурацил (Fluorouracil) определяется врачом в зависимости от успешности лечения.
Способ применения:
Если врачом не будет предписано иное, при использовании Efudix® следуйте нижеуказанной инструкции. Не изменяйте способ применения, поскольку в подобном случае препарат может оказать неправильное воздействие! Нанесение Efudix® Флуороурацил (Fluorouracil) лучше всего осуществлять при помощи прилагаемого в упаковке напальчника, неметаллического аппликатора либо подходящей для этой цели перчатки. При нанесении Efudix® Флуороурацил (Fluorouracil) незащищенными пальцами необходимо сразу после процедуры вымыть руки. Следите за тем, чтобы препарат не попал в глаза или на слизистые оболочки. Общая площадь обработанной поверхности кожи не должна превышать 500 см2 (около 23х23 см). При необходимости обработки большей площади необходимо последовательно обрабатывать одну область за другой.
Обработка актинических кератозов производится, как правило, без повязки. При иных заболеваниях рекомендуется наложение плотно прилегающей повязки (окклюзионной повязки), сменяя ее каждый день. Эта процедура показана также при кератозах ладоней. После нанесения Efudix® Флуороурацил (Fluorouracil) на больную область кожи в результате влияния действующего вещества на пораженном участке происходят определенные изменения (см. также раздел 4 «Побочное действие»). Часто возникает покраснение, за которым следует образование пузырьков, повреждение поверхности кожи, изъязвление и отмирание обработанных тканей. Данные повреждения заживают по окончании курса лечения.
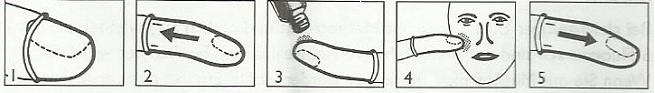
Нанесение Efudix® при помощи прилагаемого напальчника:
1. Выньте напальчник из упаковки и наденьте на кончик указательного пальца.
2. Разверните напальчник до основания пальца.
3. Выдавите достаточное количество крема на кончик пальца.
4. Нанесите тонкий слой крема на подлежащий обработке участок кожи.
5. Сверните напальчник от основания пальца к кончику.
Не используйте напальчники более одного раза.
Обратитесь к врачу или фармацевту, если Вы полагаете, что Efudix® действует слишком слабо или слишком сильно.
При превышении рекомендуемой дозировки Efudix® Флуороурацил (Fluorouracil):
При нанесении Efudix® Флуороурацил (Fluorouracil) на площадь больше максимально разрешенной (свыше 500 см2, ок. 23х23 см) существует возможность системного токсического воздействия и тем самым повышенный риск возникновения нежелательных реакций (см. также раздел «Меры особой предосторожности при применении Efudix® Флуороурацил (Fluorouracil)»).
Если Вы забыли нанести Efudix® Флуороурацил (Fluorouracil) или прекратили лечение:
При пропуске обработки, перерывах или досрочном прекращении лечения воздействие лекарственного препарата ослабляется, что может поставить под вопрос успешность всего лечения в целом. Ввиду этого применяйте Efudix® Флуороурацил (Fluorouracil) в точности согласно указаниям врача. При возникновении каких-либо вопросов проконсультируйтесь у врача или фармацевта.
4. КАКОЕ ПОБОЧНОЕ ДЕЙСТВИЕ МОЖЕТ ИМЕТЬ ДАННЫЙ ПРЕПАРАТ?
Как и любой лекарственный препарат, Efudix® Флуороурацил (Fluorouracil) также может иметь побочное действие, которое не обязательно возникает в каждом конкретном случае. Многие побочные эффекты Efudix® Флуороурацил (Fluorouracil) сводятся к местным кожным проявлениям. Кожные реакции могут являться признаком того, что Efudix® действует как предусмотрено. Воздействие Флуороурацил на обработанные поражения может привести к образованию пузырьков, струпов, рубцов, шелушению, эрозии, реэпителизации, жжению, гиперпигментации (увеличенной пигментации кожи), боли, зуду, сыпи, воспалению и изъязвлению.
Иногда может возникнуть покраснение кожи, непосредственно прилегающей к областям, обработанным кремом Efudix® Флуороурацил (Fluorouracil). По окончании лечения покраснение быстро сходит.
При обработке слишком большой площади кожи или применении препарата на открытых ранах могут возникнуть следующие побочные эффекты:
- Боли в животе, судороги, диарея, рвота
- Отечность и болезненные ощущения языка и рта
- Повышение температуры и общая усталость
При проявлении данных побочных эффектов немедленно обратитесь к врачу.
Также в ряде случаев возможно возникновение следующих побочных эффектов:
- Заболевания нервной системы: психические расстройства, бессонница, раздражительность, поражения нервов (см. также раздел «Меры особой предосторожности при применении Efudix® Флуороурацил (Fluorouracil)).
- Заболевания желудочно-кишечного тракта: привкус лекарства, воспаление слизистой оболочки рта.
- Заболевания крови и лимфатической системы: гематологические нарушения (в сочетании с системным токсическим действием Efudix® Флуороурацил (Fluorouracil), см. также раздел «Меры особой предосторожности при применении Efudix® Флуороурацил (Fluorouracil)»), эозинофилия, тромбоцитопения, токсическая гранулёма.
- Заболевания иммунной системы: повышенная чувствительность (гиперсензитивность).
- Кожные реакции: аллергический контактный дерматит, выпадение волос, образование пузырьков, буллёзный пемфигоид, незначительные боли, ихтиоз («болезнь рыбьей чешуи»), десквамация, отечность, телеангиэктазия (видимое расширение капилляров), чувствительность к нажатию, уртикария (крапивная лихорадка), кожная сыпь.
Прочие побочные эффекты: конъюнктивальная реакция (реакция слизистой оболочки глаза), роговичный рефлекс, лакримация (слезотечение), раздражение носовой слизистой оболочки, простой герпес.
Ультрафиолетовое облучение или воздействие солнечного света может привести к повышенному раздражению кожи. Во время лечения с использованием Efudix® Флуороурацил (Fluorouracil) следует избегать воздействия ультрафиолетового излучения и не принимать солнечных ванн. Метил-4-гидроксибензоат и пропил-4-гидроксибензоат могут вызвать реакции повышенной чувствительности (аллергическую реакцию замедленного типа). Каучук также может вызвать реакции повышенной чувствительности или тяжелые аллергические реакции (учтите это при нанесении крема при помощи латексного напальчника).
При проявлении какого-либо побочного действия либо побочных эффектов приема препарата, не указанных в данном вкладыше, обратитесь к врачу или фармацевту.
5. КАК ХРАНИТЬ EFUDIX® Флуороурацил (Fluorouracil)?
Храните лекарственные препараты в местах, недоступных для детей
Запрещается использовать препарат по истечении срока годности, указанного на тубе и коробке после указания «Verwendbar bis:» (или <Verw. bis>). Срок годности соответствует последнему дню указанного месяца.
Условия хранения: храните препарат в закрытой тубе при температуре не выше +25 градусов Цельсия.
Срок хранения после вскрытия тубы составляет 4 месяца. Запрещается утилизация препарата с бытовыми сточными водами или бытовым мусором. Необходимо соблюдать предписания по утилизации цитостатиков. Если у Вас больше нет необходимости в препарате, проконсультируйтесь с фармацевтом по поводу его утилизации. Данные меры помогают защищать окружающую среду.
6. ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ.
Компоненты Efudix® Флуороурацил (Fluorouracil):
Действующее вещество: Флуороурацил;
1 грамм крема содержит 50 мг Флуороурацила;
Прочие компоненты: метил-4-гидроксибензоат, пропил-4-гидроксибензоат, полисорбат 60, пропиленгликоль, стеариловый спирт, белый вазелин, дистиллированная вода.
Efudix® Флуороурацил (Fluorouracil) поставляется в упаковках, содержащих 20-граммовую тубу с кремом для кожного применения и 50 латексных напальчников.
Тэги:
- Efudix
- Флуороурацил
- Fluorouracil
- описание препарата
- кератоз
- болезнь Боуэна
Раздел:
- Статьи
Препарат Efudex
Efudex — цитостатический препарат, предназначенный для лечения патологий кожи. Продается Эфудекс в виде крема 5% весом 20 г, который содержит Fluorouracil 5 мг. Флюороурацил согласно инструкции по применению назначают при актиническом кератозе, поверхностной базилиоме, поверхностной карциноме, болезни Боуэна и некоторых предраковых состояниях кожи.
При лечении онкологии крем назначают, если хирургические методы не внедряются ввиду обширного поражения или сложной локализации. При этом диагноз должен быть подтвержден до начала терапии, поскольку эффективность препарата относительно других онкопатологий не подтверждена.
Принцип действия
Препарат Efudex содержит Флюороурацил. Это средство ингибирует деление клеток, внедряясь в структуру ДНК и угнетая активность тимидилатсинтетазы. В результате деление раковых клеток не происходит, рост опухоли приостанавливается.
Клинические исследования
Клинические исследования Fluorouracil проводились с привлечением пациентов с диагнозом «рак базальных клеток». Группа из 113 человек в возрасте от 33 до 68 лет использовала Эфудекс по схеме, указанной в инструкции по применению. В 93% случаев отмечаются значительные улучшения состояния кожи, и только у 7% не выявлено никакой реакции на терапию.
В ходе исследования Fluorouracil выздоровление проходит по схеме, составленной на основании отзывов пациентов: эритема, везикуляция, шелушение, эрозирование и эпителизация тканей.
Способ применения
Используя Флюороурацил, как и любой аналог в виде крема, необходимо пользоваться перчатками и аппликаторами (не металлическими).
Кератоз
Продолжительность лечения кератоза Флюороурацилом — от 2 до 4 недель. Наносить крем необходимо по всей поверхности кожи, пораженной патологией, дважды в день. Крем наносят, пока эпителий не покроется эрозией. Максимальный эффект достигается спустя 4-8 недель после последнего применения препарата.
Базально-клеточные карциномы
Продолжительность терапии при раке продолжается минимум 3-6 недель, максимум 10-12 недель. На протяжении лечения необходим мониторинг состояния здоровья со стороны лечащего врача.
Побочные эффекты
Список наиболее распространенных побочных эффектов от использования Эфудекс составлен на основании отзывов пациентов:
- Изменение состояния кожи на месте нанесения крема.
- Раздражение, краснота, реже образование язв органов зрения.
- Изменение вкусовых качеств.
- Ухудшение сна.
Данные состояния обратимы и проходят, как только прием препарата прекращается.
Обратится к врачу нужно, если на фоне лечения возникает рвота, боли в животе, наблюдается примесь крови в кале, появляются язвы на слизистых, есть устойчивые признаки инфекции (боль в горле, озноб, лихорадка).
Прежде чем Fluorouracil начать лечение, убедитесь, что у вас нет аллергии на компоненты крема. Аллергическая реакция проявляется в виде сыпи, зуда, отеков, головокружения, проблем с дыханием.
Во время терапии
Если терапия проводится относительно предраковых и раковых состояний, ей в обязательном порядке предшествует цитологическое исследование, подтверждающее диагноз. Также необходимо исключить аллергию на составляющие крема. Флюороурацил приобрести в аптеке можно только по рецепту врача, который и определит целесообразность такого лечения.
Нельзя наносить средство на участки кожи с ранами, инфекциями, раздражениями, покраснениями. На протяжении терапии ограничьте время пребывания на солнце, исключите посещение солярия, бассейна. Не комбинируйте Efudex с другими препаратами и косметикой: ценой такого «соседства» станут побочные эффекты со стороны кожного покрова.
Не назначают средство беременным женщинам. Во избежание зачатия во время терапии назначают негормональные барьерные контрацептивы.
Применение для лечения других форм заболевания
Крем Efudex назначают для лечения карциномы кожи, кератоза, болезни Боуэна. Фармакологическая эффективность препарата относительно других патологий не изучалась.
Аналоги и заменители
Если приобрести Эфудекс по каким-либо причинам нет возможности, лечащий врач подберет аналог с идентичным составом и фармакологическими свойствами. Самостоятельно заменять лекарственные средства на аналогичные нельзя.
Условия транспортировки и хранения
Как хранить крем Efudex, во избежание снижения его лечебных свойств, рассказано в инструкции. Хранят средство при температуре 25 °C, транспортировка допускается при в температурном диапазоне от 15 °C до 30 °C.
Fluorouracil Cream or Topical Solution
Что представляет собой это лекарство?
ФТОРУРАЦИЛ, 5-ФУ, это химиотерапевтический препарат. Он наносится на кожу для лечения рака и некоторых предраковых заболеваний кожи.
Это лекарство может применяться в других целях; если у вас возникнут вопросы, обратитесь к медицинскому работнику или фармацевту.
РАСПРОСТРАНЕННОЕ БРЕНДОВОЕ НАЗВАНИЕ (НАЗВАНИЯ): Carac, Efudex, Fluoroplex, Tolak
Что мне следует рассказать медицинскому работнику до начала приема этого лекарства?
Необходимо знать, есть ли у вас одно из следующих состояний:
- дефицит дигидропиримидиндегидрогеназы (ДПД);
- необычная или аллергическая реакция на фторурацил или другие химиотерапевтические препараты;
- необычная или аллергическая реакция на другие лекарства, пищевые продукты, красители или консерванты;
- беременность или планирование беременности;
- кормление грудью;
Как мне следует применять это лекарство?
Это лекарство предназначено только для нанесения на кожу. Следуйте указаниям на упаковке или в рецепте. Вымойте руки до и после использования. Вымойте и осторожно высушите пораженный участок кожи. Для нанесения этого лекарства пользуйтесь ватным аппликатором; если наносите его пальцами, наденьте перчатки. Если вы не надели перчатки, хорошо вымойте руки после нанесения. Избегайте попадания в глаза, нос и рот. Нанесите достаточное количество лекарства для того, чтобы покрыть пораженный участок кожи. Можно покрыть участок тонкой марлевой повязкой; не используйте плотные или воздухонепроницаемые повязки. Завершите полный курс лечения этим лекарством в соответствии с указаниями, даже если вы полагаете, что ваше состояние улучшилось. Не прекращайте прием этого лекарства без рекомендации врача.
Спросите педиатра о возможности назначения этого лекарства детям. В этом случае необходима особая осторожность.
Передозировка: Если вам кажется, что вы превысили допустимую дозу этого лекарства, немедленно обратитесь в токсикологический центр или приемное отделение для оказания неотложной помощи. ПРИМЕЧАНИЕ: Это лекарство предназначено только для вас. Не делитесь им с другими лицами.
Что произойдет в случае пропуска приема лекарства?
Если вы забыли принять лекарство, примите его как можно скорее. Если приближается время приема следующей дозы, примите только эту дозу. Не принимайте дополнительные дозы. Обратитесь к врачу или другому медицинскому работнику, если вы забыли принять лекарство более 1 раза.
С чем это лекарство может вступать во взаимодействие?
Взаимодействий не предвидится. Не применяйте любое иное средство для кожи без рекомендации врача или другого медицинского работника.
Этот перечень не содержит всех возможных взаимодействий. Предоставьте медицинскому работнику список всех принимаемых вами лекарств, лекарственных растений, безрецептурных препаратов и пищевых добавок. Также сообщите ему о курении, употреблении алкогольных напитков или наркотиков. Некоторые вещества могут вступать во взаимодействие с принимаемым вами лекарством.
На что нужно обратить внимание при использовании этого лекарства?
Регулярно посещайте врача или другого медицинского работника для наблюдения за вашим состоянием. Вам потребуется применять это лекарство в течение 2 — 6 недель. Этот период может оказаться продолжительнее в зависимости от заболевания, по поводу которого назначено лечение. Возможно, полное заживление произойдет в течение 1-2 месяцев после прекращения применения этого лекарства.
В течение нескольких недель после лечения этим лекарством обработанные участки кожи могут выглядеть непривлекательно.
Избегайте попадания лекарства в глаза. Если это произошло, промойте большим количеством прохладной воды.
Это лекарство может повысить чувствительность к солнечному свету. Избегайте воздействия солнечного света. Если вы не можете избежать пребывания на солнце, носите защитную одежду и используйте солнцезащитное средство. Не пользуйтесь УФ лампами, горизонтальным или вертикальным солярием.
В случае контакта домашнего животного с этим лекарством возможны побочные эффекты или смерть животного. Если домашнее животное лизнуло участок кожи, обработанный этим лекарством, или контактировало с контейнером, в котором хранится лекарство, незамедлительно обратитесь к ветеринару. Выбрасывайте или мойте все приспособления, используемые для нанесения лекарства. После нанесения лекарства вымойте руки. Не допускайте попадания лекарства на одежду, ковры или мебель. Если вы не можете исключить контакт домашних животных с вашей кожей, выясните у врача или другого медицинского работника, можно ли покрыть чем-либо участок(-ки) кожи, обработанный(-ые) этим лекарством.
Избегайте беременности во время приема этого лекарства и в течение 1 месяца после его прекращения. Женщинам следует сообщить врачу о планировании беременности или предположении о возможной беременности. Существует вероятность действия этого лекарства на плод. За дополнительной информацией обратитесь к врачу, другому медицинскому работнику или фармацевту.
Какие побочные эффекты могут быть при приеме этого лекарства?
Побочные эффекты, о которых вам следует как можно скорее сообщить врачу или другому медицинскому работнику:
- аллергические реакции, такие как кожная сыпь, зуд, крапивница, отечность лица, губ или языка;
- диарея с кровью;
- повышение температуры или озноб;
- боль в желудке;
- рвота; Побочные эффекты, которые обычно не требуют немедленного медицинского внимания (сообщите врачу или другому медицинскому работнику, если они продолжаются или доставляют неудобства):
- покраснение или сухость кожи;
- светочувствительность;
Этот перечень не содержит всех возможных побочных эффектов. Обратитесь к врачу за советом относительно побочных эффектов. Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-332-1088.
Где следует хранить это лекарство?
Храните в недоступном для детей и домашних животных месте.
Смотрите инструкции по хранению лекарства. Каждое лекарство может иметь различные инструкции. Следует выбрасывать все неиспользованное лекарство после истечения срока годности, указанного на этикетке или упаковке.
ПРИМЕЧАНИЕ: Этот перечень не содержит всех возможных сведений. Если у вас возникнут вопросы, касающиеся данного лекарства, обратитесь к врачу, фармацевту или другому медицинскому работнику.
© 2023 Elsevier/Gold Standard (2021-04-22 00:00:00)