Флексотрон Форте — инструкция по применению
Синонимы, аналоги
Статьи
Изделие медицинского назначения. Не является лекарством
Наименование медицинского изделия
Имплантат вязкоэластичный стерильный для внутрисуставных инъекций ФЛЕКСОТРОН® Форте (FLEXOTRON® Forte), на основе гиалуроната натрия, 10 мг/мл, 3 мл.
Имплантат представляет собой бесцветный, прозрачный, вязкий и стерильный гель (гидрогель). Имплантат не включает в себя лекарственные средства, производные клеток и тканей человека, ткани животных. Не имеет радиационных и электромагнитных свойств.
Состав:
| Ингредиент | Содержание |
| гиалуронат натрия (C14H2DNNaO11)n | 1% |
| Солевой раствор фосфатного буфера: | |
| Na2HPO4*12H2O | 0,06% |
| NaH2PO4*2H2O | 0,0048% |
| Хлорид натрия | 0,89% |
| Вода для инъекций | сколько требуется до 100% (3 мл) |
Технические характеристики:
Описание
Имплантат для замещения синовиальной жидкости ФЛЕКСОТРОН® Форте поставляется в стеклянном шприце и содержит гиалуроновую кислоту. Продукт представляет собой бесцветный, прозрачный, вязкоупругий и стерильный раствор. Гиалуроновая кислота (молекулярная масса 650000-1200000 Да) является продуктом бактериальной ферментации. Изделие предназначено только для одноразового применения.
Гиалуроновая кислота является естественным полисахаридом, который входит в состав всех тканей организма, при этом в особенно большой концентрации гиалуроновая кислота содержится в коже, подкожных тканях, а также в соединительной ткани, такой как синовиальная жидкость. Гиалуроновая кислота принадлежит к небольшой группе веществ, одинаковых для всех живых организмов, поэтому она обладает высокой биосовместимостью. В 1 мл продукта содержится 10 мг гиалуроната натрия, растворенного в физиологическом растворе. Не подлежит техническому обслуживанию.
Комплект поставки
Одна единица продукции включает:
Стерильность
Изделие проходит финишную стерилизацию автоклавированием в соответствии с EN 556-1. Валидация данного процесса осуществляется в соответствии со стандартами ISO 11138-3 и ISO 17665-1 для подтверждения стерильности.
Назначение
Вязкоэластичное протезирование синовиальной жидкости у пациентов с дегенеративно-дистрофическими и посттравматическими поражениями суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Показания к применению
Способ применения
Инъекции выполняются медицинскими специалистами в асептических условиях. Перед введением имплантата содержимое шприца должно быть визуально оценено на прозрачность и однородность. Помутнение, кристаллизация, появление окраски и/или инородных включений может свидетельствовать о нарушении правил транспортировки и хранения изделия. При появлении вышеуказанных признаков введение средства для замещения синовиальной жидкости запрещено.
Имплантат вводится внутрисуставно в асептических условиях процедурных и манипуляционных кабинетов.
Перед проведением инъекции необходимо удалить покрывающую мембрану и извлечь наполненный шприц с имплантатом из блистера.
Вручную прикрепить адаптер для пальцев к упору цилиндра шприца.
Придерживая люэровский наконечник, аккуратно открутить колпачок наконечника шприца (как показано ниже). Избегать чрезмерных нагрузок на шприц при фиксации иглы для предотвращения деформации механизма Луер-Лок.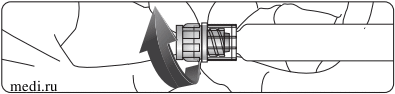
Продолжая крепко удерживать люэровский наконечник, прикрутить стерильную иглу рекомендуемым размером 21G или 23G (не входят в комплект поставки) к защелке шприца до тех пор, пока она не будет закреплена. Длина иглы выбираться врачом в соответствии с конституцией человека и толщиной подкожной клетчатки в месте пункции. Перед инъекцией выпустить из шприца пузырьки воздуха в случае их наличия.
Вводить медленно. Пациент должен избегать любых физических нагрузок или весовых нагрузок в течение 48 часов после внутрисуставной инъекции.
На курс лечения рекомендуется 3-5 шприцев. Для лечения остеоартрита / остеоартроза (OA) суставов у взрослых проводят 1 инъекцию в неделю. Количество и частота инъекций могут изменяться в зависимости от тяжести симптоматики.
Ожидаемая эффективность и принцип работы
Молекула гиалуроновой кислоты имеет спиральную длинноцепочечную структуру, которая позволяет удерживать или поглощать молекулы воды. Внутрисуставное обогащение синовиальной жидкости инъекциями гиалуроната натрия способствует улучшению или восстановлению вязкоупругих свойств естественной синовиальной жидкости. Гиалуронат натрия отвечает за вязкоупругие свойства синовиальной жидкости, таким образом вязкоэластичное протезирование позволяет компенсировать недостаточность гиалуроновой кислоты в синовиальной жидкости или снижение её вязкости, смягчить внешние нагрузки на сустав, обеспечивает смазывание, восстановление упругости и вязкости, амортизацию, увлажнение и обволакивание суставных поверхностей, покрывая смазывающим защитным слоем хрящ и рецепторы синовии. Это помогает увеличить объём движений и обеспечивает механическую защиту тканей полости сустава, что в свою очередь может улучшать течение остеоратроза / остеоартрита и других дегенеративно-дистрофических и посттравматических патологий суставов.
Ожидаемая продолжительность эффекта составляет 6 месяцев после проведения курса лечения.
Противопоказания
Меры предосторожности
По причине того, что септический артрит является серьезным побочным эффектом, необходимо соблюдать все стандартные меры предосторожности для хирургических вмешательств.
При получении аспирационной жидкости перед проведением вязкоэластичного протезирования следует провести соответствующие исследования для исключения бактериальной этиологии артрита.
Изделие предназначено для внутрисуставного введения. Необходимо избегать внутрисосудистого или внутритканевого введения изделия.
Изделие следует использовать до истечения срока годности, указанного на упаковке.
Применять с осторожностью у пациентов с аллергией, а также у пациентов с заболеваниями печени.
В первые дни после инъекции может быть рекомендован пероральный прием анальгетиков или противовоспалительных лекарственных средств.
Применение изделия совместно с четвертичными соединениями аммония запрещено.
Только для одноразового использования. Повторная стерилизация и применение изделия запрещены по причине наличия риска возникновения инфекции, перекрестной инфекции и (или) дефекта изделия. Не использовать шприц из открытой и/или поврежденной стерильной упаковки. Не использовать шприц с открытым или поврежденным колпачком стерильного шприца. При нарушении стерильности или подозрении о нарушении стерильности имплантата изделие должно быть утилизировано.
Пожилые пациенты
Применять с осторожностью ввиду общего снижения функциональной активности органов и систем организма.
Беременность и лактация
Применять в случае, если преимущество лечения превышает риск развития нежелательных явлений. Во время лечения кормление грудью следует прекратить.
Дети
Безопасность применения продукта у детей изучена недостаточно, поэтому применять с осторожностью.
Возможные побочные эффекты
Применение внутрисуставных форм гиалуроновой кислоты при дегенеративно-дистрофических и посттравматических поражениях суставов является хорошо изученным методом с установленным профилем безопасности, применяющимся на протяжении нескольких десятилетий.
К основным побочным эффектам относятся боль, отек и скованность в суставе после инъекции.
В крайне редких случаях возможно проявление местных воспалительных симптомов (повышение температуры, покраснение и отечность, увеличение содержания экссудата в полости сустава). После внутрисуставной инъекции могут возникать такие обратимые местные реакции, как кратковременное ограничение подвижности, чувство дискомфорта или тяжести в суставе. Проявление данных симптомов можно уменьшить прикладыванием льда к месту инъекции в течение 5-10 минут.
Имеются сообщения о единичных случаях аллергических реакций (например, зуд, сыпь, крапивница) и анафилактических реакций, септического артрита, внутритканевых кровоизлияниях или кровоизлияниях в полость сустава, тендинитах, флебитах, парестезиях, головокружениях, головных болях, мышечных спазмах, чувстве жара, общем недомогании, периферических отеков при внутрисуставном введении растворов гиалуроновой кислоты.
При появлении местных или общих симптомов следует проконсультироваться с врачом.
Извлечение имплантата
В случае выраженных проявлений может быть рекомендовано удаление имплантата из полости сустава, в том числе с применением лаважа согласно действующим клиническим рекомендациям. Запрещаются повторные инъекции имплантатов синовиальной жидкости в сустав до купирования симптомов острого воспаления!
Хранение и транспортировка
Хранить и транспортировать при температуре от 2 °C до 30 °C, в оригинальной упаковке. Беречь от воздействия прямых солнечных лучей. Не замораживать.
Срок годности:
3 года.
Защита окружающей среды и утилизация
Содержание шприца не является токсичным или огнеопасным. Изделия при использовании, транспортировке и хранении не оказывают негативного воздействия на окружающую среду.
Неиспользованные шприцы могут быть утилизированы в качестве бытовых отходов. Стекло следует утилизировать с осторожностью.
Неиспользованное содержимое шприца до или после истечения срока годности может быть утилизировано в качестве бытовых отходов (слить с большим количеством воды).
Уничтожение использованных медицинских изделий осуществляется в соответствии с природоохранными требованиями национальных, местных и ведомственных руководящих положений о безопасном уничтожении и утилизации.
В соответствии с санитарно-эпидемиологическими правилами и нормативами СанПиН 2.1.7.2790-10 использованные медицинские изделия (шприцы с имплантатами) относятся к медицинским отходам класса Б (эпидемиологически опасные отходы).
Расшифровка символов на упаковке
Гарантийные обязательства
Гарантийный срок соответствует сроку годности изделия. Срок годности медицинского изделия составляет 3 года.
Производитель гарантирует качество изделий и соответствие заявленным техническим спецификациям в течение всего срока годности при соблюдении условий эксплуатации, транспортирования и хранения. Производитель или его уполномоченный представитель предоставляет информацию и рекомендации в отношении рисков, а также предписания, методы и технические приемы для применения изделия.
Компания-производитель снимает с себя всю ответственность и отказывается от гарантийных обязательств в связи с травмами пациента или ущербом, который может иметь место в результате:
1. Выбранного способа применения и технического приема введения имплантата при несоблюдении установленных рекомендаций.
2. Неподходящего назначения, выбора использования для конкретного пациента.
3. Использования изделия после истечения указанного срока годности или при нарушениях правил хранения и транспортировки.
Производитель
«СайВижн Байотек Инк.», Тайвань. (SciVision Biotech Inc., 9, South 6th Rd., K.E.P.Z., Kaohsiung 806, Taiwan, R.O.C.)
Уполномоченный представитель производителя в России
Общество с ограниченной ответственностью «МКНТ Импорт» (ООО «МКНТ Импорт»), 119071, город Москва, улица Орджоникидзе, дом 12, стр. 2, Российская Федерация
Уполномоченный представитель производителя в России наделен правами обеспечения процессов прослеживаемости продукции и послерегистрационного мониторинга безопасности медицинского изделия в целях выявления и предотвращения побочных действий, не указанных в инструкции по применению, нежелательных реакций при применении медицинского изделия, особенностей взаимодействия медицинских изделий между собой, фактов и обстоятельств, создающих угрозу жизни и здоровью граждан и медицинских работников. Для выполнения данных функций ООО «МКНТ Импорт», действуя в качестве уполномоченного представителя, или/и его доверенные лица наделены правом собирать послерегистрационные данные, доводить до субъектов обращения информацию по безопасности, вовлекаться в мероприятия по выполнению корректирующих и превентивных действий, а также заключать соответствующие соглашения по обмену данными в отношении этой продукции, если это не противоречит законодательству Российской Федерации и Евразийского Экономического Союза.
Уполномоченный представитель производителя и организация, отвечающая за пострегистрационное наблюдение за безопасностью и принимающая претензии от потребителей на территории Республики Казахстан: ТОО «ТопМед», Республика Казахстан, 050067, Алматы, Бостандыкский район, Садоводческое товарищество Природа, дом 49.
Изделие соответствует требованиям следующих национальных стандартов производителя ISO 13485:2016; ISO 14630:2012; IEC 62366-1:2015; EN ISO 14971:2012; ISO 14602:2010; ISO 14155:2011; USP; Ph. Eur.; ISO 10993-1:2018; ISO 10993-3:2014; ISO 10993-5:2009; ISO 10993-6:2016; ISO 10993-10:2010; ISO 10993-11:2017; ISO 10993-12:2012; ISO 10993-18:2005; ASTM F1980-16:2016; EN 556-1:2001; ISO 11138-1:2017; ISO 11138-3:2017; ISO 11737-1:2018; ISO 11737-2:2009; ISO 17665-1:2006; ISO 14644-1:2015; ISO 14644-2:2015; ISO 13408-1:2008; ISO 11607-1:2019; ISO 11607-2:2019; ISO 80369-7:2016; ISO 15223-1:2016; BS EN 1041:2008+A1:2013
Регистрационное удостоверение № РЗН 2022/17365 от 27.05.2022 г.
Медициналық бұйымның атауы
Буынішілік инъекцияларға арналған, натрий гиалуронаты негізіндегі стерильді, тұтқыр созылғыш ФЛЕКСОТРОН® Форте (FLEXOTRON® Forte) имплантаты, 10 мг/мл, 3 мл.
Имплантат түссіз, мөлдір, тұтқыр жане стерильді гель (гидрогель) болып табылады. Имплантаттың құрамында дәрілік заттар, адам жасушалары мен тіндерінің туындылары, жануарлар тіндері жоқ. Радиациялық жане электромагниттік қасиеттері жоқ.
Құрамы:
| Ингредиент | Құрамы |
| Натрий гиалуронаты (C14H2DNNaO11)n | 1% |
| Фосфатты буфердің тұзды ерітіндісі: | |
| Na2HPO4*12H2O | 0,06% |
| NaH2PO4*2H2O | 0,0048% |
| Натрий хлориді | 0,89% |
| Инъекцияға арналған су | 100% (3 мл) дейін қажетінше |
Техникалық сипаттамалары:*
Сипаттамасы
Синовиальді сұйықтықты алмастыруға арналған ФЛЕКСОТРОН® Форте имплантаты шыны шприцте жеткізіледі жане құрамында гиалурон қышқылы бар. Өнім түссіз, мөлдір, тұтқыр серпімді жане стерильді ерітінді болып табылады. Гиалурон қышылы (молекулалық салмағы 650000-1200000 Да) микроорганизмдерден экстракцияланады. Өнім тек бір рет қолдануға арналған.
Гиалурон қышқылы организмнің барлық тіндерінің құрамына кіретін табиғи полисахарид болып табылады, сонымен қатар, асіресе, көп концентрациясында гиалурон қышқылы теріде, теріасты тіндерінде, сондай-ақ, синовиальді сұйықтық сияқты данекер тінде болады. Гиалурон қышқылы барлық тірі организмдер үшін бірдей заттардың шағын тобына жатады, сондықтан оның биоүйлесімділігі жоғары. 1 мл өнімнің құрамында физиологиялық ерітіндіде ерітілген 10 мг натрий гиалуронаты болады.
Техникалық қызмет көрсетілмейді.
Жеткізілім жиынтығы
Өнімнің бір бірлігі келесілерден құралған:
Стерильділігі
Бұйым EN 556-1ге сайкес автоклавтау арқылы ақырғы рет стерилизацилаудан өтеді. Бұл үдерісті валидациялау стерильділігін растау үшін ISO 11138-3 жане ISO 17665-1 стандарттарына сәйкес жүзеге асырылады.
Тағайындалуы
Буындардың дегенерациялық-дистрофиялық жане жарақаттан кейінгі зақымданулары бар пациенттерде, сондай-ақ, зақымданған буындарына көп күш түсетін адамдарда синовиальді сұйықтықты тұтқыр созылғыш протездеу үшін
Қолданылуы
Қолдану тәсілі
Инъекцияларды дарігер-мамандар асептикалық жағдайларда жүргізеді.
Имплантатты енгізер алдында шприцтің ішіндегісінің мөлдірлігі мен біртектілігі көзбен қарап бағалануы тиіс. Бұлыңғырлануы, кристалдануы, түсінің өзгеруі жане/немесе бөгде қосылыстардың пайда болуы бұйымды тасымалдау жане сақтау шарттарының бұзылғанын білдіруі мүмкін. Жоғарыда аталған белгілер пайда болған жағдайда, имплантатты енгізуге тыйым салынады.
Имплантат емшара жане манипуляция кабинеттерінде асептикалық жағдайларда буын ішіне енгізіледі.
Инъекция жүргізер алдында жауып тұрған жарғақшасын алып тастау жане имплантат толтырылған шприцті блистерден шығарып алыңыз.
Саусаққа арналған адаптерді шприц цилиндрінің түбіне қолмен бекемдеңіз.
Люэр ұштығынан ұстап тұрып, шприц ұштығының қалпақшасын абайлап бұрап ағытып алыңыз (төменде көрсетілгендей). Луер-Лок механизмінің деформациялануына жол бермеу үшін, инені бекемдеген кезде шприцке шамадан тыс күш салмаңыз.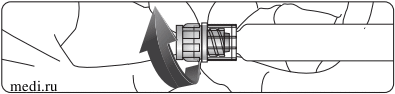
Люэр ұштығын мықтап ұстап тұрып, ұсынылған 21G немесе 23G өлшемдегі (жеткізілім жиынтығына кірмейді) стерильді инені шприцтің ілмегіне бекемделгенге дейін бұрап кіргізіңіз. Иненің ұзындығын дарігер адамның конституциясына жане пункция орнындағы теріасты шелінің қалыңдығына сайкес таңдайды. Шприцте ауа көпіршіктері болса, инъекция алдында оларды шығарып жіберу керек.
Баяу енгізу керек. Пациент кез келген буынішілік инъекциядан кейінгі 48 сағат ішінде дене жүктемелерінен немесе салмақ жүктемелерінен сақтануы тиіс.
Бір емдеу курсына 3-5 шприц ұсынылады. Ересектерде буындардың остеоартритін / остеоартрозын (OA) емдеу үшін аптасына 1 инъекциясын жүргізеді. Инъекциялардың саны мен жиілігі симптоматиканың ауырлығына байланысты өзгеріп отыруы мүмкін.
Күтілетін тиімділігі және жұмыс істеу принципі
Гиалурон қышқылының молекуласы спиральді ұзын тізбекті құрылымыға ие, ол су молекулаларын ұстап тұруға немесе сіңіруге мүмкіндік береді. Буынішілік синовиальді сұйықтықтың натрий гиалуронаты инъекцияларымен байытылуы табиғи синовиальді сұйықтықтың тұтқыр серпімді қасиеттерінің жақсаруына немесе қалпына келуіне ықпал етеді. Натрий гиалуронаты синовиальді сұйықтықтың тұтқыр серпімді қасиеттерінне жауап береді, сол арқылы тұтқыр созылғыш протездеу синовиальді сұйықтықтағы гиалурон қышқылы жеткіліксіздігінің жане оның тұтқырлығы төмендеуінің орнын толтыруға, буынға түсетін сыртқы жүктемелерді жеңілдетуге мүмкіндік береді, шеміршек пен синовия рецепторларын майлағыш қорғағыш қабатпен жаба отырып, буын беткейлерінің майлануын, серпімділігі мен тұтқырлығының қалпына келуін, амортизациясын, ылғалдануы мен жабылуын қамтамасыз етеді. Бұл қимыл-қозғалыс көлемін арттыруға көмектеседі жане буын қуысы тіндерінің механикалық қорғанысын қамтамасыз етеді, ол өз кезегінде остеоратроз / остеоартрит және буындардың басқа дегенерациялық-дистрофиялық жане жарақаттан кейінгі патологияларының ағымын жақсартуы мүмкін.
Әсерінің күтілетін ұзақтығы емдеу курсын жүргізгеннен кейін 6 айды құрайды.
Қолдануға болмайтын жағдайлар
Сақтық шаралары
Сепсистік артрит ауыр жағымсыз эсер болып табылатындығы себепті, хирургиялық араласымдарға арналған барлық стандартты сақтық шараларын сақтау қажет.
Аспирациялық сұйықтық алу кезінде тұтқыр созылғыш протездеуді енгізер алдында артриттің бактериялық этиологиясы бар-жоқтығын анықтау үшін сэйкесінше зерттеулер жүргізу керек.
Бұйым буын ішіне енгізуге арналған. Бұйымды тамыр ішіне немесе тін ішіне енгізбеу қажет.
Бұйымды қаптамасында көрсетілген жарамдылық мерзімі өткенге дейін пайдалану керек.
Аллергиясы бар пациенттерде, сондай-ақ, бауыр ауруары бар пациенттерде сақтықпен қолдану керек.
Инъекциядан кейінгі алғашқы күндері анальгетиктерді немесе қабынуға қарсы дэрілік заттарды пероральді қабылдау пайдалы болуы мүмкін. Бұйымды төртіншілік аммоний қосылыстарымен бірге қолдануға тыйым салынады.
Тек бір рет пайдалануға арналған. Инфекцияның, айқаспалы инфекцияның жане (немесе) бұйым ақауының туындау қаупінің болуы себепті, бұйымды қайта стерилизациялауға жэне қолдануға тыйым салынады. Стерильді қаптамасы ашылған жане/немесе бүлінген шприцті пайдалануға болмайды. Стерильді шприцтің қалпақшасы ашылып қалған немесе бүлінген шприцті пайдалануға болмайды. Имплантаттың стерильділігі бұзылған немесе стерильділігі бұзылғандығына күдік болған жағдайда, бұйым утилизациялануы тиіс
Егде жастағы пациенттер
Организм ағзалары мен жүйелерінің функционалдық белсенділігінің жалпы төмендейтіндігіне байланысты, сақтықпен қолдану керек.
Жүктілік және лактация
Егер емдеудің артықшылығы жағымсыз құбылыстардың даму қаупінен асып түсетін болса ғана қолдану керек. Емдеу кезінде бала емізуді тоқтату керек.
Балалар
Өнімнің балаларда қолданылуының қауіпсіздігі жеткіліксіз зерттелген, сондықтан сақтықпен қолдану керек.
Болуы мүмкін жағымсыз әсерлері
Буындардың дегенерациялық-дистрофиялық жане жарақаттан кейінгі зақымданулары кезінде гиалурон қышқылының буынішілік түрерін қолдану қауіпсіздік бейіні анықталған, бірнеше онжылдықтар бойы қолданып келе жатқан, жақсы зерттелген адіс болып табылады.
Негізгі жағымсыз асерлеріне инъекциядан кейін буынның ауыруы, ісінуі жане құрысуы жатады.
Аса сирек жағдайларда жергілікті уақытша қабыну симптомдары (температура жоғарылауы, қызару жане ісіну, буын қуысындағы экссудат мөлшерінің артуы) көрініс беруі мүмкін. Буынішілік инъекциядан кейін қимыл-қозғалыстың қысқа мерзімді шектелуі, буындағы жайсыздық немесе ауырлық сезімі, гематомалар сияқты қайтымды жергілікті реакциялар туындауы мүмкін. Ондай симптомдардың көрініс беруін инъекция орнына 5-10 минут бойы мұз басу арқылы азайтуға болады.
Гиалурон қышқылы ерітінділерін буын ішіне енгізген кездегі аллергиялық реакциялар (мысалы, қышыну, бөртпе, есекжем) мен анафилаксиялық реакциялардың бірен-саран жағдайлары, сепсистік артрит, тінішілік қан кетулер немесе буын қуысына қан құйылулар, тендениттер, флебиттер, парестезиялар, бас айналуы, бас ауыруы, бұлшықеттердің түйілулері, ысыну сезімі, жалпы дімкастану, шеткері ісінулер туралы хабарламалар бар.
Жергілікті немесе жалпы симптомдар пайда болған жағдайда, дарігермен кеңесу керек.
Имплантатты шығарып алу
Айқын көріністер болған жағдайда, имплантатты буын куысынан алып тастау, соның ішінде, қолданыстағы клиникалық ұсынымдарға сайкес лаважды қолданып алып тастау ұсынылуы мүмкін. Жедел қабыну симптомдары басылғанға дейін имплантаттарды буынға синовиальді сұйықтыққа қайта инъекциялауға тыйым салынады!
Сақтау және тасымалдау
2 °С-ден 30 °С-ге дейінгі температурада түпнұсқалық қаптамасында сақтау жане тасымалдау керек. Тікелей түсетін күн саулесінің асерінен қорғау керек. Мұздатып қатыруға болмайды.
Жарамдылық мерзімі:
3 жыл.
Қоршаған ортаны қорғау және утилизациялау.
Шприцтің ішіндегісі уытты немесе өртке қауіпті емес. Бұйымдар пайдалану, тасымалдау жане сақтау кезінде қоршаған ортаға теріс асер етпейді.
Пайдаланылмаған шприцтерді тұрмыстық қалдықтар ретінде утилизациялауға болады. Шыныларды сақтықпен утилизациялау керек. Пайдаланылмаған шприцтің ішіндегісін жарамдылық мерзімі өткенге дейін немесе өткеннен кейін тұрмыстық қалдықтар ретінде утилизациялауға (мол сумен ағызып жіберуге) болады.
Пайдаланылған медициналық бұйымдарды жою қауіпсіз жою жане утилизациялау туралы Ұлттық, жергілікті жэне ведомстволық басшылық ережелердің табиғат қорғау талаптарына сайкес жүзеге асырылады.
Санитарлық-эпидемиологиялық ережелер мен СанЕмН 2.1.7.2790-10 нормативтеріне сэйкес пайдаланылған медициналық бұйымдар (имплантанттары бар шприцтер) Б класының медициналық қалдықтарына (эпидемиологиялық қауіпті қалдықтар) жатады.
Қаптамасындағы символдардың түсіндірмесі
Кепілдік міндеттемелері
Кепілдік мерзімі бұйымның жарамдылық мерзіміне сайкес келеді. Медициналық бұйымның жарамдылық мерзімі 3 жылды құрайды.
Өндіруші бұйымдардың сапасына жэне пайдалану, тасымалдау жане сақтау шарттары сақталған жағдайда барлық жарамдылық мерзімі бойына, малімденген техникалық сипаттамаларына сайкес келетіндігіне кепілдік береді. Өндіруші немесе оның уакілетті өкілі бұйымды қолдану үшін қауіптеріне, сондай-ақ, кеңестер, адістері мен техникалық тасілдеріне қатысты ақпарат жане нұсқау береді.
Өндіруші компания келесілердің:
1. Таңдалған қолдану тасілінің жане имплантты енгізудің бекітілген ұсынымдары сақталмаған техникалық адісінің.
2. Үйлесімсіз тағайындалуының, пайдалану үшін нақты бір пациенттің таңдалуының.
3. Бұйымды жарамдылық мерзімі өткеннен кейін немесе сақтау жане тасымалдау ережелерін бұза отырып пайдаланудың натижесінде орын алуы мүмкін пациенттің жарақаттануына немесе зиян шегуіне жауап бермейді жане сонымен байланысты кепілдік міндеттемелерінен бас тартады.
Өндіруші
«СайВижн Байотек Инк.», Тайвань. (SciVision Biotech Inc., 9, South 6th Rd., K.E.P.Z., Kaohsiung 806, Taiwan, R.O.C.)
Өндірушінің Ресейдегі уәкілетті өкілі
«МКНТ Импорт» жауапкершілігі шектеуі қоғамы («МКНТ Импорт» ЖШҚ) 119071, Маскеу қаласы, Орджоникидзе көшесі, 12 үй, 2 құр., Ресей Федерациясы
Өндірушінің Ресейдегі уакілетті өкіліне медициналық бұйымды қолдану кезінде қолдану жөніндегі нұсқаулықта көрсетілмеген жағымсыз асерлерін, медициналық бұйымдардың өзара арекеттесулерінің ерекшеліктерін, азаматтар мен медицина қызметкерлерінің өмірі мен денсаулығына қауіп төндіретін фактілер мен жағдайларды анықтау жане алдын алу мақсаттарында, өнімнің қадағалану үдерістерін жане медициналық бұйымның тіркеуден кейінгі қауіпсіздігін мониторингілеуді қамтамасыз ету құқықтары берілген. Аталған функцияларды атқару үшін, уакілетті өкіл ретінде арекет ететін «МКНТ Импорт» ЖШК, жане/немесе оның сенімді тұлғаларына тіркеуден кейінгі деректерді жинақтап, қауіпсіздігі жөніндегі ақпараттар айналымы саласындағы субъектілерге хабарлау, түзетушілік жане превентивтік арекеттерді атқару шараларына қатысу, сондай-ақ, егер бұл Ресей Федерациясы мен Еуразиялық Экономикалық Одақтың заңдарына қайшы келмесе, осы өнімге қатысты деректер алмасу үшін тиісінше келісімдер жасасу құқығы берілген.
Бұйым өндірушінің келесі ұлттық стандарттарының талаптарына сайкес келеді ISO 13485:2016; ISO 14630:2012; IEC 62366-1:2015; EN ISO 14971:2012; ISO 14602:2010; ISO 14155:2011; USP; Ph. Eur.; ISO 10993-1:2018; ISO 10993-3:2014; ISO 10993-5:2009; ISO 10993-6:2016; ISO 10993-10:2010; ISO 10993-11:2017; ISO 10993-12:2012; ISO 10993-18:2005; ASTM F1980-16:2016; EN 556-1:2001; ISO 11138-1:2017; ISO 11138-3:2017; ISO 11737-1:2018; ISO 11737-2:2009; ISO 17665-1:2006; ISO 14644-1:2015; ISO 14644-2:2015; ISO 13408-1:2008; ISO 11607-1:2019; ISO 11607-2:2019; ISO 80369-7:2016; ISO 15223-1:2016; BS EN 1041:2008+A1:2013
Қазақтан Республикасы аумағында қолайсыз оқиғаларды (инциденттерді) мониторингілеу жөніндегі уәкілетті өкілдің байланыс деректері:
«ТопМед» жШс, Қазақстан Республикасы, 050067, Алматы, Бостандық ауданы, Природа бау-бақша серіктестігі 49 үй.
Осыған сәйкес медициналық мақсаттағы бұйым өндірілген нормативтік құжаттың атауы (белгіленуі):
Техникалық файл 24.07.2020
Купить Флексотрон Форте в Планета Здоровья
Купить Флексотрон Форте в ГорЗдрав
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Владелец регистрационного удостоверения:
Контакты для обращений:
МКНТ ИМПОРТ ООО
(Россия)
Лекарственная форма
| МИ | Флексотрон® Форте |
Имплантат вязкоэластичный стерильный д/внутрисуставных инъекций 10 мг/мл (1%): шприц 3 мл рег. №: РЗН 2022/17365 |
Форма выпуска, упаковка и состав
продукта Флексотрон® Форте
Имплантат вязкоэластичный стерильный для внутрисуставных инъекций в виде бесцветного, прозрачного, однородного, вязкого, апирогенного геля (гидрогеля) с отсутствием помутнения, кристаллизации, инородных включений.
Вспомогательные вещества (солевой раствор фосфатного буфера): натрия гидрофосфата додекагидрат (Na2HPO4×12H2O) — 0.06%, натрия дигидрофосфата дигидрат (NaH2PO4×2H2O) — 0.0048%, натрия хлорид — 0.89%, вода д/и — сколько требуется до 100% (3 мл).
Имплантат не включает в себя лекарственные средства, производные клеток и тканей человека, ткани животных. Не имеет радиационных и электромагнитных свойств.
3 мл — шприцы стеклянные (1) — блистеры (1) с имплантационными стикерами (3 шт.) — коробки картонные.
Свойства
Имплантат Флексотрон® Форте представляет собой медицинское изделие для внутрисуставных инъекций на основе гиалуроната натрия. В 1 мл продукта содержится 10 мг натрия гиалуроната, растворенного в физиологическом растворе.
Гиалуроновая кислота (молекулярная масса 650000-1200000 Да) является продуктом бактериальной ферментации. Гиалуроновая кислота принадлежит к небольшой группе веществ, одинаковых для всех живых организмов, поэтому она обладает высокой биосовместимостью.
Гиалуроновая кислота является естественным полисахаридом, который входит в состав всех тканей организма, при этом в особенно большой концентрации гиалуроновая кислота содержится в коже, подкожных тканях, а также в соединительной ткани, такой как синовиальная жидкость. Молекула гиалуроновой кислоты имеет спиральную длинноцепочечную структуру, которая позволяет удерживать или поглощать молекулы воды. Внутрисуставное обогащение синовиальной жидкости инъекциями гиалуроната натрия способствует улучшению или восстановлению вязкоупругих свойств естественной синовиальной жидкости. Гиалуронат натрия отвечает за вязкоупругие свойства синовиальной жидкости, таким образом вязкоэластичное протезирование позволяет компенсировать недостаточность гиалуроновой кислоты в синовиальной жидкости или снижение ее вязкости, смягчить внешние нагрузки на сустав, обеспечивает смазывание, восстановление упругости и вязкости, амортизацию, увлажнение и обволакивание суставных поверхностей, покрывая смазывающим защитным слоем хрящ и рецепторы синовии. Это помогает увеличить объем движений и обеспечивает механическую защиту тканей полости сустава, что в свою очередь может улучшать течение остеоартроза/остеоартрита и других дегенеративно-дистрофических и посттравматических патологических изменений суставов.
Флексотрон® Форте не подлежит техническому обслуживанию.
Область применения
продукта Флексотрон® Форте
- остеоартрит/остеоартроз, посттравматические и другие дегенеративные изменения коленного, тазобедренного, плечевого и голеностопного суставов;
- восстановление свойств синовиальной жидкости при ортопедической хирургии суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Рекомендации по применению
Инъекции выполняются медицинскими специалистами в асептических условиях процедурных и манипуляционных кабинетов.
Перед введением имплантата содержимое шприца должно быть визуально оценено на прозрачность и однородность. Помутнение, кристаллизация, появление окраски и/или инородных включений может свидетельствовать о нарушении правил транспортировки и хранения изделия. При появлении вышеуказанных признаков введение средства для замещения синовиальной жидкости запрещено.
Имплантат вводится внутрисуставно в асептических условиях. Вводят в объеме, содержащемся в 1 шприце (3 мл). Для лечения остеоартрита/остеоартроза суставов у взрослых проводят 1 инъекцию в неделю. На курс лечения рекомендуется 3-5 шприцев. Количество и частота инъекций могут изменяться в зависимости от тяжести симптоматики.
Ожидаемая продолжительность эффекта составляет 6 месяцев после проведения курса лечения.
Перед проведением инъекции необходимо:
- Удалить покрывающую мембрану и извлечь наполненный шприц с имплантатом из блистера.
- Вручную прикрепить адаптер для пальцев к упору цилиндра шприца.
- Придерживая люэровский наконечник, аккуратно открутить колпачок наконечника шприца (как показано ниже). Избегать чрезмерных нагрузок на шприц при фиксации иглы для предотвращения деформации механизма Луер-Лок.
- Продолжая крепко удерживать люэровский наконечник, прикрутить стерильную иглу рекомендуемым размером 21G или 23G (не входят в комплект поставки) к защелке шприца до тех пор, пока она не будет закреплена. Длина иглы выбирается врачом в соответствии с конституцией человека и толщиной подкожной клетчатки в месте пункции.
- Перед инъекцией выпустить из шприца пузырьки воздуха в случае их наличия.
Вводить медленно.
Пациент должен избегать любых физических нагрузок или весовых нагрузок в течение 48 часов после внутрисуставной инъекции.
Побочные эффекты
Применение внутрисуставных форм гиалуроновой кислоты при дегенеративно-дистрофических и посттравматических поражениях суставов является хорошо изученным методом с установленным профилем безопасности, применяющимся на протяжении нескольких десятилетий.
К основным побочным эффектам относятся боль, отек и скованность в суставе после инъекции.
Крайне редко — возможно проявление местных воспалительных симптомов (повышение температуры, покраснение и отечность, увеличение содержания экссудата в полости сустава).
Обратимые местные реакции — кратковременное ограничение подвижности, чувство дискомфорта или тяжести в суставе. Проявление данных симптомов можно уменьшить прикладыванием льда к месту инъекции в течение 5-10 минут.
В единичных случаях отмечалось развитие аллергических реакций (зуд, сыпь, крапивница) и анафилактических реакций, септического артрита, внутритканевых кровоизлияний или кровоизлияний в полость сустава, тендинитов, флебитов, парестезий, головокружений, головных болей, мышечных спазмов, чувства жара, общего недомогания, периферических отеков при внутрисуставном введении растворов гиалуроновой кислоты.
При появлении местных или общих симптомов следует проконсультироваться с врачом.
Противопоказания
- повышенная чувствительность к гиалуронату натрия;
- перенесенные или текущие инфекционные или кожные заболевания в области участка, на котором предполагается проведение инъекции.
Применение при беременности и в период лактации
При беременности имплантат применяют только в том случае, если ожидаемый положительный терапевтический эффект превосходит негативное влияние побочных эффектов.
В период лечения кормящим женщинам необходимо прервать грудное вскармливание.
Особые указания
Медицинское изделие предназначено для внутрисуставного введения. Необходимо избегать введения имплантата в кровеносные сосуды и окружающие ткани.
По причине того, что септический артрит является серьезным побочным эффектом, необходимо соблюдать все стандартные меры предосторожности для хирургических вмешательств.
При получении аспирационной жидкости перед проведением вязкоэластичного протезирования следует провести соответствующие исследования для исключения бактериальной этиологии артрита.
Применять с осторожностью у пациентов с аллергией, а также у пациентов с заболеваниями печени.
В первые дни после инъекции может быть рекомендован пероральный прием анальгетиков или противовоспалительных лекарственных средств.
Продукт предназначен только для одноразового применения. Проходит финишную стерилизацию автоклавированием. Повторная стерилизация и применение изделия запрещены по причине наличия риска возникновения инфекции, перекрестной инфекции и/или дефекта изделия. Не использовать шприц из открытой и/или поврежденной стерильной упаковки. Не использовать шприц с открытым или поврежденным колпачком стерильного шприца. При нарушении стерильности или подозрении о нарушении стерильности имплантата изделие должно быть утилизировано.
Пожилые пациенты
У пациентов пожилого возраста применять с осторожностью ввиду общего снижения функциональной активности органов и систем организма.
Использование в педиатрии
Безопасность применения имплантата у детей изучена недостаточно, поэтому применять с осторожностью.
Извлечение имплантата
В случае выраженных проявлений может быть рекомендовано удаление имплантата из полости сустава, в т.ч. с применением лаважа, согласно действующим клиническим рекомендациям. Запрещаются повторные инъекции имплантатов синовиальной жидкости в сустав до купирования симптомов острого воспаления.
Защита окружающей среды и утилизация
Содержание шприца не является токсичным или огнеопасным. Изделия при использовании, транспортировке и хранении не оказывают негативного воздействия на окружающую среду.
Неиспользованные шприцы могут быть утилизированы в качестве бытовых отходов. Стекло следует утилизировать с осторожностью.
Неиспользованное содержимое шприца до или после истечения срока годности может быть утилизировано в качестве бытовых отходов (слить с большим количеством воды).
Уничтожение использованных медицинских изделий осуществляется в соответствии с природоохранными требованиями национальных, местных и ведомственных руководящих положений о безопасном уничтожении и утилизации.
В соответствии с санитарно-эпидемиологическими правилами и нормативами СанПиН 2.1.7.2790-10 использованные медицинские изделия (шприцы с имплантатами) относятся к медицинским отходам класса Б (эпидемиологически опасные отходы).
Условия хранения продукта Флексотрон® Форте
Продукт следует хранить и транспортировать в оригинальной упаковке, при температуре от 2°С до 30°С. Беречь от воздействия прямых солнечных лучей. Не замораживать.
Срок годности продукта Флексотрон® Форте
Срок годности — 3 года. Не применять после истечения срока годности, указанного на упаковке.
Способ применения и дозировка
Инъекции выполняются медицинскими специалистами в асептических условиях.
Перед введением имплантата содержимое шприца должно быть визуально оценено на прозрачность и однородность. Помутнение, кристаллизация, появление окраски и/или инородных включений может свидетельствовать о нарушении правил транспортировки и хранения изделия. При появлении вышеуказанных признаков введение средства для замещения синовиальной жидкости запрещено.
Имплантат вводится внутрисуставно в асептических условиях процедурных и манипуляционных кабинетов.
Перед проведением инъекции необходимо удалить покрывающую мембрану и извлечь наполненный шприц с имплантатом из блистера.
Вручную прикрепить адаптер для пальцев к упору цилиндра шприца.
Придерживая люэровский наконечник, аккуратно открутить колпачок наконечника шприца. Избегать чрезмерных нагрузок на шприц при фиксации иглы для предотвращения деформации механизма Луер-Лок.
Продолжая крепко удерживать люэровский наконечник, прикрутить стерильную иглу рекомендуемым размером 21G или 23G (не входят в комплект поставки) к защелке шприца до тех пор, пока она не будет закреплена. Длина иглы выбираться врачом в соответствии с конституцией человека и толщиной подкожной клетчатки в месте пункции. Перед инъекцией выпустить из шприца пузырьки воздуха в случае их наличия.
Вводить медленно. Пациент должен избегать любых физических нагрузок или весовых нагрузок в течение 48 часов после внутрисуставной инъекции.
На курс лечения рекомендуется 3-5 шприцев. Для лечения остеоартрита / остеоартроза (OA) суставов у взрослых проводят 1 инъекцию в неделю. Количество и частота инъекций могут изменяться в зависимости от тяжести симптоматики.
Описание
Имплантат для замещения синовиальной жидкости ФЛЕКСОТРОН Форте поставляется в стеклянном шприце и содержит гиалуроновую кислоту. Продукт представляет собой бесцветный, прозрачный, вязкоупругий и стерильный раствор. Гиалуроновая кислота (молекулярная масса 650000-1200000 Да) является продуктом бактериальной ферментации. Изделие предназначено только для одноразового применения.
Гиалуроновая кислота является естественным полисахаридом, который входит в состав всех тканей организма, при этом в особенно большой концентрации гиалуроновая кислота содержится в коже, подкожных тканях, а также в соединительной ткани, такой как синовиальная жидкость. Гиалуроновая кислота принадлежит к небольшой группе веществ, одинаковых для всех живых организмов, поэтому она обладает высокой биосовместимостью.
В 1 мл продукта содержится 10 мг гиалуроната натрия, растворенного в физиологическом растворе.
Не подлежит техническому обслуживанию.
Комплект поставки
Одна единица продукции включает:
- заполненный стерильный шприц 3,0 мл в запаянном блистере;
- инструкцию пользователя;
- 3 имплантационных стикера.
Состав
содержится 10 мг гиалуроната натрия, растворенного в физиологическом растворе.
Гиалуронат натрия — 1%, солевой раствор фосфатного буфера, хлорид натрия, вода для инъекций.
Гиалуронат натрия (C14H20NNaO11)n — 1%.
Солевой раствор фосфатного буфера:
- Na2HPO4*12H2O — 0,06%;
- NaH2PO4*2H2O — 0,0048%;
- Хлорид натрия — 0,89%;
- Вода для инъекций — сколько требуется до 100% (3 мл).
Фармакотерапевтическая группа
Изделие медицинского назначения
Показания
Назначение
Вязкоэластичное протезирование синовиальной жидкости у пациентов с дегенеративно-дистрофическими и посттравматическими поражениями суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Показания к применению:
- остеоартрит / остеоартроз (ОА), посттравматические и другие дегенеративные изменения коленного, тазобедренного, плечевого и голеностопного суставов;
- восстановление свойств синовиальной жидкости при ортопедической хирургии суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Противопоказания
- Запрещается применять у пациентов, страдающих гиперчувствительностью к гиалуронату натрия.
- Запрещаются внутрисуставные инъекции в случаях перенесенных или текущих инфекционных или кожных заболеваний в области участка, на котором предполагается проведение инъекции.
Побочное действие
Применение внутрисуставных форм гиалуроновой кислоты при дегенеративно-дистрофических и посттравматических поражениях суставов является хорошо изученным методом с установленным профилем безопасности, применяющимся на протяжении нескольких десятилетий.
К основным побочным эффектам относятся боль, отек и скованность в суставе после инъекции.
В крайне редких случаях возможно проявление местных воспалительных симптомов (повышение температуры, покраснение и отечность, увеличение содержания экссудата в полости сустава).
После внутрисуставной инъекции могут возникать такие обратимые местные реакции, как кратковременное ограничение подвижности, чувство дискомфорта или тяжести в суставе. Проявление данных симптомов можно уменьшить прикладыванием льда к месту инъекции в течение 5-10 минут.
Имеются сообщения о единичных случаях аллергических реакций (например, зуд, сыпь, крапивница) и анафилактических реакций, септического артрита, внутритканевых кровоизлияниях или кровоизлияниях в полость сустава, тенденитах, флебитах, парестезиях, головокружениях, головных болях, мышечных спазмах, чувстве жара, общем недомогании, периферических отеков при внутрисуставном введении растворов гиалуроновой кислоты.
При появлении местных или общих симптомов следует проконсультироваться с врачом.
Извлечение имплантата
В случае выраженных проявлений может быть рекомендовано удаление имплантата из полости сустава, в том числе с применением лаважа согласно действующим клиническим рекомендациям. Запрещаются повторные инъекции имплантатов синовиальной жидкости в сустав до купирования симптомов острого воспаления!
Хранятся в холодильнике
Нет
Обращаем ваше внимание, что инструкция к товарам может меняться. Для уточнения актуальной информации обратитесь к оригинальной инструкции.
Самовывоз в Ростове-на-Дону
ВИТА
Ростов-на-Дону, пр-кт Ворошиловский, 89
АптекаПлюс
Ростов-на-Дону, пр-кт 40-летия Победы, 91
Низкие цены
Ростов-на-Дону, пр-кт Стачки, 207/14
Будь Здоров!
Ростов-на-Дону, пр-кт Стачки, 222
Планета Здоровья
Ростов-на-Дону, пр-кт Коммунистический, 32
Ригла
Ростов-на-Дону, ул. Пушкинская, 213
Аптеки в вашем городе 173 аптеки
Все сети аптек в вашем городе
Вокзальная ул, 21, Красногорск, МО
Донецкая ул, 10 к 1, Москва
Луганская ул, 5, Москва
Кропоткинский пер, 4с1, Москва
Вернадского пр, 105, Москва
Первомайская ул, 80, Москва
Ново-Солдатская ул, 1/1, Волоколамск, МО
Щербаковская ул, 7А, Москва
Октябрьская ул, 12/2, Королев, МО
Луговой пр-д, 11 c 1, Москва
Новая Жизнь ул, 1, Красноармейск, МО
Чкалова ул, 7, Красноармейск, МО
Сергиев Посад-6, 1А, Сергиево-Посадский р-н, МО (на въезде в Военный городок, на территории рынка)
Курыжова, 7, Южный мкр, Домодедово, МО
Семеновская пл, 7 к 17А, Москва
Вешняковская ул, 39А, Москва
Юшуньская малая. ул, 3, Москва
Рижское ш, 41А, Волоколамск, МО
Ласточкин пр-д, 16, Балашиха, МО
Маршала Жукова пр, 49, Москва
Остеоартрит (ОА) является весьма распространенным заболеванием во всем мире с предполагаемой распространенностью в 2019 году в 527,81 миллиона человек, что резко увеличилось на 113,25% по сравнению с 1990 годом [5]. Остеоартрит суставов кистей (ОА СК) оказался вторым по распространенности локализацией ОА после ОА коленных суставов, составляя примерно 23,7% от общего числа распространенных случаев ОА в 2019 году, и его распространенность увеличилась на 91,84% с 1990 по 2019 год [5].
ОА СК, наиболее распространенный периферический артрит в мире, он изучен в меньшей степени, чем ОА коленных и тазобедренных суставов. Тем не менее, процессы, происходящие при ОА в суставах кистей, являются уникальными для изучения патогенеза ОА в целом, устраняя влияние веса как фактора, влияющего на определенные звенья патогенеза. Несмотря на это, все больше доказательств указывает на ожирение как важный фактор риска развития ОА СК, а новые данные подтверждают роль лептина и жирных кислот сыворотки крови. Прогрессирование ОА СК и, в частности, эрозивного фенотипа ОА, может быть связано с диабетом. Новые данные подтверждают связь между сердечно-сосудистыми заболеваниями и симптоматическим ОА СК. Употребление алкоголя провоцирует усилением синовита и развитие эрозивного ОА СК. Таким образом, ОА СК — гетерогенное заболевание со многими модифицируемыми факторами риска, которые определяют тяжесть заболевания и могут решить спорные вопросы в патогенезе заболевания [6].
Проявления ОA СК разнообразны и включают в себя несколько вариантов это узловая форма (неэрозивная) OA, эрозивная форма ОА и ОА основания большого пальца — запястно пястного сустава (ОА ЗППС) [7, 8]. Эта неоднородность в проявлении и разнообразие возникающих симптомов и признаков делает OA СК очень сложным для изучения [9]. Действительно, его патогенетические механизмы все еще остаются неясными. Терапевтические возможности ограничены и направлены почти исключительно на лечение симптомов, в основном состоящих из местных и пероральных нестероидных противовоспалительных препаратов (НПВП), которые обладают лишь небольшим или скромным обезболивающим действием и рядом побочных эффектов [9,10,11]. Некоторые положительные, но предварительные результаты в улучшении боли и функциональности были получены в результате применения у неэрозивного и эрозивного ОА СК симптоматических препаратов замедленного действия при остеоартрите (SYSADOAs), такие как глюкозамина сульфат и хондроитина сульфат [12, 13, 14].
Традиционно считается, что ОА является заболеванием суставов с повреждением и потерей хряща, хотя в последние годы стало очевидно, что ОА является более сложным заболеванием, поражающим все ткани внутри сустава [15,16]. Кроме того, особенно при эрозивном ОА СК, была признана важность локального воспаления, и важная роль в патогенезе ОА приписывается дисбалансу цитокинов в пользу провоспалительных медиаторов, таких как фактор некроза опухоли (TNF-α), интерлейкин (IL)-1 и IL-6, которые запускают порочный круг, который приводит к активации катаболических ферментов и дезинтеграноподобной металлопротеиназы с тромбоспондиновым мотивом (ADAMTS) и, как конечный результат, к повреждению хряща [15,17]. По этим причинам в последние десятилетия были предприняты соответствующие усилия по поиску новых потенциальных терапевтических мишеней при ОА, и в настоящее время разрабатываются новые лекарственные препараты. Кроме того, ряд существующих традиционных и биологических модифицирующих заболевание противоревматических препаратов, включая гидроксихлорохин, метотрексат, ингибиторы TNF-α, IL-1 и IL-6, обычно используемых для лечения воспалительных артропатий, были апробированы для лечения ОА и исследованы также в терапии эрозивного ОА СК [11, 18]. Однако использование этих групп препаратов в лечении ОА СК не увенчалось успехом [19, 20, 21, 22, 23, 24, 25].
Ингибитор ТNF-α является хорошо известным провоспалительным цитокином, который играет важную роль в развитии и прогрессировании ОА. В частности, TNF-α ингибирует синтез компонентов протеогликанов и коллагена и усиливает деградацию компонентов внеклеточного матрикса индуцируя продукцию основных матриксных металлопротеиназ и аггреканаз и увеличивая высвобождение IL- 6 и ИЛ-8. Кроме того, он стимулирует синтез регулируемых при активации нормальных экспрессируемых и секретируемых Т-клеток и фактора роста эндотелия сосудов и индуцирует выработку индуцибельного оксида азота (iNOS), циклооксигенезы -2 (COX-2) и простагландин Е-2-синтазы [15]. Кроме того, TNF-α через высвобождение простагландина Е-2 приводит к экспрессии нейротрофинового фактора роста нервов NFG, который является одним из ключевых медиаторов боли при ОА. Таким образом, учитывая биологическую активность TNF-α, наряду с наличием признаков воспаления, таких как синовит в межфаланговых суставах пациентов с эрозивным ОА СК, была выдвинута гипотеза, что этот цитокин может быть мишенью для терапии с целью уменьшения боли и замедления прогрессирования заболевания [21]. Поэтому было предпринято несколько попыток лечения эрозивного OA СК ингибиторами TNF-α с часто ограниченными и неудовлетворительными результатами [26].
Поскольку в настоящее время отсутствует патогенетическая терапия ОА, методы лечения направлены на уменьшение боли и улучшение функциональных результатов. Распространенное нехирургичесое лечение ОА включает нестероидные противовоспалительные препараты (НПВП) и внутрисуставные инъекции глюкокортикостероидов (ГКС) [27]. Тем не менее внимание исследователей было обращено на внутрисуставное введение препаратов гиалуроновой кислоты (ГК), как приемлемый альтернативный метод лечение ОА в целом и ОАК СК в частности.
Гиалуроновая кислота (ГК) является частью синовиальной жидкости и здорового хряща. Было доказано, что реологические свойства и молекулярный состав ГК имеют важное значение для синовиальной жидкости, которая играет ключевую роль в амортизации суставов. Кроме этого, ГК – важный регулятор иммунных и анаболических процессов (взаимодействует с рецепторами хондроцитов, фибробластов и макрофагальных клеток) [28] подавляет выработку макрофагами простагландина Е2 посредством подавления NF-kappa B [29]. Также было продемонстрировано снижение экспрессии и выработки матриксных металлопротеиназ, протеаз, участвующих в деградации матриксных белков, которые способствуют целостности сустава, в присутствии ГК [30, 31, 32].
Еще в 2006 г Fuchs S. с соавторами при сравнении внутрисуставного введения ГКС и внутрисуставного введения ГК при ОА ЗППС было продемонстрировано, что действие ГК по сравнению с триамцинолоном достигается медленнее, но результаты указывают на превосходный длительный эффект гиалуроновой кислоты через 6 месяцев после окончания периода лечения [33]. Эти обнадеживающие данные подтверждены 6-месячным ретроспективным сравнительным исследованием у пациентов с эрозивным и неэрозивной формой ОАСК, в котором оценивалась эффективность препарата ГК против ацетонида триамцинолона у 100 пациентов [34]. Так же авторы исследования продемонстрировали, что гиалуроновая кислота подтвердила высокую эффективность в снижении боли и улучшение функции у пациентов с более тяжелыми симптомами в долгосрочной перспективе.
В исследовании Heyworth B.E. с соавт. оценивалась эффективность внутрисуставной терапия ОА ЗППС, где в 3-х группах, получающий ГК, плацебо и ГКС внутрисуставно было продемонстрировано, что в группах стероидов и плацебо на 4-й неделе боли были значительно меньше по сравнению с исходным уровнем, но этот эффект исчез к 12-й неделе. Только инъекции ГК продолжали обеспечивать облегчение боли через 12 и 26 недель по сравнению с исходным уровнем [35].
В рандомизированном исследовании было проведено сравнение внутрисуставного введения ГК с плацебо. Авторы продемонстрировали, что несмотря на краткосрочный анальгетический эффект плацебо, на 24-й неделе в группе, принимавшей ГК, были обнаружены статистически значимые улучшения функции (p = 0,001) и боли в ВАШ (p = 0,002) [36].
Abdelsabor Sabaah HM с соавт. провели исследование, чтобы сравнить эффективность обогащенной тромбоцитами плазмы (PRP) с инъекциями гиалуроновой кислоты (ГК) и кортикостероидами при остеоартрите запястно-пястного сустава на основе клинических и функциональных показателей результата. Результаты исследования продемонстрировали, что все три типа инъекций (PRP, ГК, стероиды) дали хорошие результаты при ОА основания большого пальца в отношении улучшения боли и функции кисти, но только ГК имела длительный эффект и наилучшие результаты при боли и функции [37].
Для разрешения разногласий по поводу внутрисуставного введения ГК, была создана Европейская консенсусная группа по внутрисуставному введению ГК (EUROVISCO), которая опубликовала подробные рекомендации по внутрисуставной терапии ее показаниях и противопоказаниях при ОА [38]. Так же была назначена многонациональная, междисциплинарная техническая экспертная группа (TEГ), для выявления предикторов эффективности внутрисуставного введения ГК и для определения критериев ее успешности [39]. Международная ТЭГ согласовала показания для внутрисуставного введение препаратов ГК, касающиеся конкретных локализаций [40]. Относительно ОА СК ТЕГ пришла к выводу, что показанием для терапии является ОА СК I-II-III степеней по Келлгрлен-Лоуренсу, а одним из противопоказанием к терапии ГК является IV степень, и в отдельных случаях: пациенты в возрасте от 50 до 75 лет с выраженными клиническими проявлениями, продолжительностью боли более трех месяцев, определяемыми как общая оценка боли в руке более 30 мм по шкале 0-100 ВАШ и функциональный индекс ОА кисти (FIHOA) >6 баллов [38,39].
Боль в плече является самой распространенной жалобой и занимает 2-ое место среди причин обращения за первичной медицинской помощью среди всех пациентов со скелетно-мышечными заболеваниями. Возраст пациента подчас является фактором, определяющим спектр патологии – травма вращательной манжеты плеча чаще наблюдается у молодых людей, тогда как адгезивный капсулит, остеоартрит аркомиально-ключичного сустава распространены в среднем и пожилом возрасте [41]
Тендинопатии становятся все более распространенной патологией, негативно влияющей на качество жизни пациентов. На сегодняшний день в патофизиологическом процессе тендинопатий идентифицировано множество механизмов. Ряд внутренних и внешних факторов риска могут способствовать их патогенезу, включая механическую перегрузку, возраст, пол, а также генетические, эндокринные и метаболические нарушения [42,43]. Воспаленные сухожилия демонстрируют разнообразие структурных изменений: повышенный апоптоз теноцитов, разрушение коллагеновых волокон со снижением выработки коллагена I типа, увеличение выработки коллагена III типа и неэффективный неоангиогенез [44]. Пациенты предъявляют жалобы на боль в области сустава, которая усиливается при активных физических нагрузках и в повседневной жизни. Другими клиническими признаками являются локальная болезненность при пальпации, ограничение объема движений и умеренный отек.
Высокая нагрузка и микротравматизация связочного аппарата суставов способны вызывать ремоделирование матрицы сухожилия посредством механизма, который включает деградацию коллагена, фагоцитоз фрагментов, полученных теноцитами, и последующий компенсаторный фибриллогенез, который восстанавливает целостность структуры сухожилия. В исследованиях было доказано, что повторные микротравмы способны ослабить структуру сухожилия в долгосрочной перспективе [45], а отсутствие нагрузки на сухожилия приводит к патологическим изменениям структуры коллагена, сходным с таковыми при чрезмерном использовании [46]. Chisari E. и соавторами было подчеркнуто, что длительное состояние низкоуровнего воспаления, обычно встречающееся при хронической тендинопатии, может рассматриваться как фактор риска «неудачной реакции заживления» после острого повреждения сухожилия [47]. В обоих случаях сухожилие теряет свою функциональную и структурную целостность с разрушением волокон и снижением устойчивости к механическому воздействию.
В лечении патологии плечевого сустава, ассоциированной с повреждением связочного аппарата, используются консервативные и хирургические методы. За последнее десятилетие было опубликовано несколько систематических обзоров, где сравнивалась эффективность лечения по ряду критериев, включая боль, объем движений, функциональные ограничения и трудоспособность. Пероральные нестероидные противовоспалительные препараты могут быть эффективны в краткосрочной перспективе людям с острым тендинитом/субакромиальным бурситом [48]. Однако большинство авторов не рекомендуют изолированный прием подобных препаратов при указанных состояниях. Инъекции глюкокортикоидов (ГКС) в субакромиальное пространство и физиотерапевтические методы, часто в комплексе, составляют основу консервативного лечения патологии ротаторной манжеты. Но в исследовании, где оценивалось сочетание внутрисуставное введение ГКС с курсом физиотерапии было продемонстрировано, что 30% пациентов после окончания курса терапии продолжали испытывать боль в плече [49].
В последние годы все активнее осуждается возможность применения ГК в терапии связочного аппарата, но до сих пор нет единого мнения о золотом стандарте лечения. Однако применение ГК может вызывать несколько модифицирующих заболевание эффектов, приводя к усилению регенерации теноцитов, восстановлению соотношения коллагена I / III типа, снижению апоптоза и ангиогенетическим изменениям [50, 51].
Первое экспериментальное наблюдение за воздействием ГК на биомеханику и восстановление сухожилий относится к 1980 году и было проведено на обезьянах. St Onge с соавторами продемонстрировали улучшение объема движений обработанного ГК сухожилия, что указывает на возможную ее роль в первичном восстановлении сухожилия [52]. С тех пор эффект применения ГК оценивался на многочисленных моделях животных, от грызунов до приматов, как in vitro, так и in vivo. ГК оказывала благоприятное воздействие как на место репарации, так и на синовиальную оболочку, уменьшая периферическую воспалительную реакцию и способствуя заживлению повреждения за счет вовлечения эпитеноновых и эндотеноновых клеток в процесс репарации.
Еще в 1985 году была продемонстрирована преимущество введения ГК 1% и 0,5% над триамцинолоном, а и также ее эффективность в предотвращении спаечного процесса и быстрому заживлению сухожилий [53]. Некоторые клинические исследования выявили благоприятное влияние ГК на вязкоупругость сухожилий [54]. Сообщалось о превосходстве инъекций ГК над другими консервативными методами лечения [55]. В нескольких исследованиях изучалась связь между ингибированием фибробластической пролиферации, индуцированной ГК, стабилизацией коллагена II типа и снижением концентрации коллагена III типа в сухожилии [56,57]. В настоящее время способность ГК стимулировать новый непрямой синтез коллагена I типа все еще обсуждается, в то время как ее способность повышать жизнеспособность и пролиферацию клеток доказана [58]. Кроме того, ГК, по-видимому, дозозависимым образом ингибирует экспрессию промежуточных факторов, которые играют ключевую роль в воспалительных путях (NF-κB). Это противовоспалительное действие дополняется способностью экзогенной ГК уменьшать фрагментацию эндогенной ГК, стимулируя синтез новой [59]. Что касается терапевтического протокола, кратность введения препарата в настоящий момент обсуждается [60].
Литература 1. Kolasinski SL, Neogi T, Hochberg MC, Oatis C, Guyatt G et. al 2019 American College of Rheumatology/Arthritis Foundation Guideline for the Management of Osteoarthritis of the Hand, Hip, and Knee. Arthritis Care Res (Hoboken). 2020 Feb;72(2):149-162. doi: 10.1002/acr.24131.
2. Burbank K, Stevenson J, Czarneck G, Dorfman J. Chronic Shoulder Pain: Part I.Evaluation and Diagnosis. Am Fam Physician. 2008; 77 (4): 453–600
3. Meislin RJ, Sperling JW, Stitik TP.
Persistent shoulder pain: epidemiology, pathophysiology, and diagnosis. AmJOrthop (Belle Mead NJ).Dec;2005;34(12Suppl):5–9. Burbank K, Stevenson J, Czarneck G,
Dorfman J. Chronic Shoulder Pain: Part I.
Evaluation and Diagnosis. Am Fam Physician.
2008;77(4):453–60
4. Shiri R, Viikari-Juntura E, Varonen H,Heliö vaara M. Prevalence and determinant soflateral and medialepicondylitis: apopulation study. Am J Epidemiol. 2006 Dec 1;164(11):1065–74.
5. Long H, Liu Q, Yin H, Wang K, Diao N, Zhang Y, Lin J, Guo A. Prevalence Trends of Site-Specific Osteoarthritis From 1990 to 2019: Findings From the Global Burden of Disease Study 2019. Arthritis Rheumatol. 2022 Jul;74(7):1172-1183. doi: 10.1002/art.42089.
6. Plotz B, Bomfim F, Sohail MA, Samuels J. Current Epidemiology and Risk Factors for the Development of Hand Osteoarthritis. Curr Rheumatol Rep. 2021 Jul 3;23(8):61. doi: 10.1007/s11926-021-01025-7
7. Marshall M, Watt FE, Vincent TL, Dziedzic K. Hand osteoarthritis: clinical phenotypes, molecular mechanisms and disease management. Nat Rev Rheumatol. 2018 Nov;14(11):641-656. doi: 10.1038/s41584-018-0095-4.
8. Favero M, Belluzzi E, Ortolan A, Lorenzin M, Oliviero F, Doria A, Scanzello CR, Ramonda R. Erosive hand osteoarthritis: latest findings and outlook. Nat Rev Rheumatol. 2022 Mar;18(3):171-183. doi: 10.1038/s41584-021-00747-3.
9. Fuggle N, Bere N, Bruyère O, Rosa MM, Prieto Yerro MC, et al Management of hand osteoarthritis: from an US evidence-based medicine guideline to a European patient-centric approach. Aging Clin Exp Res. 2022 Sep;34(9):1985-1995. doi: 10.1007/s40520-022-02176-y.
10. Kloppenburg M, Kroon FP, Blanco FJ, Doherty M, Dziedzic KS, Greibrokk E, Haugen IK, Herrero-Beaumont G, Jonsson H, Kjeken I, Maheu E, Ramonda R, Ritt MJ, Smeets W, Smolen JS, Stamm TA, Szekanecz Z, Wittoek R, Carmona L. 2018 update of the EULAR recommendations for the management of hand osteoarthritis. Ann Rheum Dis. 2019 Jan;78(1):16-24. doi: 10.1136/annrheumdis-2018-213826.
11. Ghouri A, Quicke JG, Conaghan PG. New developments in osteoarthritis pharmacological therapies. Rheumatology (Oxford). 2021 Dec 24;60(Suppl 6):vi1-vi11. doi: 10.1093/rheumatology/keab679.
12. Veronese N, Smith L, Bolzetta F, Cester A, Demurtas J, Punzi L. Efficacy of conservative treatments for hand osteoarthritis : An umbrella review of interventional studies. Wien Klin Wochenschr. 2021 Mar;133(5-6):234-240. doi: 10.1007/s00508-020-01702-0.
13. Tenti S, Giordano N, Mondanelli N, Giannotti S, Maheu E, Fioravanti A. A retrospective observational study of glucosamine sulfate in addition to conventional therapy in hand osteoarthritis patients compared to conventional treatment alone. Aging Clin Exp Res. 2020 Jun;32(6):1161-1172. doi: 10.1007/s40520-019-01305-4.
14. Tenti S, Veronese N, Cheleschi S, Seccafico I, Bruyère O, Reginster JY, Fioravanti A. Prescription-grade crystalline glucosamine sulfate as an add-on therapy to conventional treatments in erosive osteoarthritis of the hand: results from a 6-month observational retrospective study. Aging Clin Exp Res. 2022 Jul;34(7):1613-1625. doi: 10.1007/s40520-022-02151-7.
15. Molnar V, Matišić V, Kodvanj I, Bjelica R, Jeleč Ž, et al. Cytokines and Chemokines Involved in Osteoarthritis Pathogenesis. Int J Mol Sci. 2021 Aug 26;22(17):9208. doi: 10.3390/ijms22179208
16. Fioravanti A, Tenti S, Cheleschi S. Editorial: Year 2020: New Trends in Pharmacological Treatments for Osteoarthritis. Front Pharmacol. 2022 May 3;13:892934. doi: 10.3389/fphar.2022.892934.
17. Fioravanti A, Tenti S, McAllister M, Chemaly M, Eakin A, et al Exploring the Involvement of NLRP3 and IL-1β in Osteoarthritis of the Hand: Results from a Pilot Study. Mediators Inflamm. 2019 Mar 10;2019:2363460. doi: 10.1155/2019/2363460.
18. Oo WM, Little C, Duong V, Hunter DJ. The Development of Disease-Modifying Therapies for Osteoarthritis (DMOADs): The Evidence to Date. Drug Des Devel Ther. 2021 Jul 6;15:2921-2945. doi: 10.2147/DDDT.S295224.
19. Kingsbury SR, Tharmanathan P, Keding A, et al. Hydroxychloroquine effectiveness in reducing symptoms of hand osteoarthritis: a randomized trial. Ann Intern Med. 2018 Mar 20;168(6):385-395. doi: 10.7326/M17-1430.
20. Chevalier X, Ravaud P, Maheu E, et al. Adalimumab in patients with hand osteoarthritis refractory to analgesics and NSAIDs: a randomised, multicentre, doubleblind, placebo- controlled trial. Ann Rheum Dis. 2015 Sep;74(9):1697-705. doi: 10.1136/annrheumdis-2014-205348
21. Aitken D, Laslett LL, Pan F, et al. A randomised double-blind placebo-controlled crossover trial of HUMira (adalimumab) for erosive hand OsteoaRthritis- the HUMOR trial. Osteoarthritis Cartilage. 2018 Jul;26(7): 880-887. doi: 10.1016/j.joca.2018.02.899
22. Kloppenburg M. A phase 2a, placebocontrolled, randomized study of ABT-981, an anti-interleukin-1α and -1β dual variable domain immuno globulin, to treat erosive hand osteoarthritis (EHOA) [abstract OP0168]. Ann Rheum Dis. 2017;76(Suppl. 2): 122 doi: 10.1136/annrheumdis-2018-213336
23. Kedor C, Detert J, Rau R, Wassenberg S, Listing J, et all. Hydroxychloroquine in patients with inflammatory and erosive osteoarthritis of the hands: results of the OA-TREAT study-a randomised, double-blind, placebo-controlled, multicentre, investigator-initiated trial. RMD Open. 2021 Jul;7(2):e001660. doi: 10.1136/rmdopen-2021-001660.
24. Singh A, Kotlo A, Wang Z, Dissanayaka T, Das S, Antony B. Efficacy and safety of hydroxychloroquine in osteoarthritis: a systematic review and meta-analysis of randomized controlled trials. Korean J Intern Med. 2022 Jan;37(1):210-221. doi: 10.3904/kjim.2020.605.
25. Ferrero S, Wittoek R, Allado E, Cruzel C, Fontas E, et all. Methotrexate treatment in hand osteoarthritis refractory to usual treatments: A randomised, double-blind, placebo-controlled trial. Semin Arthritis Rheum. 2021 Aug;51(4):831-838. doi: 10.1016/j.semarthrit.2021.04.016.
26. Cho Y, Jeong S, Kim H, Kang D, Lee J, et all Disease-modifying therapeutic strategies in osteoarthritis: current status and future directions. Exp Mol Med. 2021 Nov;53(11):1689-1696. doi: 10.1038/s12276-021-00710-y.
27. Cooper MS. Glucocorticoids in bone and joint disease: the good, the bad and the uncertain. Clin Med (Lond). 2012 Jun;12(3):261-5. doi: 10.7861/clinmedicine.12-3-261..
28. Altman RD, Manjoo A, Fierlinger A, et al. The mechanism of action for hyaluronic acid treatment in the osteoarthritic knee: a systematic review. BMC Musculoskelet Disord. 2015 Oct 26;16:321. doi: 10.1186/s12891-015-0775-z
29. Yasuda T. Hyaluronan inhibits prostaglandin E2 production via CD44 in U937 human macrophages. Tohoku J Exp Med. 2010;220(3):229-235. doi:10.1620/tjem.220.229
30. Sasaki A, Sasaki K, Konttinen YT, et al. Hyaluronate inhibits the interleukin-1beta-induced expression of matrix metalloproteinase (MMP)-1 and MMP-3 in human synovial cells. Tohoku J Exp Med. 2004;204(2):99-107. doi:10.1620/tjem.204.99]
31. Bruyere O., Honvo G., Veronese N. et al. An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO). Semin Arthritis Rheum. 2019; 49(3): 337-50. DOI: 10.1016/j.semarthrit.2019.04.008
32. Riley N., Vella-Baldacchino M., Thurley N., Hopewell S., Carr A. J., Dean B. J. F. (2019). Injection therapy for base of thumb osteoarthritis: a systematic review and meta-analysis. BMJ Open 9, e027507. doi: 10.1136/bmjopen-2018-027507
33. Fuchs S, Mönikes R, Wohlmeiner A, Heyse T. Intra-articular hyaluronic acid compared with corticoid injections for the treatment of rhizarthrosis. Osteoarthritis Cartilage. 2006 Jan;14(1):82-8. doi: 10.1016/j.joca.2005.07.016.
34. Monfort J., Rotés-Sala D., Segalés N., Montañes F. J., Orellana C., Llorente-Onaindia J., et al. (2015). Comparative efficacy of intra-articular hyaluronic acid and corticoid injections in osteoarthritis of the first carpometacarpal joint: results of a 6-month single-masked randomized study. Jt. Bone Spine 82, 116–121. doi:10.1016/j.jbspin.2014.08.008.
35. Heyworth BE, Lee JH, Kim PD, Lipton CB, Strauch RJ, Rosenwasser MP. Hylan versus corticosteroid versus placebo for treatment of basal joint arthritis: a prospective, randomized, double-blinded clinical trial. J Hand Surg Am. 2008 Jan;33(1):40-8. doi: 10.1016/j.jhsa.2007..
36. Figen Ayhan F, Ustün N. The evaluation of efficacy and tolerability of Hylan G-F 20 in bilateral thumb base osteoarthritis: 6 months follow-up. Clin Rheumatol. 2009 May;28(5):535-41. doi: 10.1007/s10067-008-1080-0
37. Abdelsabor Sabaah HM, El Fattah RA, Al Zifzaf D, Saad H. A Comparative Study for Different Types of Thumb Base Osteoarthritis Injections: A Randomized Controlled Interventional Study. Ortop Traumatol Rehabil. 2020 Dec 31;22(6):447-454. doi: 10.5604/01.3001.0014.6055.
38. Conrozier T, Monfort J, Chevalier X, et al. EUROVISCO Recommendations for Optimizing the Clinical Results of Viscosupplementation in Osteoarthritis. Cartilage. 2020;11(1):47–59. doi: 10.1177/1947603518783455
39. Migliore A, Gigliucci G, Alekseeva L, Bannuru RR, Blicharski T, et all. Systematic Literature Review and Expert Opinion for the Use of Viscosupplementation with Hyaluronic Acid in Different Localizations of Osteoarthritis. Orthop Res Rev. 2021 Dec 2;13:255-273. doi: 10.2147/ORR.S336185
40. Филатова Ю.С., Соловьев И.Н., Гиалуроновая кислота в лечении остеоартрита различных локализаций. Обзор литературы Терапевтический архив. – 2022. – Т. 94. – № 8. – С. 1014-1019. – doi: 10.26442/00403660.2022.08.201790..
41. Шостак Н. А., Правдюк Н.Г., Тимофеев В. Т. и др. Патология плечевого сустава и мягких тканей – клинические варианты, современные возможности патогенетической терапии. Клиницист 2021;15(1–4)–К652. DOI: 10.17650/1818 8338 2021 15 1 4 К652.
42. Frizziero A., Salamanna F., Della Bella E., Vittadini F., Gasparre G., Nicoli Aldini N., Masiero S., Fini M. The Role of Detraining in Tendon Mechanobiology. Front. Aging Neurosci. 2016;8:43. doi: 10.3389/fnagi.2016.00043.,
43. Oliva F., Piccirilli E., Berardi A.C., Frizziero A., Tarantino U., Maffulli N. Hormones and tendinopathies: The current evidence. Br. Med. Bull. 2016;117:39–58. doi: 10.1093/bmb/ldv054.
44. Del Buono A., Battery L., Denaro V., Maccauro G., Maffulli N. Tendinopathy and inflammation: Some truths. Int. J. Immunopathol. Pharm. 2011;24:45–50. doi: 10.1177/03946320110241S209.,
45. Tallon C., Maffulli N., Ewen S.W. Ruptured Achilles tendons are significantly more degenerated than tendinopathic tendons. Med. Sci. Sports Exerc. 2001;33:1983–1990. doi: 10.1097/00005768-200112000-00002
46. Maganaris C.N., Narici M.V., Almekinders L.C., Maffulli N. Biomechanics and pathophysiology of overuse tendon injuries: Ideas on insertional tendinopathy. Sports Med. 2004;34:1005–1017. doi: 10.2165/00007256-200434140-00005
47. Chisari E., Rehak L., Khan W.S., Maffulli N. Tendon healing in presence of chronic low-level inflammation: A systematic review. Br. Med. Bull. 2019;132:97–116. doi: 10.1093/bmb/ldz035.
48. Kulkarni R., Gibson J., Brownson P. et al. Subacromial shoulder pain. Shoulder Elbow 2015;7(2):135–43. doi:: 10.1177/1758573215576456.
49. Cummins C.A., Sasso L.M., Nicholson D. Impingement syndrome: temporal outcomes of nonoperative treatment. J Shoulder Elbow Surg 2009;18(2):172–7. doi:: 10.1016/j. jse.2008.09.00]
50. Ciardulli M.C., Marino L., Lovecchio J., Giordano E., Forsyth N.R., et all. Tendon and Cytokine Marker Expression by Human Bone Marrow Mesenchymal Stem Cells in a Hyaluronate/Poly-Lactic-Co-Glycolic Acid (PLGA)/Fibrin Three-Dimensional (3D) Scaffold. Cells. 2020;9:1268. doi: 10.3390/cells9051268,
51. Esenyel C.Z., Tekin C., Cakar M., Bayraktar K., Saygili S., et al. Surgical treatment of the neglected achilles tendon rupture with Hyalonect. J. Am. Podiatr. Med. Assoc. 2014;104:434–443. doi: 10.7547/0003-0538-104.5.434.
52. St Onge R, Weiss C, Denlinger JL, Balazs EA. A preliminary assessment of Na-hyaluronate injection into «no man’s land» for primary flexor tendon repair. Clin Orthop Relat Res. 1980 Jan-Feb;(146):269-75.
53. Yuzawa K. [Experimental studies on the healing and restoration of gliding function of the injured digital flexor tendon. Part 9: The use of drugs to prevent adhesion formation of the injured tendon]. Nihon Seikeigeka Gakkai Zasshi. 1985 Dec;59(12):1107-18.
54. Nakamura H., Gotoh M., Kanazawa T., Ohta K., Nakamura K., et al. Effects of corticosteroids and hyaluronic acid on torn rotator cuff tendons in vitro and in rats. J. Orthop. Res. 2015;33:1523–1530. doi: 10.1002/jor.22921.
55. Frizziero A., Vittadini F., Barazzuol M., Gasparre G., Finotti P., et al. Extracorporeal shockwaves therapy versus hyaluronic acid injection for the treatment of painful non-calcific rotator cuff tendinopathies: Preliminary results. J. Sports Med. Phys. Fit. 2017;57:1162–1168. doi: 10.23736/S0022-4707.16.06408-2.
56. Wiig M., Abrahamsson S.O., Lundborg G. Effects of hyaluronan on cell proliferation and collagen synthesis: A study of rabbit flexor tendons in vitro. J. Hand Surg. Am. 1996;21:599–604. doi: 10.1016/S0363-5023(96)80010-4.
57. Dean B.J., Franklin S.L., Carr A.J. A systematic review of the histological and molecular changes in rotator cuff disease. Bone Jt. Res. 2012;1:158–166. doi: 10.1302/2046-3758.17.2000115.
58. Osti L., Berardocco M., di Giacomo V., Di Bernardo G., Oliva F., Berardi A.C. Hyaluronic acid increases tendon derived cell viability and collagen type I expression in vitro: Comparative study of four different Hyaluronic acid preparations by molecular weight. BMC Musculoskelet. Disord. 2015;16:284. doi: 10.1186/s12891-015-0735-7.
59. Ozgenel G.Y., Etoz A. Effects of repetitive injections of hyaluronic acid on peritendinous adhesions after flexor tendon repair: A preliminary randomized, placebo-controlled clinical trial. Ulus Travma Acil. Cerrahi Derg. 2012;18:11–17. doi: 10.5505/tjtes.2012.95530.
60. Kaux J.F., Samson A., Crielaard J.M. Hyaluronic acid and tendon lesions. Muscles Ligaments Tendons J. 2015;5:264–269. doi: 10.32098/mltj.04.2015.02, Tallon C., Maffulli N., Ewen S.W. Ruptured Achilles tendons are significantly more degenerated than tendinopathic tendons. Med. Sci. Sports Exerc. 2001;33:1983–1990. doi: 10.1097/00005768-200112000-00002
61. Yamamoto A., Takagishi K., Osawa T., Yanagawa T., Nakajima D., Shitara H., Kobayashi T. Prevalence and risk factors of a rotator cuff tear in the general population. J. Shoulder. Elb. Surg. 2010;19:116–120. doi: 10.1016/j.jse.2009.04.006.
62. Meloni F., Milia F., Cavazzuti M., Doria C., Lisai P., Profili S., Meloni G.B. Clinical evaluation of sodium hyaluronate in the treatment of patients with sopraspinatus tendinosis under echographic guide: Experimental study of periarticular injections. Eur. J. Radiol. 2008;68:170–173. doi: 10.1016/j.ejrad.2007.11.001
63. Flores C., Balius R., Alvarez G., Buil M.A., Varela L., Cano C., Casariego J. Efficacy and Tolerability of Peritendinous Hyaluronic Acid in Patients with Supraspinatus Tendinopathy: A Multicenter, Randomized, Controlled Trial. Sports Med. Open. 2017;3:22. doi: 10.1186/s40798-017-0089-9.
64. Petrella R.J., Cogliano A., Decaria J., Mohamed N., Lee R. Management of Tennis Elbow with sodium hyaluronate periarticular injections. Sports Med. Arthrosc. Rehabil. Ther. Technol. 2010;2:4. doi: 10.1186/1758-2555-2-4
65. Khan I.U., Awan A.S., Khan A.S., Marwat I., Meraj M. Efficacy Of A Single-Injection Sodium Hyaluronate Treatment In Lateral Epicondylitis. J. Ayub Med. Coll. Abbottabad. 2018;30:85–89.
66. Tosun H.B., Gumustas S., Agir I., Uludag A., Serbest S., Pepele D., Ertem K. Comparison of the effects of sodium hyaluronate-chondroitin sulphate and corticosteroid in the treatment of lateral epicondylitis: A prospective randomized trial. J. Orthop. Sci. 2015;20:837–843. doi: 10.1007/s00776-015-0747-z.].
67. Precerutti M, Formica M, Bonardi M, Peroni C, Calciati F. Acromioclavicular osteoarthritis and shoulder pain: a review of the role of ultrasonography. J Ultrasound. 2020 Sep;23(3):317-325. doi: 10.1007/s40477-020-00498-z.
68. Zhang B, Thayaparan A, Horner N, Bedi A, Alolabi B, Khan M. Outcomes of hyaluronic acid injections for glenohumeral osteoarthritis: a systematic review and meta-analysis. J Shoulder Elbow Surg. 2019 Mar;28(3):596-606. doi: 10.1016/j.jse.2018.09.011
69. Беляева И.Б. Современная концепция локальной инъекционной терапии остеоартрита и заболеваний околосуставных мягких тканей: фокус на препараты гиалуроновой кислоты (Флексотрон Форте). Эффективная фармакотерапия. 2022; 18 (10) doi: 10.33978/2307-3586-2022-18-10.
70. Беляева ЕА, Фатенко А.С, Авдеева ОС, Беляева СВ. Сравнительная эффективность внутрисуставного введения препаратов гиалуроновой кислоты с различными физико-химическими свойствами при остеоартрите коленного сустава. Современная ревматология. 2021;15(6):48–54. doi: 10.14412/1996-7012-2021-6-48-54
71. Попов, В. П. Оптимальное использование препаратов гиалуроновой кислоты при суставной патологии / В. П. Попов, С. А. Корощенко, М. А. Ларин // РМЖ. Медицинское обозрение. – 2017. – Т. 1, № 1. – С. 12
72. Призов АП, Загородний НВ, Лазко ФЛ, Никитин АА, Беляк ЕА, Лазко МФ, Каменчук ЯА, Ильина ЕА. Сравнение реологических и вязкоупругих свойств медицинских изделий гиалуроновой кислоты для внутрисуставного введения. Современная ревматология. 2023;17(2):50–56. doi: 10.14412/1996-7012-2023-2-50-56
Клинико-фармакологическая группа
Медицинское изделие для лечения заболеваний костно-мышечной системы
Форма выпуска, состав и упаковка
Имплантат вязкоэластичный стерильный для внутрисуставных инъекций в виде бесцветного, прозрачного, однородного, вязкого, апирогенного геля (гидрогеля) с отсутствием помутнения, кристаллизации, инородных включений.
| 1 мл | |
| натрия гиалуронат | 10 мг |
| показатель осмоляльности 0.9-1.3 к 0.9% физиологическому раствору осмоляльность 270-390 мОсм/кг pH 6.8-7.8 |
Вспомогательные вещества (солевой раствор фосфатного буфера): натрия гидрофосфата додекагидрат (Na2HPO4×12H2O) — 0.06%, натрия дигидрофосфата дигидрат (NaH2PO4×2H2O) — 0.0048%, натрия хлорид — 0.89%, вода д/и — сколько требуется до 100% (3 мл).
Имплантат не включает в себя лекарственные средства, производные клеток и тканей человека, ткани животных. Не имеет радиационных и электромагнитных свойств.
3 мл — шприцы стеклянные (1) — блистеры (1) с имплантационными стикерами (3 шт.) — коробки картонные.
Фармакологическое действие
Имплантат Флексотрон Форте представляет собой медицинское изделие для внутрисуставных инъекций на основе гиалуроната натрия. В 1 мл продукта содержится 10 мг натрия гиалуроната, растворенного в физиологическом растворе.
Гиалуроновая кислота (молекулярная масса 650000-1200000 Да) является продуктом бактериальной ферментации. Гиалуроновая кислота принадлежит к небольшой группе веществ, одинаковых для всех живых организмов, поэтому она обладает высокой биосовместимостью.
Гиалуроновая кислота является естественным полисахаридом, который входит в состав всех тканей организма, при этом в особенно большой концентрации гиалуроновая кислота содержится в коже, подкожных тканях, а также в соединительной ткани, такой как синовиальная жидкость. Молекула гиалуроновой кислоты имеет спиральную длинноцепочечную структуру, которая позволяет удерживать или поглощать молекулы воды. Внутрисуставное обогащение синовиальной жидкости инъекциями гиалуроната натрия способствует улучшению или восстановлению вязкоупругих свойств естественной синовиальной жидкости. Гиалуронат натрия отвечает за вязкоупругие свойства синовиальной жидкости, таким образом вязкоэластичное протезирование позволяет компенсировать недостаточность гиалуроновой кислоты в синовиальной жидкости или снижение ее вязкости, смягчить внешние нагрузки на сустав, обеспечивает смазывание, восстановление упругости и вязкости, амортизацию, увлажнение и обволакивание суставных поверхностей, покрывая смазывающим защитным слоем хрящ и рецепторы синовии. Это помогает увеличить объем движений и обеспечивает механическую защиту тканей полости сустава, что в свою очередь может улучшать течение остеоартроза/остеоартрита и других дегенеративно-дистрофических и посттравматических патологических изменений суставов.
Флексотрон Форте не подлежит техническому обслуживанию.
Область применения
- остеоартрит/остеоартроз, посттравматические и другие дегенеративные изменения коленного, тазобедренного, плечевого и голеностопного суставов;
- восстановление свойств синовиальной жидкости при ортопедической хирургии суставов, а также у лиц, имеющих повышенные нагрузки на поврежденные суставы.
Противопоказания
- повышенная чувствительность к гиалуронату натрия;
- перенесенные или текущие инфекционные или кожные заболевания в области участка, на котором предполагается проведение инъекции.
Рекомендации по применению
Инъекции выполняются медицинскими специалистами в асептических условиях процедурных и манипуляционных кабинетов.
Перед введением имплантата содержимое шприца должно быть визуально оценено на прозрачность и однородность. Помутнение, кристаллизация, появление окраски и/или инородных включений может свидетельствовать о нарушении правил транспортировки и хранения изделия. При появлении вышеуказанных признаков введение средства для замещения синовиальной жидкости запрещено.
Имплантат вводится внутрисуставно в асептических условиях. Вводят в объеме, содержащемся в 1 шприце (3 мл). Для лечения остеоартрита/остеоартроза суставов у взрослых проводят 1 инъекцию в неделю. На курс лечения рекомендуется 3-5 шприцев. Количество и частота инъекций могут изменяться в зависимости от тяжести симптоматики.
Ожидаемая продолжительность эффекта составляет 6 месяцев после проведения курса лечения.
Перед проведением инъекции необходимо:
1. Удалить покрывающую мембрану и извлечь наполненный шприц с имплантатом из блистера.
2. Вручную прикрепить адаптер для пальцев к упору цилиндра шприца.
3. Придерживая люэровский наконечник, аккуратно открутить колпачок наконечника шприца (как показано ниже). Избегать чрезмерных нагрузок на шприц при фиксации иглы для предотвращения деформации механизма Луер-Лок.
img_flexotron_forte.tif|jpg
4. Продолжая крепко удерживать люэровский наконечник, прикрутить стерильную иглу рекомендуемым размером 21G или 23G (не входят в комплект поставки) к защелке шприца до тех пор, пока она не будет закреплена. Длина иглы выбирается врачом в соответствии с конституцией человека и толщиной подкожной клетчатки в месте пункции.
5. Перед инъекцией выпустить из шприца пузырьки воздуха в случае их наличия.
Вводить медленно.
Пациент должен избегать любых физических нагрузок или весовых нагрузок в течение 48 часов после внутрисуставной инъекции.
Побочные действия
Применение внутрисуставных форм гиалуроновой кислоты при дегенеративно-дистрофических и посттравматических поражениях суставов является хорошо изученным методом с установленным профилем безопасности, применяющимся на протяжении нескольких десятилетий.
К основным побочным эффектам относятся боль, отек и скованность в суставе после инъекции.
Крайне редко — возможно проявление местных воспалительных симптомов (повышение температуры, покраснение и отечность, увеличение содержания экссудата в полости сустава).
Обратимые местные реакции — кратковременное ограничение подвижности, чувство дискомфорта или тяжести в суставе. Проявление данных симптомов можно уменьшить прикладыванием льда к месту инъекции в течение 5-10 минут.
В единичных случаях отмечалось развитие аллергических реакций (зуд, сыпь, крапивница) и анафилактических реакций, септического артрита, внутритканевых кровоизлияний или кровоизлияний в полость сустава, тендинитов, флебитов, парестезий, головокружений, головных болей, мышечных спазмов, чувства жара, общего недомогания, периферических отеков при внутрисуставном введении растворов гиалуроновой кислоты.
При появлении местных или общих симптомов следует проконсультироваться с врачом.
Лекарственное взаимодействие
Применение изделия совместно с четвертичными соединениями аммония запрещено.
Особые указания
Медицинское изделие предназначено для внутрисуставного введения. Необходимо избегать введения имплантата в кровеносные сосуды и окружающие ткани.
По причине того, что септический артрит является серьезным побочным эффектом, необходимо соблюдать все стандартные меры предосторожности для хирургических вмешательств.
При получении аспирационной жидкости перед проведением вязкоэластичного протезирования следует провести соответствующие исследования для исключения бактериальной этиологии артрита.
Применять с осторожностью у пациентов с аллергией, а также у пациентов с заболеваниями печени.
В первые дни после инъекции может быть рекомендован пероральный прием анальгетиков или противовоспалительных лекарственных средств.
Продукт предназначен только для одноразового применения. Проходит финишную стерилизацию автоклавированием. Повторная стерилизация и применение изделия запрещены по причине наличия риска возникновения инфекции, перекрестной инфекции и/или дефекта изделия. Не использовать шприц из открытой и/или поврежденной стерильной упаковки. Не использовать шприц с открытым или поврежденным колпачком стерильного шприца. При нарушении стерильности или подозрении о нарушении стерильности имплантата изделие должно быть утилизировано.
Пожилые пациенты
У пациентов пожилого возраста применять с осторожностью ввиду общего снижения функциональной активности органов и систем организма.
Использование в педиатрии
Безопасность применения имплантата у детей изучена недостаточно, поэтому применять с осторожностью.
Извлечение имплантата
В случае выраженных проявлений может быть рекомендовано удаление имплантата из полости сустава, в т.ч. с применением лаважа, согласно действующим клиническим рекомендациям. Запрещаются повторные инъекции имплантатов синовиальной жидкости в сустав до купирования симптомов острого воспаления.
Защита окружающей среды и утилизация
Содержание шприца не является токсичным или огнеопасным. Изделия при использовании, транспортировке и хранении не оказывают негативного воздействия на окружающую среду.
Неиспользованные шприцы могут быть утилизированы в качестве бытовых отходов. Стекло следует утилизировать с осторожностью.
Неиспользованное содержимое шприца до или после истечения срока годности может быть утилизировано в качестве бытовых отходов (слить с большим количеством воды).
Уничтожение использованных медицинских изделий осуществляется в соответствии с природоохранными требованиями национальных, местных и ведомственных руководящих положений о безопасном уничтожении и утилизации.
В соответствии с санитарно-эпидемиологическими правилами и нормативами СанПиН 2.1.7.2790-10 использованные медицинские изделия (шприцы с имплантатами) относятся к медицинским отходам класса Б (эпидемиологически опасные отходы).
Беременность и лактация
При беременности имплантат применяют только в том случае, если ожидаемый положительный терапевтический эффект превосходит негативное влияние побочных эффектов.
В период лечения кормящим женщинам необходимо прервать грудное вскармливание.
Применение в детском возрасте
Безопасность применения имплантата у детей изучена недостаточно, поэтому применять с осторожностью.
При нарушениях функции печени
Применять с осторожностью у пациентов с заболеваниями печени.
Применение в пожилом возрасте
У пациентов пожилого возраста применять с осторожностью ввиду общего снижения функциональной активности органов и систем организма.
Условия и сроки хранения
Продукт следует хранить и транспортировать в оригинальной упаковке, при температуре от 2°С до 30°С. Беречь от воздействия прямых солнечных лучей. Не замораживать.
Срок годности — 3 года. Не применять после истечения срока годности, указанного на упаковке.
Описание препарата Флексотрон Форте основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.