Виндамэкс — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-007319
Торговое наименование:
Виндамэкс
Международное (непатентованное) наименование (МНН):
тафамидис
Лекарственная форма:
капсулы
Состав на 1 капсулу:
действующее вещество:
тафамидис 61,0 мг.
вспомогательные вещества:
макрогол 400 471,1 мг, полисорбат 20 55,5 мг, повидон (К-90) 12,0 мг, бутилгидрокситолуол 0,4 мг
Состав желатиновой оболочки:
Желатин прозрачный (L3DXHBAHR) 367,9 мг состоит из: желатин (195 Кислотный тип) 217,3 мг, сорбитола специальная глицериновая смесь 150,6 мг; краситель железа оксид красный (Е172) 1,29 мг.
Количество твердых веществ из чернил для надписи остающееся на капсуле, является следовым (не более 0,8 мг/капсула).
Надпись «VYN 61» наносится белыми чернилами Opacode® (WB) NSP-78-18022.
Чернила Colorcon® Ink, White Opacode® (WB) NSP-78-18022 содержат следующие компоненты: спирт SDA 35А* (24,9% м/м), аммония гидроксид* 28% (0,9% м/м), изопропанол* (8,2% м/м), вода очищенная* (9,9% м/м), макрогол MW400 (полиэтиленгликоль) (2,3% м/м), поливинилацетата фталат (10,4% м/м), пропиленгликоль (24,0% м/м), титана диоксид (19,6% м/м).
*удаляется в процессе производства и в конечном продукте отсутствует.
Лецитин соевый и триглицериды со средней длиной цепи используются в производственном процессе в качестве лубрикантов для смазки желатиновой ленты.
Описание
Продолговатые, непрозрачные мягкие желатиновые капсулы красновато-коричневого цвета с надписью белого цвета «VYN 61». Содержимое капсулы – суспензия от белого до розового цвета.
Фармакотерапевтическая группа:
другие препараты для лечения заболеваний нервной системы
Код ATX:
N07XX08
Фармакологические свойства
Фармакодинамика
Механизм действия
Тафамидис является селективным стабилизатором транстиретина (TTR). Тафамидис связывается с ТТР в участках связывания тироксина, стабилизируя тетрамер и замедляя диссоциацию на мономеры – фактор, ограничивающий скорость, в процессе амилоидогенеза.
Фармакодинамические эффекты
Транстиретиновый амилоидоз – это тяжелое инвалидизирующее заболевание, вызываемое накоплением в тканях различных нерастворимых фибриллярных белков, или амилоида, в количестве, достаточном для нарушения нормального функционирования. Диссоциация тетрамера транстиретина на мономеры является фактором, ограничивающим скорость, в патогенезе транстиретинового амилоидоза. Свернутые мономеры подвергаются частичной денатурации для образования альтернативно свернутых мономерных амилоидогенных промежуточных продуктов. Эти промежуточные вещества впоследствии неправильным образом собираются в растворимые олигомеры, профиламенты, филаменты и амилоидные фибриллы. Тафамидис связывается с отрицательной кооперативностью с двумя участками связывания тироксина на нативной тетрамерной форме транстиретина, что препятствует диссоциации на мономеры. Ингибирование диссоциации тетрамеров ТТР обосновывает применение тафамидиса у пациентов с транстиретиновой амилоидной кардиомиопатией (ATTR-КМП).
Анализ стабилизации ТТР использовался в качестве фармакодинамического маркера и для оценки стабильности тетрамера ТТР.
Тафамидис стабилизировал как тетрамер ТТР дикого типа, так и тетрамеры 14 клинически испытанных вариантов ТТР после приема тафамидиса один раз в сутки. Тафамидис также стабилизировал тетрамер ТТР для 25 вариантов, испытанных ex vivo, демонстрируя тем самым стабилизацию 40 амилоидогенных генотипов ТТР.
В многоцентровом международном двойном слепом плацебо-контролируемом рандомизированном исследовании стабилизация ТТР наблюдалась в месяц 1 и сохранялась до месяца 30.
Биомаркеры, ассоциированные с сердечной недостаточностью (NT-proBNP и тропонин I), указывали в пользу тафамидиса относительно плацебо.
Клиническая эффективность и безопасность
Эффективность была продемонстрирована в многоцентровом международном двойном слепом плацебо-контролируемом рандомизированном исследовании 3 режимов лечения с участием 441 пациента с диким типом или с наследственным ATTR-КМП.
Пациенты были рандомизированы для получения либо тафамидиса меглюмина 20 мг (n = 88) или 80 мг [которые применялись в виде четырех капсул по 20 мг тафамидиса меглюмина] (n = 176), либо подобранного плацебо (n = 177) один раз в сутки в дополнение к стандартному лечению (например, диуретикам) на протяжении 30 месяцев. Распределение лечения стратифицировалось по наличию или отсутствию вариантного генотипа ТТР, а также по исходной степени тяжести заболевания (класс по NYHA). В таблице 1 описаны демографические данные пациентов и характеристики на исходном уровне.
Таблица 1. Демографические данные пациентов и характеристики на исходном уровне
| Характеристика | Объединенная группа терапии тафамидисом N = 264 |
Плацебо N=177 |
| Возраст – лет | ||
| Среднее значение (стандартное отклонение) |
74,5 (7,2) | 74,1 (6,7) |
| Медиана (минимум, максимум) | 75 (46, 88) | 74 (51, 89) |
| Пол – число (%) | ||
| Мужчины | 241 (91,3) | 157 (88,7) |
| Женщины | 23 (8,7) | 20 (11,3) |
| Генотип ТТР – число (%) | ||
| ATTRm | 63 (23,9) | 43 (24,3) |
| ATTRwt | 201 (76,1) | 134 (75,7) |
| Класс – по NYHA (%) | ||
| Класс I по NYHA | 24 (9,1) | 13 (7,3) |
| Класс II по NYHA | 162 (61,4) | 101 (57,1) |
| Класс III по NYHA | 78 (29,5) | 63 (35,6) |
Сокращения: ATTRm – вариантный транстиретиновый амилоид; ATTRwt – транстиретиновый амилоид дикого типа; NYHA – Нью-Йоркская кардиологическая ассоциация (New York Heart Association).
В рамках первичного анализа использовали иерархическую комбинацию, применяя метод Финкельштейна-Шенфельда для оценки смертности от всех причин и частоты госпитализации в связи заболеваниями сердечно-сосудистой системы, которую определяли как число госпитализаций пациента (т. е. поступлений в больницу) в связи с сердечнососудистым заболеванием. Используя данный метод, сравнивали каждого пациента со всеми остальными пациентами в рамках каждой страты попарно, что продолжали далее, используя иерархический подход и смертность от всех причин, за которой следовала частота госпитализаций в связи с заболеваниями сердечно-сосудистой системы, когда пациентов невозможно было дифференцировать на основании смертности.
Этот анализ показал значительное снижение (р = 0,0006) смертности от всех причин и частоты госпитализаций в связи с заболеваниями сердечно-сосудистой системы в объединенной группе, получавшей тафамидис в дозе 20 мг и 80 мг, в сопоставлении с плацебо (таблица 2).
Таблица 2. Первичный анализ с применением метода Финкельштейна-Шенфельда (Ф-Ш) для оценки смертности от всех причин и частоты госпитализации в связи заболеваниями сердечно-сосудистой системы
| Первичный анализ | Объединенная группа терапии тафамидисом N = 264 |
Плацебо N = 177 |
| Число (%) пациентов, которые оставались живы* к месяцу 30 | 186 (70,5) | 101 (57,1) |
| Среднее число госпитализаций в связи с заболеваниями сердечно-сосудистой системы в течение 30 месяцев (на пациента в год) среди пациентов, которые оставались живы к месяцу 30† | 0,297 | 0,455 |
| P-значение из метода Ф-Ш | 0,0006 |
* Трансплантация сердца и имплантация устройств для механической поддержки сердца считаются факторами, указывающими на приближение к терминальной стадии. Вследствие чего эти пациенты рассматриваются в анализе как эквивалентные смерти. Следовательно, подобных пациентов не включали в число «Число (%) пациентов, которые оставались живы к месяцу 30» даже при условии, что эти пациенты живы по результатам оценки состояния здоровья при последующем наблюдении через 30 месяцев.
† Описательное среднее значение среди тех, кто пережил 30 месяцев.
Анализ отдельных компонентов первичного анализа (смертность от всех причин и госпитализация в связи с заболеваниями сердечно-сосудистой системы) также показал значительное снижение значений для тафамидиса в сопоставлении с плацебо.
Отношение рисков для смертности от всех причин в модели пропорциональных рисков Кокса для объединенной группы получения тафамидиса составило 0,698 (95% ДИ 0,508; 0,958), что указывает на снижение риска летального исхода на 30,2% относительно группы получения плацебо (р = 0,0259). График Каплана-Майера времени до явления для смертности от всех причин представлен на рисунке 1.
Рисунок 1. Смертность от всех причин*
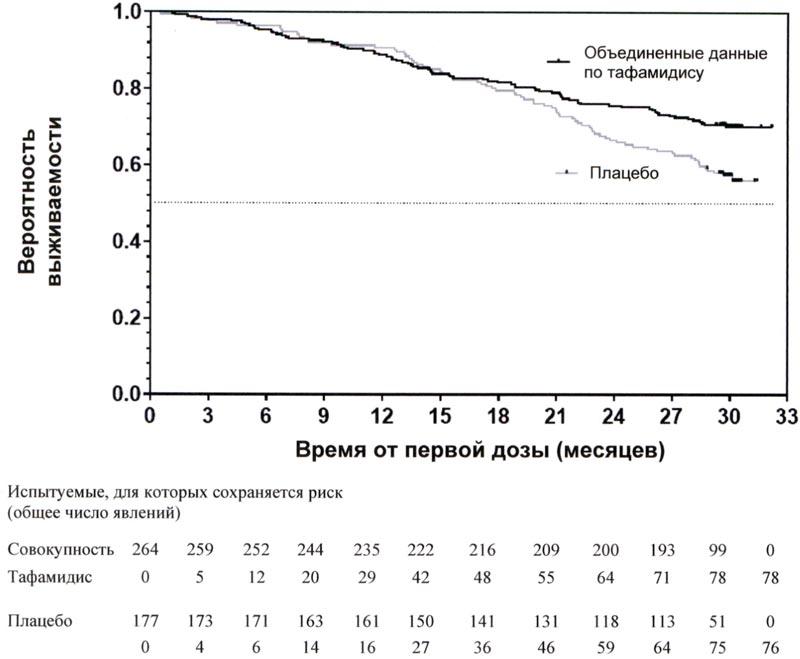
Отмечалось значительно меньше госпитализаций в связи с заболеваниями сердечнососудистой системы при применении тафамидиса в сравнении с плацебо при снижении риска на 32,4% (таблица 3).
Таблица 3. Частота госпитализаций в связи с заболеваниями сердечно-сосудистой системы
| Объединенная группа терапии тафамидисом N = 264 |
Плацебо N = 177 |
|
| Общее (%) число пациентов с госпитализациями в связи с заболеваниями сердечно-сосудистой системы | 138 (52,3) | 107 (60,5) |
| Госпитализации в связи с заболеваниями сердечно-сосудистой системы в год* | 0,4750 | 0,7025 |
| Отличие лечения в объединенной группа получения тафамидиса в сопоставлении с плацебо (отношение относительных рисков)* | 0,6761 | |
| р-значение* | <0,0001 |
Сокращение: NYHA – Нью-Йоркская кардиологическая ассоциация (New York Heart Association).
* Этот анализ был основан на модели с пуассоновской регрессией с лечением, генотипом ТТР (вариантный или дикий тип), классом по классификации Нью-Йоркской кардиологической ассоциации (NYHA) (классы I и II по NYHA вместе и класс III по NYHA) на исходном уровне, зависимостью лечения от генотипа ТТР и зависимостью лечения от класса по NYHA на исходном уровне в качестве факторов.
Эффект лечения тафамидисом на функциональную способность и состояние здоровья оценивался при помощи 6-минутного теста с ходьбой (6-Minute Walk Test (6MWT)) и оценки по Канзасскому вопросника для пациентов с кардиомиопатией – общему резюме (Kansas City Cardiomyopathy Questionnaire-Overall Summary (KCCQ-OS)) (состоящему из таких доменов, как общие симптомы, физические ограничения, качество жизни и социальные ограничения) соответственно. Значительный эффект лечения в пользу тафамидиса впервые наблюдался к месяцу 6 и оставался стабильным до месяца 30 по результатам, как расстояния в 6MWT, так и оценки по KCCQ-OS (таблица 4).
Таблица 4. 6MWT и KCCQ-OS, а также оценки по доменам, являющимся компонентами вопросника
| Конечные точки |
Средний исходный уровень (СО) | Изменение от исходного уровня к месяцу 30, среднее значение, рассчитанное методом наименьших квадратов (СО) | Отличие лечения от плацебо Среднее значение, рассчитанное методом наименьших квадратов (95% ДИ) |
Р-значение | ||
| Объединенная группа терапии тафамидисом N = 264 |
Плацебо N=177 |
Объединенная группа терапии тафамидисом | Плацебо | |||
| 6MWT* (метры) |
350,55 (121,30) |
353,26 (125,98) |
-54,87 (5,07) |
-130,55 (9,80) |
75,68 (57,56, 93,80) |
р< 0,0001 |
| KCCQ-OS* | 67,27 (21,36) |
65,90 (21,74) |
-7,16 (1,42) |
-20,81 (1,97) |
13,65 (9,48, 17,83) |
р< 0,0001 |
* Более высокие значения указывают на лучшее состояние здоровья.
Сокращения: 6MWT – 6-минутный тест с ходьбой (6-Minute Walk Test); KCCQ-OS – Канзасский вопросник для пациентов с кардиомиопатией – общее резюме (Kansas City Cardiomyopathy Questionnaire-Overall Summary); LS – метод наименьших квадратов (least squares); ДИ – доверительный интервал.
Результаты применения метода Ф-Ш, представленные коэффициентом выигрыша для объединенной конечной точки и ее компонентов (смертность от всех причин и частота госпитализаций в связи с заболеваниями сердечно-сосудистой системы), неизменно указывали в пользу тафамидиса в сопоставлении с плацебо с учетом дозы и по всем подгруппам (дикий тип, вариантный и класс I и II и III по NYHA) за исключением частоты госпитализаций в связи с заболеваниями сердечно-сосудистой системы при классе III по NYHA (рисунок 2), которая выше в группе, получавшей лечение тафамидисом, по сравнению с плацебо (см. раздел «Способ применения и дозы»). Анализы 6MWT и KCCQ-OS также были в пользу тафамидиса относительно плацебо в каждой подгруппе.
Рисунок 2. Результаты применения метода Ф-Ш и компонентов в зависимости от подгруппы и дозы
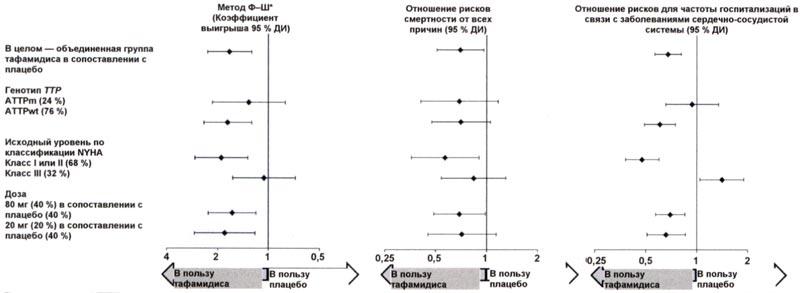
* Результаты Ф-Ш представлены с использованием коэффициента выигрыша (на основании данных по смертности от всех причин и частоте госпитализаций в связи с заболеваниями сердечно-сосудистой системы). Коэффициент выигрыша представляет собой число пар «выигрышей» пациентов, получавших лечение, разделенное на число пар «выигрышей» пациентов, получавших плацебо.
Трансплантация сердца и имплантация устройств для механической поддержки сердца учитывались как смерть.
При применении метода Ф-Ш индивидуально к каждой группе, получавшей определенную дозу, применение тафамидиса снижало объединенный показатель смертности от всех причин и частоты госпитализации в связи с заболеваниями сердечно-сосудистой системы, как для дозы 80 мг, так и для дозы 20 мг по сравнению с плацебо (р = 0,0030 и р = 0,0048 соответственно). Результаты первичного анализа, 6MWT к месяцу 30 и KCCQ-OS к месяцу 30 были статистически значимыми для обеих доз тафамидиса меглюмина, 80 мг и 20 мг, в сопоставлении с плацебо, при этом результаты для обеих дозы были сходными.
Данные по эффективности для тафамидиса 61 мг недоступны, так как эта лекарственная форма не оценивалась в двойном слепом плацебо-контролируемом рандомизированном исследовании фазы 3. Виндамэкс 61 мг (тафамидис) соответствует 80 мг тафамидиса меглюмина. Тафамидис и тафамидис меглюмин не являются взаимозаменяемыми в пересчете на мг. Относительная биодоступность тафамидиса 61 мг сходна с тафамидиса меглюмином 80 мг в равновесном состоянии (см. раздел «Фармакокинетика»).
Однократная пероральная сверхтерапевтическая доза 400 мг раствора тафамидиса меглюмина у здоровых добровольцев, как было показано, не приводила к удлинению интервала QTc.
Европейское агентство по лекарственным средствам отклонило требование о представлении результатов исследований с тафамидисом во всех подгруппах пациентов детского возраста при транстиретиновом амилоидозе (см. раздел «Способ применения и дозы» для ознакомления с информацией о применении у детей).
Фармакокинетика
Всасывание
При однократном приеме внутрь одной капсулы препарата Виндамэкс натощак максимальная концентрация в плазме (Сmax) достигалась спустя 4 часа (tmax – медиана времени достижения максимальной концентрации).
Одновременный прием высококалорийной пищи с высоким содержанием жиров снижал скорость, но не степень всасывания. Полученные результаты подтвердили возможность приема препарата Виндамэкс в независимости от приема пищи.
Распределение
Тафамидис очень хорошо связывается с белками (>99%) плазмы крови. Наблюдаемый равновесный объем распределения тафамидиса составляет 18,5 литра.
Степень связывания тафамидиса с белками плазмы крови была оценена в исследованиях с плазмой крови животных и человека. Сродство тафамидиса к TTR выше, чем к альбумину. В результате тафамидис преимущественно связывается с TTR, несмотря на то, что концентрация альбумина в плазме крови (600 мкМ) значительно превышает концентрацию TTR (3,6 мкМ).
Метаболизм и выведение
Однозначное подтверждение того, что тафамидис выводится у человека с желчью, отсутствует, однако на основании результатов доклинических исследований предполагается, что метаболизм тафамидиса протекает путем глюкуронирования с последующим выведением с желчью. Этот путь метаболизма и выведения наиболее вероятен для человека, так как примерно 59% от всей принятой дозы обнаруживается в фекалиях и примерно 22% обнаруживается в моче. Исходя из результатов популяционного фармакокинетического анализа, кажущийся пероральный клиренс тафамидиса составляет 0,263 л/ч, а средний период полувыведения для популяции – приблизительно 49 часов.
Линейность по дозе и времени
Воздействие приема однократной суточной дозы тафамидиса меглюмина увеличивалось с увеличением однократной дозы до 480 мг и многократных доз до 80 мг в сутки. В целом, увеличение было пропорционально или почти пропорционально дозе, и клиренс тафамидиса был постоянным на протяжении времени.
Относительная биодоступность тафамидиса 61 мг сходна с биодоступностью тафамидиса меглюмина 80 мг в равновесном состоянии. Тафамидис и тафамидис меглюмин не являются взаимозаменяемыми в пересчете на мг.
Фармакокинетические параметры были схожими после однократного и многократного приема тафамидиса меглюмина в дозе 20 мг, что указывает на отсутствие индукции или ингибирования метаболизма тафамидиса.
Результаты однократного ежедневного приема перорального раствора тафамидиса меглюмина в дозе от 15 до 60 мг в течение 14 дней продемонстрировали достижение равновесного (ss) состояния в 14 день.
Применение в особых популяциях
Пациенты пожилого возраста: по результатам популяционного фармакокинетического анализа у пациентов в возрасте 65 лет и старше расчетный кажущийся пероральный клиренс препарата в равновесном состоянии был в среднем на 15% ниже, чем у пациентов младше 65 лет. Однако такое различие в клиренсе вызывает увеличение на <20% средних значений Сmax и AUC в сравнении с более молодыми людьми и не является клинически значимым.
Пациенты с нарушениями функции почек: применение препарата Виндамэкс у пациентов с нарушениями функции почек специально не изучалось. Влияние клиренса креатинина на фармакокинетику (ФК) тафамидиса было изучено в популяционном фармакокинетическом анализе у пациентов с клиренсом креатинина >18 мл/мин. При вычислении фармакокинетических показателей не было выявлено никаких различий кажущегося перорального клиренса тафамидиса между пациентами с клиренсом креатинина <80 мл/мин и пациентами с клиренсом креатинина ≥ 80 мл/мин. У пациентов с нарушениями функции почек коррекция дозы препарата не требуется.
Пациенты с нарушениями функции печени: Фармакокинетические данные указывали на снижение системной экспозиции (примерно на 40%) и повышение общего клиренса (0,52 л/ч по сравнению с 0,31 л/ч) тафамидиса меглюмина у людей с нарушениями функции печени средней степени (7-9 баллов по шкале Чайлда-Пью включительно) по сравнению со здоровыми людьми, что было связано с более высокой концентрацией несвязанной фракции тафамидиса. Поскольку у пациентов с нарушениями функции печени средней степени концентрации TTR снижены в сравнении со здоровыми людьми, коррекция дозировки не требуется, так как стехиометрии тафамидиса с его белком-мишенью (TTR) будет достаточно для стабилизации тетрамера TTR. Информация об экспозиции препарата Виндамэкс у пациентов с нарушениями функции печени тяжелой степени отсутствует.
Взаимосвязь параметров фармакокинетики и фармакодинамики
Данные исследований in vitro показали, что тафамидис не оказывает значительного ингибирующего влияния на ферменты CYP1A2, CYP3A4, CYP3A5, CYP2B6, CYP2C8, CYP2C9, CYP2C19 и CYP2D6 цитохрома Р450. Ожидается, что тафамидис не будет вступать в клинически значимые межлекарственные взаимодействия, обусловленные индукцией CYP1A2, CYP2B6 или CYP3A4.
Исследования in vitro указывают на то, что маловероятно, что тафамидис будет вступать в межлекарственные взаимодействия при клинически значимых концентрациях с субстратами УДФ-глюкуронозилтрансферазы (UGT) на системном уровне. Тафамидис может ингибировать активность UGT 1А1 в кишечнике.
Тафамидис продемонстрировал низкий потенциал к ингибированию белка множественной лекарственной устойчивости (Multi-Drug Resistant Protein – MDR1) (также известного как Р-гликопротеин; P-gp) на системном уровне и в желудочно-кишечном (ЖК) тракте, переносчика органических катионов 2 (organic cation transporter 2 – ОСТ2), переносчика экструзии лекарственных препаратов и токсинов 1 (multidrug and toxin extrusion transporter 1 – MATE1) и MATE2K, полипептидного переносчика органических анионов 1В1 (organic anion transporting polypeptide 1B1 – OATP1B1) и OATP1B3 при клинически значимых концентрациях.
Показания к применению
Препарат Виндамэкс показан для лечения транстиретинового амилоидоза, обусловленного транстиретином дикого типа или наследственной формой заболевания, у взрослых пациентов с кардиомиопатией (ATTR-КМП).
Противопоказания
- гиперчувствительность к действующему веществу или к любому из вспомогательных веществ, входящих в состав препарата;
С осторожностью
Препарат Виндамэкс следует применять с осторожностью у пациентов с нарушением функции печени тяжелой степени.
Применение при беременности и в период грудного вскармливания
Женщины, способные к деторождению
Женщины, способные к деторождению, должны использовать эффективные методы контрацепции в период лечения препаратом Виндамэкс и, вследствие продолжительного периода полувыведения, в течение одного месяца после завершения лечения.
Беременность
Данные по применению препарата Виндамэкс у беременных женщин отсутствуют. Исследования на животных показали эмбриофетальную токсичность. Препарат Виндамэкс не рекомендуется применять во время беременности, а также женщинам способным к деторождению, и не использующих контрацептивы.
Период грудного вскармливания
Доступные данные у животных показали, что тафамидис проникает в грудное молоко. Нельзя исключить риск для новорожденного/младенца. Препарат Виндамэкс не следует принимать во время грудного вскармливания.
Фертильность
В доклинических исследованиях отрицательного влияния на репродуктивную функцию не наблюдалось.
Способ применения и дозы
Лечение следует начинать под контролем врача, имеющего опыт оказания медицинской помощи пациентам с амилоидозом или кардиомиопатией.
Если у пациента имеется специфический медицинский анамнез или признаки сердечной недостаточности или кардиомиопатии, этиологический диагноз должен устанавливаться врачом, обладающим знаниями по оказанию медицинской помощи пациентам с амилоидозом или кардиомиопатией, для того, чтобы подтвердить ATTR-КМП и исключить AL-амилоидоз до начала приема тафамидиса при помощи соответствующих инструментов оценки, таких как сцинтиграфия с остеотропными радиофармацевтическими препаратами и анализы крови/мочи и/или гистологическое исследование биоптатов, а также генотипирование транстиретина (ТТР) для того, чтобы охарактеризовать процесс как дикий тип или наследственный.
Режим дозирования
Рекомендуемая доза препарата Виндамэкс составляет одну капсулу 61 мг тафамидиса внутрь один раз в сутки.
Способ применения
Для приема внутрь.
Капсулы следует глотать целиком, не измельчая и не разрезая. Препарат Виндамэкс можно принимать в независимости от приема пищи.
Виндамэкс 61 мг (тафамидис) соответствует 80 мг тафамидиса меглюмина. Тафамидис и тафамидис меглюмин не являются взаимозаменяемыми в пересчете на мг.
Применение Виндамэкса следует начинать как можно раньше в течение заболевания, когда клиническая польза в отношении прогрессирования заболевания может быть более очевидной. В то же время, если обусловленное амилоидом повреждение сердца является более выраженным, как в случае класса III по NYHA, решение о начале или продолжении терапии должно приниматься на усмотрение врача, обладающего знаниями по оказанию медицинской помощи пациентам с амилоидозом или кардиомиопатией. Имеются ограниченные клинические данные у пациентов с классом IV по NYHA.
Если после приема препарата возникает рвота, и в рвотных массах обнаруживается неповрежденная капсула Виндамэкса, то при возможности следует принять дополнительную дозу Виндамэкса. Если капсула не обнаружена, то нет необходимости принимать дополнительную дозу и следует вернуться к обычному режиму приема препарата на следующий день.
Особые группы пациентов
Применение у детей
Значимые данные по применению препарата Виндамэкс у пациентов детского возраста отсутствуют. Препарат Виндамэкс не следует применять у пациентов детского возраста в связи с отсутствием данных.
Применение у пациентов пожилого возраста
У пациентов пожилого возраста (в возрасте ≥65 лет) коррекции дозы препарата не требуется (смотрите раздел «Фармакокинетика»).
Применение у пациентов с нарушением функции почек или печени
У пациентов с нарушениями функции почек или с нарушениями функции печени легкой или средней степени коррекции дозы препарата не требуется. Доступны ограниченные данные о пациентах с тяжелым нарушением функции почек (при клиренсе креатинина меньше или равном 30 мл/мин). Применение препарата Виндамэкс не изучалось у пациентов с тяжелыми нарушениями функции печени, поэтому его следует применять с осторожностью в этой группе пациентов.
Побочное действие
Резюме профиля безопасности
В данных по безопасности отражен уровень воздействия у 176 пациентов с ATTR-КМП, которые получали по 80 мг (которые принимались как 4×20 мг) тафамидиса меглюмина ежедневно в 30-месячном плацебо-контролируемом исследовании у пациентов с установленным диагнозом ATTR-КМП.
Частота нежелательных явлений у пациентов, получавших лечение с применением 80 мг тафамидиса меглюмина, была сходной и сопоставимой с плацебо.
О следующих нежелательных явлениях сообщалось чаще у пациентов, получавших лечение тафамидисом меглюмином в дозе 80 мг, в сравнении с плацебо: метеоризм [8 пациентов (4,5%) в сравнении с 3 пациентами (1,7%)] и повышение значений функциональных печеночных проб [6 пациентов (3,4%) в сравнении с 2 пациентами (1,1%)]. Причинно-следственная связь не была установлена.
Виндамэкс 61 мг (тафамидис) соответствует 80 мг тафамидиса меглюмина. Тафамидис и тафамидис меглюмин не являются взаимозаменяемыми в пересчете на мг. Данные по безопасности для тафамидиса 61 мг недоступны, так как эта лекарственная форма не оценивалась в двойном слепом плацебо-контролируемом рандомизированном исследовании фазы 3.
Передозировка
Симптомы
Объем клинических данных о случаях передозировки препаратом минимален. В ходе клинических испытаний два пациента с диагнозом ATTR-КМП случайно приняли одну дозу тафамидиса меглюмина 160 мг, не испытав при этом каких-либо нежелательных явлений. В клинических исследованиях у здоровых добровольцев наивысшая доза тафамидиса меглюмина составляла 480 мг однократно. При приеме этой дозы было зарегистрировано одно нежелательное явление, связанное с лечением в виде гордеолума легкой степени тяжести.
Лечение
В случае передозировки следует при необходимости принять стандартные меры поддерживающей терапии.
Взаимодействие с другими лекарственными средствами
В ходе клинического исследования среди здоровых добровольцев тафамидис меглюмин в дозировке 20 мг не индуцировал и не ингибировал изофермент CYP3 А4 системы цитохрома Р450.
В исследованиях in vitro тафамидис ингибирует эффлюксный переносчик BCRP (белок резистентности рака молочной железы (breast cancer resistant protein)) при дозе тафамидиса 61 мг/сутки при ИК50 на уровне 1,16 мкМ, а также может вызывать межлекарственные взаимодействия при клинически значимых концентрациях с субстратами этого переносчика (например, метотрексат, розувастатин, иматиниб).
В клиническом исследовании среди здоровых участников экспозиция розувастатина, субстрата BCRP, увеличивалась примерно в 2 раза после многократного ежедневного приема 61 мг тафамида.
Аналогичным образом тафамидис ингибирует активность переносчиков захвата ОАТ1 и ОАТ3 (переносчики органических анионов) при ИК50 на уровне 2,9 мкМ и 2,36 мкМ соответственно; и при клинически значимых концентрациях он может вызывать межлекарственные взаимодействия с субстратами этих переносчиков (например, с нестероидными противовоспалительными препаратами, буметанидом, фуросемидом, ламивудином, метотрексатом, осельтамивиром, тенофовиром, ганцикловиром, адефовиром, цидофовиром, зидовудином и зальцитабином). На основании данных in vitro максимальные прогнозируемые изменения в AUC субстратов ОАТ1 и ОАТ3, по результатам определений, были менее 1,25 для дозы 61 мг тафамидиса, следовательно, ожидается, что ингибирование тафамидисом переносчиков ОАТ1 или ОАТ3 не будет приводить к клинически значимым взаимодействиям.
Исследования лекарственного взаимодействия тафамидиса с другими лекарственными препаратами не проводились.
Отклонения от нормы результатов лабораторных исследований
Тафамидис может снижать сывороточные концентрации общего тироксина без сопутствующего изменения свободного тироксина (Т4) или тиреотропного гормона (ТТГ). Это наблюдение в отношении общих значений тироксина, вероятно, может быть результатом снижения связывания тироксина с транстиретином (TTR) или его вытеснения из-за высокой аффинности связывания тафамидиса с рецептором тироксина TTR. Никаких соответствующих клинических результатов, соответствующих дисфункции щитовидной железы, не наблюдалось.
Особые указания
Женщинам, способным к деторождению, следует использовать надлежащие методы контрацепции в период приема тафамидиса и продолжить применение надлежащего метода контрацепции на протяжении 1 месяца после прекращения лечения тафамидисом (см. раздел «Применение при беременности и в период грудного вскармливания»).
Тафамидис следует добавить к стандарту оказания медицинской помощи для пациентов с транстиретиновым амилоидозом. Врачам следует проводить наблюдение за пациентами и продолжать оценивать потребность пациента в ином лечении, включая необходимость трансплантации органа, как часть стандарта оказания медицинской помощи. В связи с отсутствием доступных данных в отношении применения тафамидиса при трансплантации органов, применение тафамидиса следует прекращать у пациентов, которым проводится трансплантация органа.
Может возникать повышение показателей функциональных печеночных проб и снижение уровня тироксина (см. раздел «Взаимодействие с другими лекарственными средствами» и «Побочное действие»).
Этот лекарственный препарат содержит не более 44 мг сорбитола в каждой капсуле. Сорбитол является источником фруктозы.
Следует учитывать аддитивный эффект принимаемых одновременно препаратов, содержащих сорбитол (или фруктозу), а также потребление сорбитола (или фруктозы) с пищей.
Содержание сорбитола в лекарственных препаратах для перорального применения может повлиять на биодоступность других лекарственных препаратов для перорального применения при одновременном применении.
Влияние на способность управлять транспортными средствами, механизмами
На основании фармакодинамического и фармакокинетического профиля можно полагать, что тафамидис не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с механизмами.
Форма выпуска
Капсулы 61 мг.
По 10 капсул в блистере ПВХ/ПА/Ал/ПВХ с подложкой из Ал/ПЭТ/бумаги.
3 блистера по 10 капсул вместе с инструкцией по применению помещают в картонную пачку с контролем первого вскрытия.
Условия хранения
Хранить при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять препарат по истечении срока годности.
Условия отпуска
По рецепту.
Юридическое лицо, на имя которого выдано регистрационное удостоверение
Пфайзер Инк., США
235 Ист 42-ая Стрит, Нью-Йорк, штат Нью-Йорк, 10017, США
Производитель
Каталент Фарма Солюшнз ЭлЭлСи, США
2725 Шерер Драйв Норт, Ст. Петербург, Флорида, 33716-1016, США
Выпускающий контроль качества
Андерсонбрекон (ЮК) Лимитед, Соединенное Королевство
Блоки 2-7, Уай Вэлли Бизнес Парк, Брекон Роуд, Хэй-Он-Уай, Херефорд, HR3 5PG, Соединенное Королевство
Претензии потребителей направлять по адресу ООО «Пфайзер Инновации»
123112 Москва, Пресненская наб., д. 10, БЦ «Башня на Набережной» (Блок С)
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Tərkibi:
Hər bir şüşə flakonun (15 ml) tərkibində:
Arı südü tozu (lioflizə olunmuş) 200 mq
Barbados albalısı ekstraktı tozu (Malpighia emarginata ) 150 mq
Qaragilə konsentratlaşdırılmış şirəsi (Vaccinium myrtillus) 750 mq
Qara kəndəlaş konsentratlaşdırılmış şirəsi (Sambucus nigra ) 500 mq
Böyürtkən (Rubus furitcosus) 375 mq
FONDOMİX-100% təbii maddələrdən ibarətdir. Bioaktivator olub, orqanizmin təbii müdafiəsinə kömək edir dondurulmuş arı südü, barbados albalısı və antasianidinlərlə zəngin bitki qarışığından (Qaragilə Qara kəndəlaş Böyürtkən) ibarətdir.
Arı südünün tərkibində orqanizmə lazım olan 20-yə yaxın aminturşu, çoxlu vitaminlər, mikroelementlər və mineral maddələr, 110-a yaxın bioloji aktiv birləşmələr vardır. Arı südü immun sistemini gücləndirir, infeksion xəstəliklərə qarşı müqaviməti artırır, maddələr mübadiləsini yaxşılaşdrır. Ümumi tonus yüksəlir, insan gümrahlaşır, cavanlaşır, daxili sekresiya vəzilərinin fəaliyyəti normallaşır. Barbados albalısı vitamin C mənbəyidir, antioksidant xüsusiyyətə malikdir, orqanizmə tonuslandırıcı, bərpaedici, virus və infeksiyalardan qoruyucu təsir göstərir.
İstifadəsinə göstərişlər:
Fondomix dəstək pıreparatı olub, əsasən orqanizmin normal fəaliyyətini nizamlayır.
- Yorğunluq dövrü.
- Orqanizmdə mövsümü dəyişikliklərlə yarana proseslər.
- Orqanizmdə gərgin işlə əlaqədar yaranan proseslər.
- Stress.
- Fondomix həmçinin uşaqlar və yaşlılar üçün dəstək preparatı sayılır. Uşaqlarda xüsusən də yeniyetmələrdə effektli təsirə malikdir. Tərkibində heç bir boya maddəsi və konservant yoxdur.Tam təbii qida əlavəsidir.
İstifadə qaydası:
Böyüklərə və 6 yaşından böyük uşaqlara gündə 1 flakon (15ml);
2 — 6 yaş arası uşaqlara gündə yarım flakon (7,5ml) təyin olunur.
Səhər yeməkdən sonra qəbulu daha yaxşıdır. Meyvə şirəsi və istənilən digər maye ilə durulaşdırıb içilir. Açıldıqdan sonra flakon soyuducuda bir neçə gün saxlana bilər.
İstifadədən əvvəl flakonu silkələyin.
Xəbərdarlıq:
Tövsiyə olunan dozanı keçməyin. Əlavələr çeşidli və balanslı pəhriz üçün əvəzedici hesab edilməməli və sağlam həyat tərzinin bir hissəsi kimi istifadə olunmalıdır. Sərin, quru qaranlıq və üç yaşına çatmamış uşaqların əli çatmayan yerdə saxlanmalıdır.
Buraxılış forması:
Hər biri 15 ml- lik 10 şüşə flakondan ibarətdir.
İstehsalçı:
VEFA İlaç San. və Tic. Ltd. Şti.
Azerbaycan Respublikasında rəsmi distribütor “Paşa-K” şirkəti.
Альфа Нормикс® (Alfa Normix®) инструкция по применению
📜 Инструкция по применению Альфа Нормикс®
💊 Состав препарата Альфа Нормикс®
✅ Применение препарата Альфа Нормикс®
📅 Условия хранения Альфа Нормикс®
⏳ Срок годности Альфа Нормикс®
Описание лекарственного препарата
Альфа Нормикс®
(Alfa Normix®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2022 года.
Дата обновления: 2023.10.23
Владелец регистрационного удостоверения:
Контакты для обращений:
АЛЬФАСИГМА РУС ООО
(Россия)
Код ATX:
A07AA11
(Рифаксимин)
Лекарственные формы
| Альфа Нормикс® |
Гранулы д/пригот. сусп. д/приема внутрь 100 мг/5 мл: фл. 24.378 г в компл. с мерн. чашечкой рег. №: ЛС-001994 |
|
|
Таб., покр. пленочной оболочкой, 200 мг: 12, 14, 24, 28, 36, 42, 60 или 70 шт. рег. №: ЛС-001993 |
Форма выпуска, упаковка и состав
препарата Альфа Нормикс®
Таблетки, покрытые пленочной оболочкой розового цвета, круглые, двояковыпуклые.
Вспомогательные вещества: карбоксиметилкрахмал натрия, глицерил пальмитостеарат, кремния диоксид коллоидный, тальк, целлюлоза микрокристаллическая, тип 102.
Состав пленочной оболочки: Опадрай OY-S-34907 розовый [гипромеллоза, титана диоксид (Е171), динатрия эдетат, пропиленгликоль, краситель железа оксид красный (Е172)].
12 шт. — блистеры (1) — пачки картонные.
12 шт. — блистеры (2) — пачки картонные.
12 шт. — блистеры (3) — пачки картонные.
12 шт. — блистеры (5) — пачки картонные.
14 шт. — блистеры (1) — пачки картонные.
14 шт. — блистеры (2) — пачки картонные.
14 шт. — блистеры (3) — пачки картонные.
14 шт. — блистеры (5) — пачки картонные.
Гранулы для приготовления суспензии для приема внутрь оранжевого цвета, с запахом вишни (дикой черешни); приготовленная суспензия однородная, желто-оранжевого цвета, с запахом вишни (дикой черешни).
Вспомогательные вещества: целлюлоза микрокристаллическая, тип 102, кармеллоза натрия, пектин, каолин, натрия сахаринат, натрия бензоат (E211), сахароза, ароматизатор вишневый (дикой черешни).
24.378 г — флаконы темного стекла с градуированным 60 мл уровнем (1) в комплекте с мерной чашечкой — пачки картонные.
Фармакологическое действие
Рифаксимин — антибиотик широкого спектра действия из группы рифамицина. Как и другие представители этой группы, необратимо связывает бета-субъединицы фермента бактерий ДНК-зависимой РНК-полимеразы и, следовательно, ингибирует синтез РНК и белков бактерий.
В результате необратимого связывания с ферментом, рифаксимин проявляет бактерицидные свойства в отношении чувствительных бактерий. Препарат обладает широким спектром противомикробной активности, включающим большинство грамотрицательных и грамположительных, аэробных и анаэробных бактерий.
Широкий антибактериальный спектр рифаксимина способствует снижению патогенной кишечной бактериальной нагрузки, которая обусловливает некоторые патологические состояния.
Препарат уменьшает:
- образование бактериями аммиака и других токсических соединений, которые в случае тяжелого заболевания печени, сопровождающегося нарушением процесса детоксикации, играют роль в патогенезе и клинических проявлениях печеночной энцефалопатии;
- повышенную пролиферацию бактерий при синдроме избыточного роста микроорганизмов в кишечнике;
- присутствие в дивертикуле ободочной кишки бактерий, которые могут участвовать в воспалении внутри и вокруг дивертикулярного мешка и возможно играют ключевую роль в развитии симптомов и осложнений дивертикулярной болезни;
- интенсивность антигенного стимула, который при наличии генетически обусловленных дефектов в иммунорегуляции слизистой и/или в защитной функции, может инициировать или постоянно поддерживать хроническое воспаление кишечника;
- риск инфекционных осложнений при колоректальных хирургических вмешательствах.
Механизм резистентности
Развитие резистентности к рифаксимину обусловлено обратимым повреждением гена rpoB, который кодирует бактериальную РНК-полимеразу. Встречаемость резистентных субпопуляций среди бактерий, выделенных у пациентов с диареей путешественника, была низкой.
По данным клинических исследований, трехдневный курс терапии рифаксимином у пациентов с диареей путешественника не сопровождался появлением резистентных грамположительных (энтерококков) и грамотрицательных (кишечная палочка) бактерий. При повторном применении рифаксимина в высоких дозах у здоровых добровольцев и у пациентов с воспалительными заболеваниями кишечника резистентные к рифаксимину штаммы появлялись, однако, они не колонизировали ЖКТ и не вытесняли рифаксимин-чувствительные штаммы.
При прекращении терапии резистентные штаммы быстро исчезали. Экспериментальные и клинические данные позволяют предполагать, что применение рифаксимина у пациентов с диареей путешественника и скрытой инфекцией Mycobacterium tuberculosis и Neisseria meningitidis не будет сопровождаться отбором рифампицин-резистентных штаммов.
Чувствительность
Тестирование чувствительности in vitro не может использоваться для определения чувствительности или резистентности бактерий к рифаксимину. В настоящее время клинических данных недостаточно, чтобы установить предельные значения для оценки тестов на чувствительность. Рифаксимин оценивали in vitro в отношении возбудителей диареи путешественника из четырех регионов мира: энтеротоксигенных и энтероагрегативных штаммов Escherichia coli, Salmonella spp., Shigella spp.,
нехолерных вибрионов, Plesiomonas spp., Aeromonas spp., и Campylobacter spp. МПК90 для выделенных штаммов составила 32 мкг/мл, и этот уровень легко достижим в просвете кишечника в результате высокой концентрации рифаксимина в фекалиях. Поскольку рифаксимин в полиморфной форме альфа обладает низкой всасываемостью из ЖКТ и действует местно в просвете кишечника, то он может быть клинически неэффективен в отношении инвазивных бактерий, даже если эти бактерии чувствительны к нему in vitro.
Фармакокинетика
Всасывание
Рифаксимин в полиморфной форме альфа практически не всасывается при приеме внутрь (менее 1%). При повторном применении у здоровых добровольцев и у пациентов с поврежденной слизистой оболочкой кишечника, при воспалительных заболеваниях кишечника концентрация в плазме очень низкая (менее 10 нг/мл). При применении препарата через 30 мин после приема жирной пищи отмечали не имеющее клинической значимости повышение системного всасывания рифаксимина.
Распределение
Рифаксимин умеренно связывается с белками плазмы. Связывание с белками у здоровых добровольцев составляет 67.5%, а у пациентов с печеночной недостаточностью 62%.
Выведение
Выводится из организма в неизмененном виде кишечником (96.9% от принятой дозы), т.к. не подвергается деградации и метаболизму при прохождении через ЖКТ. Обнаруживаемый с помощью меченых изотопов в моче рифаксимин составляет не более 0.025% от принятой внутрь дозы. Менее 0.01% от дозы выводится почками в виде 25-дезацетилрифаксимина, единственного метаболита рифаксимина, идентифицированного у человека. Выведение почками 14С рифаксимина не превышает 0.4%.
Системная экспозиция нелинейная, дозозависимая, что сопоставимо с всасыванием рифаксимина, возможно, ограниченным скоростью растворения.
Фармакокинетика у особых групп пациентов
Нет клинических данных о применении рифаксимина при почечной недостаточности.
Системная экспозиция у пациентов с печеночной недостаточностью превышает таковую у здоровых добровольцев. Повышение системной экспозиции у этих пациентов следует рассматривать в свете локального действия рифаксимина в кишечнике и его низкой системной биодоступности, а также имеющихся данных по безопасности рифаксимина у пациентов с циррозом печени.
Фармакокинетика рифаксимина у детей не изучалась.
Показания препарата
Альфа Нормикс®
Лечение инфекций ЖКТ, вызываемых бактериями, чувствительными к рифаксимину, в т.ч.:
- острых желудочно-кишечных инфекций;
- диареи путешественников;
- синдрома избыточного роста микроорганизмов в кишечнике;
- при печеночной энцефалопатии;
- при симптоматическом неосложненном дивертикулезном заболевании ободочной кишки;
- при хроническом воспалении кишечника.
Профилактика инфекционных осложнений при колоректальных хирургических вмешательствах.
Режим дозирования
Препарат принимают внутрь, запивая стаканом воды, независимо от приема пищи.
При лечении диареи взрослым и детям старше 12 лет назначают по 200 мг (1 таб. или 10 мл суспензии) каждые 6 ч. Лечение диареи путешественника не должно превышать 3 дней.
При печеночной энцефалопатии взрослым и детям старше 12 лет назначают по 400 мг (2 таб. или 20 мл суспензии) каждые 8 ч.
Для профилактики послеоперационных осложнений при колоректальных хирургических вмешательствах взрослым и детям старше 12 лет назначают по 400 мг (2 таб. или 20 мл суспензии) каждые 12 ч. Профилактику проводят за 3 дня до операции.
При синдроме избыточного бактериального роста взрослым и детям старше 12 лет назначают по 400 мг (2 таб.) каждые 8-12 ч.
При симптоматическом неосложненном дивертикулезе взрослым и детям старше 12 лет назначают по 200-400 мг (1-2 таб. или от 10 до 20 мл суспензии) каждые 8-12 ч.
При хронических воспалительных заболеваниях кишечника взрослым и детям старше 12 лет назначают по 200-400 мг (1-2 таб. или от 10 до 20 мл суспензии) каждые 8-12 ч.
Продолжительность лечения препаратом Альфа Нормикс® не должна превышать 7 дней. Повторный курс лечения следует проводить не ранее чем через 20-40 дней. Общая продолжительность лечения определяется клиническим состоянием пациентов. По рекомендации врача могут быть изменены дозы и частота приема.
Коррекция дозы у пациентов пожилого возраста и у пациентов с печеночной и почечной недостаточностью не требуется.
Правила приготовления суспензии
Гранулы для приготовления суспензии для приема внутрь находятся в герметически закрытом флаконе. Для приготовления суспензии необходимо открыть флакон, добавить воду до метки и хорошо встряхнуть флакон. Добавить воду повторно до тех пор, пока уровень суспензии не достигнет указанной отметки 60 мл.
Концентрация рифаксимина в приготовленной суспензии составляет 100 мг в 5 мл. Перед употреблением суспензию хорошо взболтать. Отмеривать готовую суспензию следует мерной чашечкой, имеющейся в упаковке.
Побочное действие
Побочные эффекты классифицированы по частоте встречаемости следующим образом: очень часто (≥1/10), часто (≥1/100-<1/10), нечасто (≥1/1000-<1/100), редко (≥1/10 000-<1/1000), очень редко (<1/10 000), неизвестно (частота не может быть установлена на основании имеющихся данных).
Со стороны сердечно-сосудистой системы: нечасто — ощущение сердцебиения, приливы крови к коже лица, повышение АД.
Со стороны системы кроветворения: нечасто — лимфоцитоз, моноцитоз, нейтропения; неизвестно — тромбоцитопения.
Со стороны иммунной системы: неизвестно — анафилактические реакции, гиперчувствительность, анафилактический шок, отек гортани.
Метаболические нарушения: нечасто — снижение аппетита, дегидратация.
Со стороны психики: нечасто — патологические сновидения, депрессивное настроение, бессонница, нервозность.
Со стороны нервной системы: часто — головокружение, головная боль; нечасто — гипестезия, мигрень, парестезия, сонливость, боль в области пазух носа; неизвестно — предобморочное состояние, возбуждение.
Со стороны органа зрения: нечасто — диплопия.
Со стороны внутреннего уха: нечасто — боль в ухе, системное головокружение.
Со стороны дыхательной системы: нечасто — одышка, сухость в горле, заложенность носа, боль в ротоглотке, кашель, ринорея.
Со стороны пищеварительной системы: часто — вздутие живота, боль в животе, запор, диарея, метеоризм, тошнота, тенезмы, рвота, позывы на дефекацию; нечасто — боль в верхней половине живота, асцит, диспепсия, нарушение моторики ЖКТ, выделение слизи и крови со стулом, сухость губ, «твердый» стул, повышение активности АСТ, агевзия; неизвестно — изменение печеночных функциональных тестов, изжога.
Со стороны мочевыделительной системы: нечасто — глюкозурия, полиурия, поллакиурия, гематурия, протеинурия.
Со стороны кожи и подкожно-жировой клетчатки: нечасто — сыпь, солнечный ожог; неизвестно — ангионевротический отек, аллергический дерматит, эксфолиативный дерматит, экзема, эритема, зуд, пурпура, крапивница, эритематозная сыпь, эритема ладоней, зуд половых органов.
Со стороны костно-мышечной системы: нечасто — боль в спине, спазм мышц, мышечная слабость, миалгия, боль в шее.
Инфекции: нечасто — кандидоз, простой герпес, назофарингит, фарингит, инфекции верхних дыхательных путей; неизвестно — клостридиальная инфекция.
Со стороны репродуктивной системы: нечасто — полименорея.
Прочие: часто — лихорадка; нечасто — астения, боль и неприятные ощущения неопределенной локализации, озноб, холодный пот, гриппоподобные симптомы, периферические отеки, гипергидроз, отек лица, усталость.
Со стороны лабораторных показателей: изменение МНО.
Противопоказания к применению
- диарея, сопровождающаяся лихорадкой и жидким стулом с кровью;
- кишечная непроходимость (в т.ч. частичная);
- тяжелое язвенное поражение кишечника;
- детский возраст до 12 лет (эффективность и безопасность не установлены);
- наследственная непереносимость фруктозы, нарушение всасывания глюкозы-галактозы, недостаточность сахаразы-изомальтазы (для лекарственной формы гранулы для приготовления суспензии для приема внутрь);
- повышенная чувствительность к рифаксимину или другим рифамицинам или к любому из компонентов, входящих в состав препарата.
С осторожностью: почечная недостаточность, одновременное применение с пероральными контрацептивами, одновременное применение с ингибитором Р-гликопротеина, таким как циклоспорин.
Применение при беременности и кормлении грудью
Данные о применении препарата Альфа Нормикс® при беременности весьма ограничены. Исследования на животных показали преходящее влияние рифаксимина на оссификацию и строение скелета у плода. Клиническая значимость этих результатов неизвестна.
Применение препарата Альфа Нормикс® при беременности не рекомендуется.
Неизвестно, проникает ли рифаксимин в грудное молоко. Нельзя исключить риск для ребенка, находящегося на грудном вскармливании. Для решения вопроса о продолжении приема рифаксимина в период грудного вскармливания необходимо оценить соотношение риска для ребенка и пользы для матери.
Применение при нарушениях функции печени
Коррекция дозы у пациентов с печеночной недостаточностью не требуется.
Применение при нарушениях функции почек
С осторожностью следует применять препарат при почечной недостаточности.
Применение у детей
Противопоказано применение препарата в детском возрасте до 12 лет.
Применение у пожилых пациентов
Коррекция дозы у пациентов пожилого возраста не требуется.
Особые указания
Клинические данные свидетельствуют, что препарат Альфа Нормикс® неэффективен при лечении кишечных инфекций, вызванных Campylobacter jejuni, Salmonella spp., Shigella spp., которые вызывают частую диарею, лихорадку, выделение крови со стулом.
Препарат Альфа Нормикс® не рекомендуется применять, если у пациентов наблюдаются лихорадка и жидкий стул с кровью. Препарат Альфа Нормикс® следует отменить, если симптомы диареи усиливаются или сохраняются более 48 ч. Следует назначить другую антибактериальную терапию. Лечение диареи путешественника не должно превышать 3 дней.
Известно, что Clostridium difficile-ассоциированная диарея, может развиться при применении почти всех антибактериальных средств, включая препарат Альфа Нормикс®. Потенциальную взаимосвязь препарата Альфа Нормикс® с развитием Clostridium difficile-ассоциированной диареи и псевдомембранозного колита нельзя исключить. Опыт применения рифаксимина совместно с другими рифамицинами отсутствует.
Следует соблюдать осторожность при сопутствующем приеме рифаксимина и ингибитора Р-гликопротеина, такого как циклоспорин.
Пациентов необходимо предупредить, что, несмотря на незначительное всасывание рифаксимина (менее 1%), препарат может вызвать окрашивание мочи в красноватый цвет. Это обусловлено активным веществом рифаксимином, который, как и большинство антибиотиков этого ряда (рифамицины), имеет красновато-оранжевую окраску.
При развитии суперинфекции микроорганизмами, нечувствительными к рифаксимину, прием препарата Альфа Нормикс® следует прекратить и назначить соответствующую терапию.
Вследствие влияния препарата Альфа Нормикс® на кишечную флору эффективность пероральных контрацептивов, содержащих эстрогены, может снизиться после его приема. Рекомендуется применять дополнительные меры контрацепции при приеме препарата Альфа Нормикс®, особенно, если содержание эстрогенов в пероральных контрацептивах менее 50 мкг.
Прием препарата Альфа Нормикс® возможен не ранее чем через 2 ч после приема активированного угля.
Гранулы для приготовления суспензии для приема внутрь содержат сахарозу, поэтому препарат Альфа Нормикс® в данной лекарственной форме нельзя применять при наследственной непереносимости фруктозы, нарушении всасывания глюкозы-галактозы, недостаточности сахаразы-изомальтазы.
Влияние на способность к управлению транспортными средствами и механизмами
Хотя головокружение и сонливость наблюдаются при применении препарата Альфа Нормикс®, он не оказывает существенного влияния на способность управлять автотранспортом и заниматься видами деятельности, требующими повышенного внимания и быстроты психомоторных реакций. В случае появления головокружения и сонливости при применении препарата, следует воздержаться от выполнения указанных видов деятельности.
Передозировка
По данным клинических исследований у пациентов с диареей путешественника дозы рифаксимина до 1800 мг/сут хорошо переносились. Даже у пациентов с нормальной бактериальной флорой кишечника рифаксимин в дозе до 2400 мг/сут в течение 7 дней не вызывал неблагоприятных симптомов.
При случайной передозировке показана симптоматическая и поддерживающая терапия.
Лекарственное взаимодействие
Исследования in vitro показывают, что рифаксимин не ингибирует изоферменты системы цитохрома Р450 (CYP1A2, 2А6, 2В6, 2С8, 2С9, 2С19, 2D6, 2Е1 и 3А4) и не индуцирует CYP1A2 и CYP2B6, но является слабым индуктором CYP3A4. Клинические исследования лекарственного взаимодействия свидетельствуют, что у здоровых добровольцев рифаксимин не оказывает значительного влияния на фармакокинетику лекарственных средств, метаболизирующихся с участием CYP3A4. У пациентов с нарушением функции печени нельзя исключить, что рифаксимин может снизить экспозицию лекарственных средств субстратов CYP3A4 (например, варфарин, противоаритмические, противосудорожные средства) при одновременном применении с ними, т.к. при печеночной недостаточности имеет более высокую системную экспозицию по сравнению со здоровыми добровольцами.
У пациентов, продолжающих прием варфарина и рифаксимина, регистрировали снижение и повышение МНО (в некоторых случаях с эпизодами кровотечений). Если совместный прием препаратов необходим, следует проводить тщательный мониторинг МНО в начале и по окончании лечения. Для поддержания желаемого уровня антикоагуляции может понадобиться подбор дозы пероральных антикоагулянтов.
Исследования in vitro позволяют предполагать, что рифаксимин является умеренным субстратом Р-гликопротеина и метаболизируется с помощью изофермента CYP3A4.
Неизвестно, повышают ли системную экспозицию рифаксимина лекарственные средства, которые ингибируют CYP3A4 при одновременном применении с ним.
У здоровых добровольцев совместный прием разовой дозы циклоспорина (600 мг), мощного ингибитора P-гликопротеина, и разовой дозы рифаксимина (550 мг) приводил к 83-кратному и 124-кратному увеличению средних значений Cmax и AUC∞ рифаксимина. Клиническая значимость такого повышения для системного воздействия не известна.
Потенциальное взаимодействие рифаксимина с другими лекарственными средствами, которые выводятся из клетки с помощью Р-гликопротеина или других транспортных белков (MRP2, MRP4, BCRP, BSEP), маловероятны.
Условия хранения препарата Альфа Нормикс®
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°C.
Срок годности препарата Альфа Нормикс®
Срок годности — 3 года. Не применять по истечении срока, указанного на упаковке.
Срок годности готовой к применению суспензии — 7 дней при комнатной температуре не выше 30°C.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
АЛЬФАСИГМА РУС ООО
(Россия)

|
|
125009 Москва, ул. Тверская, д. 22/2, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Буфомикс Изихейлер
МНН: Будесонид, Формотерол
Производитель: Орион Корпорейшн
Анатомо-терапевтическо-химическая классификация: Формотерол в комбинации с другими препаратами
Номер регистрации в РК:
№ РК-ЛС-5№022199
Информация о регистрации в РК:
15.06.2021 — 15.06.2031
Информация о реестрах и регистрах
- Скачать инструкцию медикамента
Торговое название
Буфомикс Изихейлер
Международное непатентованное название
Нет
Лекарственная форма
Порошок для ингаляций 160/4.5 мкг, 60 и 120 доз
Состав
1 ингаляция (доза, выходящая из мундштука) содержит:
активные вещества — будесонид — 160.0 мкг
формотерола фумарата дигидрат — 4.5 мкг,
вспомогательные вещества: лактозы моногидрат.
Описание
Белый или белый с желтоватым оттенком порошок, не содержащий недиспергируемые агломераты.
Фармакотерапевтическая группа
Средства, действующие на респираторную систему. Средства, применяемые при обструктивных заболеваниях дыхательных путей. Адренергические препараты для ингаляционного применения. Адренергические средства в комбинации с кортикостероидами или другими препаратами за исключением антихолинергических средств. Формотерол и будесонид.
Код АТХ R03AK07
Фармакологические свойства
Фармакокинетика
Всасывание
Было показано, что комбинация фиксированных доз Буфомикс Изихейлер (будесонида и формотерола) и Симбикорт Турбухейлер являются биоэквивалентными по сравнению с общим системным воздействием и влиянием через легкие. Было показано, что комбинация фиксированных доз Симбикорт Турбухейлер (будесонида и формотерола) и соответствующие монопрепараты биоэквивалентны по системному воздействию будесонида и формотерола соответственно. Несмотря на это, после введения комбинации фиксированных доз наблюдалось незначительное повышение подавления кортизола по сравнению с монопрепаратами. Считается, что разница не влияет на клиническую эффективность.
Отсутствуют доказательства фармакокинетических взаимодействий между будесонидом и формотеролом.
Фармакокинетические параметры соответствующих веществ были сопоставимы после введения будесонида и формотерола в качестве монопрепаратов или в качестве комбинации фиксированных доз. Для будесонида параметр площади под кривой был немного выше, скорость всасывания больше, а максимальная концентрация в плазме крови выше после введения фиксированной комбинации. Для формотерола максимальная концентрация в плазме крови была подобной после введения фиксированной комбинации.
Ингаляционный будесонид быстро всасывается, а максимальная концентрация в плазме крови достигается в течение 30 минут после ингаляции. В исследованиях среднее попавшего в легких будесонида после ингаляции с помощью порошкового ингалятора менялось от 32% до 44% доставленной дозы. Системная биодоступность составляла примерно 49% доставленной дозы. У детей в возрасте от 6 до 16 лет попадание в легких находится в том же диапазоне, что и у взрослых для той же заданной дозы. Результирующие концентрации в плазме крови не определялись.
Ингаляционный формотерол быстро абсорбируется, а максимальная концентрация в плазме крови достигается в течение 10 минут после ингаляции. В исследованиях среднее попадание в легких формотерола после ингаляции с помощью порошкового ингалятора менялось от 28% до 49% доставленной дозы. Системная биодоступность составляла примерно 61% доставленной дозы.
Распределение и метаболизм
Связывание с белками плазмы составляет около 50% для формотерола и 90% для будесонида. Объем распределения составляет приблизительно 4 л/кг для формотерола и 3 л/кг для будесонида. Формотерол инактивируется в результате реакций конъюгации (формируются активные О-деметилированные и деформулированные метаболиты, однако они преимущественно наблюдаются как инактивированные конъюгаты). Будесонид подвергается значительной (около 90%) биотрансформации при первом прохождении через печень в метаболитов с низкой глюкокортикостероидной активностью. Глюкокортикостероидная активность основных метаболитов — 6-β-гидрокси-будесонида и 16-α-гидрокси-преднизолона — менее 1% от ГКС активности будесонида. Отсутствуют признаки какого-либо метаболических взаимодействий или каких-либо реакций замещения между формотеролом и будесонидом.
Выведение
Большая часть дозы формотерола трансформируется путем печеночного метаболизма, за которым следует вывод через почки. После ингаляции 8-13% доставленной дозы формотерола выводится с мочой в неизмененном виде. Формотерол имеет высокий системный клиренс (примерно 1,4 л/мин.), А период окончательного полувыведения в среднем составляет 17 часов.
Будесонид выводится путем метаболизма, преимущественно под действием катализатора, которым выступает фермент CYP3A4. Метаболиты будесонида выводятся с мочой в чистом виде или в конъюгированной форме. В моче обнаруживаются лишь очень незначительные количества неизменного будесонида. Будесонид имеет высокий системный клиренс (примерно 1,2 л/мин.), а период полувыведения после введения дозы составляет 4 часов.
Фармакокинетика формотерола у детей не изучалась. Фармакокинетика будесонида или формотерола у пациентов с почечной недостаточностью неизвестна. Влияние будесонида и формотерола может повыситься у пациентов с заболеванием печени.
Фармакодинамика
Буфомикс Изихейлер содержит формотерол и будесонид, которые имеют разный способ действия и демонстрируют аддитивные эффекты по уменьшению обострений бронхиальной астмы. Специфические свойства будесонида и формотерола позволяют использовать комбинацию в качестве поддерживающей и облегчающей терапии или в качестве поддерживающей терапии бронхиальной астмы.
Будесонид — это глюкокортикостероид, при ингаляции имеет зависимую от дозы противовоспалительное действие в дыхательных путях, в результате которой уменьшаются симптомы и обострения бронхиальной астмы. Ингаляционный будесонид характеризуется менее тяжелыми побочными эффектами, чем системные кортикостероиды. Точный механизм, ответственный за противовоспалительный эффект глюкокортикостероидов, неизвестен.
Формотерол — это селективный агонист β2-адренорецепторов, который при ингаляции обеспечивает быструю и длительную релаксацию гладкой мускулатуры бронхов у пациентов с обратной обструкцией дыхательных путей. Бронхорасширяющий эффект зависим от дозы и наступает в течение 1-3 минут. Продолжительность эффекта не менее 12 часов после принятия одиночной дозы.
Показания к применению
Бронхиальная астма
Буфомикс Изихейлер показан для регулярного лечения бронхиальной астмы, когда уместно использование комбинации (ингаляционных кортикостероидов и агонистов β2-адренорецепторов длительного действия):
— пациентам, у которых не достигается адекватный контроль с помощью ингаляционных кортикостероидов и агонистов β2-адренорецепторов кратковременной действия «по требованию»,
или
— пациентам, у которых уже достигнут адекватный контроль при применении как ингаляционных кортикостероидов, так и агонистов β2-адренорецепторов длительного действия.
Хроническая обструктивная болезнь легких (ХОБЛ)
— симптоматическое лечение больных тяжелой формой ХОБЛ (объем форсированного выдоха за 1 с <50% от расчетной нормальной величины), имеющих повторные обострения в анамнезе, у которых остаются существенные симптомы, несмотря на регулярное лечение бронходилататорами длительного действия.
Способ применения и дозы
Бронхиальная астма
Буфомикс Изихейлер не предназначен для начального лечения бронхиальной астмы. Дозирование компонентов препарата Буфомикс Изихейлер индивидуален и его следует корректировать в зависимости от тяжести заболевания. Это следует учитывать не только в начале лечения препаратами комбинации, но и при корректировке поддерживающей дозы. Если отдельный пациент нуждается в комбинации доз, которые отличаются от имеющихся в ингаляторе комбинаций, следует прописать соответствующие дозы агонистов β2-адренорецепторов и/или кортикостероидов из отдельных ингаляторов.
Дозу нужно титровать до минимальной дозы, при которой обеспечивается эффективный контроль симптомов. Пациент должен регулярно проходить осмотр у медицинского специалиста/врача, который прописал препарат, чтобы доза Буфомикс Изихейлер оставалась оптимальной. Когда самая низкая рекомендуемая доза позволяет длительное время контролировать симптомы, следующий шаг может включать испытания одного только ингаляционного кортикостероида.
Для препарата Буфомикс Изихейлер есть два варианта лечения:
А. Поддерживающая терапия: Буфомикс Изихейлер принимают в виде регулярного поддерживающего лечения с отдельным быстродействующим бронходилататором в качестве спасательного средства.
В. Поддерживающая и облегчающая терапия: Буфомикс Изихейлер принимают в виде регулярного поддерживающего лечения и по требованию в ответ на появление симптомов.
А. Поддерживающая терапия
Пациента нужно предупредить о необходимости постоянно держать при себе отдельный быстродействующий бронходилататор в качестве спасательного средства.
Рекомендуемые дозы:
Взрослые (18 лет и старше): 1-2 ингаляции дважды в сутки. Некоторым пациентам может потребоваться до 4 ингаляций два раза в сутки (максимальная доза).
Дети
Подростки (12-17 лет): 1-2 ингаляции дважды в сутки.
Дети в возрасте до 12 лет
Буфомикс Изихейлер не рекомендуется детям до 12 лет.
В обычной практике, когда достигается контроль симптомов в режиме дважды в сутки, титрование до минимальной эффективной дозы может включать применение препарата Буфомикс Изихейлер один раз в сутки, когда, по мнению медицинского специалиста, который прописал препарат, для поддержания контроля понадобится бронходилататор длительного действия.
Рост использования отдельного быстродействующего бронходилататора свидетельствует об ухудшении основного заболевания и указывает на необходимость пересмотра терапии бронхиальной астмы.
В. Поддерживающая и облегчающая терапия
Пациенты принимают дневную поддерживающую дозу препарата Буфомикс Изихейлер и дополнительно применяют Буфомикс Изихейлер по требованию в ответ на появление симптомов. Пациентов нужно предупредить о необходимости постоянно держать при себе препарат Буфомикс Изихейлер в качестве спасательного средства.
Поддерживающую и облегчающую терапию следует рассмотреть особенно для пациентов:
• у которых не достигнут адекватный контроль и которые часто требуют облегчающие средства
• у которых в прошлом были обострения бронхиальной астмы, требующие медицинского вмешательства.
Нужно тщательно следить за связанными с дозой побочными эффектами у пациентов, которые часто делают большое количество ингаляций препарата Буфомикс Изихейлер по требованию.
Рекомендуемые дозы:
Взрослые (18 лет и старше): рекомендуемая поддерживающая доза составляет 2 ингаляции в сутки или по одной ингаляции утром и вечером, или 2 ингаляции утром или вечером. Для некоторых пациентов адекватной поддерживающей дозой может быть по две ингаляции дважды в сутки. Пациенты должны сделать 1 дополнительную ингаляцию при необходимости в ответ на появление симптомов. Если симптомы не исчезают через несколько минут, следует сделать еще одну ингаляцию. В каждом отдельном случае разрешается делать не более 6 ингаляций.
Общая суточная доза более 8 ингаляций обычно не требуется, однако в течение ограниченного периода может использоваться общая суточная доза до 12 ингаляций. Пациентам, которые делают более 8 ингаляций в сутки, настоятельно рекомендуется обратиться к врачу.
Нужно провести их повторный осмотр и пересмотреть их поддерживающую терапию.
Дети
Дети и подростки до 18 лет
Для детей и подростков не рекомендуется поддерживающая и облегчающая терапия.
В случае доз, которых невозможно достичь с использованием препарата Буфомикс Изихейлер, в наличии другие дозировки лекарственных средств будесонида/формотерола.
Хроническая обструктивная болезнь легких (ХОБЛ)
Рекомендуемые дозы:
Взрослые: 2 ингаляции дважды в сутки.
Общая информация
Особые категории пациентов:
Отсутствуют особые требования к дозировке для пожилых пациентов. Отсутствуют данные о применении препарата Буфомикс Изихейлер пациентов с печеночной или почечной недостаточностью. Поскольку будесонид и формотерол преимущественно выводятся из организма путем печеночного метаболизма, можно ожидать повышенное воздействие у больных циррозом печени тяжелой степени.
Способ применения:
Для ингаляции.
Инструкции по правильному применению препарата Буфомикс Изихейлер
Ингалятор управляется вдыхаемым потоком воздуха. Это означает, что когда пациент вдыхает воздух через мундштук, вещество попадает в дыхательные пути вместе с вдыхаемым воздухом.
Примечание: важно обратить внимание пациента на следующее:
— внимательно ознакомиться с инструкциями по использованию в листке-вкладыше с информацией для пациента, вложенный в упаковку с каждым препаратом Буфомикс Изихейлер
— стряхивать устройство и приводить его в действие перед каждой ингаляцией
— вдыхать через мундштук достаточно активно и глубоко, чтобы обеспечить поступление в легкие оптимальной дозы вещества
— не выдыхать через мундштук, поскольку это приведет к снижению доставленной дозы. Если это все-таки случилось, необходимо постучать ингалятором по поверхности стола или по ладони руки, чтобы удалить порошок из мундштука, а затем повторить процедуру приема препарата.
— не приводить устройство в действие более одного раза без ингаляции порошка. Если это все-таки случилось, пациенту необходимо постучать ингалятором по поверхности стола или по ладони руки, чтобы удалить порошок из мундштука, а затем повторить процедуру приема препарата.
— всегда ставить на место пылезащитный колпачок (и закрывать защитную крышку, если она используется) после использования ингалятора, чтобы предотвратить случайное распылению порошка из устройства (которое может привести или к передозировке или в ингаляции недостатка препарата при последующем использовании ингалятора)
— промывать рот водой после ингаляции назначенной дозы, чтобы свести к минимуму риск развития кандидоза полости рта. Если возникает кандидоз полости рта, пациенты должны промывать рот водой после ингаляций по требованию.
— регулярно прочищать мундштук сухой тряпочкой. Для очистки нельзя использовать воду, поскольку порошок гигроскопичен.
— заменять ингалятор Буфомикс Изихейлер, когда на счетчике появляется ноль, даже если внутри устройства все еще видны определенное количество порошка.
Побочные действия
Поскольку Буфомикс Изихейлер содержит как будесонид, так и формотерол, может случаться тот же набор побочных эффектов, что характерно для этих двух веществ. После одновременного приема двух соединений не наблюдалось повышения частоты нежелательных реакций. Часто связанные с лекарственным средством нежелательные явления соответствуют фармакологически прогнозируемым побочным эффектам лечения β2-агонистами, такие как тремор и учащенное сердцебиение, обычно незначительны и исчезают через несколько дней. В 3-летнем клиническом исследовании будесонида для лечения ХОБЛ, синяки и пневмония встречались с частотой 10% и 6% соответственно по сравнению с 4% и 3% в группе плацебо (р <0,001 и p <0,01 соответственно).
Ниже по системам органов и частоте развития приведены нежелательные реакции, которые ассоциируют с формотеролом. Частота определяется по следующей шкале: очень часто (> 1/10), часто (> 1/100 до <1/10), нечасто (> 1/1000 дo <1/100), редко (> 1/10000 дo <1 / 1000), очень редко (<1/10000).
Таблица 1
|
Класс системы органов |
Частота |
Нежелательная реакция на лекарственное средство |
|
Инфекционные и паразитарные заболевания |
Часто |
Орофарингеальный кандидоз |
|
Нарушения со стороны имунной системы |
Редко |
Немедленные или замедленные реакции повышенной чувствительности, такие как сыпь, крапивница, зуд, дерматит, ангионевротический отек и анафилактическая реакция |
|
Нарушения со стороны эндокринной системы |
Очень редко |
Синдром Кушинга, угнетение функции коры надпочечников, задержка роста, пониженная минеральная плотность костей |
|
Нарушения со стороны обмена веществ и питания |
Редко |
Гипокалиемия |
|
Очень редко |
Гипергликемия |
|
|
Психические расстройства |
Нечасто |
Агрессия, психомоторная гиперактивность, тревога, нарушения сна |
|
Очень редко |
Депрессия, изменения поведения (преимущественно у детей) |
|
|
Нарушения со стороны нервной системы |
Часто |
Головная боль, тремор |
|
Нечасто |
Головокружение |
|
|
Очень редко |
Нарушение вкуса |
|
|
Нарушения со стороны органа зрения |
Очень редко |
Катаракта и глаукома |
|
Нарушения со стороны сердца |
Часто |
Учащенное серцебиение |
|
Нечасто |
Тахикардия |
|
|
Редко |
Сердечная аритмия, например, фибрилляция предсердий, суправентрикулярная тахикардия, экстрасистолия. |
|
|
Очень редко |
Стенокардия, удлинение интервала QTc |
|
|
Нарушения со стороны сосудов |
Очень редко |
Колебания артериального давления |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Часто |
Умеренное раздражение в горле, кашель, охриплость. |
|
Редко |
Бронхоспазм |
|
|
Нарушения со стороны желудочно-кишечного тракта. |
Нечасто |
Тошнота |
|
Нарушения со стороны кожи и подкожной клетчатки |
Нечасто |
Синяки |
|
Со стороны костно-мышечной и соединительной ткани |
Нечасто |
Мышечные судороги |
Орофарингеальный кандидоз вызванный отложением лекарственных средств. Нужно посоветовать пациенту промывать ротовую полость водой после каждой дозы, чтобы минимизировать риск. Орофарингеальный кандидоз обычно отвечает на местное противогрибковое лечение без необходимости отмены ингаляционных кортикостероидов.
Как и при других видах ингаляционной терапии, в редких случаях может развиться парадоксальный бронхоспазм, который поражает 1 из 10 000. В этом случае у пациента сразу после приема дозы растет хрип и одышка. Парадоксальный бронхоспазм отвечает на быстродействующие ингаляционные бронходилататоры, и лечить его нужно безотлагательно. Нужно немедленно прекратить прием препарата Буфомикс Изихейлер, осмотреть пациента и при необходимости назначить альтернативную терапию.
Системные последствия приема ингаляционных кортикостероидов могут наблюдаться, в частности, при назначении высоких доз на длительный период времени. Эти последствия гораздо менее вероятны, чем последствия приема оральных кортикостероидов. К возможным системным эффектам относятся синдром Кушинга, кушингоидная внешность, адренальная супрессия, задержка роста у детей и подростков, снижение минеральной плотности костей, катаракта, глаукома. Может случаться повышение восприимчивости к инфекциям и ухудшение способности адаптироваться к стрессу. Эти эффекты, вероятно, зависят от дозы, времени воздействия, одновременного или предварительного приема стероидов и индивидуальной чувствительности.
Лечение β2-агонистами может привести к повышению уровня инсулина, свободных жирных кислот, глицерина и кетоновых тел в крови.
Дети
Рекомендуется регулярно контролировать рост у детей, которые получают длительное лечение ингаляционными кортикостероидами.
Противопоказания
— повышенная чувствительность к будесониду, формотеролу или лактозе (которая содержит небольшое количество молочного белка)
— непереносимость фруктозы, дефицит фермента Lapp-лактазы, мальабсорбция глюкозы-галактозы
— детский возраст до 12 лет
Лекарственные взаимодействия
Фармакокинетические взаимодействия
Мощные ингибиторы CYP3A4 (кетоконазол, итраконазол, вориконазол, посаконазол, кларитромицин, телитромицин, нефазодон и ингибиторы протеазы ВИЧ) с большой вероятностью могут увеличить уровни будесонида в плазме крови, поэтому следует избегать их одновременного применения. Если это невозможно, интервалы между приемами взаимодействующих препаратов следует устанавливать максимально большими (см. п.4.4). Для пациентов, которые применяют мощные ингибиторы CYP3A4, поддерживающая и облегчающая терапия не рекомендуется.
Мощный ингибитор CYP3A4 кетоконазол в дозе 200 мг один раз в сутки повышает уровни будесонида в плазме крови, что принимается одновременно перорально (одиночная доза 3 мг) в среднем в шесть раз. Когда кетоконазол принимали через 12 часов после будесонида, концентрация в среднем увеличивалась только в три раза, что свидетельствует о том, что разделение времени введения может снизить повышению в плазме крови. Ограниченные данные об этом взаимодействии высоких доз ингаляционного будесонида указывают на то, что может произойти существенное повышение уровней в плазме крови (в среднем в четыре раза) при одновременном приеме с ингаляционным будесонидом (одиночная доза 1000 мкг) итраконазола в дозе 200 мг один раз в сутки.
Фармакодинамические взаимодействия
Бета-адреноблокаторы могут ослабить или подавить эффект формотерола. Поэтому Буфомикс Изихейлер не следует применять вместе с β-адреноблокаторами (в том числе глазными каплями), если отсутствуют неоспоримые причины для их применения.
Одновременное лечение хинидином, дизопирамидом, прокаинамидом, фенотиазины, антигистаминными препаратами (терфенадином), ингибиторами МАО и трициклическими антидепрессантами может удлинять интервал QTc и повышать риск развития желудочковой аритмии.
Кроме того, леводопа, левотироксин, окситоцин и алкоголь могут ухудшить толерантность сердца к β2-симпатомиметиков.
Одновременное лечение ингибиторами МАО, в том числе средствами с подобными свойствами, такими как фуразолидон и прокарбазин, может вызывать гипертонические реакции.
Риск развития аритмий увеличивается на фоне проведения анестезии препаратами галогенизированных углеводородов.
Одновременное применение других β-адренергетикив или антихолинергических препаратов потенциально может усилить бронхорасширяющий эффект.
Гипокалиемия может повысить склонность к сердечной аритмии у пациентов, которые лечатся гликозидами наперстянки.
Не наблюдалось взаимодействия будесонида и формотерола с какими другими лекарствами, которые используются для лечения бронхиальной астмы.
Дети
Изучения взаимодействия препарата с другими лекарственными препаратами представлены только для взрослых.
Особые указания
Рекомендуется постепенно снижать дозу при отказе от препарата и не делать резкого прекращения приема.
Если пациенты обнаруживают, что лечение неэффективно, или превышают наивысшую рекомендованную дозу препарата Буфомикс Изихейлер, им следует обратиться к врачу. Внезапное и прогрессивное ухудшение контроля бронхиальной астмы или ХОБЛ потенциально опасное для жизни, поэтому пациент должен немедленно пройти медицинское обследование. В таком случае следует рассмотреть необходимость в усилении терапии кортикостероидами, например, курс оральных кортикостероидов или лечения антибиотиками при наличии инфекции.
Пациентов нужно предупредить о необходимости постоянно держать при себе свой спасательный ингалятор — или Буфомикс Изихейлер (для больных бронхиальной астмой, которые используют Буфомикс Изихейлер в качестве поддерживающей и облегчающей терапии), или отдельный быстродействующий бронходилататор (для всех пациентов, которые используют Буфомикс Изихейлер только в качестве поддерживающей терапии).
Пациентам следует напомнить, что необходимо принимать поддерживающую дозу препарата Буфомикс Изихейлер в соответствии с рецептом, даже при отсутствии симптомов. Профилактическое использование препарата Буфомикс Изихейлер, например, перед физической нагрузкой, не изучали. Облегчающие ингаляции препарата Буфомикс Изихейлер нужно делать в ответ на симптомы бронхиальной астмы, при этом они не предназначены для регулярного профилактического применения, например, перед физической нагрузкой. Для каждого использования следует рассмотреть отдельный быстродействующий бронходилататор.
Только симптомы бронхиальной астмы взяты под контроль, следует рассмотреть вопрос постепенного снижения дозы препарата Буфомикс Изихейлер. Важно регулярно осматривать пациентов по мере снижения дозы. Используйте самую низкую эффективную дозу препарата Буфомикс Изихейлер.
Не следует начинать лечение препаратом Буфомикс Изихейлер при обострениях или значительного ухудшения или резкого осложнения бронхиальной астмы.
Во время лечения Буфомикс Изихейлер могут возникать серьезные связанные с бронхиальной астмой нежелательные явления и обострения. Пациентам нужно сообщить о необходимости продолжения лечения и одновременного обращения к врачу, если симптомы бронхиальной астмы не контролируются или ухудшаются после начала приема препарата Буфомикс Изихейлер.
Как и при других видах ингаляционной терапии, существует риск развития парадоксального бронхоспазма. В этом случае у пациента сразу после приема дозы растет хрип и одышка. Если у пациента возникает парадоксальный бронхоспазм, нужно немедленно прекратить прием препарата Буфомикс Изихейлер, осмотреть пациента и при необходимости назначить альтернативную терапию. Парадоксальный бронхоспазм отвечает на быстродействующие ингаляционные бронходилататоры, и лечить его нужно безотлагательно.
Системные последствия приема ингаляционных кортикостероидов могут наблюдаться, в частности, при назначении высоких доз на длительный период времени. Эти последствия гораздо менее вероятны, чем последствия приема оральных кортикостероидов. К возможным системным эффектам относятся синдром Кушинга, кушингоидная внешность, адренальная супрессия, задержка роста у детей и подростков, снижение минеральной плотности костей, катаракта, глаукома и, гораздо реже, различные психологические и поведенческие отклонения, включая психомоторную гиперактивность, нарушения сна, тревогу, депрессию или агрессивность (особенно у детей).
У детей, получающих длительную терапию ингаляционными кортикостероидами, рекомендуется регулярно измерять рост. Если рост замедляется, следует пересмотреть схему лечения с целью снижения дозы ингаляционного кортикостероида, по возможности, в минимальной, обеспечивающей сохранение эффективного контроля течения бронхиальной астмы. Следует тщательно взвесить преимущества лечения кортикостероидами и возможные риски для подавления роста. Кроме того, необходимо направить пациента к педиатру-пульмонологу.
Ограниченные данные длительных исследований свидетельствуют о том, что большинство детей и подростков, проходящих лечение ингаляционным будесонидом, в конце концов достигают целевого роста во взрослом возрасте. При этом наблюдалось изначально не большое временное снижение роста (примерно на 1 см). В общем оно случается в течение первого года лечения.
Следует рассмотреть потенциальное влияние на плотность костей, особенно у пациентов, принимающих высокие дозы в течение длительного периода времени и в которых параллельно есть факторы риска развития остеопороза. Длительные исследования ингаляционного будесонида на детях при среднесуточных дозах 400 мкг (отмеренная доза) или на взрослых при суточных дозах 800 мкг (отмеренная доза) не показали существенного влияния на минеральную плотность костей. Отсутствует информация о влиянии высоких доз.
Если есть основания предполагать ухудшение функции коры надпочечников через предварительную системную стероидную терапию, следует быть осторожным при переводе пациентов на терапию препаратом Буфомикс Изихейлер.
Преимущества терапии ингаляционным будесонидом обычно минимизируют потребность в оральных стероидах, однако пациенты, которые переходят с оральных стероидов могут продолжать находиться под угрозой снижения резерва коры надпочечников в течение длительного времени. Восстановление может занять много времени после прекращения терапии оральными стероидами, поэтому пациенты, зависимые от терапии оральными стероидами, которые переводятся на ингаляционный будесонид, могут длительное время оставаться под угрозой пониженного резерва коры надпочечников. В таком случае нужно регулярно контролировать функцию «гипоталамус — гипофиз — кора надпочечников».
Длительное лечение высокими дозами ингаляционных кортикостероидов, особенно выше рекомендованных доз, может привести к клинически существенному угнетению функции коры надпочечников. Поэтому в стрессовые периоды, такие как тяжелые инфекции и плановые операции, нужно рассмотреть дополнительное системное лечение кортикостероидами. Быстрое снижение дозы стероидов может спровоцировать острую недостаточность функции коры надпочечников. Симптомы и признаки, которые можно наблюдать при острой недостаточности функции коры надпочечников, могут быть несколько нечеткими, однако к ним может относиться анорексия, боль в животе, потеря веса, усталость, головная боль, тошнота, рвота, пониженный уровень сознания, припадки, гипотония и гипогликемия.
Лечение дополнительными системными стероидами или ингаляционным будесонидом нельзя резко прекращать.
При переводе с приема оральных препаратов на Буфомикс Изихейлер наблюдается общее низкое системное действие стероидов, что может привести к появлению аллергических или артритических симптомов, таких как ринит, экземы, боли в мышцах и суставах. В этом случае нужно начать специфическое лечение. Следует подозревать общий недостаточный эффект глюкокортикостероидов, если в отдельных случаях появляются такие симптомы, как усталость, головная боль, тошнота и рвота. В таких случаях иногда требуется временно увеличить дозу оральных глюкокортикостероидов.
С целью уменьшения риска развития орального кандидоза пациентам нужно тщательно промывать полость рта водой после ингаляции поддерживающей дозы. В случае появления орального кандидоза пациенты должны промывать ротовую полость водой также после ингаляций по требованию.
Следует избегать одновременного лечения итраконазолом, ритонавиром или другими мощными ингибиторами CYP3A4. Если это невозможно, интервалы между приемами взаимодействующих препаратов следует устанавливать максимально большими. Для пациентов, которые применяют мощные ингибиторы CYP3A4, поддерживающая и облегчающая терапия не рекомендуется.
Следует с осторожностью назначать Буфомикс Изихейлер пациентам с тиреотоксикозом, феохромацитомою, сахарным диабетом, нелеченной гипокалиемией, гипертрофической обструктивной кардиомиопатией, идиопатический подклапанный аортальным стенозом, тяжелой гипертензией, аневризмой или другими тяжелыми сердечно-сосудистыми расстройствами, такими как ишемическая болезнь сердца, тахиаритмия и тяжелая сердечная недостаточность.
Следует соблюдать осторожность при лечении пациентов с удлиненным интервалом QTc. Сам формотерол может вызвать удлинение интервала QTc.
У пациентов с активной или неактивной формой туберкулеза легких, грибковой и вирусной инфекцией в дыхательных путях нужно провести повторную оценку потребности и дозы ингаляционных кортикостероидов.
При лечении высокими дозами агонистов β2-адренорецепторов может развиваться потенциально опасная для жизни гипокалиемия. Возможный гипокалиемический эффект агонистов β2-адренорецепторов может усиливаться при одновременном лечении агонистами β2-адреноцепторов с лекарственными средствами, которые могут вызывать гипокалиемию или усиливать гипокалиемический эффект, например, производными ксантинов, стероидами и диуретиков. Особенно осторожными нужно быть при нестабильной бронхиальной астме при непостоянном использовании спасательных бронходилататоров, при острой тяжелой бронхиальной астме, так как связанный с этим риск может усиливаться гипоксией, а также в других состояниях, когда повышается риск гипокалиемии. В этих случаях рекомендуется контролировать уровень калия в сыворотке крови.
Как и для всех агонистов β2-адренорецепторов, у больных сахарным диабетом рекомендуется проводить дополнительный контроль концентрации глюкозы в крови.
Буфомикс Изихейлер содержит примерно 4 мг лактозы на одну ингаляцию. Обычно такое количество не вызывает проблем у лиц, страдающих от непереносимости лактозы. Вспомогательное вещество лактоза содержит небольшое количество молочных белков, которые могут вызвать аллергические реакции.
Дети
У детей, получающих длительную терапию ингаляционными кортикостероидами, рекомендуется регулярно измерять рост. Если рост замедляется, следует пересмотреть схему лечения с целью снижения дозы ингаляционного кортикостероида, по возможности, в минимальной, обеспечивающей сохранение эффективного контроля течения бронхиальной астмы. Следует тщательно взвесить преимущества лечения кортикостероидами и возможные риски для подавления роста. Кроме того, необходимо направить пациента к педиатру-пульмонологу.
Ограниченные данные длительных исследований свидетельствуют о том, что большинство детей и подростков, проходящих лечение ингаляционным будесонидом, в конце концов достигают целевого роста во взрослом возрасте. При этом наблюдалось изначально не большое временное снижение роста (примерно на 1 см). В общем оно случается в течение первого года лечения.
Беременность
Для препарата Буфомикс Изихейлер или одновременного лечения формотеролом и будесонидом отсутствуют клинические данные о влиянии на беременность. Данные исследования развития эмбриона-плода у крыс не продемонстрировали никакого дополнительного эффекта комбинации.
Отсутствуют достаточные данные об использовании формотерола у беременных женщин. В исследованиях на животных формотерол вызвал побочные эффекты в исследованиях влияния на репродуктивную систему при очень высоких уровнях системного воздействия.
Данные примерно с 2000 исследованных случаев беременности не показали повышенного тератогенного риска, связанного с использованием ингаляционного будесонида. В исследованиях на животных было показано, что ГКС вызывают пороки развития . Это — маловероятно для людей, которые получают рекомендуемые дозы.
В исследованиях на животных также было выявлено влияние чрезмерного количества перинатальных глюкокортикоидов на повышенный риск внутриматочной задержки роста, сердечно-сосудистые заболевания взрослых, необратимое изменение плотности рецепторов глюкокортикоидов, оборота нейромедиаторов и поведение при концентрациях, ниже диапазона тератогенных доз.
Во время беременности Буфомикс Изихейлер следует применять только, если ожидаемая польза превосходит потенциальный риск. Нужно использовать самую низкую эффективную дозу будесонида, необходимую для поддержания адекватного контроля бронхиальной астмы.
Период лактации
Будесонид переходит в грудное молоко. Однако при терапевтических дозах не ожидается никакого влияния на ребенка, находящегося на грудном вскармливании. Неизвестно, переходит ли формотерол в грудное молоко. В материнском молоке крыс было обнаружено небольшое количество формотерола. Прием препарата Буфомикс Изихейлер женщинами, которые кормят грудью, следует рассматривать только, если ожидаемая польза для матери превышает возможный риск для плода.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Буфомикс Изихейлер не имеет никакого влияния на способность управлять транспортными средствами и использовать машины или этим влиянием можно пренебречь.
Передозировка
Симптомы: передозировка формотеролом с большой вероятностью сопровождается симптомами, которые обычно наблюдаются при передозировке агонистами β2-адренорецепторов: тремором, головной болью, учащенным сердцебиением. В отдельных случаях сообщалось о таких симптомах, как тахикардия, гипергликемия, гипокалиемия, удлинение интервала QTc, аритмия, тошнота и рвота. Доза 90 мкг, принятая в течение трех часов у пациентов с острой бронхиальной обструкцией, не вызывала проблем с безопасностью.
При острой передозировке будесонида, даже при чрезмерных дозах, клинические проблемы не ожидаются. При хроническом использования чрезмерных доз могут появляться глюкокортикостероидные эффекты, такие как гиперкортицизм и подавление функции коры надпочечников.
Если терапию препаратом Буфомикс Изихейлер нужно прекратить из-за передозировки формотеролом компонентом лекарственного средства, нужно рассмотреть обеспечение соответствующей терапии ингаляционными кортикостероидами.
Лечение: Может быть показано поддерживающее и симптоматическое лечение.
Форма выпуска и упаковка
По 60 доз или 120 доз в ингаляторе с защитным колпачком в ламинированном пакете.
По 1 ламинированному пакету и защитному контейнеру для ингалятора вместе с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке.
По 60 доз или 120 доз в ингаляторе с защитным колпачком в ламинированном пакете.
По 1 ламинированному пакету вместе с инструкцией по медицинскому применению на государственном и русском языках в картонной коробке.
Условия хранения
При температуре не выше 25 ºС в защищенном от влаги месте.
Хранить в недоступном для детей месте!
Срок хранения
2 года
После вскрытия алюминиевого пакета использовать в течение 4 месяцев.
Не применять по истечении срока годности.
Условия отпуска
По рецепту
Производитель
Орион Корпорейшн
Орионинтие 1, 02200 Эспоо, Финляндия
Владелец регистрационного удостоверения
Орион Корпорейшн
Орионинтие 1, 02200 Эспоо, Финляндия
Наименование и адрес организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей; ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «ORION PHARMA EAST (ОРИОН ФАРМА ИСТ)»
050000, г. Алматы, ул. Толе Би, дом 69, офис 19.
Тел.: 8 (727) 272-61-10, 272-61-11
Факс: 8(727) 272-62-09
Электронная почта: assel.alshynbayeva@orionpharma.com
| 615735351477976220_ru.doc | 144.5 кб |
| 781151781477977481_kz.doc | 186.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
