Эральфон — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛСР-000971/10
Торговое наименование препарата
Эральфон®
Международное непатентованное наименование
Эпоэтин альфа
Лекарственная форма
раствор для внутривенного и подкожного введения
Состав
1 шприц (0,3 мл) содержит в качестве активного вещества эпоэтин альфа (эритропоэтин человека рекомбинантный) 3000 ME или 5000 ME.
Вспомогательные вещества: альбумина раствор в пересчете на сухой альбумин — 0,75 мг, натрия цитрата пентасесквигидрат — 1,74 мг или натрия цитрата дигидрат — 1,4328 мг, натрия хлорид — 1,752 мг, лимонной кислоты моногидрат — 0,0171 мг, вода для инъекций — до 0,3 мл.
1 шприц (0,5 мл) содержит в качестве активного вещества эпоэтин альфа (эритропоэтин человека рекомбинантный) 20000 ME.
Вспомогательные вещества: альбумина раствор в пересчете на сухой альбумин 1,25 мг, натрия цитрата пентасесквигидрат — 2,9 мг или натрия цитрата дигидрат — 2,388 мг, натрия хлорид — 2,92 мг, лимонной кислоты моногидрат — 0,0285 мг , вода для инъекций — до 0,5 мл.
1 шприц (0,6 мл) содержит в качестве активного вещества эпоэтин альфа (эритропоэтин человека рекомбинантный) 20000 ME.
Вспомогательные вещества: альбумина раствор в пересчете на сухой альбумин — 1,5 мг, натрия цитрата пентасесквигидрат- 3,48 мг или натрия цитрата дигидрат — 2,8656 мг, натрия хлорид — 3,504 мг, лимонной кислоты моногидрат — 0,0342 мг, вода для инъекций — до 0,6 мл.
Описание
прозрачная бесцветная жидкость.
Фармакотерапевтическая группа
гемопоэза стимулятор
Код АТХ
B03XA
Фармакодинамика:
Эпоэтин альфа — гликопротеид, специфически стимулирующий эритропоэз, активирует митоз и созревание эритроцитов из клеток-предшественников эритроцитарного ряда. Рекомбинантный эпоэтин альфа синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий человеческий эритропоэтин. По своему составу, биологическим и иммунологическим свойствам эпоэтин альфа идентичен природному эритропоэтину человека. Введение эпоэтина альфа приводит к повышению уровней гемоглобина и гематокрита, улучшению кровоснабжения тканей и работы сердца. Наиболее выраженный эффект от применения эпоэтина альфа наблюдается при анемиях, обусловленных хронической почечной недостаточностью. В очень редких случаях, при длительном применении эритропоэтина для терапии анемических состояний может наблюдаться образование нейтрализующих антител к эритропоэтину с развитием парциальной красноклеточной аплазии или без неё.
Фармакокинетика:
При внутривенном введении эпоэтина альфа у здоровых лиц и больных с уремией период полувыведения составляет 5-6 ч. При подкожном введении эпоэтина альфа его концентрация в крови нарастает медленно и достигает максимума в период от 12 до 18 ч после введения, период полувыведения составляет 16-24 часа. Биодоступность эпоэтина альфа при подкожном введении составляет 25-40%. Не кумулирует.
Показания:
— анемия у больных с хронической почечной недостаточностью, в том числе, находящихся на гемодиализе;
— профилактика и лечение анемий у больных с солидными опухолями, анемия у которых стала следствием проведения противоопухолевой терапии;
— профилактика и лечение анемий у больных инфицированных вирусом иммунодефицита человека (ВИЧ), вызванных применением зидовудина, при концентрации эндогенного эритропоэтина менее 500 МЕ/мл;
— профилактика и лечение анемий у больных с миеломной болезнью, неходжскинскими лимфомами низкой степени злокачественности, хроническим лимфолейкозом;
— в рамках предепозитной программы перед обширным хирургическим вмешательством у больных с уровнем гематокрита, равным 33-39%, для облегчения сбора аутологичной крови и уменьшения риска, связанного с использованием аллогенных гемотрансфузий, если ожидаемая потребность в переливаемой крови превышает количество, которое можно получить методом аутологичного сбора без применения эпоэтина альфа;
— перед проведением обширной операции с ожидаемой кровопотерей 900-1800 мл у взрослых пациентов, не имеющих анемии или с легкой и средней степенью анемии (концентрация гемоглобина 100-130 г/л) для уменьшения потребности в аллогенных гемотрансфузиях и облегчения восстановления эритропоэза.
Противопоказания:
— повышенная чувствительность к препарату или его компонентам;
— парциальная красноклеточная аплазия после ранее проведенной терапии каким-либо эритропоэтином;
— неконтролируемая артериальная гипертензия;
— невозможность проведения адекватной антикоагулянтной терапии;
— при тяжелых окклюзионных заболеваниях коронарных, сонных, мозговых и периферических артерий и их последствиях, включая острый и недавно перенесенный инфаркт миокарда и острое нарушение мозгового кровообращения (в рамках предепозитной программы сбора крови перед хирургическими операциями).
С осторожностью:
Злокачественные новообразования, эпилептический синдром (в т.ч. при наличии в анамнезе), тромбоцитоз, тромбоз (в анамнезе), серповидно-клеточная анемия, железо-, В12- или фолиеводефицитные состояния, порфирия, хроническая печеночная недостаточность
Беременность и лактация:
Так как нет достаточного опыта применения эритропоэтина при беременности и лактации у человека, эпоэтин альфа следует назначать только в том случае, если ожидаемые преимущества от его применения для матери превышают возможный риск для плода. Неизвестно, выделяется ли эпоэтин альфа с грудным молоком, поэтому при лечении препаратом Эральфон® необходимо прекратить грудное вскармливание.
Способ применения и дозы:
Лечение анемии у больных с хронической почечной недостаточностью
Взрослые пациенты, находящиеся на гемодиализе
Эральфон® вводят подкожно или внутривенно в конце сеанса диализа. При изменении способа введения препарат вводят в прежней дозе, затем, дозу при необходимости корректируют (при подкожном способе введения препарата, для достижения одинакового терапевтического эффекта требуется доза на 20-30% меньше, чем при внутривенном введении). Лечение препаратом включает два этапа:
Этап коррекции: при подкожном введении препарата начальная разовая доза составляет 30 МЕ/кг 3 раза в неделю. При внутривенном введении препарата начальная разовая доза составляет 50 МЕ/кг. Период коррекции длится до момента достижения оптимального содержания гемоглобина (100-120 г/л у взрослых и 95-110 г/л у детей) и гематокрита (30-35 %). Эти показатели необходимо контролировать еженедельно.
Возможны следующие ситуации:
1) Гематокрит повышается от 0,5 до 1,0% в неделю. В этом случае дозу не изменяют до достижения оптимальных показателей.
2) Скорость прироста гематокрита менее 0,5% в неделю. В этом случае необходимо повышение разовой дозы в 1,5 раза.
3) Скорость прироста более 1,0% в неделю. В этом случае необходимо снизить разовую дозу препарата в 1,5 раза.
4) Гематокрит остается низким или снижается. Необходимо проанализировать причины резистентности.
Эффективность терапии зависит от правильно подобранной индивидуальной схемы лечения.
1. Этап поддерживающей терапии: для поддержания гематокрита на уровне 30-35% дозу препарата, применяемую на этапе коррекции следует уменьшить в 1,5 раза. Затем поддерживающую дозу препарата подбирают индивидуально, с учетом динамики показателей гематокрита и гемоглобина.
При подкожном введении недельную дозу можно вводить за 1 прием или делить на 3 введения в неделю. При стабилизации состояния на фоне введения 1 раз в неделю можно перейти на введение 1 раз в 2 недели, в этом случае может понадобиться увеличение дозы.
У детей, находящихся на гемодиализе, начальная разовая доза составляет 50 МЕ/кг 3 раза в неделю подкожно или внутривенно. При необходимости разовую дозу повышают 1 раз в 4 нед на 25 МЕ/кг до достижения оптимальной концентрации гемоглобина. Поддерживающая разовая доза у детей с массой тела менее 10 кг — 75-150 МЕ/кг (в среднем 100 МЕ/кг), 10-30 кг — 60-150 МЕ/кг (в среднем 75 МЕ/кг), более 30 кг — 30-100 МЕ/кг (в среднем 33 МЕ/кг) 3 раза в неделю.
Взрослым преддиализным пациентам начальная доза вводится подкожно или внутривенно 3 раза по 50 МЕ/кг в неделю. При необходимости разовую дозу увеличивают один раз в 4 нед на 25 МЕ/кг до достижения оптимальной концентрации гемоглобина. Поддерживающая доза — 17- 33 МЕ/кг 3 раза в неделю подкожно или внутривенно.
Профилактика и лечение анемии у больных с солидными опухолями
Перед началом лечения рекомендуется провести определение концентрации эндогенного эритропоэтина. При концентрации эритропоэтина в сыворотке крови менее 200 МЕ/мл, начальная разовая доза препарата составляет при внутривенном способе введения 150 МЕ/кг 3 раза в неделю. Если через 4 недели лечения концентрация гемоглобина повысилась и составляет не менее 10 г/л или количество ретикулоцитов увеличилось более чем на 40 000 клеток/мкл свыше исходного значения, то доза препарата остается прежней (150 МЕ/кг массы тела). Если через 4 недели лечения повышение концентрации гемоглобина составляет менее 10 г/л и повышение количества ретикулоцитов составляет менее 40 000 клеток/мкл по сравнению с исходным, то в течение следующих 4 недель дозу увеличивают до 300 МЕ/кг массы тела. Если после дополнительных 4 недель лечения при дозе препарата 300 МЕ/кг концентрация гемоглобина повысилась и составляет не менее 10 г/л или количество ретикулоцитов увеличилось более чем на 40 000 клеток/мкл, то сохраняют существующую дозу препарата (300 МЕ/ кг массы тела). Если через 4 недели лечения в дозе 300 МЕ/кг массы тела концентрация гемоглобина повышается менее чем на 10 г/л и повышение количества ретикулоцитов составляет менее 40 000 клеток/мкл по сравнению с исходным, лечение следует прекратить. В случае повышения концентрации гемоглобина более чем на 20 г/л в течение месяца, дозу препарата необходимо уменьшить на 25%. Если концентрация гемоглобина превышает 140 г/л, необходимо приостановить лечение до снижения концентрации ниже 120 г/л и затем продолжить введение препарата в дозе на 25% ниже первоначальной.
Терапия препаратом должна продолжаться в течение одного месяца после окончания курса химиотерапии.
Содержание ферритина сыворотки необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости дополнительно назначается препарат железа.
Профилактика и лечение анемии у больных с ВИЧ инфекцией
Рекомендуется до начала лечения препаратом Эральфон® определить исходное содержание эндогенного эритропоэтина в сыворотке крови. Проведенные исследования показывают, что при содержании эритропоэтина более 500 МЕ/мл эффект от терапии препаратом маловероятен.
1. Этап коррекции: препарат назначается в разовой дозе 100 МЕ/кг 3 раза в неделю подкожно или внутривенно в течение 8 недель. Если по истечении 8 недель терапии не удалось достичь удовлетворительного эффекта (например, снизить потребность в гемотрансфузиях или добиться повышения концентрации гемоглобина), доза может поэтапно увеличиваться (не чаще, чем 1 раз в 4 недели) на 50-100 МЕ/кг 3 раза в неделю. Если не удалось достигнуть удовлетворительного эффекта от терапии препаратом Эральфон® в разовой дозе 300 МЕ/кг 3 раза в неделю, то появление ответа на дальнейшую терапию в более высоких дозах маловероятно.
2. Этап поддерживающей терапии: после достижения удовлетворительного эффекта в фазе коррекции анемии поддерживающая доза должна обеспечить гематокрит в пределах 30-35% в зависимости от изменения дозы зидовудина, наличия сопутствующих инфекционных или воспалительных заболеваний. При гематокрите более 40%, следует прекратить введение препарата до снижения гематокрита до 36%. При возобновлении терапии доза эпоэтина альфа должна быть снижена на 25% с последующей корректировкой для поддержания требуемого гематокрита. Содержание ферритина сыворотки необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости дополнительно назначается препарат железа.
Профилактика и лечение анемии у больных с миеломной болезнью, неходжскинскими лимфомами низкой степени злокачественности и с хроническим лимфолейкозом
У этих больных целесообразность лечения эпоэтином альфа обусловливается неадекватным синтезом эндогенного эритропоэтина на фоне развития анемии. При концентрации гемоглобина ниже 100 г/л и содержания эритропоэтина в сыворотке крови ниже 100 МЕ/мл Эральфон® вводят подкожно в стартовой разовой дозе 100 МЕ/кг три раза в неделю. Лабораторный контроль гемодинамических показателей проводят еженедельно. При необходимости дозу препарата корректируют в сторону увеличения или уменьшения каждые 3-4 недели. Если при достижении недельной дозы 600 МЕ/кг увеличение концентрации гемоглобина не наблюдается, дальнейшее применение эпоэтина альфа следует отменить как неэффективное.
Взрослые пациенты, участвующие в программе сбора аутологичной крови перед хирургическими вмешательствами
Рекомендуется использовать внутривенное введение препарата. Эпоэтин альфа следует вводить по окончании процедуры сбора крови. Перед назначением препарата следует учесть все противопоказания к сбору аутологичной крови. Перед хирургическим вмешательством Эральфон® следует назначать 2 раза в неделю в течение 3 недель. При каждом посещении врача у больного забирают порцию крови (если гематокрит >33% и/или концентрация гемоглобина >110 г/л) и сохраняют для аутологичной трансфузии. Рекомендуемая разовая доза препарата Эральфон® — 600 МЕ/кг массы тела 2 раза в неделю.
Содержание ферритина сыворотки необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости дополнительно назначается препарат железа. При наличии анемии ее причина должна быть установлена до начала терапии эпоэтином альфа. Необходимо в кратчайшие сроки обеспечить адекватное поступление железа в организм, назначив препарат железа в дозе 200 мг/сут (из расчета на элементарное железо) и поддерживать поступление железа на данном уровне в течение всего курса терапии.
Пациенты в пред- и послеоперационном периоде, не участвующие в программе сбора аутологичной крови
Рекомендуется использовать подкожное введение препарата в дозе 600 МЕ/кг массы тела в неделю в течение 3 недель, предшествующих операции (21-й, 14-й и 7-й дни перед операцией), и в день операции. При необходимости, когда по медицинским показаниям необходимо сократить предоперационный период, Эральфон® можно назначать ежедневно в дозе 300 МЕ/кг массы тела в течение 10 дней до операции, в день операции и в течение 4 дней после операции. Если концентрация гемоглобина в предоперационном периоде достигает 150 г/л и выше, применение эпоэтина альфа следует прекратить. До начала терапии эпоэтином альфа необходимо убедиться в отсутствии у пациентов дефицита железа.
Все пациенты должны получать адекватное количество железа (200 мг/сут из расчета на элементарное железо) на протяжении всего курса лечения. По возможности следует обеспечить дополнительное поступление железа до начала терапии эпоэтином альфа для обеспечения адекватного депо железа в организме больного.
Указания по применению
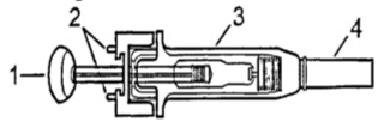
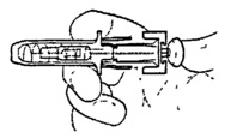
Устройство и порядок работы шприца с автоматическим устройством защиты иглы
1.Перед инъекцией
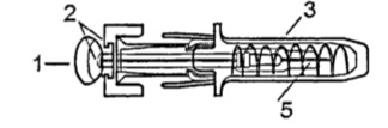
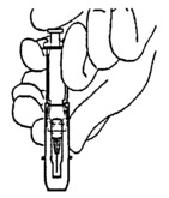
2. После инъекции
Составные части:
Шток
Зажимы
Защитный кожух
Защитный колпачок
Игла
После завершения инъекции игла и шприц переместятся назад в защитное устройство.
Внимание! Избегайте контакта с зажимами в течение подготовки шприца! Устройство активируется путем нажатия на шток до зажимов.
1.
Внимательно осмотрите преднаполненный стеклянный шприц с защитным устройством. Снимите защитный колпачок с иглы.
2.
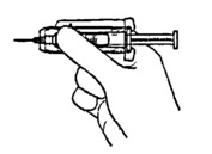
Проведите инъекцию согласно стандартной процедуре.
3.
Нажмите на шток большим пальцем и удерживайте до тех пор, пока вся доза препарата не будет введена. Защитное устройство не активируется, пока вся доза препарата не будет введена.
4.
Извлеките иглу, отпустите шток, позвольте защитному кожуху переместится вперед до тех пор пока игла полностью не будет защищена и заблокирована на месте
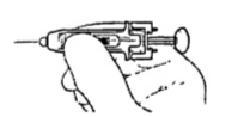
Порядок работы шприца с неавтоматическим устройством защиты иглы
1.
Проведите инъекцию согласно стандартной процедуре. Внимание! При проведении инъекции держите пальцы на защитном кожухе, чтобы предотвратить преждевременную активацию защитного устройства.
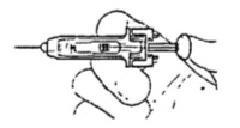
2.
После инъекции переместите защитное устройство вдоль иглы. Звуковой щелчок укажет на правильность действия. Во время всей процедуры пальцы должны находиться позади иглы.
Побочные эффекты:
В начале лечения может отмечаться гриппоподобная симптоматика: головокружение, сонливость, лихорадочное состояние, головная боль, миалгия, артралгия.
Со стороны сердечно-сосудистой системы: дозозависимое повышение артериального давления, ухудшение течения артериальной гипертензии (чаще всего у пациентов с хронической почечной недостаточностью), в отдельных случаях — гипертонический криз, резкое повышение артериального давления с симптомами энцефалопатии (головная боль, спутанность сознания) и генерализованными тонико-клоническими судорогами.
Со стороны органов кроветворения: тромбоцитоз, в отдельных случаях — тромбозы шунта или артериовенозной фистулы (у пациентов на гемодиализе со склонностью к артериальной гипотензии или с аневризмой, стенозом и т.д.), парциальная красноклеточная аплазия.
Аллергические реакции: кожная сыпь (слабо или умеренно выраженная), экзема, крапивница, зуд, ангионевротический отек.
Местные реакции: гиперемия, жжение, слабая или умеренная болезненность в месте введения (чаще возникают при подкожном введении).
Со стороны лабораторных показателей: снижение концентрации ферритина в сыворотке, при уремии — гиперкалиемия, гиперфосфатемия.
Прочие: осложнения, связанные с нарушением дыхания или со снижением артериального давления, иммунные реакции (индукция образования антител), обострение порфирии.
Передозировка:
Симптомы: усиление побочных эффектов.
Лечение: симптоматическое. При высокой концентрации гемоглобина — кровопускание.
Взаимодействие:
Снижает концентрацию циклоспорина из-за увеличения степени связывания его с эритроцитами (может возникнуть необходимость в коррекции дозы циклоспорина). Фармацевтически несовместим с растворами других лекарственных средств.
Особые указания:
Во время лечения необходимо еженедельно контролировать артериальное давление и проводить общий анализ крови (включая подсчет тромбоцитов), определение гематокрита и содержания ферритина в сыворотке крови. В пред- и послеоперационном периоде концентрацию гемоглобина следует контролировать чаще, если исходная концентрация составляла менее 140 г/л. Необходимо помнить, что эпоэтин альфа при лечении анемии не заменяет гемотрансфузию, но снижает необходимость ее повторного применения.
У больных с контролируемой артериальной гипертензией или тромботическими осложнениями в анамнезе может потребоваться повышение дозы гипотензивных лекарственных средств и/или антикоагулянтов соответственно.
При назначении пациентам с печеночной недостаточностью возможно замедление метаболизма эпоэтина альфа и выраженное усиление эритропоэза. Безопасность применения препарата у этой категории пациентов не установлена.
Хотя препарат стимулирует эритропоэз, нельзя полностью исключить возможность воздействия эпоэтина альфа на рост некоторых типов опухолей, в т.ч. костного мозга.
Следует учитывать возможность того, что предоперационное повышение концентрации гемоглобина может служить предрасполагающим фактором к развитию тромботических осложнений. Перед проведением планового хирургического вмешательства пациенты должны получать адекватную профилактическую антиагрегантную терапию. В пред- и послеоперационном периоде препарат не рекомендуют назначать пациентам с исходным уровнем гемоглобина более 150 г/л.
У взрослых пациентов с хронической почечной недостаточностью, клинически выраженной ишемической болезнью сердца или хронической сердечной недостаточностью концентрация гемоглобина не должна превышать 100-120 г/л.
Перед началом лечения следует исключить возможные причины неадекватной реакции на препарат (дефицит железа, фолиевой кислоты, цианокобаламина, тяжелое отравление солями алюминия, сопутствующие инфекции, воспалительные процессы и травмы, скрытые кровотечения, гемолиз, фиброз костного мозга различной этиологии) и при необходимости скорректировать лечение.
До начала лечения следует оценить запасы железа в организме. У большинства больных с хронической почечной недостаточностью, у онкологических и ВИЧ-инфицированных пациентов концентрация ферритина в плазме уменьшается одновременно с увеличением уровня гематокрита. Концентрацию ферритина необходимо определять в течение всего курса лечения. Если она составляет менее 100нг/мл, рекомендуется заместительная терапия препаратами железа для приема внутрь из расчета 200-300 мг/сут (100-200 мг/сут для детей). Недоношенным детям пероральная терапия препаратами железа в дозе 2 мг/сутки должна назначаться как можно раньше. Пациенты, сдающие аутологичную кровь и находящиеся в пред- или послеоперационном периоде, должны также получать адекватное количество железа внутрь в дозе 200 мг/сут.
У пациентов с хронической почечной недостаточностью коррекция анемии может вызвать улучшение аппетита и увеличение всасывания калия и белков. Может потребоваться периодическая коррекция параметров диализа для поддержания концентрации мочевины, креатинина и калия в пределах нормы.
У пациентов с хронической почечной недостаточностью необходимо контролировать содержание электролитов в сыворотке крови.
По имеющимся данным, применение эпоэтина альфа у преддиализных пациентов может предупреждать прогрессирование хронической почечной недостаточности. Из-за повышения гематокрита часто требуется увеличить дозу гепарина во время гемодиализа. При неадекватной гепаринизации возможны закупорка диализной системы, тромбоз сосудистого доступа, особенно у больных с тенденцией к гипотензии или с осложнениями артериовенозной фистулы (стеноз, аневризма и др.). У таких больных рекомендуется профилактика тромбозов.
При применении у женщин репродуктивного возраста с анемией на фоне хронической почечной недостаточности возможно возобновление менструаций. Пациентку следует предупредить о возможности наступления беременности и необходимости применения надежных методов контрацепции до начала терапии. В экспериментальных исследованиях на крысах и кроликах не обнаружено тератогенное действие при внутривенном введении в дозах до 500 ЕД/кг массы тела в сутки; в более высоких дозах отмечено слабое, статистически незначимое снижение фертильности.
В период лечения, до установления оптимальной поддерживающей дозы, пациентам с хронической почечной недостаточностью, необходимо соблюдать осторожность при вождении автотранспорта и занятии другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (увеличение риска повышения артериального давления в начале терапии).
Учитывая возможный более выраженный эффект препарата, его доза не должна превышать дозу рекомбинантного эритропоэтина, использовавшегося в предыдущем курсе лечения. В течение первых двух недель дозу не изменяют, оценивают соотношение доза/ответ. После этого доза может быть уменьшена или увеличена (см. раздел «Способ применения и дозы»).
Форма выпуска/дозировка:
Раствор для внутривенного и подкожного введения 3000 ME, 5000 ME или 20 000 ME.
Упаковка:
По 0,3 мл 3000 ME; по 0,3 мл 5000 ME; по 0,5 мл или но 0,6 мл 20 000 ME в шприцы с дополнительным автоматическим или неавтоматическим устройством для защиты иглы после использования шприца или без него.
По 1 или 3 шприца помещают в контурную ячейковую упаковку с покрытием.
1 или 2 контурные ячейковые упаковки с инструкцией по применению помещают в пачку из картона.
Пачка с двух сторон заклеивается наклейками из самоклеящегося материала для контроля вскрытия.
Условия хранения:
При температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Срок годности:
2 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
Закрытое акционерное общество «ФармФирма «Сотекс» (ЗАО «ФармФирма «Сотекс»), 141345, Московская обл., Сергиево-Посадский муниципальный район, сельское поселение Березняковское, пос. Беликово, д. 10, д. 11, д. 12, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ЗАО «ФармФирма «Сотекс»
Купить Эральфон в Планета Здоровья
Купить Эральфон в ГорЗдрав
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакологическое действие
Рекомбинантный эритропоэтин человека, представляет собой очищенный гликопротеин. Стимулирует эритропоэз. Синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий эритропоэтин человека. По биологическим и иммунологическим свойствам идентичен эритропоэтину человека, выделяемому из мочи. Синтез эндогенного эритропоэтина осуществляется в почках и зависит от уровня оксигенации крови.
Фармакокинетика
После п/к введения концентрация активного вещества в плазме повышается медленно, достигая максимального уровня через 12-18 ч.
После многократного в/в введения T1/2 у взрослых здоровых пациентов составляет 4 ч, у пациентов с почечной недостаточностью — около 6 ч; у детей — около 6 ч.
Показания активного вещества
ЭПОЭТИН АЛЬФА
Лечение анемии, связанной с хронической почечной недостаточностью у взрослых и детей, находящихся на гемо- или перитонеальном диализе.
Профилактика и лечение анемии у онкологических больных (получающих или не получающих химиотерапию) при немиелоидных опухолях.
Лечение анемии у ВИЧ-инфицированных пациентов, получающих терапию зидовудином, (при уровне эндогенного эритропоэтина ≤ 500 МЕ/мл).
В рамках предепозитной программы перед обширной хирургической операцией у пациентов с уровнем гематокрита 33-39%, для облегчения сбора аутологичной крови и уменьшения риска, связанного с использованием аллогенных гемотрансфузий (при ожидаемой потребности в переливаемой крови выше, чем количество, которое можно получить без применения эпоэтина альфа).
Перед проведением обширной операции с ожидаемой средней кровопотерей (2-4 единицы или 900-1800 мл) у взрослых пациентов с легкой или средней анемией (гемоглобин >10 и ≤13 г/дл) для уменьшения потребности в аллогенных гемотрансфузиях и улучшения восстановления эритропоэза.
Режим дозирования
Вводят п/к или в/в. Режим дозирования устанавливают индивидуально, в зависимости от показаний, наличия сопутствующих заболеваний, схемы терапии, возраста пациента.
Побочное действие
Со стороны системы кроветворения: редко — тромбоцитемия, парциальная красноклеточная аплазия (ПККА), опосредованная через антитела к эритропоэтину.
Со стороны иммунной системы: нечасто — реакции повышенной чувствительности; редко — анафилактические реакции.
Со стороны обмена веществ: нечасто — гиперкалиемия; редко — порфирия.
Со стороны нервной системы: часто — головная боль; нечасто — судороги; частота неизвестна — инсульт, включающий церебральный инфаркт и внутримозговое кровоизлияние, транзиторная ишемическая атака, гипертоническая энцефалопатия.
Со стороны органа зрения: частота неизвестна — тромбоз сосудов сетчатки.
Со стороны сердечно-сосудистой системы: часто — венозные или артериальные тромбозы, артериальная гипертензия; частота неизвестна — гипертонический криз.
Со стороны дыхательной системы: часто — кашель; нечасто — застойные явления в дыхательных путях.
Со стороны пищеварительной системы: очень часто — диарея, тошнота, рвота.
Со стороны кожи и подкожных тканей: часто — кожная сыпь; нечасто — крапивница; частота неизвестна — ангионевротический отек.
Со стороны костно-мышечной системы: часто — артралгия, миалгия, боль в костях, боль в конечностях.
Прочие: очень часто — повышение температуры тела; часто — озноб, гриппоподобный синдром, периферические отеки, положительный тест на антитела к эритропоэтину, местные реакции.
Противопоказания к применению
Повышенная чувствительность к эпоэтину альфа; неконтролируемая артериальная гипертензия, парциальная красноклеточная аплазия (ПККА), возникшая после лечения эритропоэтином; пациенты, которые по каким-либо причинам не могут получать эффективное лечение для профилактики тромбозов; пациентам с тяжелой патологией коронарных, сонных, мозговых и периферических сосудов, включая недавно перенесших инфаркт миокарда или острое нарушение мозгового кровообращения (в рамках предепозитной программы сбора крови перед обширной хирургической операцией); беременность, период грудного вскармливания.
С осторожностью
Злокачественные новообразования, эпилептический синдром (в т.ч. в анамнезе), артериальная гипертензия, хроническая печеночная недостаточность, тромбоцитоз, тромбоз (в анамнезе), острая кровопотеря, серповидно-клеточная, гемолитическая анемия, дефицит железа, В12 или фолиевой кислоты, облитерирующие заболевания периферических сосудов и другие сосудистые осложнения, подагра, порфирии, ИБС.
Применение при беременности и кормлении грудью
Противопоказано применение эпоэтина альфа при беременности за исключением тех случаев, когда предполагаемая польза для матери значительно превышает риск для плода. Применение эпоэтина альфа не рекомендовано в период беременности пациенткам, участвующим в программе сбора аутологичной крови перед проведением хирургических операций.
При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания. Применение эпоэтина альфа не рекомендовано у кормящих матерей, участвующих в программе сбора аутологичной крови перед проведением хирургических операций.
Применение при нарушениях функции печени
С осторожностью следует применять у пациентов с хронической печеночной недостаточностью.
Применение при нарушениях функции почек
У пациентов с хронической почечной недостаточностью и клинически выраженной ИБС или застойной сердечной недостаточностью поддерживающий уровень гемоглобина не должен превышать верхний предел оптимального рекомендованного уровня (не более 10-12 г/дл у взрослых).
Применение у детей
Возможно применение у детей по показаниям, в рекомендуемых дозах и схемах.
Особые указания
Эпоэтин альфа следует с осторожностью применять у пациентов с эпилепсией, наличием судорожных припадков в анамнезе или состояниями, предрасполагающими к повышению судорожной готовности, такими как инфекции ЦНС или метастатическое поражение головного мозга.
Увеличение частоты развития тромботических осложнений наблюдалось у пациентов, получающих препараты, стимулирующие эритропоэз. Осложнения включают в себя тромбозы вен и артерий (в т.ч. летальные случаи), такие как тромбоз глубоких вен, эмболию легочной артерии, тромбоз сетчатки глаза и инфаркт миокарда. Также отмечались случаи острого нарушения мозгового кровоснабжения (включая ишемический инсульт, геморрагический инсульт и транзиторную ишемическую атаку). Пациентам с повышенным риском развития тромбоза или других сосудистых осложнений требуется тщательный медицинский контроль.
С осторожностью применяют при подагре.
До начала применения следует убедиться, что пациенты с артериальной гипертензией получали эффективную антигипертензивную терапию.
На фоне применения необходимо контролировать уровень АД, обращая внимание на возникновение или усиление необычных головных болей. При этом может потребоваться коррекция проводимой терапии или назначение антигипертензивных средств. Если несмотря на адекватную терапию АД не снижается, эпоэтин альфа следует отменить.
До начала применения эпоэтина альфа следует оценить состояние депо железа в организме. У большинства больных с хронической почечной недостаточностью, у онкологических и ВИЧ-инфицированных больных уровень ферритина в плазме крови уменьшается одновременно с увеличением гематокрита. Уровень ферритина необходимо определять в течение всего курса лечения. Если он составляет менее 100 нг/мл, рекомендуется заместительная терапия препаратами железа. Пациенты, сдающие аутологичную кровь и находящиеся в пред- или послеоперационном периоде, также должны получать дополнительно адекватное количество железа.
В период применения следует контролировать уровень гемоглобина, по крайней мере, 1 раз в неделю до достижения стабильного уровня, затем несколько реже.
С осторожностью следует применять у пациентов с порфирией. При хронической почечной недостаточности на фоне терапии эпоэтином альфа возможно обострение порфирии.
Пациентам, находящимся на гемодиализе, на фоне терапии эпоэтином альфа часто требуется увеличение дозы гепарина во время диализа из-за повышения гематокрита. При неадекватной дозе гепарина возможна окклюзия диализной системы.
У пациентов с хронической почечной недостаточностью и клинически выраженной ИБС или застойной сердечной недостаточностью поддерживающий уровень гемоглобина не должен превышать верхний предел оптимального рекомендованного уровня (не более 10-12 г/дл у взрослых).
При применении у пациентов с нарушениями функции печени возможно замедление биотрансформации эпоэтина альфа и выраженное усиление эритропоэза.
Нельзя полностью исключить возможность влияния эпоэтина альфа на рост некоторых типов опухолей, особенно на злокачественные новообразования костного мозга.
Следует соблюдать все специальные предупреждения и меры предосторожности, связанные с программой сбора аутологичной крови (это распространяется на всех пациентов, получающих эпоэтин альфа).
Терапевтическая эффективность эпоэтина альфа может уменьшиться при дефиците железа, фолиевой кислоты, витамина B12, интоксикации алюминием, интеркуррентных заболеваниях, скрытом кровотечении, гемолизе, фиброзе костного мозга.
Влияние на способность к управлению транспортными средствами и механизмами
При применении эпоэтина альфа до установления оптимальной поддерживающей дозы пациентам с ХПН следует избегать занятий потенциально опасными видами деятельности из-за увеличения риска развития артериальной гипертензии в начале терапии.
Лекарственное взаимодействие
Действие эпоэтина альфа может усиливаться при одновременном введении препаратов крови.
Одновременное применение препаратов, подавляющих эритропоэз, может приводить к снижению эффективности эпоэтина альфа.
При одновременном применении эпоэтина альфа с циклоспорином возможно снижение концентрации последнего в плазме из-за увеличения степени его связывания с эритроцитами (при применении данной комбинации необходимо контролировать концентрацию циклоспорина в плазме и при необходимости увеличить его дозу).
Эпоэтин альфа нельзя смешивать с растворами других лекарственных средств.
Эпоэтин альфа
Epoetin alfa
Фармакологическое действие
Эпоэтин альфа — препарат, стимулирующий эритропоэз, активирует митоз, стимулирует образование эритроцитов из клеток-предшественников эритроцитарного ряда. Очищенный гликопротеин, синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий эритропоэтин человека. По биологическим и иммунологическим свойствам идентичен эритропоэтину человека, выделяемому из мочи. Приводит к повышению гематокрита и гемоглобина, улучшению кровоснабжения тканей и работы сердца. Наиболее выраженный эффект при анемиях, обусловленных хроническими заболеваниями почек. Повышение показателя гематокрита проявляется через 4 недели после начала лечения.
Фармакокинетика
Биодоступность при подкожном введении — 25 %, время достижения максимальной плазменной концентрации (TCmax) — 12–18 часов; после подкожного введения Cmax (максимальная концентрация в плазме крови) значительно ниже, чем после внутривенного. Период полувыведения (T½) — 16–24 часа при подкожном введении и 5–6 часов при внутривенном. Не кумулирует.
Показания
Анемия (для профилактики и лечения): при хронической почечной недостаточности у взрослых и детей, в том числе находящихся на гемо- или перитонеальном диализе, а также у преддиализных пациентов; у ВИЧ-инфицированных пациентов на фоне лечения зидовудином (при концентрации эндогенного эритропоэтина 500 ME/мл или менее); при немиелоидных опухолях (в том числе на фоне цитостатической терапии).
Подготовка пациентов к операции с ожидаемой массивной кровопотерей (2–4 единицы или 900–1 800 мл) без анемии, а также с лёгкой или средней анемией (гемоглобин 100–130 г/л) для уменьшения потребности в аллогенных гемотрансфузиях и улучшения эритропоэза.
Подготовка пациентов с гематокритом 33–39 % к обширным хирургическим вмешательствам в рамках предепозитной программы для облегчения сбора аутологичной крови и уменьшения риска, связанного с использованием аллогенных гемотрансфузий (при ожидаемой потребности в переливаемой крови выше, чем количество, которое можно получить без применения эпоэтина альфа).
Противопоказания
Гиперчувствительность; парциальная красноклеточная аплазия после ранее проведённой терапии каким-либо эритропоэтином, неконтролируемая артериальная гипертензия; невозможность проведения адекватной антикоагулянтной терапии, беременность, период лактации.
В рамках предепозитной программы сбора крови перед хирургическими операциями — тяжёлые окклюзионные заболевания коронарных, сонных, мозговых и периферических артерий и их последствия (в том числе острый и недавно перенесённый инфаркт миокарда и острое нарушение мозгового кровообращения).
С осторожностью
Злокачественные новообразования, эпилептический синдром (в том числе в анамнезе, эпилепсия), тромбоцитоз, тромбоз (в анамнезе), серповидно-клеточная анемия, железо-, B12— или фолиеводефицитные состояния, порфирия, печёночная недостаточность, облитерирующие заболевания периферических сосудов и другие сосудистые осложнения, подагра.
Беременность и грудное вскармливание
Категория действия на плод по FDA — C.
Надлежащие контролируемые исследования применения эпоэтина альфа у женщин во время беременности не проводились. По результатам исследований на животных выявлена репродуктивная токсичность. Вследствие этого, пациенткам с хронической почечной недостаточностью следует применять эпоэтин альфа во время беременности, только если предполагаемая польза для матери значительно превышает риск для плода. Применение эпоэтина альфа не рекомендовано в период беременности или лактации пациентам, участвующим в программе сбора аутологичной крови перед хирургической операцией.
Способ применения и дозы
Подкожно или внутривенно.
Разовая доза 30–100 ЕД/кг, кратность введения и длительность применения устанавливаются индивидуально.
Побочные действия
Гриппоподобная симптоматика (в начале лечения)
Головокружение, сонливость, лихорадочное состояние, головная боль, миалгия, артралгия.
Аллергические реакции
Кожная сыпь (слабо или умеренно выраженная), экзема, крапивница, зуд, ангионевротический отёк.
Со стороны сердечно-сосудистой системы
Дозозависимое повышение артериального давления, ухудшение течения артериальной гипертензии (чаще всего у пациентов с хронической почечной недостаточностью), в отдельных случаях — гипертонический криз, резкое повышение артериального давления с симптомами энцефалопатии (головная боль, спутанность сознания) и генерализованными тонико-клоническими судорогами.
Со стороны органов кроветворения
Тромбоцитоз, в отдельных случаях — тромбозы шунта (у пациентов на гемодиализе со склонностью к артериальной гипотензии или с аневризмой, стенозом и т.д.), аплазия эритроцитарного ростка.
Местные реакции
Гиперемия, жжение, слабая или умеренная болезненность в месте введения (чаще возникают при подкожном введении введении).
Со стороны лабораторных показателей
Снижение концентрации ферритина в сыворотке, при уремии — гиперкалиемия, гиперфосфатемия.
Прочие
Осложнения, связанные с нарушением дыхания или со снижением артериального давления; иммунные реакции (индукция образования антител), обострение порфирии.
Передозировка
Симптомы
Возможно усиление дозозависимых побочных эффектов.
Лечение
Проведение симптоматической терапии. При высоком гемоглобине и гематокрите показано кровопускание.
Взаимодействие
При одновременном применении эпоэтина альфа с циклоспорином повышается связывание последнего с эритроцитами (может потребоваться коррекция дозы циклоспорина, требуется дополнительный контроль концентрации циклоспорина в крови с возможной последующей коррекцией его дозы.
На основании имеющегося к настоящему времени опыта клинического применения эпоэтина альфа не выявлено фактов его фармакологической несовместимости с другими лекарственными препаратами.
Тем не менее, во избежание возможной несовместимости или снижения активности эпоэтина альфа его нельзя смешивать с растворами других лекарственных препаратов.
Меры предосторожности
Во время лечения необходимо еженедельно контролировать артериальное давление и проводить общий анализ крови (включая тромбоциты, гематокрит, ферритин).
В пред- и послеоперационном периоде гемоглобин следует контролировать чаще, если исходный составлял менее 140 г/л. Необходимо помнить, что эпоэтин альфа при лечении анемии не заменяет гемотрансфузию, но снижает необходимость её повторного применения. У больных с контролируемой артериальной гипертензией или тромботическими осложнениями в анамнезе может потребоваться повышение дозы гипотензивных средств и антикоагулянтов соответственно.
При назначении пациентам с печёночной недостаточностью возможно замедление метаболизма эпоэтина альфа и выраженное усиление эритропоэза. Безопасность применения препарата у этой категории пациентов не установлена.
Хотя препарат стимулирует эритропоэз, нельзя полностью исключить возможность воздействия эпоэтина альфа на рост некоторых типов опухолей, в том числе костного мозга.
Следует учитывать возможность того, что предоперационное повышение геиоглобина может служить предрасполагающим фактором к развитию тромботических осложнений. Перед проведением планового хирургического вмешательства пациенты должны получать адекватную профилактическую антиагрегантную терапию. В пред- и послеоперационном периоде не рекомендуют назначать пациентам с исходным гемоглобином более 150 г/л. У взрослых пациентов с хронической почечной недостаточностью и клинически выраженной ишемической болезнью сердца или хронической сердечной недостаточностью гемоглобин не должен превышать 100–120 г/л.
Перед началом лечения следует исключить возможные причины неадекватной реакции на препарат (дефицит железа, фолиевой кислоты, цианокобаламина, тяжёлое отравление алюминием, сопутствующие инфекции, воспалительные процессы и травмы, скрытые кровотечения, гемолиз, фиброз костного мозга различной этиологии) и при необходимости скорректировать лечение. До начала лечения следует оценить запасы железа в организме.
У большинства больных с хронической почечной недостаточностью, у онкологических и ВИЧ-инфицированных пациентов концентрация ферритина в плазме уменьшается одновременно с увеличением гематокрита. Концентрацию ферритина необходимо определять в течение всего курса лечения. Если она составляет менее 100 нг/мл, рекомендуется заместительная терапия препаратами железа для приёма внутрь из расчёта 200–300 мг/сут (100–200 мг/сут для детей). Пациенты, сдающие аутологичную кровь и находящиеся в пред- или послеоперационном периоде, должны также получать адекватное количество железа внутрь в дозе 200 мг/сут.
У пациентов с хронической почечной недостаточностью коррекция анемии может вызвать улучшение аппетита и увеличение всасывания калия и белков. Может потребоваться периодическая коррекция параметров диализа для поддержания концентрации мочевины, креатинина и K+ в пределах нормы.
У пациентов с хронической почечной недостаточностью необходимо контролировать электролиты в сыворотке крови. По имеющимся данным, применение эпоэтина альфа у преддиализных пациентов не ускоряет прогрессирование хронической почечной недостаточности.
Из-за повышения гематокрита часто требуется увеличить дозу гепарина во время гемодиализа. При неадекватной гепаринизации возможны закупорка диализной системы, тромбоз шунтов, особенно у больных с тенденцией к гипотензии или с осложнениями артериовенозной фистулы (стеноз, аневризма и др.). У таких больных рекомендуется ранняя ревизия шунта и своевременная профилактика тромбозов (например, ацетилсалициловая кислота).
Применение при беременности и в период лактации возможно только в тех случаях, когда потенциальная польза для матери превышает потенциальный риск для плода. Неизвестно, выделяется ли эпоэтин альфа с грудным молоком. При применении у женщин репродуктивного возраста с анемией на фоне хронической почечной недостаточности возможно возобновление менструаций. Пациентку следует предупредить о возможности наступления беременности и необходимости применения надёжных методов контрацепции до начала терапии. В экспериментальных исследованиях на крысах и кроликах не обнаружено тератогенное действие при внутривенном введении в дозах до 500 ЕД/кг массы тела в сутки; в более высоких дозах отмечено слабое, статистически незначимое снижение фертильности.
При исследовании хронической токсичности (на крысах и собаках) эпоэтина альфа выявлено развитие субклинического фиброза тканей костного мозга. В ходе 13 недельного исследования у собак, которым подкожно или внутривенно вводили препарат в дозе 80, 240 или 520 ЕД/кг/сут, развилась анемия без или с признаками гипоплазии костного мозга. В связи с тем что, эпоэтин альфа является гликопротеином человека, признано, что эти изменения могли быть вызваны действием антител к эпоэтину альфа. Аналогичные явления отмечались в отдельных случаях при использовании препарата в ветеринарной практике и объяснялись появлением антител к эпоэтину альфа.
Исследований канцерогенности не проводилось.
Эпоэтин альфа не вызывает мутаций генов у бактерий (тест Эймса), хромосомных аберраций в клетках млекопитающих, микронуклии у мышей, а также мутаций генов в локусе HGRT.
Пациентов можно переводить с одного стимулятора на другой только по согласованию с лечащим врачом.
Влияние на способность к вождению автотранспорта и управлению механизмами
В период лечения, до установления оптимальной поддерживающей дозы пациентам с хронической почечной недостаточностью, необходимо соблюдать осторожность при управлении транспортными средствами и занятии др. потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (увеличение риска повышения артериального давления в начале терапии).
Классификация
-
АТХ
B03XA01
-
Фармакологическая группа
-
Коды МКБ 10
-
Категория при беременности по FDA
C
(риск не исключается)
Информация о действующем веществе Эпоэтин альфа предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Эпоэтин альфа, содержатся в инструкции производителя, прилагаемой к упаковке.
МНН: Эпоэтин альфа
Производитель: ИДТ Биологика ГмбХ
Анатомо-терапевтическо-химическая классификация: Erythropoietin
Номер регистрации в РК:
№ РК-ЛС-5№021025
Информация о регистрации в РК:
05.09.2019 — бессрочно
Информация о реестрах и регистрах
- Скачать инструкцию медикамента
Торговое название
Бинокрит®
Международное непатентованное название
Эпоэтин альфа
Лекарственная форма
Раствор для инъекций 1000 МЕ/0.5 мл, 2000 МЕ/1.0 мл, 40000 МЕ/1.0 мл
Описание
Прозрачный бесцветный раствор
Состав
Один шприц содержит
активное вещество — эпоэтин альфа (HX575) — 1000 МЕ (8.4 мкг) или
2000 МЕ (16.8 мкг) или 40000 МЕ (336 мкг),
вспомогательные вещества: натрия дигидрофосфата дигидрат, динатрия гидрофосфата дигидрат, натрия хлорид, глицин, полисорбат 80, кислота хлороводородная 0.1 М, натрия гидроксида 0.1 М раствор, вода для инъекций.
Фармакотерапевтическая группа
Препараты влияющие на кроветворение и кровь.
Прочие стимуляторы гемопоэза. Эритропоэтин.
Код АТХ В03ХА01
Фармакологические свойства
Фармакокинетика
АбсорбцияБиодоступность эпоэтина альфа при подкожном введении значительно ниже, чем при внутривенном введении, и составляет около 20%.
Выведение
Внутривенный путь введения
Период полувыведения после многократного внутривенного введения составляет около 4 часов у здоровых добровольцев и около 5 часов у пациентов с почечной недостаточностью. У детей период полувыведения составляет около 6 часов.
Подкожный путь введения
После подкожного введения, концентрации эпоэтина альфа в сыворотке крови значительно ниже уровней, чем после внутривенного введения; концентрация эпоэтина альфа повышается медленно и достигает максимального значения через 12-18 часов после подкожного введения. Максимальная концентрация после подкожного введения ниже максимальной концентрации после внутривенного введения (около 1/20 от концентрации после внутривенного введения).
Кумуляции активного вещества не происходит: через 24 часа после первой инъекции и через 24 часа после последней инъекции наблюдаются одинаковые уровни концентрации.
При подкожном пути введения трудно оценить период полувыведения, и он оценивается примерно в 24 часа.
Фармакодинамика
Лекарственное средство Бинокрит является биосимиляром инновационного препарата эпоэтина альфа.
Эпоэтин альфа, активное вещество представляет собой рекомбинантный человеческий эритропоэтин получаемый с помощью технологии рекомбинантной ДНК из клеток яичника китайского хомячка (СНО). Эпоэтин альфа представляет собой гликопротеин, который по своему аминокислотному и углеводному составу не отличается от человеческого эритропоэтина, который был изолирован из мочи пациентов, страдающих анемией.
Эритропоэтин является гликопротеином, который как митоз-стимулирующий фактор и дифференцирующий гормон стимулирует образование эритроцитов из стволовых клеток-предшественников.
Средняя молекулярная масса эритропоэтина составляет 32000-40000 дальтон. Белковая фракция составляют около 58% молекулярной массы, состоит из 165 аминокислот. Четыре углеводных цепи связаны с белком посредством трех N-гликозидных и одной О-гликозидной связи.
Бинокрит имеет максимально высокую степень очистки в соответствии с современными технологическими возможностями. В частности, не обнаруживаются следовые количества клеток продуцентов (СНО) активного вещества.
Эритропоэтин является фактором роста, который преимущественно стимулирует образование эритроцитов. Рецепторы к эритропоэтину могут присутствовать на поверхности различных опухолевых клеток.
После введения эпоэтина альфа число эритроцитов, ретикулоцитов, концентрация гемоглобина и скорость поглощения 59Fe возрастают. Исследования на культуре клеток костного мозга человека показали, что эпоэтин альфа специфически стимулирует эритропоэз и не оказывает влияние на лейкопоэз. Не было обнаружено цитотоксического действия эпоэтина альфа на клетки костного мозга.
Показания к применению
— лечение симптоматической анемии, связанной с хронической почечной
недостаточностью (ХПН), у взрослых и детей с 1 года:
-
анемии, связанной с хронической почечной недостаточностью у детей и взрослых, получающих гемодиализ и взрослых пациентов, получающих перитонеальный диализ
-
тяжелые формы анемии почечного генеза, сопровождающиеся
клиническими симптомами у взрослых пациентов с почечной недостаточностью без диализа
— лечение анемии у взрослых пациентов, получающих химиотерапию солидных опухолей, злокачественной лимфомы или множественной миеломы, для которых переливание крови имеет высокий риск при таких состояниях как, патология сердечно-сосудистой системы или наличие анемии в начале химиотерапии, как альтернатива гемотрансфузиям
— умеренно выраженная анемия у взрослых пациентов, не имеющих дефицита железа (уровень гемоглобина 10-13 г/дл или 6.2-8.1 ммоль/л), перед плановой ортопедической операцией, при наличии высокого риска осложнений при проведении гемотрансфузии.
Способ применения и дозы
Лечение лекарственным средством Бинокрит должно назначаться под контролем врачей, имеющих опыт лечения пациентов с вышеуказанными показаниями.
Лечение симптоматической анемии у взрослых и детей с хронической почечной недостаточностью (ХПН)
Пациентам с хронической почечной недостаточностью Бинокрит должен вводиться в виде внутривенной инъекции.
Симптомы и осложнения анемии могут варьировать в зависимости от возраста, пола и общей тяжести заболевания; необходимо проведение врачом оценки индивидуального клинического течения заболевания и состояния пациента.
Рекомендуемый диапазон концентрации гемоглобина находится между 10 г/дл до 12 г/дл (6,2 до 7,5 ммоль/л).
Бинокрит должен вводиться в виде внутривенной инъекции для увеличения уровня гемоглобина не выше 12 г/дл (7.5 ммоль/л).
Следует избегать повышения уровня гемоглобина более чем на 2 г/дл (1.25 ммоль/л) в течение 4 недель. Если это наблюдается, должна быть сделана соответствующая корректировка дозы. Вследствие вариабельности между пациентами, время от времени могут наблюдаться индивидуальные колебания значений гемоглобина у пациента выше или ниже требуемого уровня гемоглобина. Колебания уровней гемоглобина следует регулировать путем корректировки дозы, с учетом необходимого диапазона гемоглобина от 10 г/дл (6.2 ммоль/л) до 12 г/дл (7.5 ммоль/л). У педиатрических больных требуемый диапазон гемоглобина составляет от 9.5 до 11 г/дл (5.9-6.8 ммоль/л).
Следует избегать устойчивого уровня гемоглобина выше 12 г/дл (7.5 ммоль/л). Если гемоглобин повышается более чем на 2 г/дл (1.25 ммоль/л) в месяц, или, если устойчивый уровень гемоглобина составляет более 12 г/дл (75 ммоль/л), следует уменьшить дозу Бинокрита на 25%. Если уровень гемоглобина превышает 13 г/дл (8.1 ммоль/л), следует прекратить терапию, пока гемоглобин не опустится ниже 12 г/дл (7.5 ммоль/л), а затем возобновить терапию Бинокритом в дозе на 25% ниже предыдущей дозы.
Необходим тщательный контроль пациентов для гарантии того, что применяется самая низкая доза из диапазона утвержденных доз Бинокрита, позволяющая обеспечить адекватный контроль анемии и ее симптомов, поддерживая концентрацию гемоглобина ниже или на уровне 12 г/дл (7,45 ммоль/л).
Статус содержания железа следует оценивать до и во время лечения, и при необходимости назначать дополнительные препараты железа. Кроме того, другие причины анемии, такие как дефицит витамина B12 или фолиевой кислоты, должны быть исключены до начала применения терапии Бинокритом. Отсутствие терапевтического эффекта лечения Бинокритом может иметь следующие причины: недостаток железа, фолиевой кислоты или витамина В12, алюминиевая интоксикация, интеркуррентные инфекции, случаи воспаления или травмы, скрытая кровопотеря, гемолиз или фиброз тканей костного мозга любого происхождения.
Взрослые пациенты, получающие гемодиализ
Лечение делится на две фазы – фаза коррекции и поддерживающая фаза.
1) Фаза коррекции
По 50 МЕ/кг 3 раза в неделю внутривенно. При необходимости коррекции дозы, ее следует проводить поэтапно, с промежутком между изменениями дозы минимум в четыре недели. На каждом этапе увеличение или снижение дозы должно составлять 25 МЕ/кг 3 раза в неделю.
2) Поддерживающая фаза
Коррекция дозы для поддержания гемоглобина на требуемом уровне от 10 до 12 г/дл (6.2-7.5 ммоль /л).
Рекомендуемая общая недельная доза составляет от 75 до 300 МЕ/кг и вводится внутривенно.
Имеющиеся клинические данные показывают, что пациентам, у которых начальный уровень гемоглобина был очень низким (<6 г/дл или <3.75 ммоль /л), могут потребоваться более высокие поддерживающие дозы, чем тем пациентам, которые имели менее тяжелую степень начальной анемии (Нb> 8 г/дл или > 5 ммоль /л).
Дети в возрасте от 1 года и старше, получающие гемодиализ
Лечение состоит из двух этапов:
1)Фаза коррекции
По 50 МЕ/кг 3 раза в неделю внутривенно. При необходимости коррекции дозы, ее следует проводить поэтапно с увеличением или снижением дозы на каждом этапе по 25 МЕ/кг 3 раза в неделю с интервалами между изменениями дозы минимум в четыре недели до достижения желаемой цели.
2) Поддерживающая фаза
Следует производить коррекцию дозы для поддержания концентрации гемоглобина в требуемом диапазоне от 9.5 г/дл до 11 г/дл (от 5.9 до 6.8 ммоль/л).
Как правило, для детей с весом до 30 кг требуются более высокие поддерживающие дозы по сравнению с детьми с весом более 30 кг и взрослыми.
Следующие поддерживающие дозы были установлены в ходе клинических исследований через 6 месяцев после начала лечения:
|
Доза (ME /кг 3 раза в неделю) |
||
|
Вес (кг) |
Среднее значение |
Обычная поддерживающая доза |
|
<10 |
100 |
75-150 |
|
10-30 |
75 |
60-150 |
|
>30 |
33 |
30-100 |
Имеющиеся клинические данные показывают, что детям, у которых начальный уровень гемоглобина был очень низким (<6.8 г/дл или <4.25 ммоль /л), могут потребоваться более высокие поддерживающие дозы, чем тем, которые имели менее тяжелую степень начальной анемии (> 6.8 г/дл или > 4.25 ммоль /л).
Взрослые пациенты, получающие перитонеальный диализ
Лечение состоит из двух этапов:
1) Фаза коррекции
Начальная доза составляет 50 МЕ/кг два раза в неделю внутривенно.
2) Поддерживающая фаза
Коррекция дозы для поддержания концентрации гемоглобина в требуемом диапазоне от 10 до 12 г/дл (6.2-7.5 ммоль /л). Поддерживающая доза составляет от 25 до 50 МЕ/кг два раза в неделю путем введения дозы в виде 2 равных инъекций.
Взрослые пациенты с почечной недостаточностью, не получающие диализ
Лечение состоит из двух этапов:
1) Фаза коррекции
Начальная доза составляет 50 МЕ/кг 3 раза в неделю внутривенно, а затем при необходимости дозу увеличивают с шагом повышения дозы 25 МЕ/кг (3 раза в неделю), до достижения оптимального уровня гемоглобина (коррекцию дозы следует проводить поэтапно с интервалом не менее четырех недель).
2) Поддерживающая фаза
Соответствующая коррекция дозы должна быть сделана для поддержания концентрации гемоглобина в требуемом диапазоне от 10 до 12 г/дл (6.2-7.5 ммоль/л). Расширение интервалов дозирования может потребовать увеличения дозы.
Максимальная доза не должна превышать 150 МЕ/кг 3 раза в неделю.
Лечение больных анемией, вызванной химиотерапией
Пациентам с анемией (концентрация гемоглобина ≤10 г/дл (6.2 ммоль /л)) Бинокрит следует вводить подкожно. Симптомы и осложнения анемии могут варьировать в зависимости от возраста, пола и общей тяжести заболевания; необходимо проведение врачом оценки индивидуального клинического течения заболевания и состояния пациента.
Вследствие вариабельности между пациентами, время от времени могут наблюдаться индивидуальные колебания значений гемоглобина для пациента выше или ниже требуемого уровня гемоглобина. Колебания уровней гемоглобина следует регулировать путем корректировки дозы, сучетом целевого диапазона гемоглобина от 10 г/дл (6.2 ммоль/л) до 12 г/дл (7.5 ммоль/л). Следует избегать устойчивого уровня гемоглобина, превышающего 12 г/дл (7.5 ммоль/л); руководство по соответствующей коррекции дозы при уровнях гемоглобина, превышающих 12 г/дл (7.5 ммоль /л), представлено ниже.
Терапия Бинокритом должна продолжаться в течение одного месяца после окончания химиотерапии.
Начальная доза составляет 150 МЕ/кг подкожно 3 раза в неделю. В качестве альтернативы, Бинокрит может вводиться в начальной дозе 450 МЕ/кг подкожно один раз в неделю.
Если уровень гемоглобина увеличился, по крайней мере, на 1 г/дл (>0.62 ммоль/л) или число ретикулоцитов увеличилось на ≥ 40 000 клеток / мкл выше исходного уровня через 4 недели лечения, доза должна оставаться на уровне 150 МЕ/кг 3 раза в неделю или 450 МЕ/кг один раз в неделю.
Если повышение уровня гемоглобина составляет <1 г/дл (<0.62 ммоль /л) и число ретикулоцитов увеличивается на <40000 клеток/мкл по сравнению с исходным уровнем, дозу следует увеличить до 300 МЕ/кг 3 раза в неделю. Если после дополнительных 4 недель лечения при введении 300 МЕ/кг 3 раза в неделю, гемоглобин повышается на ≥ 1 г/дл (≥ 0.62 ммоль/л) или число ретикулоцитов увеличивается на ≥ 40000 клеток/мкл, доза должна оставаться на уровне 300 МЕ/кг 3 раза в неделю. Однако, если уровень гемоглобина повышается на <1 г/дл (<0.62 ммоль/л) и число ретикулоцитов увеличивается на <40 000 клеток/мкл по сравнению с исходным уровнем, терапевтический эффект на прием Бинокрита у таких пациентов маловероятен и лечение должно быть прекращено.
Пациенты должны подвергаться тщательному мониторингу, чтобы убедиться в том, что применяется самая низкая разрешенная доза Бинокрита для обеспечения адекватного контроля симптомов анемии.
Коррекция дозы для поддержания концентрации гемоглобина между 10 г/дл-12 г/дл (6.2-7.5 ммоль/л)
Если уровень гемоглобина повышается более чем на 2 г/дл (1.25 ммоль/л) в месяц, или если уровень гемоглобина составляет более 12 г/дл (7.5 ммоль /л), доза Бинокрита должна быть снижена примерно на 25 — 50%. Если уровень гемоглобина превышает 13 г/дл (8.1 ммоль/л), следует прекратить лечение, пока он не опустится ниже 12 г/дл (7.5 ммоль /л), после чего возобновить терапию Бинокритом в дозе на 25% ниже предыдущей.
В качестве альтернативы гемотрансфузиям у взрослых пациентов, не имеющих дефицита железа, перед плановой ортопедической операцией
Бинокрит вводят подкожно.
Рекомендуемый режим дозирования Бинокрита составляет 600 МЕ/кг подкожно один раз в неделю в течение 3 недель, предшествующих операции (за 21, 14 и 7 дней до операции), а также в день операции (день 0). В случаях медицинской необходимости сокращения времени подготовки к операции до менее трех недель, дозу 300 МЕ/кг Бинокрит следует вводить подкожно ежедневно в течение 10 последовательных дней до операции, в день операции и в течение четырех дней непосредственно после проведения операции. При проведении оценки гематологических показателей в течение предоперационного периода, если уровень гемоглобина достигает 15 г/дл (9.38 ммоль/л), или превышает этот уровень, введение Бинокрит должно быть прекращено и дальнейшие дозы вводить не следует.
Необходимо следить за тем, чтобы на начальном этапе лечения у пациентов не было дефицита железа.
Все пациенты, получающие Бинокрит, должны также получать адекватные дозы восполнения железа (например, препараты железа по 200 мг Fe2+ в сутки) на протяжении всего курса лечения Бинокрит. При возможности, прием препаратов железа следует начинать до начала терапии Бинокритом для достижения адекватных запасов железа.
Способ введения
Как с любым другим лекарственным средством для инъекций, проверьте, чтобы в растворе не имелось посторонних частиц, и не было изменения цвета. Бинокрит является стерильным лекарственным средством, не содержит консервантов и предназначен только для однократного применения. Рекомендуется вводить только требуемый объем лекарственного средства.
Перед применением, отложите Бинокрит на 15-30 минут до достижения им комнатной температуры.
Бинокрит не следует вводить путем внутривенной инфузии или смешивать с другими лекарственными средствами (см. раздел «Особые указания» для более подробной информации).
Лечение симптоматической анемии у взрослых с хронической почечной недостаточностью.
Бинокрит следует вводить внутривенно.
Лечение взрослых пациентов с анемией вызванной химиотерапией
Бинокрит следует вводить в виде подкожных инъекций.
Лечение взрослых пациентов перед операцией участвующих в программе заготовки крови
Бинокрит следует вводить внутривенно.
Лечение взрослых пациентов перед большой плановой ортопедической операцией
Бинокрит следует вводить в виде подкожной инъекции.
Лечение симптоматической анемии в детей с хронической почечной недостаточностью получающих гемодиализ
Бинокрит следует назначать внутривенно.
Внутривенные инъекции: продолжительность инъекции от 1 минуты до 5 минут, в зависимости от общего объема дозы.
Пациентам на гемодиализе Бинокрит может вводиться путем болюсной инъекции в течение процедуры диализа через подходящий венозный порт катетера для диализа. Альтернативно, инъекция может быть проведена в конце процедуры диализа через трубку фистульной иглы, после чего вводят 10 мл изотонического раствора для промывки трубки и обеспечения удовлетворительного введения Бинокрита в кровяное русло.
Более медленная инъекция является предпочтительной у пациентов, которые реагируют на лечение появлением «гриппоподобных» симптомов.
Не следует назначать Бинокрит в виде внутривенной инфузии или в сочетании с другими растворами лекарственных средств.
Подкожное введение: как правило, максимальный объем не должен превышать 1 мл при введении на одном участке кожи. В случае больших объемов, должно быть выбрано больше одного участка для инъекций или инъекции выполняют в разные участки тела. Инъекции следует вводить в бедро или переднюю брюшную стенку.
В тех ситуациях, в которых пациент или лицо, осуществляющее уход за больным, могут безопасно и эффективно вводить Бинокрит подкожно, должны быть предоставлены инструкции в отношении надлежащей дозы и введения.
Бинокрит не должен использоваться:
— если раствор имеет окраску или в нем наблюдаются частицы;
— если нарушена целостность упаковки;
— если известно или предполагается, что раствор был случайно заморожен;
— если произошло отключение холодильника.
Предварительно заполненные шприцы являются готовыми к использованию. Предварительно заполненный шприц не следует встряхивать. Не встряхивайте предварительно заполненный шприц. Продолжительное интенсивное встряхивание может повредить лекарственное средство Бинокрит. Если лекарственное средство Бинокрит подвергалось сильному встряхиванию, не используйте его.
Бинокрит предназначен для одноразового использования.
Использование предварительно заполненного шприца с устройством защиты иглы
Устройство защиты иглы закрывает иглу после инъекции для предотвращения случайного укола. Оно не влияет на нормальное функционирование шприца. Следует нажимать на поршень медленно и плавно, до введения всей дозы и до упора поршня. Сохраняя давление на поршень, извлечь шприц из кожи. Устройство защиты иглы закроет иглу при отпускании поршня.
Не вводите инъекции самостоятельно, если Вы не были обучены делать это Вашим лечащим врачом или медсестрой.
Как самостоятельно сделать инъекцию Бинокрита с помощью предварительно заполненного шприца.
1.Достаньте шприц из холодильника. Раствор необходимо довести до комнатной температуры. Обычно это занимает от 15 до 30 минут.
2.Проверьте шприц на правильность дозировки, срок хранения, отсутствие повреждений, а также прозрачность раствора и отсутствие его замораживания
3.Выберите место инъекции. Подходящими местами для инъекции является верхняя область бедра и передняя брюшная стенка, кроме околопупочной области. Ежедневно чередуйте места инъекций.
4.Вымойте руки.
5.Удалите упаковку со шприца, держа за корпус шприца и стягивая упаковку без ее перекручивания. Запрещается нажимать на поршень, дотрагиваться до иглы или встряхивать шприц.
Шприцы маркированы градуированными кольцами для частичного использования содержимого, в случае необходимости. Каждое кольцо градуировки соответствует объему 0.1 мл. Из шприца вводят только одну требуемую дозу, ненужный объем раствора необходимо удалить из шприца перед инъекцией.
6.Очистите место инъекции тампоном с антисептиком для его дезинфекции.
7.Сформируйте кожную складку между большим и указательным пальцами руки. Не стягивайте ее.
8.Введите иглу на всю длину.
9.Определите вероятность прокола кровеносного сосуда. Слегка оттяните поршень. Если в шприц поступает кровь, извлеките иглу и попробуйте провести инъекцию в другом месте.
10.Нажимайте на поршень до конца, для инъекции всего раствора. Нажимайте на него без усилия и равномерно, продолжая зажимать кожную
складку. Устройство защиты иглы не активируется до введения полной дозы.
11.При максимально возможном продвижении поршня, извлеките иглу и расправьте кожную складку.
12.Отнимите большой палец с поршня. Позвольте игле переместиться до полного ее покрытия защитной насадкой.
13.Прижмите тампон с антисептиком к месту инъекции на несколько секунд после ее завершения.
14.Поместите использованный Вами шприц в безопасный контейнер.
Используйте только по одной дозе из каждого шприца. Если после инъекции в шприце остается раствор, все равно необходимо выбросить шприц, а не использовать его повторно.
Побочные действия
Частота развития неблагоприятных реакций определяется следующим образом: очень часто (≥ 1/10); часто (≥ 1/100 — <1/10); нечасто (≥ 1/1 000 — <1/100); редко (≥1/10 000 — <1/1000); очень редко (<1/10 000); частота неизвестна (не может быть оценена на основании имеющихся данных).
Очень часто
— диарея
— рвота
— головная боль (у онкологических больных)
— тошнота
— артралгия (у пациентов с хронической почечной недостаточностью)
— повышение температуры (у онкологических больных)
— гриппоподобный синдром (у пациентов с хронической почечной
недостаточностью)
Часто
— пароксизмы (у пациентов с хронической почечной недостаточностью)
— головная боль (у пациентов с хронической почечной недостаточностью)
— венозный и артериальный тромбоз3
— инсульт
— тромбоз глубоких вен2 (у онкологических больных.)
— гипертензия
— кашель
— сыпь
— артралгия, боль в костях, миалгия, боль в конечностях
— озноб, гриппоподобный синдром, реакции в месте инъекции, периферические отеки
— эмболия легочной артерии1 (в том числе случаи летального исхода у онкологических больных)
— диарея (у онкологических больных)
— рвота
— ангионевротический отёк (отек Квинке)
— крапивница
— артралгия (у онкологических больных)
— гриппоподобный синдром (у онкологических больных)
— тромбозы экстракорпорального русла диализных аппаратов (у пациентов с хронической почечной недостаточностью)
Нечасто
— гиперкалиемия3
— судороги
— застой в респираторном тракте
— тромбоцитемия (у онкологических больных)
— кровоизлияние в мозг2
— пароксизмы (у онкологических больных)2
— диарея (у пациентов с хронической почечной недостаточностью)
— миалгия (у онкологических больных)
Очень редко
— истинная эритроцитарная аплазия костного мозга, вызванная антителами к эритропоэтину1,4
— тромбоцитэмия1
Частота неизвестна
— истинная эритроцитарная аплазия костного мозга, вызванная антителами к эритропоэтину1
— тромбоцитемия (у пациентов с хронической почечной недостаточностью)
— анафилактическая реакция, гиперчувствительность
— анафилактическая реакция4, гиперчувствительность4
— гипертонический криз
— нарушение мозгового кровообращения2
— гипертоническая энцефалопатия
— транзиторные ишемические атаки
— тромбоз сетчатки глаза
— инфаркт миокарда
— тромбоз глубоких вен2 (у пациентов с хронической почечной
недостаточностью)
— артериальный тромбоз
— гипертонический криз
— эмболия легочной артерии2 (у пациентов с хронической почечной
недостаточностью)
— миалгия (у пациентов с хронической почечной недостаточностью)
— ангионевротический отек
— крапивница
— порфирия
— отсутствие эффективности лекарственного средства
— периферический отек
— повышение температуры (у пациентов с хронической почечной
недостаточностью)
— реакция в участке введения
— положительный тест на наличие антител к эритропоэтину1
1 Определено во время постмаркетингового опыта и категория частоты оценена из спонтанных отчетов.
2 Обычно при диализе.
3 Включает артериальные и венозные, летальные и не летальные случаи, такие как тромбоз глубоких вен, легочная эмболия, ретинальный тромбоз, артериальный тромбоз (включая инфаркт миокарда), цереброваскулярные несчастные случаи (включая церебральный инфаркт и церебральные кровотечения) транзиторные ишемические атаки, тромбозы шунта (включая оборудование для диализа) и тромбоз в пределах аневризмы артериовенозного шунта.
4См раздел «Особые указания».
Описание некоторых неблагоприятных реакций
Сообщалось о реакциях гиперчувствительности, включая случаи сыпи (включая крапивницу), анафилактические реакции, и ангионевротический отек.
Гипертонический криз с энцефалопатией и судорогами, требующий немедленного внимания врача и интенсивную лекарственную терапию, так же имел место во время лечения эпоэтином альфа у пациентов с предыдущим нормальным или низким артериальным давлением. Особое внимание следует уделять внезапным колющим мигренеподобным головным болям как возможному предупредительному сигналу.
Очень редко, в <1/10 000 случаях на пациент-год, сообщалось об истинной эритроцитарной аплазии костного мозга, вызванной антителами к эритропоэтину после месяцев и годов лечения эпоэтином альфа.
Дети с хронической почечной недостаточностью получающие гемодиализ
Данные о подверженности детей с хронической почечной недостаточностью, получающих гемодиализ, в клинических испытаниях и постмаркетинговом опыте ограничены. Ранее в разделе «Побочные действия» не упоминалось о специфических детских побочных действиях или о любых согласующихся с заболеванием для данной группы.
Пациенты с хронической почечной недостаточностью
У пациентов с хронической почечной недостаточностью уровни гемоглобина свыше 12 г/дл (7.5 ммоль/л) могут быть связаны с повышенным риском развития сердечно-сосудистых осложнений, включая летальный исход.
Тромбозы шунта имели место у пациентов на гемодиализе, особенно у пациентов со склонностью к гипотонии или осложнениями артериовенозных свищей (например, стеноз, аневризма и др.)
Онкологические больные
Повышение частоты тромбоэмболических явлений наблюдалось среди онкологических больных, получавших стимуляторы эритропоэза, в том числе Бинокрит.
Пациенты с хирургическим вмешательством
У пациентов с большой плановой ортопедической операцией, с исходным уровнем гемоглобина от 10 до 13 г/дл (6.2-8.1 ммоль/л), частота тромботических / сосудистых явлений (большинство из которых были тромбозами глубоких вен) в общей популяции пациентов клинических исследований оказалась примерно одинаковой во всех группах с разной дозировкой Бинокрита и в группе плацебо, хотя клинический опыт является ограниченным.
Кроме того, у пациентов с исходным уровнем гемоглобина >13 г/дл (8.1 ммоль/л) нельзя исключать вероятность того, что лечение Бинокритом может быть связано с повышением риска послеоперационных тромботических / сосудистых осложнений.
Предоставление сообщений о подозреваемых побочных реакциях
Предоставление сообщений о подозрительных побочных реакциях лекарственного средства имеет большое значение. Это позволяет продолжать мониторинг соотношения «польза/риск» лекарственного средства. Медицинским работникам необходимо сообщать о любых подозреваемых побочных реакциях путем заполнения желтых карт и последующее предоставление в органы здравоохранения Казахстана.
Противопоказания
-
повышенная чувствительность к активному веществу или к любому из вспомогательных веществ
-
истинная эритроцитарная аплазия костного мозга, возникшая после лечения любыми эритропоэтинами (не должны получать Бинокрит или любой другой эритропоэтин)
-
неконтролируемая артериальная гипертензия
-
хирургические пациенты, которые по каким-либо причинам не могут получить адекватное лечение для профилактики тромбозов (геморрагические осложнения, тяжелая сердечная недостаточность и т.д.)
-
детский возраст до 1 года (включая хроническую почечную недостаточностью (ХПН) на гемодиализе)
-
беременность и период лактации
-
повторный риск тромбоза глубоких вен и тромбоэмболии, особенно для аутогемотрансфузий
-
все противопоказания, связанные с программой предварительного донорства аутологичной крови (предепозитная программа заготовки аутологичной крови), должны быть приняты во внимание для пациентов, получающих Бинокрит
-
наличие тяжелой степени заболеваний коронарных сосудов, периферических артерий, сонных артерий или церебральных сосудов, включая недавно перенесённый инфаркт миокарда или острое нарушение мозгового кровообращения, нестабильная стенокардия, большая плановая ортопедическая операция без участия в программе предварительного донорства аутологичной крови (предепозитная программа заготовка аутологичной крови)
Лекарственные взаимодействия
Нет данных о взаимодействии Бинокрита с другими лекарственными средствами.
Лекарственные средства, снижающие уровень эритропоэтина, могут снижать ответ на Бинокрит.
Однако, при одновременном применении с циклоспорином возможно взаимодействие, поскольку препарат Бинокрит связывается с эритроцитами. Если лечение Бинокритом проводится одновременно с циклоспорином, необходимо контролировать уровень циклоспорина в крови и корректировать дозу циклоспорина в зависимости от степени повышения гематокрита.
Нет данных о взаимодействии между Бинокритом и гранулоцитарным колониестимулирующим фактором (G-CSF) или гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) в отношении гематологической дифференциации или пролиферации образцов биопсии опухоли в условиях in vitro нет.
У пациентов с метастазирующим раком груди, совместное применение Бинокрита в дозе 40000 МЕ/1.0 мл с 6 мг/кг трастузумабом при подкожном введении не оказало влияния на фармакокинетику трастузумаба.
Дети
Исследования лекарственного взаимодействия не проводились у детей и подростков.
Особые указания
Всем пациентам, получающим Бинокрит, следует проводить тщательный мониторинг и, по мере необходимости, осуществлять контроль уровня артериального давления. Бинокрит следует с осторожностью использовать при наличии нелеченой, неадекватно леченой или плохо контролируемой гипертензии. Возможно, станет необходимым добавление или усиление антигипертензивного лечения. Если артериальное давление не может контролироваться лечением или антигипертензивными препаратами, лечение Бинокритом должно быть прекращено.
Гипертензивный криз с энцефалопатией и судорогами, требующий немедленного внимания врача и интенсивной лекарственной терапии, так же встречались во время лечения Бинокритом у пациентов с предшествующим нормальным или низком артериальным давлением. Особое внимание следует обратить на внезапные колющие мигренеподобные головные боли, как на возможный предупредительный сигнал.
Бинокрит следует с осторожностью применять при наличии эпилепсии, судорог в анамнезе и при таких состояниях, которые предрасполагают к развитию судорог, как инфекции ЦНС и метастазы в мозге, хроническая печеночная недостаточность.
Безопасность препарата Бинокрит у пациентов с нарушением функции печени не установлена. Вследствие сниженного метаболизма у пациентов с нарушением функции печени при применении препарата Бинокрит может происходить усиление эритропоэза.
У пациентов, получавших препараты эритропоэтинов, наблюдалось повышение частоты тромботических сосудистых явлений (ТСЯ). К ним относились венозные и артериальные тромбозы и эмболии (включая несколько случаев со смертельным исходом), такие как тромбоз глубоких вен, эмболия легочной артерии, тромбоз сетчатки и инфаркт миокарда. Отмечались нарушения мозгового кровообращения (включая инфаркт головного мозга, кровоизлияние в головной мозг и транзиторные ишемические атаки).
Сообщающийся риск ТСЯ должен быть тщательно взвешен по сравнению с пользой от лечения Бинокритом в частности у пациентов с предшествующим фактором риска ТСЯ, включая ожирение и ТСЯ в анамнезе (например, тромбоз глубоких вен, легочная эмболия и цереброваскулярные случаи).
Пациентам с хронической почечной недостаточностью и пациентам с онкологическими заболеваниями, принимающим Бинокрит, необходимо регулярно определять уровень гемоглобина до достижения его устойчивого уровня и периодически после этого.
У всех пациентов следует производить тщательный мониторинг концентрации гемоглобина из-за потенциального повышения риска тромбоэмболических явлений и смертельных исходов, если концентрации гемоглобина выше диапазона, являющегося показанием к применению.
Во время терапии Бинокритом может наблюдаться умеренное дозозависимое повышение количества тромбоцитов в пределах нормального диапазона. Этот показатель возвращается к исходному значению в ходе продолжающейся терапии. Кроме того, сообщалось о случае тромбоцитемии выше нормального уровня. Рекомендуется проводить регулярный мониторинг количества тромбоцитов в течение первых 8 недель терапии.
Перед началом терапии с применением Бинокрита, следует произвести оценку и лечение других причин анемии (дефицит железа, гемолиз, потеря крови, дефицит витамина В12 или фолиевой кислоты).
В большинстве случаев уровень ферритина в сыворотке крови падает одновременно с ростом показателя гематокрита. Для достижения оптимального терапевтического ответа на терапию Бинокритом, должно быть обеспечено адекватное восполнение содержания железа:
— препараты железа, например, с 200-300 мг элементарного железа сутки перорально для взрослых (для детей доза 100-200 мг элементарного железа в сутки) рекомендуется назначать пациентам с хронической почечной недостаточностью и уровнем сывороточного ферритина ниже 100 нг/мл
— пероральные препараты железа (200-300 мг элементарного железа в сутки) рекомендуются для пациентов с онкологическими заболеваниями с показателем насыщения трансферрина ниже 20%.
— для пациентов, участвующих в предепозитарной программе заготовки аутологичной крови, препараты железа (200 мг элементарного железа в сутки перорально) следует назначать за несколько недель до начала аутологичной заготовки для того, чтобы достигнуть высокого уровня запасов железа до начала терапии Бинокритом и в течение курса терапии Бинокритом.
— для пациентов перед большой плановой ортопедической операцией, препараты железа (200 мг элементарного железа в сутки перорально) следует назначать в течение курса терапии Бинокритом для достижения адекватных запасов железа.
Все эти аддитивные факторы анемии следует внимательно учитывать при принятии решений об увеличении дозы Бинокрита у онкологических больных.
Очень редко наблюдалось развитие или обострение порфирии у больных, получающих лечение Бинокритом. Бинокрит следует использовать с осторожностью у пациентов с порфирией.
Для того чтобы лучше отслеживать лекарственные средства, стимулирующие эритропоэз (erythropoiesis‑stimulating agents, ESA), торговое название применяемого лекарственного средства — стимулятора эритропоэза — должно быть четко записано (или заявлено) в документах пациента.
Пациенты должны переключаться с применения одного стимулятора эритропоэза на другой только под строгим контролем.
Истинная эритроцитарная аплазия костного мозга
Случаи развития истинной эритроцитарной аплазии костного мозга, вызванного антителами к эритропоэтину, при терапии от нескольких месяцев до нескольких лет с подкожным введением эритропоэтина, были очень редкими.
Случаи заболевания также были зарегистрированы у пациентов с гепатитом С, получавших лечение интерфероном и рибавирином, при одновременном использовании Бинокрита. Бинокрит не одобрен для лечения анемии, связанной с гепатитом С.
У пациентов, у которых внезапно развивается отсутствие эффективности, характеризующееся снижением уровня гемоглобина (от 1 до 2 г/дл или 0.62 до 1.25 ммоль/л в месяц) с увеличением потребности в переливании крови, необходимо провести подсчет количества ретикулоцитов и обследовать на наличие предполагаемых потенциальных причин отсутствия ответа на терапию (например, дефицит железа, фолиевой кислоты или витамина В12, алюминиевая интоксикация, инфекция или воспаление, потеря крови и гемолиз, фиброз костного мозга любого происхождения).
Парадоксальное снижение уровня гемоглобина и развитие симптомов тяжелой анемии в связи с низким содержанием ретикулоцитов, указывает на необходимость прекращения лечения Бинокритом и проведения анализа на присутствие антител к эритропоэтину. Исследование костного мозга также должно быть рассмотрено для диагностики истинной эритроцитарной аплазии.
Терапия другими стимуляторами эритропоэза не должна начинаться из-за риска перекрестной реакции.
Лечение симптоматической анемии у взрослых и детей с хронической почечной недостаточностью
Данные по иммуногенности при подкожном введении Бинокрита пациентам с риском развития истинной эритроцитарной аплазии, индуцированной антителами, то есть, у пациентов с анемией почечного генеза, не являются достаточными. Поэтому пациентам с анемией почечного генеза Бинокрит должен вводиться внутривенно.
Пациенты, с хронической почечной недостаточностью, получающие лечение Бинокритом, должны регулярно измерять уровень гемоглобина до достижения стабильного эффекта и периодически после этого.
При хронической почечной недостаточности скорость повышения уровня гемоглобина должна составлять приблизительно 1 г/дл (0.62 ммоль/л) в месяц, и не должна превышать 2 г/дл (1.25 ммоль/л) в месяц, чтобы минимизировать риски развития гипертензии.
Концентрация гемоглобина
У пациентов с хронической почечной недостаточностью, поддерживающая концентрация гемоглобина не должна превышать верхней границы концентрационного уровня гемоглобина. В клинических исследованиях наблюдался повышенный риск смертности и серьезных сердечно-сосудистых явлений, при введении стимуляторов эритропоэза пациентам при достижении уровня гемоглобина выше 12 г/дл (7.5 ммоль/л).
Следует соблюдать осторожность при повышении доз Бинокрита у пациентов с хронической почечной недостаточностью, так как высокие куммулятивные дозы Бинокрита могут быть ассоциированы с высоким риском смертности, серьезными кардиоваскулярными и цереброваскулярными последствиями. У пациентов со слабым ответом гемоглобина на эпоэтины, следует рассмотреть альтернативные обоснования слабого ответа гемоглобина.
Контролируемые клинические исследования не показали существенных преимуществ применения Бинокрита в случаях, когда концентрация гемоглобина выходила за пределы уровня, необходимого для контроля симптомов анемии и устранения необходимости переливания крови.
У некоторых пациентов с расширенным интервалом дозирования (больше чем один раз в неделю) Бинокрита могут не поддерживаться надлежащие уровни гемоглобина, и может потребоваться увеличение дозы Бинокрита. Уровень гемоглобина необходимо проверять регулярно.
У пациентов на гемодиализе, особенно со склонностью к гипотензии, и с осложнениями артериовенозных фистул (такими, как стеноз, аневризма и др.) наблюдались тромбозы шунтов диализатора. Указанным пациентам рекомендуется своевременная ранняя проверка шунта и профилактика тромбозов, например, приемом ацетилсалициловой кислоты.
Гиперкалиемия наблюдалась в единичных случаях, хотя ее причинно-следственная связь с применением Бинокрита не установлена.
У пациентов с хронической почечной недостаточностью необходимо контролировать уровень электролитов сыворотки. Если уровень калия в сыворотке крови повышен или увеличивается, то в дополнение к соответствующей терапии гиперкалиемии, необходимо прекратить введение Бинокрита вплоть до коррекции уровня калия в сыворотке.
В ходе терапии Бинокритом часто требуется повышение дозы гепарина во время проведения гемодиализа в связи с повышением гематокрита. При неадекватной дозе гепарина возможна окклюзия диализной системы.
Основываясь на имеющейся информации, коррекция анемии введением Бинокрита у взрослых пациентов с почечной недостаточностью, не находящихся на диализе, не ускоряет скорость прогрессирования почечной недостаточности.
Лечение пациентов с анемией, вызванной химиотерапией
У онкологических больных, которые получают лечение Бинокритом, необходимо регулярно измерять уровень гемоглобина до достижения стабильного уровня и периодически после этого.
Эритропоэтины являются факторами роста, которые в первую очередь стимулируют продукцию красных кровяных телец. Рецепторы к эритропоэтину могут экспрессироваться на поверхности различных опухолевых клеток. Как и для всех факторов роста, есть опасения, что эпоэтины могут стимулировать рост опухолей. В нескольких контролируемых исследованиях эпоэтины не приводили к повышению общей выживаемости или снижению риска прогрессирования опухоли у пациентов с анемией, ассоциированной с раком.
В контролируемых клинических исследований, применение Бинокрита и других стимуляторов эритропоэза приводило к:
-
снижению локорегионарного контроля у пациентов с прогрессивными злокачественными опухолями головы и шеи, получающих лучевую терапию, при введении Бинокрита до достижения требуемого уровня гемоглобина выше 14 г/дл (8.7 ммоль/л),
-
сокращению общей выживаемости и увеличению смертности в связи с прогрессированием заболевания через 4 месяца у пациентов с метастазирующим раком молочной железы, получающих химиотерапию, при введении Бинокрита до достижения требуемого уровня гемоглобина 12-14 г/дл (7.5-8.7 ммоль/л),
-
повышению риска летального исхода при введении Бинокрита до достижения целевого уровня гемоглобина 12 г/дл (7.5 ммоль/л) у пациентов с активным злокачественным заболеванием, не получающим ни химиотерапию, ни лучевую терапию. Стимуляторы эритропоэза не показаны для применения в этой популяции пациентов.
В свете вышеизложенного, в некоторых клинических ситуациях переливание крови должно быть предпочтительным методом лечения анемии у онкологических больных. Решение о назначении рекомбинантного эритропоэтина должно быть основано на оценке соотношения пользы и риска с участием конкретного пациента, и должно учитывать конкретную клиническую ситуацию. Факторы, которые следует учитывать при оценке, должны включать в себя тип и стадию опухоли; степень тяжести анемии; продолжительность жизни, условия, в которых пациент получает лечение; также предпочтения пациента к определенному методу лечения.
Для онкологических больных, получающих химиотерапию, при оценке целесообразности применения терапии Бинокритом (для пациентов с риском необходимости переливания крови) следует учитывать 2-3 недельную задержку между приемом Бинокрита и появлением стимулированных эритропоэтином эритроцитов.
Для онкологических больных, получавших стимуляторы эритропоэза, наблюдалось повышение частоты развития тромботических сосудистых осложнений. Этот риск должен быть тщательно взвешен относительно пользы, полученной от терапии Бинокритом, особенно у онкологических больных, с повышенным риском развития тромботических сосудистых осложнений, таких как пациенты с ожирением или наличием в анамнезе тромботических сосудистых явлений (например, тромбоз глубоких вен или легочная эмболия).
Пациенты с плановой хирургической операцией, находящиеся на программе предварительного донорства аутологичной крови (предепозитная программа заготовки аутологичной крови)
Должны соблюдаться все особые указания и меры предосторожности, связанные с программой предварительного донорства аутологичной крови (предепозитная программа заготовки аутологичной крови), особенно для стандартного восполнения объема крови.
Пациенты с большой плановой ортопедической операцией
У пациентов, которым назначена большая плановая ортопедическая операция, перед началом лечения Бинокритом должна быть установлена причина анемии и предпринято необходимое лечение, если это возможно. В этой популяции может существовать риск тромботических явлений, что должно быть тщательно взвешено по отношению к пользе, которая может быть получена от лечения в этой группе пациентов.
Пациенты, которым назначена большая плановая ортопедическая операция, должны получать надлежащую профилактику тромботических явлений, поскольку после операции могут развиться тромботические и сосудистые явления, особенно при наличии сопутствующего сердечно-сосудистого заболевания. В дополнение, специальные меры предосторожности должны быть приняты для пациентов с предрасположенностью к развитию тромбоза глубоких вен. Кроме того, у пациентов с исходным уровнем гемоглобина >13 г/дл (>8.1 ммоль/л) не исключается риск послеоперационных тромботических/сосудистых осложнений связанный с терапией Бинокритом. Таким образом, Бинокрит не должен применяться у пациентов с исходным уровнем гемоглобина >13 г/дл (>8.1 ммоль/л).
Для амбулаторного применения пациент может извлечь предварительно заполненный шприц из холодильника и хранить его при температуре не выше 25 °С не более 3 дней.
Вспомогательные вещества
Бинокрит содержит менее 1 ммоль натрия (23 мг) в предварительно заполненном шприце, то есть, по существу, является безнатриевым лекарственным средством.
Беременность и период лактации
Имеется ограниченное количество данных об использовании Бинокрита у беременных женщин. Исследования на животных свидетельствовали о репродуктивной токсичности Бинокрита. Следовательно беременным пациенткам применение Бинокрита не рекомендуется.
Неизвестно, выводится ли Бинокрит в человеческое молоко.
ФертильностьДанных о фертильности нет.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Бинокрит не оказывает или оказывает незначительное влияние на способность управлять автомобилем и работать с механизмами.
Передозировка
Передозировка Бинокритом может вызвать симптомы, которые являются продолжениями фармакологических эффектов гормона.
Лечение: при чрезмерно высоких уровнях гемоглобина возможно применение кровопусканий. В случае необходимости назначается дополнительная поддерживающая терапия.
Форма выпуска и упаковка
По 0.5 мл (для дозировки 1000 МЕ/0.5 мл) и 1 мл (для дозировок 2000 МЕ/ 1.0 мл и 40000 МЕ/1.0 мл) препарата разливают в одноразовые шприцы прозрачного бесцветного боросиликатного стекла гидролитического класса I вместимостью 1 мл, снабженных поршнем из бромбутила, покрытым фторполимером и инъекционной иглой из нержавеющей стали с защитным колпачком и внешним колпачком из полипропилена (для предотвращения затупления иглы), а также специальным колпачком безопасности для иглы после проведенной инъекции (для предупреждения травматизации вследствие укола иглой по неосторожности).
По 1 или 3 предварительно заполненных шприца помещают в контурные ячейковые упаковки (блистер).
По 1 контурной ячейковой упаковке (блистеру) с 1 предварительно заполненным шприцем или по 2 контурных ячейковых упаковки (блистера) с 3 предварительно заполненными шприцами вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в пачку из картона.
Условия хранения
Хранить при температуре от 2 оС до 8 оС (в холодильнике) в оригинальной упаковке в защищенном от света месте. Не замораживать!
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не применять после истечения срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель/Упаковщик
ИДТ Биологика ГмбХ, Германия
Am Pharmapark D-06861 Dessau-Rosslau, Germany
Владелец регистрационного удостоверения
Сандоз ГмбХ, Австрия
Biochemiestrasse 10, A-6250 Kundl, Austria
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции ( товара),
ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
Представительство АО «Сандоз Фармасьютикалс д.д.» в Республике Казахстан
Республика Казахстан, 050051, г. Алматы, ул. Луганского, 96, Бизнес-Центр «Керуен», Тел +7 (727) 2581048 Факс: +7 (727) 2581047,
e-mail: kzsdz.drugsafety@sandoz.com
8 800 080 0066 – бесплатный номер дозвона по Казахстану
| 464537681477976597_ru.doc | 183 кб |
| 455057811477977753_kz.doc | 233 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
В/в, п/к.
Лечение анемии у больных с хронической почечной недостаточностью
Взрослые, находящиеся на гемодиализе. Эральфон® вводят п/к или в/в в конце сеанса диализа. При изменении способа введения препарат применяют в прежней дозе, затем дозу при необходимости корректируют (при п/к способе введения препарата для достижения одинакового терапевтического эффекта требуется доза на 20–30% меньше, чем при в/в введении). Лечение препаратом включает два этапа.
1. Этап коррекции: при п/к введении препарата начальная разовая доза — 30 МЕ/кг 3 раза в неделю. При в/в введении препарата начальная разовая доза — 50 МЕ/кг 3 раза в неделю. Период коррекции длится до момента достижения оптимального уровня Hb (100–120 г/л у взрослых и 95–110 г/л у детей) и гематокрита (30–35%). Эти показатели необходимо контролировать еженедельно.
Возможны следующие ситуации:
— гематокрит повышается от 0,5 до 1% в неделю. В этом случае дозу не изменяют до достижения оптимальных показателей;
— скорость прироста гематокрита менее 0,5% в неделю. В этом случае необходимо повышение разовой дозы в 1,5 раза;
— скорость прироста более 1% в неделю. В этом случае необходимо снизить разовую дозу препарата в 1,5 раза;
— гематокрит остается низким или снижается. Необходимо проанализировать причины резистентности, прежде чем увеличить дозу препарата.
Эффективность терапии зависит от правильно подобранной индивидуальной схемы лечения.
2. Этап поддерживающей терапии: для поддержания гематокрита на уровне 30–35% дозу препарата, применяемую на этапе коррекции, следует уменьшить в 1,5 раза. Затем поддерживающую дозу препарата подбирают индивидуально, с учетом динамики уровней гематокрита и Hb.
Дети, находящиеся на гемодиализе. Начальная доза — 50 ЕД/кг 3 раза в неделю. При необходимости разовую дозу повышают 1 раз в 4 нед на 25 ЕД/кг до достижения оптимальной концентрации Hb. Поддерживающая доза у детей с массой тела менее 10 кг — 75–150 ЕД/кг (в среднем 100 ЕД/кг) 3 раза в неделю; 10–30 кг — 60–150 ЕД/кг (в среднем 75 ЕД/кг) 3 раза в неделю; более 30 кг — 30–100 ЕД/кг (в среднем 33 ЕД/кг) 3 раза в неделю.
Взрослые преддиализные пациенты. Начальная доза вводится п/к или в/в 3 раза по 50 ЕД/кг/нед. При необходимости разовую дозу увеличивают 1 раз в 4 нед на 25 ЕД/кг до достижения оптимальной концентрации Hb. Поддерживающая доза — 17–33 ЕД/кг 3 раза в неделю.
Профилактика и лечение анемии у больных с сóлидными опухолями
Перед началом лечения рекомендуется провести определение уровня эндогенного эритропоэтина. При концентрации сывороточного эритропоэтина менее 200 МЕ/мл начальная доза препарата составляет при в/в способе введения 150 МЕ/кг 3 раза в неделю. Если через 4 нед лечения уровень Hb повышается и составляет не менее 10 г/л или количество ретикулоцитов увеличилось более чем на 40000 клеток/мкл свыше исходного уровня, то доза препарата остается прежней (150 МЕ/кг 3 раза в неделю).
Если через 4 нед лечения повышение уровня Hb составляет менее 10 г/л и увеличение количества ретикулоцитов — менее 40000 клеток/мкл по сравнению с исходным уровнем, то в течение следующих 4 нед дозу увеличивают до 300 МЕ/кг 3 раза в неделю. Если после дополнительных 4 нед лечения при дозе препарата 300 МЕ/кг уровень Hb повысился и составляет не менее 10 г/л или количество ретикулоцитов увеличивается более чем на 40000 клеток/мкл, то сохраняют существующую дозу препарата (300 МЕ/кг 3 раза в неделю). Если через 4 нед лечения в дозе 300 МЕ/кг уровень Hb повысился менее чем на 10 г/л и повышение количества ретикулоцитов составляет менее 40000 клеток/мкл по сравнению с исходным уровнем, лечение следует прекратить. В случае повышения уровня Hb более чем на 20 г/л в течение месяца, дозу препарата необходимо уменьшить на 25%. Если уровень Hb превышает 140 г/л, необходимо приостановить лечение до снижения уровня Hb ниже 120 г/л и затем продолжить введение препарата в дозе на 25% ниже первоначальной.
Терапия препаратом должна продолжаться в течение 1 мес после окончания курса химиотерапии.
Уровень ферритина сыворотки (или уровень сывороточного железа) необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости назначается дополнительный прием железа.
Профилактика и лечение анемии у больных с ВИЧ-инфекцией
Рекомендуется до начала лечения препаратом Эральфон® определить исходный уровень эндогенного эритропоэтина в сыворотке крови. Проведенные исследования показывают, что при уровне эритропоэтина более 500 МЕ/мл эффект от терапии препаратом маловероятен.
Лечение препаратом включает 2 этапа.
1. Этап коррекции: препарат назначается в дозе 100 МЕ/кг 3 раза в неделю п/к или в/в в течение 8 нед. Если по истечении 8 нед терапии не удалось достичь удовлетворительного эффекта (например снизить потребность в гемотрансфузиях или добиться повышения уровня Hb), доза может поэтапно увеличиваться (не чаще чем 1 раз в 4 нед) на 50–100 МЕ/кг 3 раза в неделю. Если не удалось достигнуть удовлетворительного эффекта от терапии препаратом Эральфон® в дозе 300 МЕ/кг 3 раза в неделю, то появление ответа на дальнейшую терапию в более высоких дозах маловероятно.
2. Этап поддерживающей терапии: после достижения удовлетворительного эффекта в фазе коррекции анемии поддерживающая доза должна обеспечить уровень гематокрита в пределах 30–35%, в зависимости от изменения дозы зидовудина, наличия сопутствующих инфекционных или воспалительных заболеваний. При гематокрите более 40% следует прекратить введение препарата до снижения гематокрита до 36%. При возобновлении терапии доза эпоэтина альфа должна быть снижена на 25% с последующей корректировкой для поддержания требуемого уровня гематокрита. Уровень ферритина сыворотки (или уровень сывороточного железа) необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости назначается дополнительный прием железа.
Профилактика и лечение анемии у больных с миеломной болезнью, неходжкинскими лимфомами низкой степени злокачественности и хроническим лимфолейкозом
У этих больных целесообразность лечения эпоэтином альфа обусловливается неадекватным синтезом эндогенного эритропоэтина на фоне развития анемии. При уровне Hb ниже 100 г/л и сывороточного эритропоэтина ниже 100 МЕ/мл Эральфон® вводят п/к в стартовой дозе 100 МЕ/кг 3 раза в неделю. Лабораторный контроль гемодинамических показателей проводят еженедельно. При необходимости дозу препарата корректируют в сторону увеличения или уменьшения каждые 3–4 нед. Если при достижении недельной дозы 600 МЕ/кг увеличение уровня Hb не наблюдается, дальнейшее применение эпоэтина альфа следует отменить как неэффективное.
Профилактика и лечение анемии у больных с ревматоидным артритом
У больных с ревматоидным артритом наблюдается подавление синтеза эндогенного эритропоэтина под влиянием повышенной концентрации провоспалительных цитокинов. Лечение анемии у этих больных проводят препаратом при п/к введении в дозе 50–75 МЕ/кг 3 раза в неделю. При увеличении уровня Hb менее чем на 10 г/л через 4 нед лечения дозу препарата увеличивают до 150–200 МЕ/кг 3 раза в неделю. Дальнейшее повышение дозы представляется нецелесообразным.
Лечение и профилактика анемии у недоношенных детей, родившихся с низкой массой тела
Эральфон® вводят п/к в дозе 200 МЕ/кг 3 раза в неделю, начиная с 6-го дня жизни до достижения целевых показателей уровней Hb и гематокрита, но не более 6 нед.
Взрослые пациенты, участвующие в программе сбора аутологичной крови перед хирургическими вмешательствами
Рекомендуется использовать в/в путь введения препарата. Эпоэтин альфа следует вводить по окончании процедуры сбора крови.
Перед назначением препарата следует учесть все противопоказания к сбору аутологичной крови. Перед хирургическим вмешательством Эральфон® следует назначать 2 раза в неделю в течение 3 нед. При каждом посещении врача у больного забирают порцию крови (если гематокрит ≥33% и/или уровень Hb ≥110 г/л) и сохраняют для аутологичной трансфузии. Рекомендуемая доза препарата Эральфон® — 600 МЕ/кг в/в 2 раза в неделю.
Уровень ферритина сыворотки (или уровень сывороточного железа) необходимо определять у всех пациентов до начала и в процессе лечения препаратом. При необходимости назначается дополнительный прием железа.
При наличии анемии ее причина должна быть установлена до начала терапии эпоэтином альфа. Необходимо в кратчайшие сроки обеспечить адекватное поступление железа в организм, назначив перорально препарат железа в дозе 200 мг/сут (из расчета на двухвалентное железо), и поддерживать поступление железа на данном уровне в течение всего курса терапии.
Пациенты в пред- и послеоперационном периоде, не участвующие в программе сбора аутологичной крови
Рекомендуется использовать п/к введение препарата в дозе 600 МЕ/кг в неделю в течение 3 нед, предшествующих операции (21, 14 и 7-й дни перед операцией), и в день операции. При необходимости, когда по медицинским показаниям необходимо сократить предоперационный период, Эральфон® можно назначать ежедневно в дозе 300 МЕ/кг в течение 10 дней до операции, в день операции и в течение 4 дней после операции. Если уровень Hb в предоперационном периоде достигает 150 г/л и выше, применение эпоэтина альфа следует прекратить. До начала терапии эпоэтином альфа необходимо убедиться в отсутствии у пациентов дефицита железа.
Все пациенты должны получать адекватное количество железа (перорально 200 мг/сут из расчета на двухвалентное железо) на протяжении всего курса лечения. По возможности, следует обеспечить дополнительное пероральное поступление железа до начала терапии эпоэтином альфа для обеспечения адекватного депо железа в организме больного.
Устройство и порядок работы со шприцем с автоматическим устройством защиты иглы

Перед инъекцией.

После инъекции.
Составные части:
1. Шток.
2. Зажимы.
3. Защитный кожух.
4. Защитный колпачок.
5. Игла.
После завершения инъекции игла и шприц переместятся назад в защитное устройство.
Внимание! Следует избегать контакта с зажимами во время подготовки шприца! Устройство активируется путем нажатия на шток до зажимов.

Внимательно осмотреть преднаполненный стеклянный шприц с защитным устройством. Снять защитный колпачок с иглы.

Провести инъекцию согласно стандартной процедуре.

Нажать на шток большим пальцем и удерживать до тех пор, пока вся доза препарата не будет введена. Защитное устройство не активируется, пока вся доза препарата не будет введена.

Извлечь иглу, отпустить шток, позволить защитному кожуху переместиться вперед до тех пор, пока игла полностью не будет защищена и заблокирована на месте.
Порядок работы со шприцем с неавтоматическим устройством защиты иглы

Провести инъекцию согласно стандартной процедуре. Внимание! При проведении инъекции необходимо держать пальцы на защитном кожухе, чтобы предотвратить преждевременную активацию защитного устройства.

После инъекции переместить защитное устройство вдоль иглы. Звуковой щелчок укажет на правильность действия. Во время всей процедуры пальцы должны находиться позади иглы.