Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Рекомбинантное человеческое моноклональное антитело (IgG4), которое блокирует передачу сигналов интерлейкина-4 (ИЛ-4) и интерлейкина-13 (ИЛ-13) путем специфического связывания с IL-4Rα-субъединицей, общей для рецепторных комплексов ИЛ- 4 и ИЛ-13. Блокирует передачу сигналов ИЛ-4 через рецепторы I типа (IL-4Rα/γc) и общую передачу сигналов ИЛ-4 и ИЛ-13 через рецепторы II типа (IL-4Rα/IL-13Rα). ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2-го типа (в т.ч. продуцируемые и Тh2-лимфоцитами), вовлеченными в патогенез атопических заболеваний.
Воспаление 2-го типа играет важную роль в патогенезе многих атопических заболеваний, включая бронхиальную астму, способствует ограничению воздушного потока и увеличивает риск обострений. ИЛ-4 и ИЛ-13 выступают в качестве основных факторов воспаления 2-го типа, активируя множественные типы клеток (например, тучные клетки, лимфоциты, эозинофилы, нейтрофилы, макрофаги) и индуцируя множественные медиаторы (например, иммуноглобулин Е, гистамин, эйкозаноиды, лейкотриены, хемокины и цитокины, включая эотаксин/CCL11, TARC/CCL17 и ИЛ-5), участвующие в воспалении 2-го типа. Блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом у пациентов снижает концентрации многих из этих маркеров воспаления 2-го типа, включая иммуноглобулин Е, периостин и множественные провоспалительные цитокины и хемокины (например, эотаксин, TARC), а также снижает уровень фракции оксида азота в выдыхаемом воздухе (FeNO) — маркер воспаления в легких. Было показано, что блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом в гуманизированных моделях животных предотвращает последующие действия этих цитокинов и хемокинов, в т.ч. гиперплазию бокаловидных клеток, гиперреактивность гладкомышечных клеток дыхательных путей, эозинофильное воспаление в легких, другие воспалительные процессы в легких, а также предотвращает нарушение функции легких; при этом снижение выраженности эозинофильного воспаления в легких происходит независимо от нормального или повышенного уровня эозинофилов в крови.
Дупилумаб производится с помощью технологии рекомбинантной ДНК в суспензионной культуре клеток яичника китайского хомячка. Дупилумаб имеет молекулярную массу приблизительно 147 кДа
Фармакокинетика
Фармакокинетика дупилумаба аналогична у пациентов с атопическим дерматитом и бронхиальной астмой.
После однократного п/к введения дупилумаба в дозе 75-600 мг медиана Тmax составляла 3-7 дней. Абсолютная биодоступность дупилумаба после п/к введения сходна между пациентами с атопическим дерматитом и бронхиальной астмой и составляет 61-64% (установлена при популяционном фармакокинетическом анализе).
Введение однократной нагрузочной дозы в первый день приводит к быстрому достижению клинически эффективных концентраций в течение 2 недель.
При схеме лечения 200 мг или 300 мг 1 раз в 2 недели, начиная с нагрузочной дозы 400 мг или 600 мг, Css обычно достигаются в среднем к 16-й неделе лечения. В равновесном состоянии средняя остаточная концентрация перед введением следующей дозы составляла 39 мг/л при применении 200 мг 1 раз в 2 нед. и 70-74 мг/л при применении 300 мг 1 раз в 2 нед.
При еженедельном п/к введении дупилумаба 300 м, начиная с нагрузочной дозы 600 мг, Css обычно достигаются в среднем после 13 недель лечения. В состоянии достижения равновесных концентраций средняя остаточная концентрация перед введением следующей дозы составляла 189 мг/л. Из-за нелинейности клиренса системная экспозиция дупилумаба, определяемая по значению AUC, увеличивается быстрее, непропорционально увеличению дозы после однократного п/к введения в дозах от 75 мг до 600 мг. Vd дупилумаба составляет приблизительно 4.6 л, что указывает на его распределение главным образом в сосудистой системе.
Предполагается, что дупилумаб расщепляется до низкомолекулярных пептидов и отдельных аминокислот.
Выведение дупилумаба осуществляется параллельно линейными и нелинейными путями. При более высоких концентрациях выведение дупилумаба осуществляется главным образом через не насыщаемый протеолитический путь, в то время как при более низких концентрациях выведение преимущественно осуществляется через нелинейное насыщаемое связывание с мишенью IL-4Rα.
После введения последней дозы в равновесном состоянии медиана времени до неопределяемых концентраций дупилумаба, составляет 9 недель при введении 200 мг 1 раз/2 нед., 10-11 недель при введении 300 мг 1 раз/2 нед. и 13 недель при введении 300 мг 1 раз/нед.
Показания активного вещества
ДУПИЛУМАБ
Атопический дерматит среднетяжелого и тяжелого течения у взрослых пациентов при недостаточном ответе на терапию топическими лекарственными препаратами или в случае, когда такие препараты не рекомендованы к применению. Можно применять в качестве монотерапии или одновременно с топическими лекарственными препаратами.
В качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов в возрасте 12 лет и старше с эозинофильным фенотипом или у пациентов с гормональнозависимой бронхиальной астмой, получающих пероральные ГКС.
Режим дозирования
Для п/к введения.
Доза и схема лечения устанавливаются индивидуально, в зависимости от показаний и клинической ситуации.
Побочное действие
Инфекционные заболевания: часто — герпес ротовой полости, простой герпес.
Со стороны системы кроветворения: часто — эозинофилия.
Со стороны органа зрения: часто — конъюнктивит, в т.ч. аллергический, бактериальный; зуд в глазах, блефарит, синдром «сухого» глаза.
Аллергические реакции: очень редко — анафилаксия.
Местные реакции: очень часто — реакции в месте инъекции, эритема; часто — отек, зуд в месте инъекции.
Противопоказания к применению
Повышенная чувствительность к дупилумабу; детский возраст до 18 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения; детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения.
Применение при беременности и кормлении грудью
При беременности возможно применение только в случаях, когда ожидаемая польза терапии для матери превышает потенциальный риск для плода.
Неизвестно, выделяется ли дупилумаб с грудным молоком у человека. Следует, с учетом пользы грудного вскармливания для ребенка и преимущества дальнейшего применения препарата для матери, принят решение о прекращении кормления грудью или отмене дупилумаба в течение периода грудного вскармливания
Применение у детей
Противопоказания: детский возраст до 18 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения; детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения.
Особые указания
При возникновении системной реакции гиперчувствительности лечение средством следует немедленно прекратить, и начать соответствующую терапию. Сообщалось об одном случае развития реакции, подобной сывороточной болезни, и об одном случае развития сывороточной болезни после применения дупилумаба. При применении средства при бронхиальной астме сообщалось об одном случае развития анафилаксии.
Конъюнктивит чаще отмечался у пациентов с атопическим дерматитом, получавших дупилумаб. Большинство пациентов с конъюнктивитом выздоровели или выздоравливали в течение периода лечения. Среди пациентов с бронхиальной астмой частота конъюнктивита была низкой. Следует рекомендовать пациентам незамедлительно сообщать о первом появлении или ухудшении симптомов со стороны глаз своему лечащему врачу.
У пациентов с бронхиальной астмой может развиться серьезная системная эозинофилия, иногда в виде клинических признаков эозинофильной пневмонии или васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, которые часто лечатся системными кортикостероидами. Эти события, как правило, но не всегда, могут быть связаны с сокращением приема пероральных кортикостероидов. Врачи должны быть внимательны к васкулитной сыпи, ухудшающимся легочным симптомам, сердечным осложнениям и/или нейропатии, возникающим у их пациентов с эозинофилией. Имеются сообщения о случаях эозинофильной пневмонии и васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, при применении дупилумаба. Связь между применением дупилумаба и этими состояниями не была установлена.
Средство не следует назначать для лечения симптомов остро возникшего ухудшения или обострений астмы. Дупилумаб не применяют для лечения острого бронхоспазма или астматического статуса.
Не следует резко прерывать применение системных, местных или ингаляционных ГКС после начала терапии дупилумабом. Сокращение дозы глюкокортикостероидов, при необходимости, должно быть постепенным и должно выполняться под непосредственным наблюдением врача. Уменьшение дозы ГКС может сопровождаться системными симптомами отмены и/или манифестацией состояний, которые ранее не проявлялись из-за системной терапии ГКС.
Неизвестно, может ли дупилумаб повлиять на иммунный ответ при гельминтозах. Необходимо провести лечение пациентов с имеющимся гельминтозом перед тем, как начинать лечение дупилумабом. Если во время лечения пациент заражается гельминтозом, а антигельминтные препараты оказываются неэффективными, следует прекратить лечение дупилумабом до излечения паразитарного заболевания.
Пациентам с атопическим дерматитом и с сопутствующей бронхиальной астмой следует рекомендовать не изменять своего лечения, не проконсультировавшись с лечащим врачом. Прекращая лечение дупилумабом, следует принимать во внимание возможные эффекты на течение других атопических заболеваний
Дупиксент — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005440
Торговое наименование препарата:
Дупиксент®.
Международное непатентованное наименование:
дупилумаб.
Лекарственная форма:
раствор для подкожного введения.
Состав
| Ингредиент | Количество (дозировка 50 мг/мл) | Количество (дозировка 175 мг/мл) | ||
| в 1 мл | в шприцеa | в 1 мл | в шприцеb | |
| Действующее вещество | ||||
| Дупилумаб | 150 мг | 300 мг | 175 мг | 200 мг |
| Вспомогательные вещества | ||||
| L-гистидин | 3,1 мгc | 6,2 мгc | 3,1 мгc | 3,54 мгc |
| L-гистидина гидрохлорида моногидрат | ||||
| L-аргинина гидрохлорид | 4,35 мгd | 8,7 мгd | 10,51 мгe | 12,01 мгe |
| Натрия ацетата тригидрат | 0,75 мгf | 1,5 мгf | 0,75 мгf | 0,86 мгf |
| Уксусная кислота ледяная | ||||
| Сахароза | 50 мгg | 100 мг | 49,88 мгg | 57,00 мг |
| Полисорбат-80 | 2 мгi | 4 мг | 2 мгi | 2,28 мг |
| Вода для инъекций | до 1,0 мл | до 2,0 мл | до 1,0 мл | до 1,14 мл |
a) В расчете на 2,0 мл препарата.
b) В расчете на 1,14 мл препарата.
c) Содержание L-гистидина и L-гистидина гидрохлорида приведено в пересчете на L-гистидин (М=155,16 г/моль), исходя из общей концентрации гистидина в препарате 20 мМ.
d) Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 25 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) в одном шприце составляет 10,5 мг.
e) Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М= 174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 50 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) для дозировки 175 мг/мл составляет 9,93 мг.
f) Содержание натрия ацетата тригидрата и уксусной кислоты ледяной приведено, исходя из общей концентрации ацетат иона в препарате 12,5 мМ.
g) Содержание сахарозы приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации сахарозы в препарате 5%.
h) Содержание полисорбата-80 приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации полисорбата-80 в препарате 0,2%.
Описание
Прозрачная или слегка опалесцирующая, бесцветная или желтоватого цвета жидкость.
Фармакотерапевтическая группа:
ингибиторы интерлейкина.
Код ATX:
D11AH05.
Фармакологические свойства
Механизм действия
Препарат Дупиксент® является рекомбинантным человеческим моноклональным антителом (IgG4), которое блокирует передачу сигналов интерлейкина-4 (ИЛ-4) и интерлейкина-13 (ИЛ-13) путем специфического связывания с 1L-4Rа-субъединицей, общей для рецепторных комплексов ИЛ-4 и ИЛ-13. Препарат Дупиксент® блокирует передачу сигналов ИЛ-4 через рецепторы I типа (IL-4Rα/γc) и общую передачу сигналов ИЛ-4 и ИЛ-13 через рецепторы II типа (IL-4Rα/IL-13Ra). ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2-го типа (в том числе продуцируемые и Th2-лимфоцитами), вовлеченными в патогенез атопических заболеваний.
Воспаление 2-го типа играет важную роль в патогенезе многих атонических заболеваний, включая бронхиальную астму, способствует ограничению воздушного потока и увеличивает риск обострений. ИЛ-4 и ИЛ-13 выступают в качестве основных факторов воспаления 2-го типа, активируя множественные типы клеток (например, тучные клетки, лимфоциты, эозинофилы, нейтрофилы, макрофаги) и индуцируя множественные медиаторы (например, иммуноглобулин Е, гистамин, эйкозаноиды, лейкотриены, хемокины и цитокины, включая эотаксин/CCL11, TARC/CCL17 и ИЛ-5), участвующие в воспалении 2-го типа. Блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом у пациентов снижает концентрации многих из этих маркеров воспаления 2-го типа, включая иммуноглобулин Е, периостин и множественные провоспалительные цитокины и хемокины (например, эотаксин, TARC), а также снижает уровень фракции оксида азота в выдыхаемом воздухе (FeNO) – маркер воспаления в легких. Было показано, что блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом в гуманизированных моделях животных предотвращает последующие действия этих цитокинов и хемокинов, в том числе гиперплазию бокаловидных клеток, гиперреактивность гладкомышечных клеток дыхательных путей, эозинофильное воспаление в легких, другие воспалительные процессы в легких, а также предотвращает нарушение функции легких; при этом снижение выраженности эозинофильного воспаления в легких происходит независимо от нормального или повышенного уровня эозинофилов в крови.
Дупилумаб производится с помощью технологии рекомбинантной ДНК в суспензионной культуре клеток яичника китайского хомячка.
Дупилумаб имеет молекулярную массу приблизительно 147 кДа.
Фармакодинамика
Атопический дерматит
В клинических исследованиях лечение препаратом Дупиксент® приводило к снижению в сыворотке крови концентраций биомаркеров, связанных с цитокинами воспаления 2-го типа, таких как тимус ассоциированного регуляторного хемокина (TARC/CCL17), общего сывороточного иммуноглобулина Е и аллерген-специфического иммуноглобулина Е. Также наблюдалось снижение активности лактатдегидрогеназы (ЛДГ), биомаркера, связанного со степенью тяжести атопического дерматита и его активностью. Препарат Дупиксент® уже в начале 2-й недели лечения вызывал супрессию хемокина TARC по сравнению с плацебо, с тенденцией продолжения его снижения до максимальной и устойчивой супрессии к 12-й неделе лечения.
У пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели и в дозе 300 мг 1 раз в неделю, общий сывороточный иммуноглобулин Е к 52-й неделе терапии снизился на -74,8% и -73,9% (медиана изменения по сравнению с исходным уровнем), соответственно, по сравнению с -0% в группе плацебо. Аналогичные тенденции наблюдались в отношении антиген-специфических иммуноглобулинов Е, в том числе энтеротоксина А, специфического для золотистого стафилококка (S. aureus), аллергенов трав и деревьев.
Бронхиальная астма
В соответствии с ингибированием передачи сигналов ИЛ-4 и ИЛ-13, лечение дупилумабом заметно уменьшало уровень FeNO и концентрации эотаксина-3, общего иммуноглобулина Е, аллерген-специфического иммуноглобулина Е, TARC и периостина у пациентов с бронхиальной астмой по сравнению с плацебо. Эти снижения уровней биомаркеров воспаления были сопоставимы для режимов дозирования 200 мг 1 раз в 2 недели и 300 мг 1 раз в 2 недели и были близки к максимальному подавлению через 2 недели лечения, за исключением иммуноглобулина Е, который уменьшался медленнее. Описанные эффекты были устойчивыми во время лечения.
Клиническая эффективность
Атонический дерматит
Эффективность и безопасность препарата Дупиксент® в монотерапии или в сочетании с топическими глюкокортикостероидами (ГКС) оценивали в трех основных рандомизированных, двойных слепых, плацебо-контролируемых исследованиях (SOLO 1, SOLO 2 и CHRONOS) с участием 2119 пациентов в возрасте 18 лет и старше со среднетяжелым и тяжелым течением атопического дерматита
16-недельные исследования монотерапии (SOLO 1 и SOLO 2)
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й неделе лечения в клиническом исследовании SOLO 1 достигли 37,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 37,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 10,3% пациентов в группе плацебо, а в исследовании SOLO 2 – 36,1% и 36,4% против 8,5%, пациентов, соответственно.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й неделе лечения в исследовании SOLO 1 достигли 51,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 52,5% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 14,7% пациентов в группе плацебо, а в исследовании SOLO 2 – 44,2% и 48,1% против 11,9%, соответственно.
Не менее чем 4-бального уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда (NRS) к 16-й неделе лечения в исследовании SOLO 1 достигли 40,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 40,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 12,3% пациентов в группе плацебо, а в исследовании SOLO 2 – 36,0% и 39,0% пациентов против 9,5%, соответственно. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение уже на 2-й неделе), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением на подгруппы по массе тела, возрасту, полу, расе и сопутствующей терапии, в том числе с применением иммунодепрессантов) в исследованиях SOLO 1 и SOLO 2 в целом согласуются с результатами, полученными в общей исследуемой популяции.
52-недельное клиническое исследование с одновременным применением топических ГКС (CHRONOS)
IGA 0 или 1 к 16-й неделе лечения достигли 38,7% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 39,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 12,4% пациентов в группе плацебо, а к 52-й неделе – 36,0% и 40,0% против 12,5% пациентов, соответственно.
EASI-75 к 16-й неделе лечения достигли 68,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 63,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 23,2% пациентов в группе плацебо + топические ГКС, а к 52-й неделе – 65,2% и 64,1% против 21,6% пациентов, соответственно.
Не менее чем 4-бального улучшения по шкале тяжести зуда NRS к 16-й неделе лечения достигли 58,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 50,8% пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 19,7% пациентов в группе плацебо + топические ГКС, а к 52-й неделе – 51,2% и 39,0% против 12,9% пациентов, соответственно. Более значительный процент пациентов, получавших препарат Дупиксент® + топические ГКС, достигал быстрого улучшения по шкале тяжести зуда NRS по сравнению с пациентами в группе плацебо + топические ГКС (определяемого как >4-балльное улучшение уже на 2-й неделе; р <0,05), причем доля пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжала увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением по массе тела, возрасту, полу, расе и сопутствующей терапии, в том числе с применением иммунодепрессантов) в исследовании CHRONOS в целом согласуются с результатами, полученными в общей исследуемой популяции.
Клиническая эффективность у пациентов, которым не рекомендовалось лечение циклоспорином
У пациентов, которым не рекомендовалось лечение циклоспорином или оно было неэффективно, монотерапия препаратом Дупиксент® в обеих группах лечения, приводила к значительному улучшению признаков и симптомов атопического дерматита по сравнению с плацебо. Больший процент пациентов, получавших Дупиксент®, по сравнению с группой плацебо достигал IGA 0 или 1 и снижения по сравнению с исходным значением на ≥2 балла к 16-й неделе (29,5% против 6,8%), EASI-75 к 16-й неделе (38% против 11,4%), а также снижения не менее чем на 4 балла индекса тяжести зуда от исходного значения к 16-й неделе (34,9% по сравнению с 8%) (р <0,001 для всех 3 конечных точек). Аналогичные результаты наблюдались у пациентов, получавших Дупиксент® одновременно с топическими ГКС. Эффективность комбинации препарата Дупиксент® + топические ГКС сохранялась до 52-й недели терапии.
Бронхиальная астма
Было проведено три рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых исследования в параллельных группах (DRI12544, QUEST и VENTURE) продолжительностью от 24 до 52 недель с участием 2888 пациентов (в возрасте 12 лет и старше). Во все три исследования пациенты были включены независимо от минимального исходного уровня эозинофилов или другого биомаркера воспаления 2-го типа (например, уровня FeNO или иммуноглобулина Е).
Обострения бронхиальной астмы
В исследованиях DRI12544, QUEST и VENTURE оценивали частоту тяжелых обострений астмы независимо от минимального количества эозинофилов или любых других биомаркеров воспаления 2-го типа (например, FeNO или иммуноглобулин Е) в начале исследования. В общей популяции, независимо от содержания эозинофилов и других биомаркеров воспаления 2-го типа, у пациентов, получавших 200 или 300 мг препарата Дупиксент® один раз в две недели, произошло значительное снижение частоты тяжелых обострений астмы по сравнению с группой плацебо. В исследованиях DRI12544 и QUEST частота тяжелых обострений при применении препарата Дупиксент® в дозе 200 мг 1 раз в 2 недели снижалась на 70% и 48%; а при применении в дозе 300 мг 1 раз в 2 недели – на 70% и 46%, соответственно; и на 59% в исследовании VENTURE.
В объединенном анализе исследований DRI12544 и QUEST частота тяжелых обострений, приводящих к госпитализации и/или посещениям отделений неотложной помощи, снизилась на 25,5% и 46,9% при применении препарата Дупиксент® в дозах 200 мг или 300 мг 1 раз в 2 недели, соответственно.
Кумулятивное среднее число тяжелых обострений было более низкое у пациентов, получавших препарат Дупиксент® по сравнению с плацебо в исследованиях DRI12544, QUEST и VENTURE (в общей популяции и в популяции с исходным числом эозинофилов ≥150 клеток/мкл или FeNO ≥25 ppb) в течение 24- или 52-недельного периода лечения в обеих группах режимов дозирования препарата.
В исследовании QUEST у пациентов, получавших ингаляционные глюкокортикостероиды (ИКС) в средней дозе, наблюдалось сходное снижение частоты тяжелых обострений астмы по сравнению с пациентами, получавшими ИКС в высокой дозе.
Функция легких
Клинически значимое увеличение предбронходилатационного значения объема форсированного выдоха за 1-ю секунду (ОФВ1) наблюдалось на 12-й неделе в общей популяции независимо от уровня эозинофилов или других биомаркеров воспаления 2-го типа (например, FeNO или иммуноглобулин Е). В исследованиях DRI12544, QUEST и VENTURE, по сравнению с плацебо, большее улучшение ОФВ1 наблюдалось также у пациентов с FeNO ≥25 ppb. Улучшение ОФВ1 было одинаковым, независимо от того, получали ли пациенты ИКС в средней дозе, ИКС в высокой дозе или пероральные глюкокортикостероиды (ОКС).
Значительные улучшения ОФВ1 наблюдались уже в течение второй недели (DRI12544, QUEST и VENTURE) после первой инъекции препарата Дупиксент® в дозе как 200 мг, так и 300 мг и сохранялись в течение 24 недель (DRI12544 и VENTURE) и 52 недель (QUEST).
Скорректированная средняя разность абсолютных значений ОФВ1 была 0,20 л и 0,14 л в группах, получавших Дупиксент® 200 мг 1 раз в 2 недели, по сравнению с плацебо; 0,16 и 0,13 л в группах, получавших 300 мг 1 раз в 2 недели по сравнениюс плацебо, соответственно в исследованиях DR112544 и QUEST. Соответствующее процентное изменение ОФВ1 составляло от 9,2 до 11,9% для дозы 200 мг 1 раз в 2 недели и от 9,4 до 11,7% для дозы 300 мг 1 раз в 2 недели. Скорректированная средняя разность абсолютных значений пре-бронходилатационного ОФВ1 от исходного уровня к 24-й неделе (достаточное время для достижения максимального снижения дозы пероральных глюкокортикостероидов) в исследовании VENTURE составила 0,22 л в группе применения препарата Дупиксент® по сравнению с плацебо, что соответствовало улучшению на 15,1% по сравнению с исходным уровнем.
Кроме того, у пациентов, получавших препарат Дупиксент®, значительно улучшился пост-бронходилатационный показатель ОФВ1 по сравнению с исходным уровнем на 12-й и 52-й неделях по сравнению с плацебо, что указывает на то, что препарат Дупиксент® улучшает фиксированную обструкцию дыхательных путей. В группе применения препарата Дупиксент® в течение года наблюдения не было зарегистрировано снижения функции легких с учетом значения пост-бронходилатационного значения ОФВ1.
Снижение дозы пероральных глюкокортикостероидов
В исследовании VENTURE оценивалось влияние препарата Дупиксент® на снижение применения поддерживающих пероральных глюкокортикостероидов. Исходная средняя доза пероральных кортикостероидов составляла 11,75 мг в группе плацебо и 10,75 мг в группе, получавшей препарат Дупиксент®. По сравнению с плацебо, у пациентов, получавших Дупиксент®, отмечалось большее снижение ежедневной дозы пероральных глюкокортикостероидов при сохранении контроля над астмой. Среднее общее снижение ежедневной дозы пероральных глюкокортикостероидов при сохранении контроля над астмой составляло 70,1% по сравнению с исходным уровнем у пациентов, получавших Дупиксент® и 41,9% в группе плацебо.
Исходы, сообщаемые пациентами
Кроме того, во всех 3-х исследованиях Дупиксент® обеспечил клинически значимое улучшение показателей контроля бронхиальной астмы в общей популяции по сравнению с группой плацебо, о чем свидетельствуют показатели ACQ-5 и соответствующее улучшение качества жизни, измеренное по шкале AQLQ(S). Улучшение показателей ACQ-5 и AQLQ(S) были зарегистрированы уже через 2 недели и это улучшение сохранялось на протяжении 24-х недель в исследовании DRI12544 и 52-х недель в исследовании QUEST. В общей популяции исследования QUEST доля пациентов, ответивших на лечение, что выражалось в достижении минимального клинически-значимого различия показателей ACQ-5 и AQLQ(S), была существенно выше к 52-й неделе в группе, получавшей обе дозы препарата Дупиксент®.
Фармакокинетика
Фармакокинетика дупилумаба аналогична у пациентов с атопическим дерматитом и бронхиальной астмой.
Абсорбция
После однократного подкожного введения 75-600 мг дупилумаба, медиана времени достижения максимальной концентрации в сыворотке крови (Тmax) составляла 3-7 дней. Абсолютная биодоступность дупилумаба после введения подкожной дозы сходна между пациентами с атопическим дерматитом и бронхиальной астмой и составляет 61-64% (установлена при популяционном фармакокинетическом анализе).
Введение однократной нагрузочной дозы в первый день приводит к быстрому достижению клинически эффективных концентраций в течение 2-х недель.
При схеме лечения 200 мг или 300 мг 1 раз в 2 недели, начиная с нагрузочной дозы 400 мг или 600 мг, равновесные концентрации дупилумаба обычно достигаются в среднем к 16-й неделе лечения. В состоянии достижения равновесных концентраций средняя остаточная концентрация перед введением следующей дозы составляла 39 мг/л при применении 200 мг 1 раз в 2 недели и 70-74 мг/л при применении 300 мг 1 раз в 2 недели.
При еженедельном подкожном введении 300 мг препарата Дупиксент®, начиная с нагрузочной дозы 600 мг, равновесные концентрации обычно достигаются в среднем после 13 недель лечения. В состоянии достижения равновесных концентраций средняя остаточная концентрация перед введением следующей дозы составляла 189 мг/л.
Линейность дозы
Из-за нелинейности клиренса системная экспозиция дупилумаба, определяемая по площади под фармакокинетической кривой «концентрация-время» (AUC), увеличивается быстрее, непропорционально увеличению дозы после однократного подкожного введения препарата в дозах от 75 мг до 600 мг.
Распределение
Объем распределения дупилумаба составляет приблизительно 4,6 л, что указывает на его распределение главным образом в сосудистой системе.
Метаболизм
Поскольку дупилумаб является белком, специальных исследований его метаболизма не проводилось. Предполагается, что дупилумаб расщепляется до низкомолекулярных пептидов и отдельных аминокислот.
Выведение
Выведение дупилумаба осуществляется параллельно линейными и нелинейными путями. При более высоких концентрациях выведение дупилумаба осуществляется главным образом через не насыщаемый протеолитический путь, в то время как при более низких концентрациях выведение препарата преимущественно осуществляется через нелинейное насыщаемое связывание с мишенью IL-4Rα.
После введения последней дозы в состоянии равновесной концентрации медиана времени до неопределяемых концентраций дупилумаба, составляет 9 недель при введении 200 мг 1 раз в 2 недели, 10-11 недель при введении 300 мг 1 раз в 2 недели и 13 недель при введении 300 мг 1 раз в неделю.
Особые группы пациентов
Пол
Пол пациента не влиял на фармакокинетические показатели препарата. Дупиксент®.
Возраст
Возраст пациента не влиял на фармакокинетические показатели препарата. Дупиксент®.
Пациенты пожилого возраста
По данным популяционного анализа фармакокинетических показателей возраст пациентов не влиял на эффективность и безопасность препарата Дупиксент®.
Пациенты детского возраста
Фармакокинетика дупилумаба у детей и подростков до 18 лет с атопическим дерматитом и у детей с бронхиальной астмой младше 12 лет не изучалась. Эффективность и профиль нежелательных реакций у подростков с бронхиальной астмой старше 12 лет были схожи с таковыми у взрослых.
Расовая принадлежность
Согласно результатам популяционного фармакокинетического анализа расовая принадлежность не влияла на фармакокинетические показатели препарата Дупиксент®.
Печеночная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной печеночной элиминации. Клинические исследования для оценки влияния печеночной недостаточности на фармакокинетику дупилумаба не проводились.
Почечная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной почечной элиминации. Клинические исследования для оценки влияния почечной недостаточности на фармакокинетику дупилумаба не проводились. Результаты популяционных фармакокинетических анализов показали, что нарушение функции почек легкой и средней степени тяжести существенным образом не влияет на системную экспозицию дупилумаба. Нет данных о применении дупилумаба у пациентов с тяжелой почечной недостаточностью.
Масса тела
Не требуется коррекции режима дозирования в зависимости от массы тела пациента.
Показания к применению
- Атопический дерматит среднетяжелого и тяжелого течения у взрослых пациентов при недостаточном ответе на терапию топическими лекарственными препаратами или в случае, когда такие препараты не рекомендованы к применению.
Препарат Дупиксент® может применяться в монотерапии или одновременно с топическими лекарственными препаратами. - В качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов в возрасте 12 лет и старше с эозинофильным фенотипом или у пациентов с гормональнозависимой бронхиальной астмой, получающих пероральные глюкокортикостероиды.
- В качестве дополнительной поддерживающей терапии взрослых пациентов с плохо контролируемым тяжелым хроническим полипозным риносинуситом (ХПРС)
Противопоказания
Повышенная чувствительность к дупилумабу или любому из вспомогательных веществ препарата (см. раздел «Особые указания).
Детский возраст до 18 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью.
Детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью.
С осторожностью
При беременности (только если ожидаемая польза превышает потенциальный риск для плода).
Применение при беременности и в период грудного вскармливания
Беременность
Имеются лишь ограниченные данные по применению дупилумаба у беременных женщин. В исследованиях, проведенных на животных, прямых и косвенных неблагоприятных эффектов в отношении репродуктивной токсичности не обнаружено. Препарат Дупиксент® можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода.
Период грудного вскармливания
Неизвестно, экскретируется ли дупилумаб в грудное молоко человека. Следует, с учетом пользы грудного вскармливания для ребенка и преимущества дальнейшего применения препарата для матери, принять решение о прекращении кормления грудью или отмене препарата Дупиксент® в течение периода грудного вскармливания.
Способ применения и дозы
Общие рекомендации
Препарат Дупиксент® вводится подкожно.
Атопический дерматит
• Рекомендуемая доза препарата Дупиксент® у взрослых пациентов: начальная доза – 600 мг (2 инъекции по 300 мг), далее – по 300 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг еженедельно.
Бронхиальная астма
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов и детей (12 лет и старше):
• начальная доза – 400 мг (2 инъекции по 200 мг), далее – по 200 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг каждые 2 недели.
• начальная доза – 600 мг (2 инъекции по 300 мг), далее – по 300 мг каждые 2 недели для пациентов с глюкокортикостероидозависимой бронхиальной астмой или с сопутствующим среднетяжелым или тяжелым атопическим дерматитом, при котором показано применение препарата Дупиксент®.
В случае пропуска дозы пациент должен получить инъекцию как можно скорее и затем продолжить лечение в соответствии с назначенным ему режимом введения препарата.
Особые группы пациентов
Дети
Безопасность и эффективность препарата Дупиксент® у детей и подростков до 18 лет с атопическим дерматитом не установлена.
Безопасность и эффективность препарата Дупиксент® у детей в возрасте до 12 лет с бронхиальной астмой не установлена.
Пациенты пожилого возраста
У пациентов пожилого возраста коррекции дозы не требуется (см. раздел «Фармакокинетика»).
Печеночная недостаточность
Отсутствуют данные по применению препарата у пациентов с печеночной недостаточностью (см. раздел «Фармакокинетика»).
Почечная недостаточность
У пациентов с легкой или средней степенью тяжести почечной недостаточности коррекции дозы не требуется. Отсутствуют данные по применению препарата у пациентов с тяжелой почечной недостаточностью (см. раздел «Фармакокинетика»).
Масса тела
Не требуется коррекции режима дозирования в зависимости от массы тела пациента (см. раздел «Фармакокинетика»).
Способ применения
Перед введением препарата следует осмотреть его на предмет наличия в растворе твердых частиц или появления нехарактерной окраски раствора. Если в препарате содержатся твердые частицы или у раствора появилась нехарактерная окраска, вводить препарат нельзя.
Раствор в предварительно заполненном шприце с системой защиты или предварительно заполненном шприце перед проведением инъекции препарата Дупиксент® должен нагреться до комнатной температуры. Для этого рекомендуется выдержать его при комнатной температуре в течение 45 мин (для дозировки 300 мг) или 30 мин (для дозировки 200 мг).
В случае необходимости предварительно заполненный шприц можно хранить при комнатной температуре (до 25 °С) в течение максимум 14 дней. Препарат нельзя хранить при температуре выше 25 °С. После извлечения из холодильника Дупиксент® должен быть использован в течение 14 дней или утилизирован.
Шприцы следует защищать от нагревания и воздействия прямого солнечного света.
Если начальная доза составляет 600 мг, следует сделать две инъекции по 300 мг в разные места для инъекций.
Если начальная доза составляет 400 мг, следует сделать две инъекции по 200 мг в разные места для инъекций.
Лечение препаратом Дупиксент® следует проводить под медицинским наблюдением. Инъекцию препарата может делать себе либо сам пациент, либо лицо, ухаживающее за ним.
Необходимо до начала применения препарата Дупиксент® обучить пациентов и/или ухаживающих за ними лиц подготовке и проведению инъекции препарата Дупиксент®, согласно указаниям в «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты», «Инструкции по подготовкеи проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце» и «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты».
Препарат Дупиксент® может вводиться самим пациентом подкожно с помощью предварительно заполненного одноразового шприца в область бедра или живота, за исключением области диаметром 5 см непосредственно вокруг пупка. Если инъекцию проводит другой человек, препарат также можно вводить в верхнюю часть плеча.
Рекомендуется менять места инъекций при каждом введении препарата.
Инъекцию препарата Дупиксент® не следует проводить в участки с болезненной и поврежденной кожей, в места с кровоподтеками или рубцами.
Все остатки неиспользованного препарата и расходные материалы должны утилизироваться в соответствии с требованиями местного законодательства.
Побочное действие
Атопический дерматит
Для описания частоты встречаемости нежелательных реакций используется следующая классификация: очень часто ≥10%; часто ≥1% и <10%; нечасто ≥0,1% и <1%; редко ≥0,01% и <0,1%; очень редко <0,01%; частота неизвестна (невозможно определить по имеющимся данным частоту встречаемости нежелательной реакции).
Табл. 1. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с атопическим дерматитомa
| Системно-органный класс | Частота | Нежелательные реакции |
| Инфекционные и паразитарные заболевания | Часто | Конъюнктивит (4,0%) |
| Герпес ротовой полости (3,8%) | ||
| Бактериальный конъюнктивит (1,9%) | ||
| Простой герпес (Herpes simplex)b (1,7%) | ||
| Нарушения со стороны крови и лимфатической системы | Часто | Эозинофилия (1,7%) |
| Нарушения со стороны органа зрения | Часто | Аллергический конъюнктивит (7,0%) |
| Зуд в глазах (2,9%) | ||
| Блефарит (4,5%) | ||
| Синдром сухого глаза (1,8%) | ||
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Реакции в месте инъекции (15,9%) |
a Объединенные данные плацебо-контролируемых клинических исследований с проведением монотерапии (SOLO 1, SOLO 2 и исследования по подбору доз 2 фазы) и плацебо-контролируемого исследования CHRONOS с одновременным применением топических ГКС для лечения атопического дерматита: пациенты получали препарат в дозе 300 мг 1 раз в 2 недели и 300 мг 1 раз в неделю с или без топических ГКС в течение 16 недель.
b В клинических исследованиях случаи с герпетическими инфекциями (Herpes simplex) проявлялись поражениями кожи и слизистых оболочек, обычно были легкой или средней степени тяжести и не включали герпетическую экзему. О случаях герпетической экземы сообщалось отдельно, частота таких случаев была ниже у пациентов, получавших препарат Дупиксент®, по сравнению с группой плацебо.
Профиль безопасности комбинированного лечения препаратом Дупиксент® + топические ГКС в течение 52 недель соответствует профилю его безопасности, наблюдавшемуся к 16-й неделе.
Бронхиальная астма
Табл. 2. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с бронхиальной астмой
| Системно-органный класс | Частота | Нежелательные реакции |
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Эритема в месте инъекции (14,6%) |
| Часто | Отек в месте инъекции (4,8%) | |
| Часто | Зуд в месте инъекции (4,7%) | |
| Очень редко | Анафилаксия (0,04%) |
Описание отдельных нежелательных реакций
Конъюнктивит
За время 52-недельного периода лечения в клиническом исследовании с одновременным применением топических ГКС (CHRONOS) конъюнктивит был зарегистрирован в 16% случаев в группе пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС (20 на 100 пациенто-лет), и в 9% случаев, в группе плацебо + топические ГКС (10 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота конъюнктивита была схожей в группах, получающих препарат Дупиксент® или плацебо.
Герпетическая экзема и Herpes zoster
В клинических исследованиях у пациентов с атопическим дерматитом частота герпетической экземы была схожей в группах, получающих препарат Дупиксент® и в группе плацебо. По данным 16-недельных исследований монотерапии, Herpes zoster был зарегистрирован в <0,1% случаев в группе, получающей Дупиксент® (<1 на 100 пациенто-лет) и <1% в группе плацебо (1 на 100 пациенто-лет). В 52-недельном клиническом исследовании с одновременным применением топических ГКС (CHRONOS) Herpes zoster был зарегистрирован в 1% случаев в группе, получающей Дупиксент® + топические ГКС (1 на 100 пациенто-лет) и в 2% в группе плацебо (2 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота Herpes zoster была схожей в группах, получающих препарат Дупиксент® или плацебо.
Гиперчувствительность
В клинических исследованиях при атопическом дерматите сообщалось об одном случае развития сывороточной болезни и одном случае реакции, подобной сывороточной болезни, после введения препарата Дупиксент® (оба нежелательных явления оценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном серьезном случае развития анафилаксии после введения препарата Дупиксент® (см. раздел «Особые указания»).
Эозинофилы
У пациентов, получавших препарат Дупиксент®, наблюдалось более высокое среднее начальное увеличение от исходного уровня эозинофилов по сравнению с пациентами, получавшими плацебо. Количество эозинофилов снижалось почти до базовых уровней во время исследования.
Частота эозинофилии, вызванной лечением (≥ 500 клеток/мкл), была сходной в группах пациентов, получавших препарат Дупиксент® и плацебо.
Эозинофилия, вызванная лечением (≥5000 клеток/мкл), была зарегистрирована менее чем у 2% пациентов, получавших препарат Дупиксент®, и менее чем у 0,5% пациентов, получавших плацебо.
Инфекции
В клинических исследованиях не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 16-недельных клинических исследованиях, в которых проводилась монотерапия препаратом Дупиксент®, были зарегистрированы серьезные инфекции у 1,0% пациентов, получавших плацебо, и у 0,5% пациентов, получавших дупилумаб. В 52-недельном исследовании CHRONOS серьезные инфекции были зарегистрированы у 0,6% пациентов, получавших плацебо, и у 0,2% пациентов, получавших препарат Дупиксент®.
В клинических исследованиях у пациентов с бронхиальной астмой не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 24-недельном клиническом исследовании были зарегистрированы серьезные инфекции у 1,0% пациентов, получавших дупилумаб, и у 1,1% пациентов, получавших плацебо. В 52-недельном исследовании QUEST серьезные инфекции были зарегистрированы у 1,3% пациентов, получавших дупилумаб, и у 1,4% пациентов, получавших плацебо.
Сердечно-сосудистые события
В 1-летнем плацебо контролируемом исследовании у пациентов с бронхиальной астмой (QUEST) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,2%) в группе пациентов, получавших Дупиксент® 200 мг 1 раз в 2 недели; в 4 случаях (0,6%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели и в 2 случаях (0,3%) в группе плацебо. В 1-летнем плацебо контролируемом исследовании у пациентов с атопическим дерматитом (CHRONOS) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,9%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели + топические ГКС; в 0 случаев (0,0%) в группе пациентов, Дупиксент® 300 мг 1 раз в неделю + топические ГКС и в 1 случае (0,3%) в группе плацебо + топические ГКС.
Иммуногенность
Как и все белковые лекарственные препараты, препарат Дупиксент® может вызывать аллергические реакции.
Примерно у 6% пациентов с атопическим дерматитом или бронхиальной астмой, которые получали препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител против дупилумаба (АТ); приблизительно у 2% пациентов АТ стойко сохранялись и приблизительно 2% имели нейтрализующие антитела.
Примерно у 9% пациентов с бронхиальной астмой, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител против дупилумаба; приблизительно у 4% АТ стойко сохранялись и приблизительно 4% имели нейтрализующие антитела.
Приблизительно 5% пациентов в группах плацебо в 52-недельных исследованиях имели положительные антитела к препарату Дупиксент®; приблизительно у 2% АТ стойко сохранялись и приблизительно 1% имел нейтрализующие антитела.
Реакция образования антител обычно не влияла на системную экспозицию дупилумаба, безопасность или эффективность препарата. Менее чем у 0,4% пациентов были выявлены высокие титры антител к дупилумабу, ассоциирующиеся со снижением его системной экспозиции и эффективности. Кроме того, у одного пациента была обнаружена сывороточная болезнь, а у другого реакция, подобная сывороточной болезни (<0,1%), ассоциировавшиеся с высокими титрами антител (см. раздел «Особые указания»).
Наблюдаемая частота стойкого сохранения АТ и нейтрализующей активности в значительной степени зависят от чувствительности и специфичности используемого аналитического метода. Кроме того, наблюдаемая частота АТ-положительного статуса в анализе может зависеть от нескольких факторов, в том числе методики анализа, способа обработки проб, времени сбора проб, сопутствующих препаратов, а также статуса основного заболевания в каждом отдельном случае. По этим причинам сравнение частоты образования антител к дупилумабу с частотой выработки антител к другим препаратам может ввести в заблуждение.
Передозировка
В клинических исследованиях не было выявлено проблем, связанных с безопасностью, при однократном внутривенном введении доз до 12 мг/кг.
Специфического антидота при передозировке препаратом Дупиксент® не существует. В случае передозировки необходимо контролировать состояние пациента для своевременного выявления признаков и симптомов нежелательных явлений и незамедлительно назначать соответствующее симптоматическое лечение.
Взаимодействие с другими лекарственными средствами
Живые вакцины
Применение препарата Дупиксент® с живыми вакцинами не изучалось.
Во время лечения препаратом Дупиксент® не следует проводить вакцинацию живыми вакцинами.
Неживые (инактивированные) вакцины
Иммунные реакции на вакцинацию изучались в исследовании, в котором пациенты с атопическим дерматитом получали еженедельно препарат Дупиксент® в дозе 300 мг в течение 16 недель. После 12 недель терапии дупилумабом пациентов вакцинировали вакциной Tdap (Т-клеточно-зависимая, Adacel®) и менингококковой полисахаридной вакциной (Т-клеточно-независимая, Menomune®) и оценивали иммунные реакции по истечении 4 недель. У пациентов, получавших как дупилумаб, так и плацебо, реакции с образованием антител к противостолбнячной и менингококковой полисахаридной вакцинам были сходными. В этом исследовании не было обнаружено нежелательных взаимодействий между любой из этих неживых вакцин и дупилумабом.
Взаимодействие с субстратами изоферментов СУР450
В клиническом исследовании, проведенном у пациентов с атопическим дерматитом, оценивались эффекты дупилумаба на фармакокинетику субстратов изоферментов CYP. Данные, полученные в этом исследовании, не указывают на клинически значимое влияние дупилумаба на активность изоферментов CYP1A2, CYP3A, CYP2C19, CYP2D6 или CYP2C9.
Взаимодействие с другими лекарственными средствами для лечения бронхиальной астмы
Влияние дупилумаба на фармакокинетику одновременно назначаемых препаратов не ожидается. Данные, полученные на основании популяционного анализа, не указывают на влияние одновременно назначаемых препаратов на фармакокинетику дупилумаба у пациентов со среднетяжелым или тяжелым течением бронхиальной астмы.
Особые указания
Гиперчувствительность
При возникновении системной реакции гиперчувствительности лечение препаратом Дупиксент® должно быть немедленно прекращено, и начата соответствующая терапия. В клинических исследованиях при применении препарата Дупиксент® при атопическом дерматите сообщалось об одном случае развития реакции, подобной сывороточной болезни, и одном случае развития сывороточной болезни после введения препарата (обе нежелательные реакции расценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном случае развития анафилаксии после введения препарата Дупиксент® (см. раздел «Побочное действие»).
Конъюнктивит
Конъюнктивит чаще встречался у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. Большинство пациентов с конъюнктивитом выздоровели или выздоравливали в течение периода лечения. Среди пациентов с бронхиальной астмой частота конъюнктивита была низкой и сходной в группах, получавших препарат Дупиксент® и плацебо. Пациенты должны сообщать о первом появлении или ухудшении симптомов со стороны глаз своему лечащему врачу.
Эозинофильные состояния
У пациентов с бронхиальной астмой может развиться серьезная системная эозинофилия, иногда в виде клинических признаков эозинофильной пневмонии или васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, которые часто лечатся системными кортикостероидами. Эти события, как правило, но не всегда, могут быть связаны с сокращением приема пероральных кортикостероидов. Врачи должны быть внимательны к васкулитной сыпи, ухудшающимся легочным симптомам, сердечным осложнениям и/или нейропатии, возникающим у их пациентов с эозинофилией. Сообщалось о случаях эозинофильной пневмонии и васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, при применении препарата Дупиксент® у взрослых пациентов, которые участвовали в клиническом исследовании препарата при бронхиальной астме. Связь между применением препарата Дупиксент® и этими состояниями не была установлена.
Симптомы обострения бронхиальной астмы или ухудшающееся состояние
Препарат Дупиксент® не следует назначать для лечения симптомов остро возникшего ухудшения или обострений астмы. Препарат Дупиксент® не применяется для лечения острого бронхоспазма или астматического статуса.
Снижение дозы глюкокортикостероидов
Не следует резко прерывать применение системных, местных или ингаляционных глюкокортикостероидов после начала терапии препаратом Дупиксент®. Сокращение дозы глюкокортикостероидов, при необходимости, должно быть постепенным и должно выполняться под непосредственным наблюдением врача. Уменьшение дозы глюкокортикостероидов может сопровождаться системными симптомами отмены и/или манифестацией состояний, которые ранее не проявлялись из-за системной терапии глюкокортикостероидами.
Гельминтозы (глистные инвазии)
Пациенты с обнаруженным гельминтозом не включались в клинические исследования. Неизвестно, может ли препарат Дупиксент® повлиять на иммунный ответ при гельминтозах. Необходимо провести лечение пациентов с имеющимся гельминтозом перед тем, как начинать лечение препаратом Дупиксент®. Если во время лечения препаратом Дупиксент® пациент заражается гельминтозом, а антигельминтные препараты оказываются неэффективными, следует прекратить лечение препаратом Дупиксент® до излечения паразитарного заболевания.
Сопутствующие атопические заболевания
Пациентам с атопическим дерматитом и с сопутствующей бронхиальной астмой следует рекомендовать не изменять своего лечения, не проконсультировавшись с лечащим врачом. Прекращая лечение препаратом Дупиксент®, следует принимать во внимание возможные эффекты на течение других атопических заболеваний.
Влияние на способность управлять транспортными средствами и механизмами
Препарат Дупиксент® не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с другими механизмами.
Форма выпуска
Раствор для подкожного введения, 150 мг/мл, 175 мг/мл.
Для дозировки 150 мг/мл:
По 2,00 мл в одноразовый шприц/шприц с системой защиты из прозрачного стекла (тип I), снабженный несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и).
По 1 или 2 шприца/шприца с системой защиты с инструкцией по применению в картонную пачку с заклеенными клапанами.
Или
По 2 шприца/шприца с системой защиты в промежуточную картонную упаковку, по 3 промежуточных картонных упаковки с инструкцией по применению в картонную пачку с заклеенными клапанами.
На каждую картонную пачку нанесен анти контрафактный стикер.
Для дозировки 175 мг/мл:
По 1,14 мл в одноразовый шприц с системой защиты из прозрачного стекла (тип I), снабженный несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и).
По 1 или 2 шприца с системой защиты с инструкцией по применению в картонную пачку с заклеенными клапанами.
Или
По 2 шприца с системой защиты в промежуточную картонную упаковку, по 3 промежуточных картонных упаковки с инструкцией по применению в картонную пачку с заклеенными клапанами.
На каждую картонную пачку нанесен анти контрафактный стикер.
Условия хранения
Хранить при температуре от 2 до 8 °С в оригинальной упаковке для защиты от света. Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
Для дозировки 150 мг/мл – 24 мес.
Для дозировки 175 мг/мл – 18 мес.
Не использовать после окончания срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Юридическое лицо, на имя которого выдано регистрационное удостоверение
АО Санофи-авентис груп, Франция.
Производитель
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Фасовщик (первичная упаковка)
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Упаковщик (вторичная (потребительская) упаковка)
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Выпускающий контроль качества
Санофи-Авентис Дойчланд ГмбХ, Германия (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Sanofi-Aventis Deutschland GmbH, Germany.
Industriepark Hoechst – Brueningstrasse 50
H500, H590, H600 65926 Frankfurt am Main, Germany.
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Sanofi Winthrop Industrie, France.
1051 boulevard Industriel 76580 Le Trait, France.
Претензии потребителей направлять по адресу в России:
АО «Санофи Россия».
125009, г. Москва, ул. Тверская, 22.
В случае использования одноразового шприца с системой защиты, содержащего 300 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
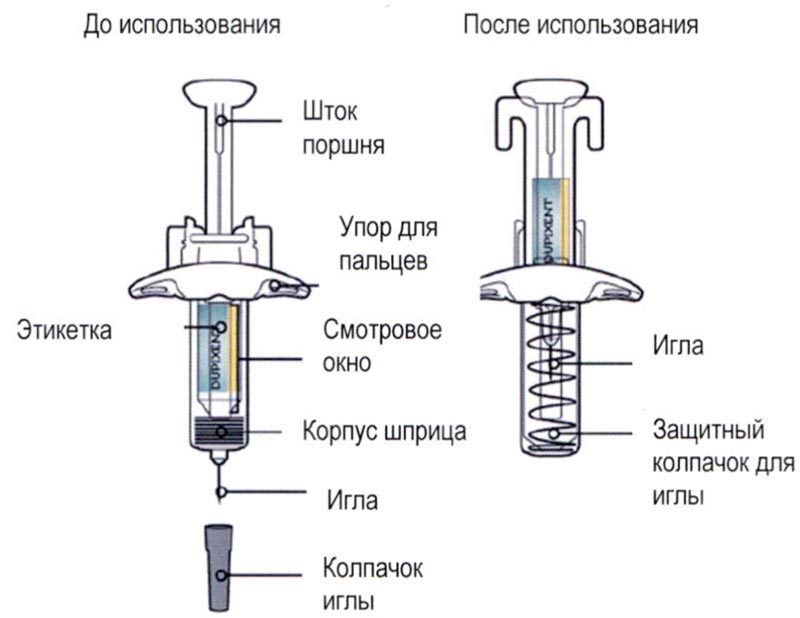
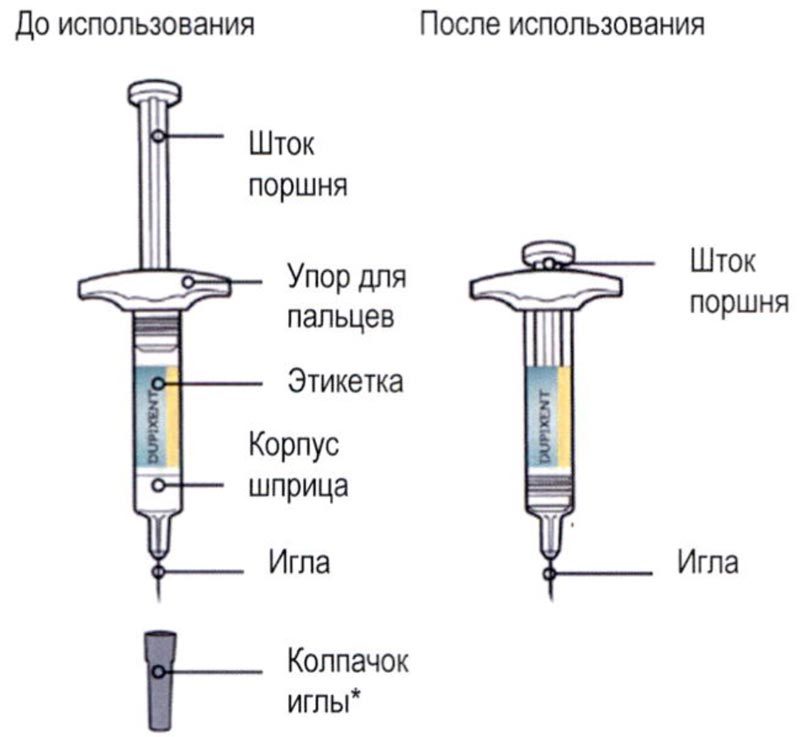
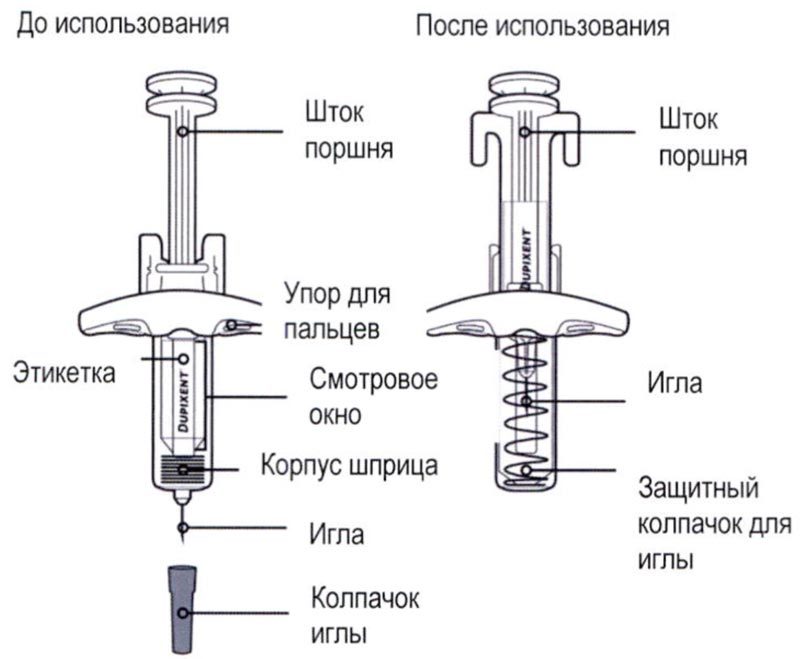
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как Вы провели инъекцию.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
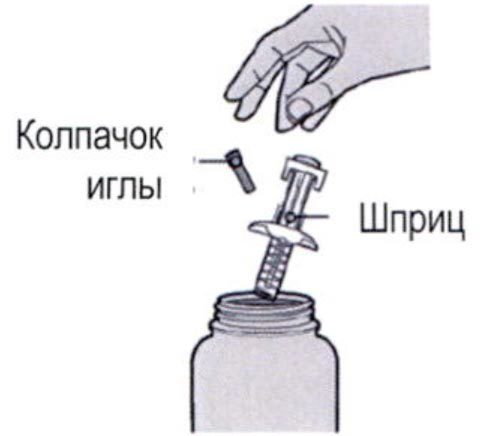
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твёрдую поверхность или повреждён.
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
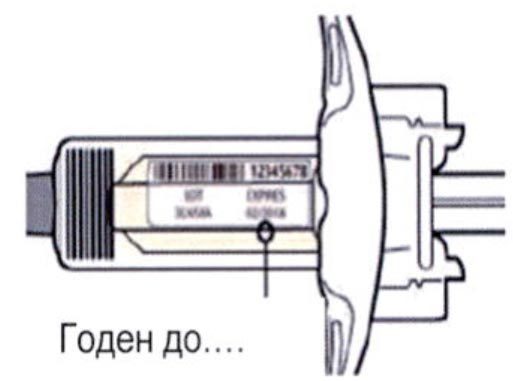
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
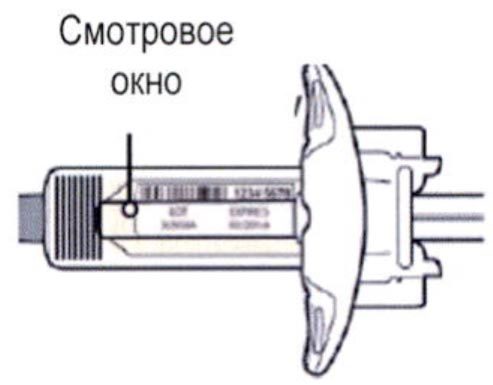
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
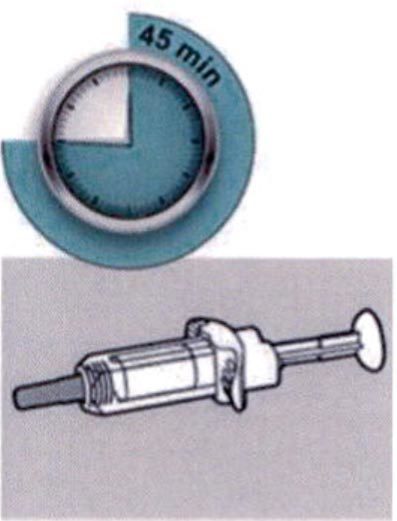
Шаг 4: Подождите 45 мин
Положите шприц на плоскую поверхность, не менее чем на 45 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
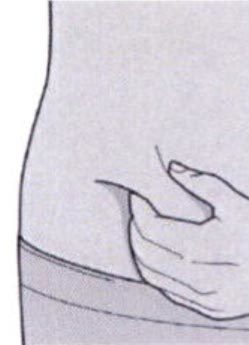
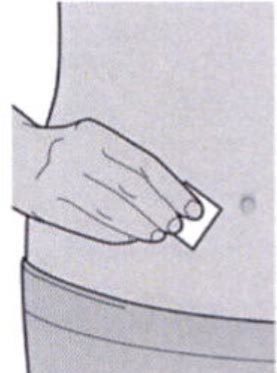
Шаг 5: Выбор места инъекции
Выберите место инъекции.
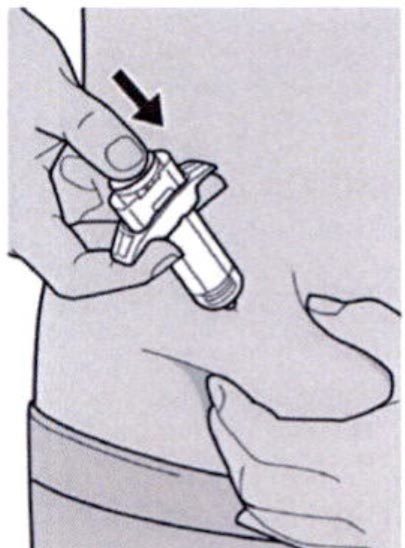
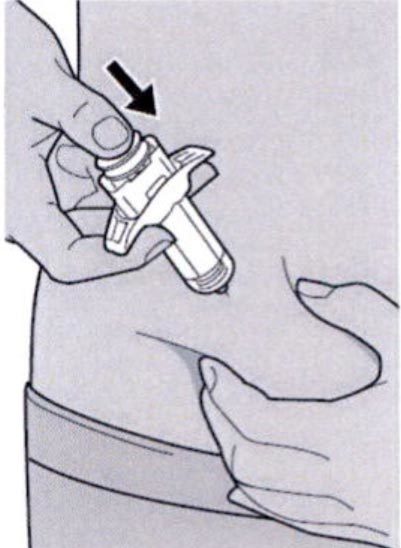
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Шаг 6: Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
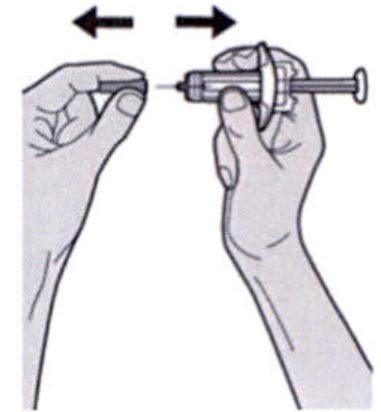
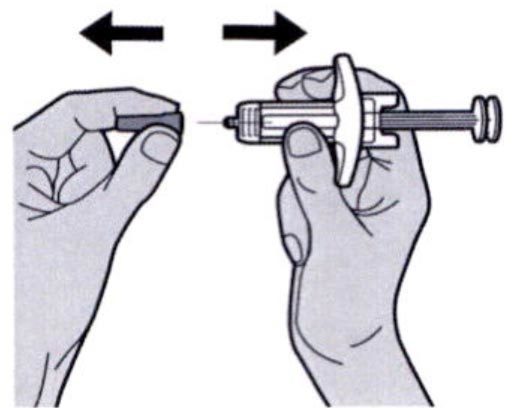
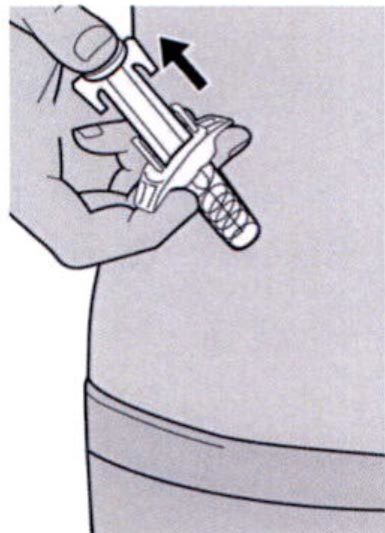
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
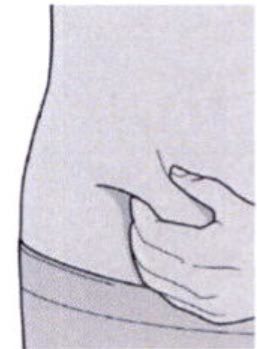
Шаг 8: Формирование складки кожи
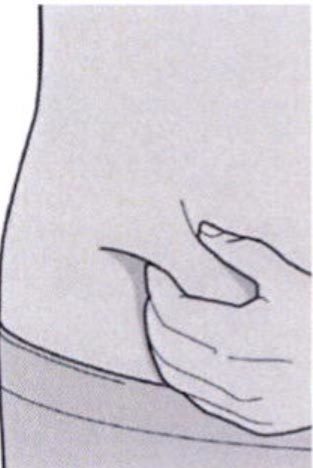
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
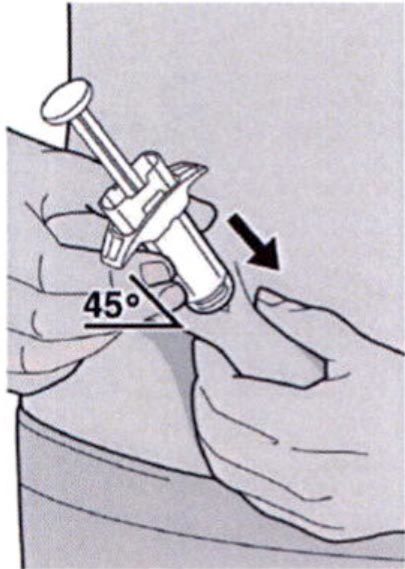
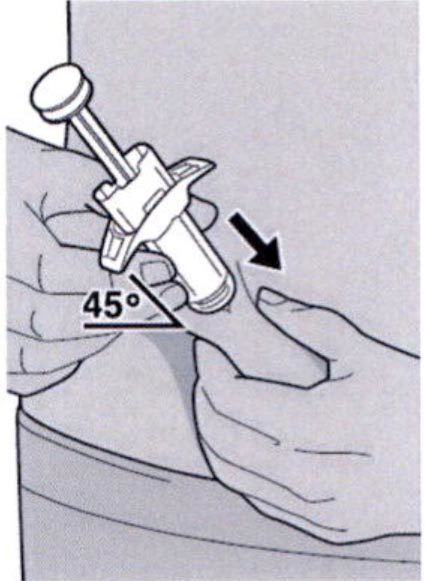
Шаг 9: Введение иглы
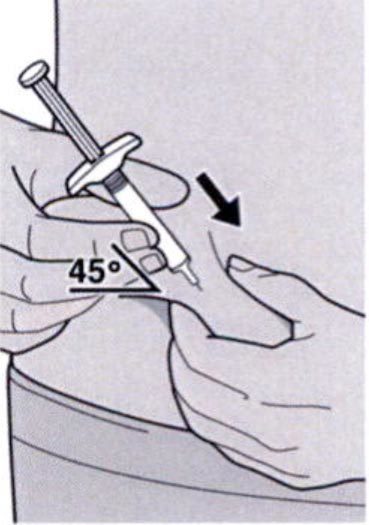
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10: Введение раствора
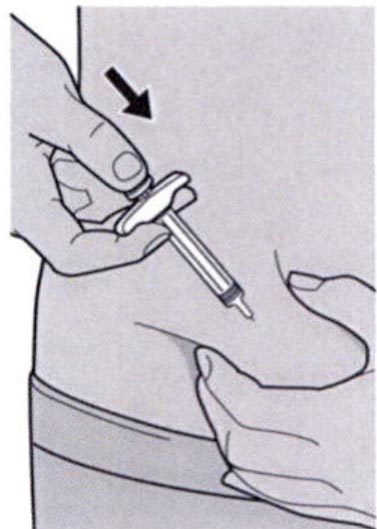
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11: Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
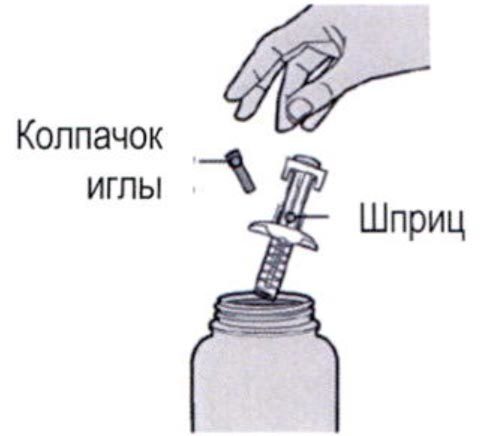
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
В случае использования одноразового шприца, содержащего 300 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце внимательно прочитайте эту инструкцию. Элементы предварительно заполненного шприца показаны на рисунке ниже:
* Шприц может иметь твердый или мягкий колпачок иглы.
Данное устройство представляет собой предварительно заполненный одноразовый шприц (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока Вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как проводить инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он был повреждён.
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
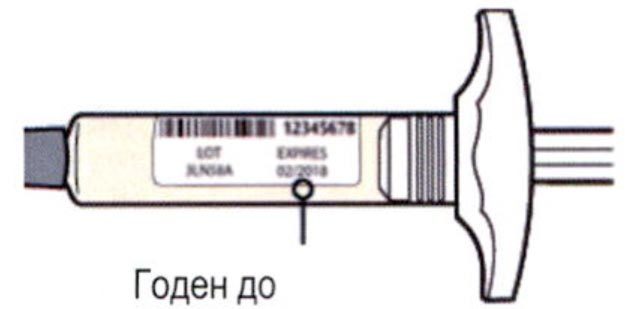
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотрите раствор в шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок. Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4: Подождите 45 мин
Положите шприц на плоскую поверхность, не менее чем на 45 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей. Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5: Выбор места инъекции
Выберите место инъекции.
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Этап 6: Обработка участка инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
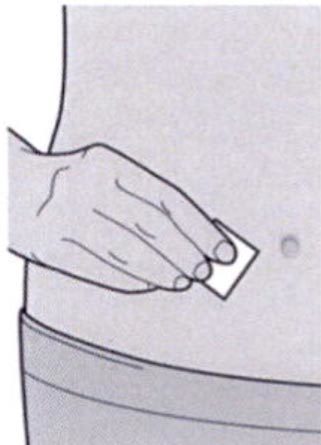
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок иглы.
Не надевайте колпачок иглы обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8: Формирование складки кожи
Сформируйте складку кожи на участке инъекции, как показано на рисунке.
Шаг 9: Введение иглы
Полностью введите иглу в сформированную складку под углом приблизительно 45°.
Шаг 10: Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
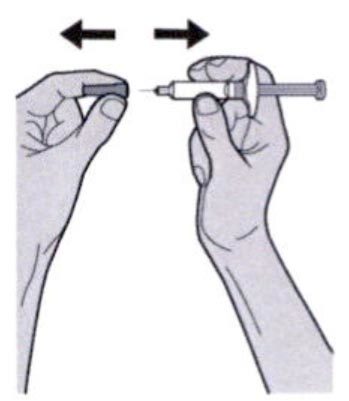
Шаг 11: Извлечение иглы
Извлеките иглу из кожи под тем же углом, под которым она была введена.
Не надевайте колпачок иглы снова на иглу.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не растирайте кожу после инъекции.
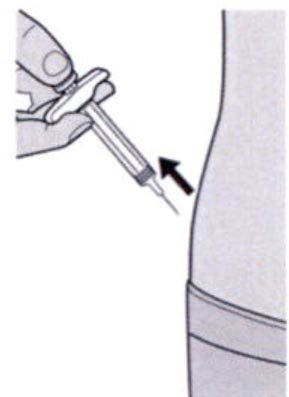
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
В случае использования одноразового шприца с системой защиты, содержащего 200 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 200 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как Вы провели инъекцию.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 30 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твёрдую поверхность или повреждён.
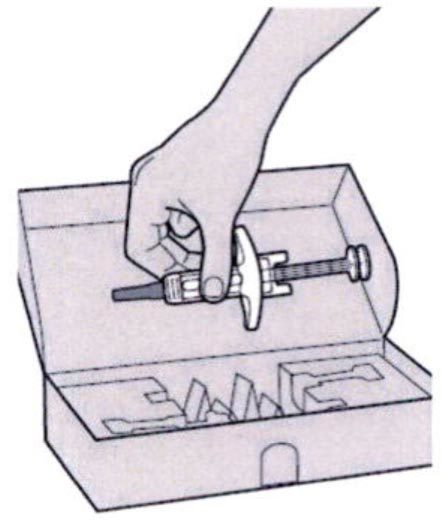
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
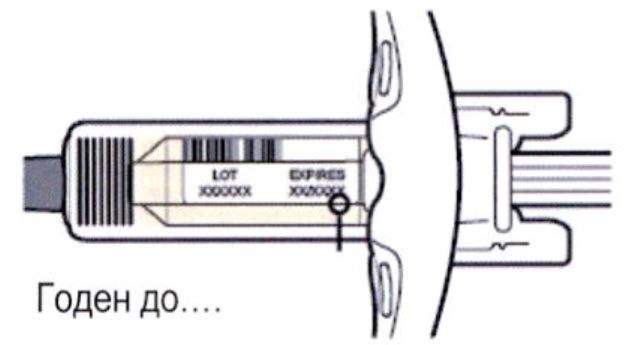
Шаг 3. Проверка
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
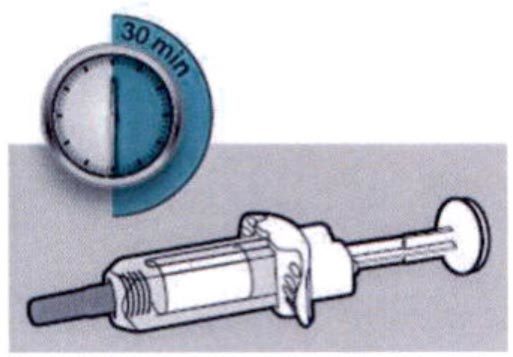
Шаг 4: Подождите 30 мин
Положите шприц на плоскую поверхность, не менее чем на 30 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5: Выбор места инъекции
Выберите место инъекции.
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Шаг 6: Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8: Формирование складки кожи
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
Шаг 9: Введение иглы
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10: Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11: Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Маршани З.Б.
ФГБУ «Поликлиника №1» Управления делами Президента Российской Федерации, Москва, Россия
Ушакова Д.В.
Отделение аллергологии и иммунологии ФГБУ «Поликлиника №1» УДП РФ, Москва, Россия
Ойноткинова О.Ш.
ФГБУ «3-й Центральный военный клинический госпиталь им. А.А. Вишневского» Минобороны России, Московская область, Красногорск, Россия
Дупилумаб в практике врача: клинический случай пациента с тяжелой формой атопического дерматита
Авторы:
Свечникова Е.В., Маршани З.Б., Ушакова Д.В., Ойноткинова О.Ш.
Как цитировать:
Свечникова Е.В., Маршани З.Б., Ушакова Д.В., Ойноткинова О.Ш. Дупилумаб в практике врача: клинический случай пациента с тяжелой формой атопического дерматита. Клиническая дерматология и венерология.
2019;18(6):768‑775.
Svechnikova EV, Marshani ZB, Ushakova DV, Oinotkinova OSh. Dupilumab in the clinical practice: Clinical case of severe atopic dermatitis. Klinicheskaya Dermatologiya i Venerologiya. 2019;18(6):768‑775. (In Russ.)
https://doi.org/10.17116/klinderma201918061768
Термин атопия, впервые введенный A. Coca и R. Cooke в 1923 г., означает предрасположенность к развитию иммуноглобулин E (IgE) опосредованных реакций гиперчувствительности I типа [1]. В последние десятилетия распространенность атопических заболеваний, включая атопический дерматит (АтД), бронхиальную астму (БА), аллергический ринит (АР) и пищевую аллергию (ПА), имеет тенденцию к росту в общемировой популяции. Атопические заболевания нередко связаны между собой на протяжении жизни пациента в рамках такого явления, как атопический марш. Данный термин подразумевает прогрессирование с течением времени от АтД к АР, БА и ПА, а АтД считают «точкой входа» для последующих атопических заболеваний [2].
АтД является распространенным многофакторным заболеванием кожи, характеризующимся истинным полиморфизмом высыпаний и выступающим в качестве первого проявления атопического марша [3, 4]. Международные критерии постановки диагноза АтД были сформулированы в 1980 г. M. Hanifin и N. Rajka [5]. Диагностические критерии отражены в таблице.
Клинические проявления АтД являются результатом синергетического действия генетических и иммунных факторов в сочетании с влиянием окружающей среды (климат, питание, индустриализация и т. д.). АтД характеризуется хроническим воспалением, иммунной дисрегуляцией, дисфункцией кожного барьера и наличием у большинства больных (10—40% пациентов) IgE-опосредованной сенсибилизации к пище и аллергенам окружающей среды [2]. Как фенотип АтД представляется очень гетерогенным с позиции этиологии заболеванием. Выделяют три основных вида дефектов при АтД: дефекты барьерной функции эпидермиса, врожденного иммунитета и иммунной регуляции. По данным литературы, у 80% детей, страдающих АтД, отмечается отягощенный семейный анамнез, при этом наличие атопических заболеваний хотя бы у одного из родителей повышает риск развития АтД у ребенка до 45—50%, что формально соответствует аутосомно-доминантному типу наследования — 50% риск передачи заболевания [6, 7].
В патогенезе АтД важную роль отводят мутациям в гене белка филаггрина (FLG). Так, J. Thyssen и соавт. описали наблюдение пациентов с АтД, у которых отмечалась сниженная экспрессия FLG на участках как непораженной, так и пораженной кожи. Приблизительно у 50% пациентов с АтД средней или тяжелой степени выявлена как минимум одна мутация в гене FLG, а уменьшение количества копий гена FLG увеличивало риск развития АтД. Также у пациентов с АтД были продемонстрированы пониженные уровни белка FLG на участках пораженной кожи, несмотря на отсутствие мутаций в гене FLG [8].
Возможным объяснением отсутствия мутаций в гене FLG у половины больных является наличие нарушений функционирования других генов в рамках модели АтД как олигогенного заболевания или наличие генов-модификаторов [7]. Гены-кандидаты связаны с функционированием иммунной системы, формированием кожного барьера и с нарушениями обмена веществ. Также фенотип АтД (или сходные изменения кожи) встречается на фоне моногенных наследственных заболеваний обмена веществ (чаще у детей раннего возраста) [2, 7].
Филаггрин является ключевым белком, участвующим в дифференцировке клеток эпидермиса и осуществлении его барьерной функции; образуется в ходе окончательной дифференцировки зернистых клеток эпидермиса, когда профилаггрин кератогиалиновых гранул протеолитически расщепляется на молекулы филаггрина, которые быстро агрегируют с кератиновым цитоскелетом, что приводит к коллапсу зернистых клеток в плоские безъядерные чешуйки. Образовавшийся роговой слой является барьером, предотвращающим не только потерю воды, но и проникновение аллергенов и инфекционных агентов [4]. В большинстве исследований показано, что отсутствие структурных и функциональных эпидермальных молекул не только нарушает структуру эпидермального барьера, но и является медиатором иммунных и аллергических процессов. Существует обратная связь между дисфункцией кожного барьера и иммунным ответом в патогенезе АтД [2]. Таким образом, нарушенная барьерная функция кожи, с одной стороны, позволяет проникать различным аллергенам/гаптенам, поллютантам окружающей среды и токсинам, возникающим в результате бактериальной колонизации, а с другой — способствует сенсибилизации к аллергенам [9]. Аллергены стимулируют дендритные клетки кожи, которые в свою очередь активируют Th2-лимфоциты, что приводит к продукции ими провоспалительных цитокинов (IL-4, IL-5 и IL-13). IL-4 и IL-13 индуцируют переключение класса синтеза иммуноглобулинов на IgE, подавляют экспрессию структурных белков кожи, таких как филаггрин, лорикрин, инволюкрин и десмоглеин, и вызывают изменения липидного барьера [10]. Кроме того, IL-13 опосредует ремоделирование кожи, способствуя повышенному отложению коллагена и фиброзу ткани. IL-5 является фактором выживания эозинофилов и определяет их развитие и миграцию. В недавних общегеномных исследованиях АтД определены цитокины, ассоциированные с Th2-клетками, такие как KIF3A, IL-4 и IL-13, как основные молекулы, вовлеченные в воспалительный каскад. АтД характеризуется значительной активацией ассоциированных с Th2-лимфоцитами сигнальных и эффекторных путей в пораженной коже, кроме того, в ряде исследований была продемонстрирована роль Th1-, Th17— и Th22-клеток в инициации и поддержании АтД [11, 12]. На ранних стадиях АтД доминируют сигналы Th2 и Th22, в то время как хронизации заболевания способствует параллельная с ними активация Th1-каскада [13]. Системный характер воспаления при АтД отражает патологические изменения и повышенную экспрессию цитокинов не только в пораженной, но и в непораженной коже пациентов.
В последние годы отмечается значительный рост частоты аллергических заболеваний, ведущее место среди которых занимает АтД [7]. Являясь одним из наиболее распространенных кожных заболеваний, АтД встречается во всех странах, у лиц обоего пола и в разных возрастных группах [14]. В настоящее время во всем мире данным заболеванием страдают до 20—30% детского и до 3% взрослого населения [2]. Согласно данным Федерального статистического наблюдения, в 2016 г. в Российской Федерации заболеваемость АтД составила 203 случая на 100 тыс. населения, а распространенность — 439 случаев на 100 тыс. всего населения [14].
АтД оказывает существенное негативное влияние на качество жизни пациентов и их семей, вызывает физические (зуд, нарушение сна), эмоциональные (поведенческие девиации, раздражительность) и социальные (социальная изоляция) проблемы. В сравнительном исследовании качества жизни у детей с хроническими заболеваниями АтД был идентифицирован как состояние со вторым по величине влиянием на качество жизни пациента и его семьи (после церебрального паралича). Для пациентов старших возрастных групп с АтД характерно преобладание физических и эмоциональных нарушений с меньшим воздействием на социальную сферу [15].
Помимо заболеваний, ассоциированных с атопией, таких как бронхиальная астма и аллергический ринит, пациенты с АтД имеют повышенный риск развития кожных инфекций, заболеваний сердечно-сосудистой системы и онкологических заболеваний. Кроме того, среди сопутствующих заболеваний у пациентов с АтД часто встречаются психические расстройства, такие как синдром дефицита внимания, депрессия, тревога, суицидальные мысли и аутизм [15].
В Российском национальном согласительном документе по наружной терапии атопического дерматита, а также в работах Г.И. Смирновой и P. Arkwright выделяются три основные степени тяжести атопического дерматита: легкое течение заболевания, среднетяжелое и тяжелое [16—18]. При среднетяжелом течении отмечается распространенный характер поражений кожи с обострениями до 3—4 раз в год и тенденцией к упорному течению с отсутствием выраженного эффекта от проводимой терапии. При этом несмотря на применение всего арсенала современных методов лечения, в заметной части случаев не удается добиться продолжительной и стойкой ремиссии АтД, т. е. приходится констатировать торпидное течение заболевания. В федеральных клинических рекомендациях по ведению больных АтД предлагается ступенчатый подход для выбора адекватной терапии, который включает три аспекта, где каждая последующая ступень лечения является дополнением предыдущей, а в случае присоединения инфекции к лечению необходимо добавить антибактериальные препараты. При неэффективности терапии необходимо исключить нарушение комплаентности и уточнить диагноз. Так, при тяжелом АтД (индекс Scoring Atopic Dermatitis [SCORAD] превышает 40 баллов, регистрируют упорное течение АтД, т. е. непрерывное обострение) в качестве дополнительного лечения, соответствующего данной степени тяжести АтД, рекомендуется системная иммуносупрессивная терапия системными глюкокортикостероидами (ГКС) короткими курсами и циклоспорином А. Применение данной терапии весьма ограниченно ввиду выраженных побочных эффектов и возможности развития обострения процесса после отмены препаратов (системные ГКС), значительной токсичности (циклоспорин А) и сложности при ведении пациентов (особенно детского возраста) [19]. Затруднения, возникающие при лечении больных с тяжелым АтД, в совокупности с существенным негативным влиянием заболевания на качество жизни пациентов требуют поиска новых методов лечения. Результаты современных исследований показывают, что биологическая терапия оказалась революционной не только в онкологии, она может успешно применяться для лечения таких иммуноопосредованных заболеваний, как бронхиальная астма и псориаз. Первое свидетельство обнадеживающего прорыва в терапии АтД появилось в 2014 г., когда FDA (Food and Drug Administration — Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) присвоило препарату дупилумаб статус «терапии прорыва» [20].
Дупилумаб получил разрешение на маркетинг от FDA и EMA (European Medicines Agency, Европейское агентство лекарственных средств) в 2017 г., и в настоящее время данный препарат доступен в Евросоюзе и США в качестве первого иммунотерапевтического средства для лечения пациентов с АтД [21]. В Российской Федерации дупилумаб был зарегистрирован в апреле 2019 г. для лечения АтД средней и тяжелой степени у взрослых пациентов [22]. Дупилумаб является рекомбинантным, полностью человеческим моноклональным антителом, направленным против альфа-субъединицы рецептора интерлейкина-4 (IL-4Rα) — общей субъединицы рецепторов IL-4 и IL-13. В клинических исследованиях III фазы с участием 1379 взрослых пациентов с АтД средней и тяжелой степени, недостаточно реагирующих на применение местного лечения, монотерапия дупилумабом сопровождалась улучшением признаков и симптомов заболевания, включая зуд, беспокойство, депрессию и качество жизни больных [23]. В группах терапии дупилумабом, по сравнению с плацебо, значительно реже наблюдалось развитие кожных инфекций. Согласно результатам данных клинических исследований, обе изученные схемы дозирования (300 мг подкожно каждую неделю или 300 мг подкожно каждые 2 нед в течение 16 нед) продемонстрировали схожую эффективность и безопасность. Наиболее частыми побочными эффектами были реакции в месте инъекции и конъюнктивиты [24].
Клинический случай
В настоящей статье приведен опыт успешного применение препарата дупилумаб у пациентки с тяжелым течением АтД.
Пациентка З., 37 лет, больна АтД с детского возраста, выраженные проявления — до 14 лет. Ранее при обследовании у пациентки выявлялась бытовая, грибковая, эпидермальная и пыльцевая аллергия. После переезда в США (штат Калифорния) 2 года назад произошел дебют АК, по поводу которого пациентка обращалась к офтальмологу и получала лечение с незначительным положительным эффектом. При возвращении в Москву конъюнктивит регрессировал. На фоне первой беременности у пациентки отмечалось обострение АК, появление высыпаний на коже туловища и конечностей, кроме того, во время пребывания в США был диагностирован холестаз беременных. По этому поводу пациентка получала лечение антигистаминными препаратами, а также топическими ГКС (ТГКС) наружно — с временным положительным эффектом.
АтД носил хронический, рецидивирующий характер с обострениями 2 раза в год, однако на протяжении последних 2 лет течение заболевания приобрело непрерывно рецидивирующий характер, устойчивый к терапии. Ранее пациентка получала лечение в виде системных ГКС короткими курсами, стандартной наружной противовоспалительной терапии, антигистаминной и десенсибилизирующей терапии, что сопровождалось кратковременным положительным эффектом, однако после прекращения терапии высыпания возобновились. Также у аллерголога поликлиники пациентка получала курс иммуноглобулина противоаллергического 2,0 внутримышечно № 5 — без выраженного эффекта. Кроме того, периодически наблюдалось вторичное инфицирование кожных высыпаний, ввиду которого пациентка получала внутрь и наружно антибактериальные препараты, с кратковременным положительным эффектом.
Учитывая тяжелое рецидивирующее течение АтД, врач-аллерголог в США назначил терапию генно-инженерным биологическим препаратом дупилумаб.
На момент осмотра на приеме у дерматолога в Поликлинике № 1 до начала биологической терапии кожный процесс носил распространенный, подостровоспалительный характер, был локализован на коже лица, туловища, конечностей и представлен множественными эритематозно-сквамозными высыпаниями застойно-розового цвета, множественными экскориациями, покрытыми геморрагическими корками (рис. 1).
При обследовании у врача-аллерголога был поставлен диагноз: «Аллергический ринит, персистирующего течения. Аллергический конъюнктивит, вне обострения. Бытовая, эпидермальная, пыльцевая, грибковая аллергии».
По результатам лабораторных исследований были определены следующие показатели: в клиническом анализе крови — эозинофилы 22%, IgE общий — 383,4 МЕ/мл.
Пациентке был назначен дупилумаб согласно инструкции по применению (в начальной дозе 600 мг, т. е. 2 инъекции по 300 мг, подкожно однократно и далее в дозе 300 мг каждые 2 нед).
После четырех инъекций дупилумаба в сочетании со стандартной наружной терапией отмечался регресс высыпаний и зуда на 50—70% по сравнению с исходным состоянием, однако появились свежие высыпания на коже голеней, возникновение которых пациентка связывала с предшествующей эпиляцией. Серьезные побочные эффекты на фоне лечения не выявлены. Через неделю после третьей инъекции дупилумаба пациентка отметила зуд и покраснение век, была консультирована в экстренном порядке офтальмологом и аллергологом, был поставлен диагноз «аллергический блефароконъюнктивит», в связи с чем на приеме экстренно введен дексаметазон в дозе 8 мг внутримышечно, назначены антигистаминные пероральные препараты, получен клинический эффект. Тогда же пациентка явилась на прием к дерматологу с жалобами на сохраняющиеся зудящие высыпания, на заложенность носа, чередующуюся с ринореей, зуд век, слезотечение, появление которых она связывала с аллергией на полынь. На фоне дерматологического лечения отмечался регресс папуло-пустул на коже голеней.
Объективно на момент осмотра после четырех инъекций дупилумаба: патологический кожный процесс носил хронический воспалительный характер, был локализован в области кожи лица, разгибательной и сгибательной поверхностей плеч, предплечий, на кистях, нижних конечностях, спине, животе, представлен эритематозно-сквамозными элементами в стадии регресса, при этом вторичная пиодермия отсутствовала, оценка SCORAD составила 34 балла (рис. 2).
Таким образом, представленный клинический случай демонстрирует высокую эффективность дупилумаба в терапии тяжелого АтД. За 1-й месяц терапии был достигнут быстрый результат в отношении снижения индекса SCORAD — с 68 до 34 баллов, который сохранялся в дальнейшем на протяжении наблюдения пациентки в России. Во время терапии дупилумабом развился блефароконъюнктивит, однако несмотря на подтверждение смежными специалистами его аллергического генеза, нельзя с уверенностью сказать, стал ли он следствием цветения полыни или нежелательным явлением от проводимой терапии. В целом пациентка с сопутствующими атопическими заболеваниями, не отвечающая эффективно на стандартные методы лечения АтД, хорошо перенесла лечение дупилумабом, что подтверждает безопасность и высокую эффективность данного средства.
Сведения об авторах
Свечникова Е.В. — https://orcid.org/0000-0002-5885-4872
Маршани З.Б. — https://orcid.org/0000-0002-7971-5097
Ушакова Д.В. — https://orcid.org/0000-0003-4401-612X
Ойноткинова О.Ш. — https://orcid.org/0000-0002-9856-8643
КАК ЦИТИРОВАТЬ:
Свечникова Е.В., Маршани З.Б., Ушакова Д.В., Ойноткинова О.Ш. Дупилумаб в практике врача: клинический случай пациента с тяжелой формой атопического дерматита. Клиническая дерматология и венерология. 2019;18(6):768-775. https://doi.org/10.17116/klinderma201918061768
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.
DOI: 10.24412/2409-6636-2022-12937
Дупилумаб: аспекты применения при тяжелой бронхиальной астме в реальной клинической практике
Э.В. Чурюкина
Бронхиальная астма (БА) — хроническое воспалительное гетерогенное заболевание, характеризующееся различными фенотипами и эндотипами. В зависимости от типа иммунного ответа выделяют не-Т2-воспаление и Т2-воспаление, лежащее в основе Т2-ассоциированных заболеваний, в том числе Т2-БА. К числу ключевых ци-токинов Т2-воспаления относятся интерлейкин-4 и интерлейкин-13, блокирование сигнальных путей которых является механизмом действия полностью человеческого моноклонального антитела — дупилумаба. Эффективность этого биологического препарата в лечении тяжелой эозинофильной БА (Т2-БА) продемонстрирована на клиническом примере из реальной практики.
Ключевые слова: бронхиальная астма, генно-инженерная биологическая терапия, дупилумаб, назальные полипы.
Бронхиальная астма (БА) — хроническое воспалительное заболевание дыхательных путей с известной клинической картиной (свистящие хрипы, одышка, стеснение в груди, кашель). Воспаление респираторного тракта приводит к патофизиологическим последствиям: гиперреактивности, ремоделированию дыхательных путей, бронхообструкции, обострениям заболевания [1, 2].
Концепция воспаления при БА со временем претерпела значительные изменения, которые обусловлены пониманием и признанием того, что это заболевание гетерогенное. Понятие гетерогенности БА легло в основу современного учения о фенотипировании БА и закреплено экспертами руководства Глобальная инициатива по бронхиальной астме (Global Initiative for Asthma, GINA) в 2014 г. в определении заболевания [3]. И это чрезвычайно важно, поскольку означает признание наличия разных клинико-патогене-тических вариантов БА, а следовательно, и необходимости разных подходов к терапии. Это име-
Элла Витальевна Чурюкина — канд. мед. наук, доцент, нач. отдела аллергических и аутоиммунных заболеваний в педиатрии Научно-исследовательского института акушерства и педиатрии ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России; доцент кафедры клинической иммунологии, аллергологии и лабораторной диагностики ФПК и ППС ФГБОУ ВО «Кубанский государственный медицинский университет» Минздрава России, Краснодар. Контактная информация: echuryukina@mail.ru
ет особую значимость для пациентов с тяжелой БА (ТБА), которые часто остаются рефрактерными к проводимой базисной терапии и у которых отмечается высокая частота обострений, незапланированных визитов к врачу, обращений за неотложной помощью, госпитализаций [3, 4].
Как известно, в 2021 г. определение ТБА было изменено, теперь оно не соотносится со ступенями GINA, так как они могут изменяться со временем, и на сегодняшний день считается, что ТБА (severe asthma) — это БА, которая остается неконтролируемой, несмотря на оптимизированное лечение высокими дозами ингаляционных глюкокортикостероидов (ИГКС)/длительнодей-ствующих Р2-агонистов (ДДБА), или требует использования высоких доз ИГКС/ДДБА для сохранения контроля [1].
Тяжелая БА также является гетерогенной и различается по клиническим (фенотипическим) признакам и патобиологическим (воспалительным или молекулярным — эндотипическим) характеристикам [1, 3]. Известно множество клинических фенотипов и как минимум 2 эндотипа, или типа, воспаления — Т2 и не-Т2 [3]. Т2-иммунный ответ формируется определенными эффекторны-ми клетками: дендритными, Т-хелперами 2-го типа (Th2), врожденными лимфоидными клетками 2-го типа (ILC2), секретируемыми ими цитокинами — интерлейкином-4 (ИЛ-4), ИЛ-5, ИЛ-9, ИЛ-13 и иммуноглобулином E (IgE), — приводя к эозинофильному воспалению, ремоделиро-
ванию эпителия и подслизистого слоя бронхов [3, 4]. Не-Т2-иммунный ответ формируется преимущественно ТМ, ТМ7, возможно ^С1 и ^С3, ци-токинами ИЛ-17, ИЛ-10 и фактором некроза опухоли а, приводя к нейтрофильному или малогра-нулоцитарному воспалению в бронхах [3].
Т2-воспаление и связанная с ним БА (Т2-БА) ассоциируются с аллергическим фенотипом и/или эозинофильным неаллергическим фенотипом [3]. По результатам исследований, Т2-БА отмечается у значительной доли пациентов (50-70%) [2, 3]. А это означает, что у большинства больных БА имеется эозинофильное воспаление в слизистой нижних дыхательных путей с высоким уровнем экспрессии Т2-цитокинов (ИЛ-4, ИЛ-5, ИЛ-13) [5]. Бронхиальная астма, обусловленная воспалением 2-го типа, включает ряд фенотипов: аллергический, неаллергический, аспириновая БА, БА физического усилия [1]. Возможен перекрест этих фенотипов [1].
Общепринятыми маркерами Т2-эндотипа являются эозинофилия мокроты, эозинофилия крови, повышенная фракция оксида азота в выдыхаемом воздухе (FeNO), периостин [6]. С точки зрения патофизиологии БА, а также из-за сложности определения большинства биомаркеров Т2-БА в повседневной клинической практике ни один из них, взятый по отдельности, не может в полной мере характеризовать воспаление 2-го типа у пациентов с неконтролируемой пер-систирующей БА [6].
Т2-бронхиальная астма часто сопровождается рядом сопутствующих заболеваний, вызванных воспалением 2-го типа, что приводит к различным клиническим проявлениям, зависящим от пораженных тканей [7- 9].
Одним из основных биомаркеров восходящего пути воспаления 2-го типа (активация №2-кле-ток) является ^Е, который при перекрестном связывании молекул, закрепленных на базофи-лах и тучных клетках, опосредует высвобождение медиаторов воспаления (гистамин, проста-гландины, ИЛ-4, ИЛ-13, ИЛ-5), тем самым дополнительно усиливая иммунный ответ 2-го типа [7].
Таким образом, наряду с БА, атопическим дерматитом, пищевой аллергией, аллергическим ринитом и конъюнктивитом существует широкий спектр других состояний с клиническими признаками воспаления 2-го типа, таких как хроническая идиопатическая крапивница, хронический полипозный риносинусит (ХПРС) и эозинофильный эзофагит [7-9]. То есть Т2-вос-паление может лежать в основе широкого спектра заболеваний как аллергического, так и неаллергического генеза, формируя понятие «Т2-ас-социированные заболевания» [7-9].
Воспалительный путь 2-го типа реализуется при участии механизмов как врожденного (неспецифического), так и приобретенного (специфического, возникшего в ответ на действие определенных аллергенов или патогенов) иммунитета, опосредованного цитокинами 2-го типа [7]. Воздействие ирритантов или аллергенов на эпителиальный барьер активирует врожденный иммунный ответ посредством высвобождения цитокинов эпителиального происхождения -ИЛ-25, ИЛ-33 и тимусного стромального лимфо-поэтина (TSLP) [7]. Эти цитокины эпителиального происхождения стимулируют ^С2, в результате чего происходит дифференциация и продукция важных цитокинов 2-го типа — ИЛ-13 и ИЛ-5 [7]. Дендритные клетки являются критически важными элементами врожденного иммунитета в области эпителиального барьера, включая легкие, поскольку их отростки, проникая через плотные контакты эпителия в просвет дыхательных путей, вступают в контакт с антигенами [9]. Дендритные клетки выступают связующим звеном между механизмами врожденного и приобретенного иммунитета. В рамках адаптивного иммунного ответа ИЛ-4 обеспечивает дифференциацию №0-лимфоцитов в ^2-лимфоциты [7, 10].
Цитокины ИЛ-4, ИЛ-13 и ИЛ-5, участвующие в воспалении 2-го типа, вырабатываются клетками врожденного (^С2) и приобретенного (№2) иммунитета [7, 11]. Цитокины 2-го типа ИЛ-4 и ИЛ-13 играют ключевую роль в развитии воспаления 2-го типа, облегчая многие процессы, в том числе дифференциацию №0- и ^2-лим-фоцитов (ИЛ-4), переключение класса изотипа В-лимфоцитов на синтез ^Е, активацию макрофагов и накопление эозинофилов в местах повреждения ткани [4, 7, 10, 12]. Интерлейкин-13 также участвует в таких тканевых реакциях, как секреция слизи, сократимость и гиперплазия гладкомышечных клеток; ИЛ-4, ИЛ-13 и ИЛ-5 участвуют в активации и накоплении эози-нофилов [7, 11, 12].
Понимание патогенеза Т2-воспаления является основой для выбора мишени при назначении таргетной терапии БА. На сегодняшний день в Российской Федерации зарегистрировано 5 генно-инженерных биологических препаратов (ГИБП), 6-я молекула (анти-TSLP), включенная в GINA 2022 г., проходит регистрацию. Точками приложения генно-инженерной биологической терапии (ГИБТ) являются: ИЛ-4, ИЛ-13 — для моноклонального антитела (МАТ) дупилумаба; ИЛ-5/^5И (рецептор к ИЛ-5) — для МАТ мепо-лизумаба, реслизумаба, бенрализумаба; ^Е -для омализумаба [1-3].
Как уже отмечалось выше, ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2-го типа [4, 7]. Они вырабатываются ^С2 и ТИ2-лимфоцитами, ИЛ-4 также вырабатывается дендритными клетками [7-9]. Интерлейкин-4 и ИЛ-13 высокогомологичны друг другу, их называют «родственными цитокинами», так как они экспрессируются многими одинаковыми типами иммунных и эффекторных клеток и используют одни и те же сигнальные пути; их функции в значительной мере пересекаются за счет общих механизмов передачи сигналов через гетеродимер-ные мембранные рецепторы, содержащие общую субъединицу — ^4Иа (а-субъединица рецептора к ИЛ-4) [7]. Рецептор к ИЛ-4 состоит из а- и у-субъединиц, которые вместе формируют гете-родимер 1-го типа, участвующий в сигнальном пути ИЛ-4 [7]. Еще один рецептор состоит из а-субъединицы ИЛ-4 и а1-субъединицы ИЛ-13, которые вместе формируют гетеродимер 2-го типа [7]. Таким образом, а-субъединица ИЛ-4 является общей для ИЛ-4 и ИЛ-13 [7]. Интерлей-кин-4 способен связываться с рецептором 1-го или 2-го типа, в то время как ИЛ-13 может связываться лишь с рецептором 2-го типа [7]. Указанные рецепторы широко представлены на клетках иммунной системы (В-лимфоциты, Т-лимфоциты, моноциты, эозинофилы) и на других типах клеток (эпителиальных, гладкомы-шечных, фибробластах), что и объясняет многообразие эффектов ИЛ-4 и ИЛ-13 [13, 14]. Так, в частности, рецептор 1-го типа экспрессируется на В-лимфоцитах, Т-лимфоцитах, моноцитах, эозинофилах, фибробластах, в то время как рецептор 2-го типа — на эпителиальных клетках, гладкомышечных клетках, фибробластах, моноцитах, активированных В-лимфоцитах [13, 14].
Блокирование ^4Иа приводит к подавлению функции обоих цитокинов — ИЛ-4 и ИЛ-13 [15]. Дупилумаб представляет собой рекомбинантное полностью (100%) человеческое МАТ класса IgG4, которое связывается с ^4Иа и таким образом подавляет связывание обоих цитокинов, ИЛ-4 и ИЛ-13, с рецепторами 1-го и/или 2-го типа [16]. Создание полностью человеческого МАТ представляется самой совершенной на сегодняшний день стратегией, направленной на снижение иммуногенности. Так, антитела к дупилумабу были обнаружены у 4,2% пациентов в группе с дозой препарата 200 мг 1 раз в 2 нед и у 2,1% пациентов в группе с дозой 300 мг 1 раз в 2 нед, но они не оказывали значимого влияния на эффективность или безопасность терапии [16]. Данная стратегия означает уменьшение риска нежелательных явлений при высокой терапевтической эффективности МАТ, подавлении активности
эозинофильного воспаления в дыхательных путях либо других тканях-мишенях [7, 13, 14]. При этом важно, что уменьшение выраженности эозинофильного воспаления происходит независимо от нормального или повышенного уровня эозинофилов в периферической крови [14].
Надо отметить, что все остальные ГИБП, зарегистрированные в настоящее время в РФ для биологической терапии БА, относятся к гуманизированным МАТ, о чем свидетельствует суффикс «-зумаб» в их международном непатентованном названии (омализумаб, реслизумаб, ме-полизумаб, бенрализумаб) [1, 2]. Поэтому они могут обладать более высоким уровнем иммуно-генности [16].
Дупилумаб включен в российские клинические рекомендации по БА 2021 г. [2]. Препарат имеет высокий уровень доказательности, обладает масштабной доказательной базой [2].
Показания к назначению дупилумаба следующие: БА среднетяжелого и тяжелого течения с 12 лет; атопический дерматит среднетяжелого и тяжелого течения с 6 лет; ХПРС у взрослых с 18 лет [17]. Дупилумаб (Дупиксент) вводится подкожно. Препарат содержится в предварительно заполненном одноразовом шприце; не требуется коррекции режима дозирования в зависимости от массы тела пациента (при БА и ХПРС); в случае необходимости Дупиксент можно хранить при комнатной температуре (до 25°С) в течение 14 дней; инъекцию может делать либо сам пациент (в область бедра или живота), либо лицо, ухаживающее за ним (в верхнюю часть плеча) [17].
В основном документе Всемирной организации здравоохранения, регламентирующем все положения по БА, — докладе GINA, в последней редакции 2022 г. представлена отдельная глава, в которой обновлены положения по дополнительной поддерживающей терапии биологическими препаратами. В частности, приведен алгоритм выбора биологического препарата [1]:
1) произвести оценку фенотипа ТБА, определить тип воспаления (с учетом доступных маркеров, характера ответа на глюкокортикостероиды (ГКС), объема базисной терапии и др.);
2) оценить возможность коррекции базисной терапии (т.е. устранить все погрешности терапии).
И если после устранения всех модифицирующих факторов, затрудняющих достижение контроля БА, заболевание по-прежнему не контролируется либо у пациента имеются коморбидные заболевания, отягощающие течение БА, которые послужили дополнительными показаниями к назначению ГИБТ (ХПРС, атопический дерма-
тит и др.), рассматривается вопрос о назначении биологической терапии. Надо отметить, что при любой тяжелой эозинофильной БА (ТЭБА) (т.е. и аллергической, и неаллергической, и Т2-БА) можно рассматривать анти-^4Иа-терапию, являющуюся универсальной стратегией, учитывая сигнальный путь ИЛ-4 и ИЛ-13. При этом не требуется строгого определения маркеров, а также обязательного условия в виде повышенного уровня эозинофилов крови. Достаточно оценить наличие частых обострений, подтвердить эозино-фильный характер воспаления либо необходимость использования пероральных ГКС для базисной терапии. Оценку результатов ГИБТ проводят через 16 нед [1]. Если ответ хороший, то терапия продолжается столько, сколько возможно (длительно, постоянно); если ответ сомнительный, терапия продолжается в течение 6-12 мес с последующей оценкой эффективности (целесообразности применения); если ответа нет, рассматривается возможность перевода пациента на другой ГИБП либо отмена ГИБТ эозино-фильного воспаления (возможно, имеет место другой тип воспаления) [1].
В качестве демонстрации эффективности ду-пилумаба (Дупиксент) в лечении ТЭБА приводим клиническое наблюдение из реальной практики.
Клиническое наблюдение
Пациентка Я., 54 года, профессор, заведующая кафедрой. Обратилась в отдел аллергических и аутоиммунных заболеваний ФГБОУ ВО «Ростовский государственный медицинский университет» 13.07.2021 г. с жалобами на одышку в покое и при физической нагрузке, приступы затрудненного дыхания до 2-3 раз в сутки, купирующиеся бронхолитиками, хрипы, свисты в груди, кашель с трудноотделяемой светлой мокротой, ночные пробуждения из-за кашля, выраженное затруднение носового дыхания, отсутствие обоняния в последние 9 лет, перебои в работе сердца, периодическое повышение артериального давления (АД) до 150/90 мм рт. ст., изжогу. Немаловажной жалобой больной была невозможность выполнять профессиональные обязанности: «Трудно читать лекции! Не хватает дыхания, не хватает сил до перерыва».
Анамнез заболевания. Болеет с 42 лет, однако длительно лечилась по поводу хронического бронхита, в 47 лет пульмонологом верифицирован диагноз БА, назначенную базисную терапию (будесонид/формотерол 160/4,5 мкг по 1 дозе 2 раза в сутки) получала нерегулярно. С 45 лет беспокоит заложенность носа, выделения из носовых ходов слизисто-гнойного характера, сни-
жение обоняния; в 47,5 года оториноларингологом выставлен диагноз полипозного риносинуси-та, в качестве базисной терапии назначен моме-тазона фуроат (50 мкг по 2 дозы 2 раза в сутки). В 48 лет после приема нестероидных противовоспалительных средств (НПВС) (ибуклин, пентал-гин), назначенных по поводу травмы нижней конечности, отмечались снижение АД, насморк, удушье. В связи с неконтролируемым течением БА пульмонологом проведена коррекция ранее подобранной базисной терапии — будесонид/формотерол 160/4,5 мкг по 2 дозы 2 раза в сутки, достигнуто понимание необходимости регулярного приема препарата. Тем не менее продолжались неоднократные госпитализации по поводу обострений БА (до 4-5 раз в год) в пульмонологические отделения ГБУ РО «Ростовская областная клиническая больница», Ростовской клинической больницы ФГБУЗ «Южный окружной медицинский центр» ФМБА России, вызовы скорой медицинской помощи (СМП) с необходимостью приема системных ГКС (СГКС) курсами.
Наследственность по аллергопатологии отягощена (у матери ТБА). Аллергоанамнез: лекарственная аллергия — на прием НПВС (потеря сознания, снижение АД, бронхоспазм); пищевая — отрицает; бытовая — на домашнюю пыль (кашель, чихание, насморк); эпидермальная -отрицает; пыльцевая — в течение 4 лет с четкой сезонностью симптомов в 1-ю палинацию (май); инсектная — отрицает; химическая — на стиральный порошок (кашель, чихание, насморк). Курит по 0,5 пачки сигарет в течение 25 лет, индекс курения 12,5. Профессиональные вредности: библиотечная пыль.
На момент обращения получает терапию: будесонид/формотерол 160/4,5 мкг по 1-2 ингаляции 2 раза в день, сальбутамол по потребности (5-7 раз в неделю); мометазона фуроат интрана-зально по 50 мкг — по 2 дозы в каждый носовой ход 1 раз в сутки; деконгестанты.
При оценке контроля БА показатель по АСQ (Asthma Control Questionnaire — опросник по контролю БА) составил 3,5 балла, по АСТ (Asthma Control Test — тест по контролю БА) -10 баллов, что свидетельствует об отсутствии контроля заболевания. Согласно показателям по AQLQ (Asthma Quality of Life Questionnaire -опросник качества жизни при БА), у пациентки отмечался низкий уровень качества жизни (общий балл по шкалам «симптомы», «эмоции», «активность», «окружающая среда» 3,5).
Данные объективного осмотра. На момент осмотра состояние удовлетворительное. Кожные покровы обычной окраски и влажности, высыпаний нет. Носовое дыхание резко затруднено, обо-
Бронхиальная астма
няние отсутствует. При аускультации дыхание жесткое, выслушиваются рассеянные сухие свистящие хрипы по всем полям аускультации легких. Частота дыхательных движений 19 в 1 мин, SpO2 (сатурация, измеренная методом пульсок-симетрии) 96%. Тоны сердца ясные, ритм правильный, частота сердечных сокращений 77 в 1 мин, АД 135/90 мм рт. ст. Живот мягкий, безболезненный при пальпации.
При эндоскопическом исследовании носоглотки и ротоглотки оториноларингологом выявлено стекание слизи по задней стенке глотки, отек слизистой, наличие полипов крупных размеров в носовых ходах с обеих сторон, больше слева, показатель по NPS (Numeric Pain Scale — числовая шкала боли) 5 баллов. Отсутствие обоняния, показатель по SNOT-22 (Sino-Nasal Outcomes Test (22 questions) — тест по оценке исходов болезней носа и околоносовых пазух (22 вопроса)) 77 баллов.
Лабораторно-инструментальные данные. При обследовании в общем анализе крови уровень эозинофилов 947 клеток/мкл. Рентгенологическое исследование органов грудной клетки: легочные поля без патологических теней; легочный рисунок усилен в прикорневых зонах; корни тяжистые; диафрагма и синусы дифференцируются; аорта и сердце — без особенностей.
При проведении спирометрии, выполненной с учетом рекомендаций авторов [18], была выявлена бронхиальная обструкция: до приема бронхо-литика объем форсированного выдоха за 1-ю секунду (ОФВх) 2,75 л (65% от должного), форсированная жизненная емкость легких (ФЖЕЛ) 3,02 л (71% от должной), ОФВ/ФЖЕЛ 66,4%. Тест с бронхолитиком положительный.
По результатам измерения FeNO выявлена высокая активность воспаления в нижних дыхательных путях (FeNO 47 ppb).
При аллергологическом обследовании (лабораторном in vitro (IgE общий), кожном тестировании) сенсибилизации не выявлено.
Общий анализ мокроты: цвет — серый; консистенция — вязкая; характер — слизисто-гнойная; лейкоциты — до 20 в поле зрения; эритроциты -нет; эпителий плоский — значительное количество; эпителий альвеолярный — большое количество; кристаллы Шарко-Лейдена — нет; эозино-филы — единичные; другое: цилиндрический эпителий — небольшое количество.
Фиброэзофагогастродуоденоскопия от
25.01.2021 г.: грыжа пищеводного отверстия диафрагмы I стадии; поверхностный гастрит, дуоденит; рубцово-язвенная деформация луковицы двенадцатиперстной кишки.
Данные общего анализа крови и общего IgE по истории болезни за предшествующие визиту
12 мес: 16.08.2019 г. лейкоциты 7,53 х 109/л, эозинофилы 10,4% (783,12 клеток/мкл);
15.09.2019 г. лейкоциты 13,0 х 109/л, эозинофилы 1% (130 клеток/мкл), IgE общий 336,7 МЕ/мл; 21.01.2020 г. лейкоциты 12,6 х х 109/л, эозинофилы 2% (252 клеток/мкл);
23.04.2020 г. лейкоциты 13,43 х 109/л, эозинофилы 2,2% (0,29 х 109/л; 295,46 клеток/мкл);
21.06.2020 г. лейкоциты 8,2 х 109/л, эозинофилы 6% (492 клеток/мкл), IgE общий 502,0 МЕ/мл;
27.05.2021 г. лейкоциты 7,23 х 109/л, эозинофилы 13,1% (947,13 клеток/мкл). Представленная динамика уровня эозинофилов в общем анализе крови указывает на необходимость анализировать не менее 2-3 результатов в разные периоды в случае нормальных либо невысоких уровней эозинофилов периферической крови.
С учетом дообследования различных специалистов (результаты которых не представлены в данной статье ввиду иных целей изложения материала) был выставлен клинический диагноз: БА, эозинофильный фенотип, неаллергическая форма, тяжелого течения, неконтролируемая; осложнения основного заболевания: дыхательная недостаточность II степени; сопутствующие заболевания и состояния: ХПРС; лекарственная непереносимость (НПВС); аспириновая триада; гипертоническая болезнь, II стадия, 2-я степень, группа риска 3; гастроэзофагеальная рефлюкс-ная болезнь; хронический гастродуоденит; руб-цовая деформация луковицы двенадцатиперстной кишки; дистальный пептический рефлюкс-эзофагит; стеатогепатоз; аутоиммунный тиреои-дит, диффузная форма; гипотиреоз, стадия медикаментозной компенсации; дисгормональ-ная миокардиодистрофия; сахарный диабет 2-го типа, целевой уровень гликированного гемоглобина (НЬ) <7%; диабетическая полиневропатия нижних конечностей II стадии.
Такая коморбидность часто является фактором, затрудняющим достижение контроля БА. Больной были даны рекомендации: диспансерное наблюдение аллерголога-иммунолога, терапевта, пульмонолога, эндокринолога, гастроэнтеролога, оториноларинголога; соблюдение гипоаллерген-ной диеты, гипохолестериновой, с ограничением легкоусвояемых углеводов, жиров животного происхождения; исключение приема НПВС, ацетилсалициловой кислоты, тартразина. Назначена фармакотерапия: будесонид/формотерол 160/4,5 мкг по 2 дозы 2 раза в день — длительно + + по потребности (MART (maintenance and reliever therapy — поддерживающая и симптоматическая терапия)); тиотропия бромид 2,5 мкг 2 дозы (5 мг) в обед — длительно; монтелукаст натрия 10 мг 1 таблетка в сутки — длительно; мометазона фуро-
Динамика показателей пациентки Я. в процессе лечения дупилумабом
Показатель До лечения После лечения
через 3 мес через 6 мес через 9 мес через 12 мес
Эозинофилия крови, клеток/мкл 947,13 648,48 655,20 331,20 374,22
^Е общий, МЕ/мл 502,00 121,00 153,25 91,48 86,40
ЕСР, нг/мл 74,2 — 57,9 — —
FeNO, ррЬ 47 36 29 14 8
ОФВ1, л (% от должного) 2,75 (65) 2,12 (79) 2,30 (84) 2,41 (90) 2,92 (93)
АСТ, баллы 10 21 23 23 23
ACQ-5, баллы 3,5 0,8 0,5 0,5 0
AQLQ, баллы 3,5 5,8 6,5 6,8 6,8
Число обострений в год, абс. 4-5 0 0 0 0
SNOT-22, баллы 77 — 26 — 2
NPS, баллы 5 — 0 — 0
Шкала Lund-Mackay, баллы 20 — 5 — 1
Обозначения: ЕСР — eosinophil cationic protein (эозинофильный катионный белок).
ат интраназально 50 мкг/доза по 2 спрей-дозы (100 мкг) в каждый носовой ход 1 раз в сутки -длительно; коррекция коморбидных патологий: L-тироксин 50 мкг 1 раз в день утром, за 40 мин до еды, с контролем тиреотропного гормона (ТТГ), свободного тироксина (Т4), ультразвукового исследования (УЗИ) щитовидной железы через 5 мес; контроль глюкозы крови, гликированный НЬ — контроль 1 раз в 3 мес; антигипертензивные и гиполипидемические препараты; а также небу-лайзерная терапия (компрессорный ингалятор) при обострении (будесонид + короткодействующие бронхолитики + + муколитики (амброксол)); элиминационная терапия (орошение слизистой носа и ротовой полости солевыми изотоническими растворами 2 раза в сутки, утром и вечером); барьерные препараты перед контактом с возможным триггером до 8 раз в сутки по потребности; пикфлоуметрия ежедневно (утром и вечером), ведение дневника самонаблюдения.
На фоне указанной терапии были стабилизированы коморбидные состояния, но симптомы БА возникали не менее 3 раз в неделю, чаще в ночное время, отмечались ночные пробуждения из-за кашля, «свистов», назальной обструкции.
С учетом рефрактерности к проводимой амбулаторной терапии, отрицательной клинической и инструментальной (спирометрия, пикфлоумет-рия) динамики течения БА, частых госпитализаций и вызовов СМП с необходимостью приема СГКС, в целом отсутствия контроля заболевания на фоне приема высоких доз ИГКС/ДДБА, дли-тельнодействующих антихолинергических препаратов, антилейкотриеновых препаратов, а также наличия ХПРС, было принято решение о подключении ГИБТ дупилумабом по стандартной
схеме (инициация лечения с дозы 600 мг (2 инъекции по 300 мг) подкожно 1 раз в день, с последующим введением по 300 мг каждые 2 нед).
Результаты терапии дупилумабом: через 2 нед от начала лечения пациентка отметила значительное улучшение самочувствия: появилось обоняние, улучшилось назальное дыхание, уменьшились кашель и одышка, через 3 нед восстановилось носовое дыхание. Надо отметить, что одна из важнейших назальных функций -обоняние, нами была объективно исследована с помощью UPSIT (University of Pennsylvania Smell Identification test — идентификационный обонятельный тест Пенсильванского университета) согласно алгоритму [19]. При мониториро-вании состояния через 3, 6 и 12 мес от начала терапии у пациентки отмечалось улучшение показателей спирометрии, контроля симптомов БА, дальнейшее уменьшение одышки, приступов затрудненного дыхания, увеличение толерантности к физической нагрузке, что сопровождалось устойчивым снижением уровня IgE общего, FeNO (таблица). Количество эозинофилов в периферической крови снизилось через 3 мес от начала терапии, в дальнейшем указанная тенденция сохранялась, однако этот показатель оставался в пределах выше референтных значений (см. таблицу). За 12 мес наблюдения и лечения обострений БА не отмечалось (см. таблицу).
При осмотре оториноларингологом (эндоскопическое исследование через 6 и 12 мес): нос -произведен осмотр жестким эндоскопом; носовое дыхание незначительно затруднено; наружный нос без особенностей, слизистая оболочка розовая, носовые раковины гипертрофированы, носовая перегородка искривлена в передних отде-
лах вправо, в средних носовых ходах свободно, полипозной ткани нет. Данные компьютерной томографии представлены на рисунке.
Через 6 мес была пересмотрена базисная терапия: снижена доза ИГКС/ДДБА (будесо-нид/формотерол 160/4,5 мкг по 1 дозе 2 раза в сутки) с сохранением приема монтелукаста и тиотропия бромида. Продолжено лечение сопутствующих заболеваний ^-тироксин, нолипрел, крестор, глюкофаж; контроль ТТГ, свободного Т4, УЗИ щитовидной железы через 5 мес, контроль глюкозы крови, гликированный НЬ — контроль 1 раз в 3 мес; контроль липидограммы, аланинаминотрансферазы, аспартатаминотранс-феразы), проведение пикфлоуметрии ежедневно (утром и вечером), ведение дневника самонаблюдения. При осмотре оториноларингологом через 6 мес было отмечено значительное уменьшение полипозных вегетаций, через 12 мес — их полное отсутствие. Кроме того, пациентка отметила уменьшение потребности в топических ГКС, а также появление обоняния (через 2 нед от начала лечения). Пациентке была продолжена терапия дупилумабом (Дупиксент) в прежней дозе. В ходе клинического наблюдения в течение 12 мес не было зафиксировано обострений БА, вызовов СМП, обращений за неотложной помощью.
Вывод: включение дупилумаба (Дупиксент) в терапию ТЭБА значительно улучшило ее течение у пациентки:
1) не отмечено повышения уровня эозинофи-лов на фоне терапии, напротив, хотя этот показатель и оставался повышенным относительно нормы, наблюдалась тенденция к его снижению: исходно — 947,13 клеток/мкл, через 3 мес — 648,48 клеток/мкл, через 6 мес -655,20 клеток/мкл, через 9 мес — 331,20 кле-ток/мкл, через 12 мес — 374,22 клеток/мкл;
2) отмечалось улучшение контроля симптомов БА, увеличение ОФВХ;
3) прием препарата способствовал сокращению числа обострений (с 4-5 до 0 в год), отсутствию потребности в СГКС (курсовое лечение), снижению дозы ИГКС, уменьшению активности воспаления (снижение FeNO);
4) по данным эндоскопического исследования носоглотки было выявлено сокращение размеров полипов (вплоть до их отсутствия) при снижении выраженности воспалительных изменений слизистой оболочки околоносовых пазух по шкале Lund-Mackay, что свидетельствует о возможности обратного развития полипозного процесса на фоне применения МАТ (дупилумаб);
5) отмечалось улучшение качества жизни, подтвержденное результатами опросников AQLQ, SNOT-22;
Компьютерные томограммы придаточных пазух носа пациентки Я. до лечения (а) и через 6 мес лечения дупилумабом (б).
6) на фоне ГИБТ дупилумабом нежелательных явлений не зафиксировано. Переносимость препарата оценена как «отличная»;
7) больная свободно решает все свои профессиональные задачи, бодра, оптимистично настроена на будущее, мотивирована на дальнейшее лечение.
Таким образом, представленное клиническое наблюдение согласуется с результатами многочисленных рандомизированных клинических исследований: ГИБТ дупилумабом, направленная на блокирование ключевых цитокинов (ИЛ-4/ИЛ-13), участвующих в формировании эозинофильного воспаления, эффективна и безопасна в лечении ТЭБА. Лечение МАТ (дупилу-маб) больных ТЭБА, в том числе при наличии у них ассоциированных с эозинофильным воспалением заболеваний, в частности ХПРС, приводит не только к улучшению контроля симптомов БА, но и к значительному регрессу назальных симптомов, т.е. положительной динамике ко-морбидных ассоциированных с Т2-воспалением состояний. У пациентки с ТЭБА и сопутствующим ХПРС, получавшей ГИБТ дупилумабом, отмечались клинические, эндоскопические и рентгенологические признаки снижения выраженности назальных симптомов, а также улучшение контроля симптомов БА, подтвержденное результатами исследования функции внешнего дыхания, данными опросников АСТ и ACQ, и в целом улучшение течения БА с учетом комор-бидных заболеваний, что сопровождалось улучшением качества жизни, подтвержденным результатами опросников AQLQ, SNOT-22.
Список литературы
1. Global Initiative for Asthma. Global strategy for asthma management and prevention. Updated 2022. Available from: https://ginasthma.org/wp-content/uploads/2022/09/GINA-2022-Main-Report_FINAL_22_09_28-WMS.pdf Accessed 2022 Dec 09.
2. Министерство здравоохранения РФ; Российское респираторное общество; Российская ассоциация аллергологов и клинических иммунологов; Союз педиатров России. Клинические рекомендации. Бронхиальная астма. Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: J45, J46. Год утверждения (частота пересмотра): 2021. Возрастная категория: взрослые, дети. Год окончания действия: 2023. М., 2021. 114 с. Доступно по: https://cr.minzdrav.gov.ru/ schema/359_2 Ссылка активна на 09.12.2022.
3. Ненашева Н.М. Т2-бронхиальная астма: характеристика эндотипа и биомаркеры. Пульмонология 2019;29(2):216-28.
4. Чурюкина Э.В., Сизякина Л.П., Ващенко Т.Б. Эффективность и безопасность интерлейкина-2 в комплексном лечении больных гормонозависимой бронхиальной астмой тяжелого течения. Российский аллергологический журнал 2006;4:17-21.
5. Israel E, Reddel HK. Severe and difficult-to-treat asthma in adults. The New England Journal of Medicine 2017 Sep;377(10):965-76.
6. Kim H, Ellis AK, Fischer D, Noseworthy M, Olivenstein R, Chapman KR, Lee J. Asthma biomarkers in the age of biologics. Allergy, Asthma and Clinical Immunology 2017 Nov;13:48.
7. Gandhi NA, Bennett BL, Graham NMH, Pirozzi G, Stahl N, Yancopoulos GD. Targeting key proximal drivers of type 2 inflammation in disease. Nature Reviews. Drug Discovery 2016 Jan;15(1):35-50.
8. Tan BK, Chandra RK, Pollak J, Kato A, Conley DB, Peters AT, Grammer LC, Avila PC, Kern RC, Stewart WF, Schleimer RP, Schwartz BS. Incidence and associated premorbid diagnoses of patients with chronic rhinosinusitis. The Journal of Allergy and Clinical Immunology 2013 May;131(5):1350-60.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
9. Marcus P, Arnold RJG, Ekins S, Sacco P, Massanari M, Stanley Young S, Donohue J, Bukstein D; CHARIOT Study Investigators. A retrospective randomized study of asthma control in the US: results of the CHARIOT study. Current Medical Research and Opinion 2008 Dec;24(12):3443-52.
10. Blander JM. The many ways tissue phagocytes respond to dying cells. Immunological Reviews 2017 May;277(1):158-73.
11. Fahy JV. Type 2 inflammation in asthma — present in most, absent in many. Nature Reviews. Immunology 2015 Jan;15(1):57-65.
12. Condon TV, Sawyer RT, Fenton MJ, Riches DW. Lung dendritic cells at the innate-adaptive immune interface. Journal of Leukocyte Biology 2011 Nov;90(5):883-95.
13. Santini G, Mores N, Malerba M, Mondino C, Anzivino R, Macis G, Montuschi P. Dupilumab for the treatment of asthma. Expert Opinion in Investigational Drugs 2017 Mar;26(3):357-66.
14. Brusselle GG, Maes T, Bracke KR. Eosinophils in the spotlight: eosinophilic airway inflammation in nonallergic asthma. Nature Medicine 2013 Aug;19(8):977-9.
15. Castro M, Corren J, Pavord ID, Maspero J, Wenzel S, Rabe KF, Busse W, Ford L, Sher L, FitzGerald JM, Katelaris C, Tohda Y, Zhang B, Staudinger H, Pirozzi G, Amin N, Ruddy M, Akin-lade B, Khan A, Chao J, Martincova R, Graham NMH, Hamilton JD, Swanson BN, Stahl N, Yancopoulos GD, Teper A. Dupilumab efficacy and safety in moderate-to-severe uncontrolled asthma. The New England Journal of Medicine 2018 Jun;378(26):2486-96.
16. U.S. Food & Drug Administration. Regulatory information. Guidance document. Immunogenicity assessment for therapeutic protein products, August 2014. Available from: http://www.fda.gov/downloads/Drugs/ GuidanceComplianceRegulatoryInformation/Guidances/ UCM338856.pdf Accessed 2022 Dec 09.
17. Инструкция по медицинскому применению лекарственного препарата Дупиксент®. РУ № ЛП-005440 от 04.04.19 с изменениями от 16.04.2021.
18. Чурюкина Э.В., Никанорова М.В. Диагностический алгоритм спирометрической верификации диагноза бронхиальной астмы. Аллергология и иммунология 2016;17(2):131-2.
19. Чурюкина Э.В., Уханова О.П. Современные лечебно-диагностические инструменты оценки назальной функции и нарушений обоняния у пациентов с аллергическим ринитом. Алгоритм комплексной терапии. Русский медицинский журнал 2020;28(12):56-60.
Dupilumab: Aspects of Use for Severe Asthma in Real Clinical Practice
E.V. Churyukina
Asthma is a heterogeneous chronic inflammatory disease characterized by various phenotypic and endotypic characteristics. Depending on the type of immune response, T2- and non-T2-inflammation is isolated, underlying T2-associ-ated diseases, including T2-asthma. One of the key cytokines of T2-inflammation are interleukins 4 and 13. Blocking their signaling pathways is the mechanism of action of a completely human monoclonal antibody dupilumab. The effectiveness of this biological drug in the treatment of severe eosinophilic asthma, or T2-asthma, is presented on a real clinical example.
Key words: asthma, genetically engineered biological therapy, dupilumab, nasal polyps.
Новые возможности в терапии бронхиальной астмы и полипозного риносинусита: дупилумаб
Известно, что при бронхиальной астме с эндотипом Т2 – опосредованного эозинофильного воспаления ведущие позиции занимают интерлейкины (ИЛ) 4, 5 и 13. Данные цитокины играют важную роль в патогенезе БА, где ИЛ-5 отвечает за дифференцировку, созревание и выживание эозинофилов, а ИЛ-4 и ИЛ-13 участвуют в рекрутировании эозинофилов в дыхательных путях (где они способствуют повреждению эпителия), стимуляции бокаловидных клеток дыхательных путей к секреции слизи и синтезу оксида азота. Эти цитокины стимулируют также продукцию иммуноглобулина Е (IgE).
Полипозный риносинусит (ПРС) следует рассматривать как фактор риска формирования тяжёлой плохо контролируемой БА. Патогенез ПРС в большинстве случаев также характеризуется T2-опосредованным эозинофильным воспалением.
Таким образом, в связи с особенностями патогенеза БА и ПРС, в патогенезе которых участвуют схожие биомишени, дупилумаб, действующий направленно на сигнализацию ИЛ-4 и ИЛ-13, стал своеобразным прорывом.
В настоящее время, дупилумаб не только прошел все этапы клинического исследования, но и зарекомендовал себя как безопасное и эффективное лечебное средство.
На IIB и III фазе клинического исследования у взрослых и подростков с умеренной и тяжёлой БА подкожные введения дупилумаба в дозе 200 и 300 мг на срок до 52 недель способствовали снижению концентрации оксида азота в выдыхаемом воздухе, общего IgE в сыворотке крови, провоспалительных цитокинов и хемокинов в сравнении с плацебо (p <0,001).
В настоящее время дупилумаб, изученный по меньшей мере у 3000 пациентов с БА, атопическим дерматитом, ПРС и эозинофильным эзофагитом, показал приемлемый профиль безопасности в плацебоконтролируемых исследованиях по всей стране.
Доказано, что добавление дупилумаба приводило к снижению частоты обострений БА у взрослых и подростков, которые ранее не контролировались средними и высокими дозами ингаляционных или системных ГК. Была продемонстрирована более высокая, в сравнении с плацебо, вероятность снижения суточной дозы ГК у пациентов с тяжелой БА до уровня <5 мг, а также более высокая вероятность полной отмены ГК.
При оценке эффективности дупилумаба в качестве дополнительного лечения к стандартной терапии у взрослых с тяжёлой формой ПРС, выявили, что у пациентов, согласно данным эндоскопического осмотра, значительно уменьшились размеры полипов, купировались синоназальные симптомы. Лечение дупилумабом, по сравнению с плацебо, значительно сократило использование системных ГК и долю пациентов, перенёсших полисинусотомию.
Следует отметить, что, на сегодняшний день, дупилумаб является единственным иммунобиологическим препаратом, одобренным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) для лечения полипозного риносинусита (июнь, 2019).
Таким образом, по мнению авторов, дупилумаб ― значительный прогресс в лечении БА и ПРС, и в первую очередь ― при их сочетании. Однако, на сегодняшний день необходимо понять, какие пациенты отвечают на данную терапию наиболее эффективно. Это подчёркивает необходимость будущих исследований для выявления соответствующих биомаркеров и их глубокого анализа с целью прогнозирования эффективности терапии дупилумабом.
Источник: Дынева М.Е., Аминова Г.Э., Курбачева О.М., Ильина Н.И. Дупилумаб: новые возможности в терапии бронхиальной астмы и полипозного риносинусита // Российский аллергологический журнал. 2021. Т. 18. № 1. С. 18–31. DOI: https://doi.org/10.36691/RJA1408