Алмовитае (Алмотриптан)
МНН: Алмотриптана D,L — малата (эквивалентно алмотриптана основанию)
Анатомо-терапевтическо-химическая классификация: Селективные агонисты 5НТ1-рецепторов
Номер регистрации в РК:
№ РК-ЛС-5№025000
Информация о регистрации в РК:
22.04.2021 — 22.04.2026
- Скачать инструкцию медикамента
Торговое название
Международное непатентованное название
Алмотриптан
Лекарственная
форма, дозировка
Таблетки,
покрытые пленочной оболочкой, 12.5 мг
Фармакотерапевтическая группа
Нервная
система.
Анальгетики. Противомигренозные препараты. Селективные агонисты
серотониновых 5-HT1-рецепторов.
Алмотриптан.
Код АТХ
N02CC05
Показания к применению
Неотложное
лечение головной боли при приступах мигрени с аурой или без нее.
Перечень
сведений, необходимых до начала применения
Противопоказания
-
Повышенная
чувствительность к активному или одному из вспомогательных веществ
препарата. -
Как
и в случае с другими агонистами 5-HT1B/1D-рецепторов,
алмотриптан не следует применять пациентам с анамнезом, симптомами /
признаками ишемической болезни сердца (инфаркт миокарда,
стенокардия, документально подтвержденная бессимптомная ишемия,
стенокардия Принцметала) или тяжелой гипертонией и неконтролируемой
легкой/умеренной гипертонией. -
Пациентам
с перенесенным инсультом (CVA) или транзиторной ишемической атакой
(TIA). -
Периферические
сосудистые заболевания. -
Одновременное
применение с эрготамином, производными эрготамина (включая
метизергид) и другими агонистами 5-HT1B/1D
противопоказано. -
Пациентам
с тяжелой печеночной недостаточностью. -
Детский и
подростковый возраст до 18 лет.
Необходимые
меры предосторожности при применении
Алмотриптан
следует применять только при наличии четкого диагноза мигрени. Не
следует использовать его для лечения базилярной, гемиплегической или
офтальмоплегической мигрени.
Как и в случае
других методов лечения острой мигрени, до лечения головных болей
пациентов, ранее не диагностированных как страдающие мигренью, и у
страдающих мигренью, имеющих атипичные симптомы, следует позаботиться
об исключении других потенциально серьезных неврологических
состояний. Сообщалось об инсультах у пациентов, получавших агонисты
5-HT1B/1D.
Следует отметить, что болеющие мигренью могут подвергаться
повышенному риску определенных цереброваскулярных инцидентов
(например, инсульт, транзиторная ишемическая атака).
В очень редких
случаях, как и в случае с другими агонистами 5-HT1B/1D-рецепторов,
сообщалось о коронарном спазме и инфаркте миокарда. Следовательно,
алмотриптан не следует назначать пациентам, у которых может быть
недиагностированное коронарное заболевание без предварительной оценки
потенциального основного сердечно-сосудистого заболевания. К таким
пациентам относятся женщины в постменопаузе, мужчины старше 40 лет и
пациенты с другими факторами риска развития ишемической болезни
сердца, такими как неконтролируемая гипертензия, гиперхолестеринемия,
ожирение, диабет, курение или явный наследственный анамнез
сердечно-сосудистых заболеваний. Эти оценки, однако, могут не
идентифицировать каждого пациента с сердечным заболеванием, и в очень
редком случае серьезные сердечные события имели место у пациентов без
основного сердечно-сосудистого заболевания, когда вводились агонисты
5-HT1.
После
введения алмотриптан может быть связан с переходящими симптомами,
включая боль в груди и чувство сжимания
горла, которые могут быть
интенсивными и затрагивать горло. В случае если такие симптомы
указывают на ишемическую болезнь сердца, дальнейшая доза не должна
приниматься и должна проводиться соответствующая оценка.
Следует
соблюдать осторожность при назначении алмотриптана пациентам с
известной повышенной чувствительностью к сульфонамидам.
Синдром
серотонина (включая измененный психический статус, вегетативную
нестабильность и нервно-мышечные нарушения) был зарегистрирован после
сопутствующего лечения триптанами и селективными ингибиторами
обратного захвата серотонина (СИОЗС) или ингибиторами обратного
захвата норадреналина серотонина (ИОЗНС).
Эти реакции могут быть серьезными. Если сопутствующее лечение
алмотриптаном и СИОЗС или ИОЗНС
является клинически оправданным, рекомендуется соответствующее
наблюдение за пациентом, особенно во время начала лечения, с
увеличением дозы или с добавлением другого серотонинергического
препарата.
Рекомендуется
подождать не менее 6 часов после использования алмотриптана перед
приемом эрготамина. Не менее 24 часов должно пройти после приема
эрготаминсодержащего препарата перед приемом алмотриптана.
Пациентам с
тяжелой почечной недостаточностью не следует принимать более одной
таблетки по 12,5 мг в течение 24 часов.
Следует
соблюдать осторожность пациентам с заболеваниями печени легкой и
средней степени тяжести, а лечение противопоказано пациентам с
тяжелыми заболеваниями печени.
Нежелательные
реакции могут быть более частыми при одновременном применении
триптанов и растительных препаратов, содержащих зверобой (Hypericum
perforatum).
Как и в случае
с другими агонистами 5-HT1B/1D-рецепторов,
алмотриптан может вызывать умеренное, кратковременное повышение
артериального давления, которое может быть более выраженным у пожилых
людей.
Головная боль
от чрезмерного использования лекарств (MOH)
Длительное
использование любого обезболивающего при головных болях может
усугубить их. Если такая ситуация возникла или есть подозрения,
следует получить медицинскую консультацию и прервать лечение. Диагноз
МЗ следует подозревать у пациентов с частыми или ежедневными
головными болями, несмотря на (или из-за) регулярного использования
лекарств от головной боли.
Максимальная
рекомендуемая доза алмотриптана не должна превышаться.
Взаимодействия
с другими лекарственными препаратами
Исследования
взаимодействия проводились с ингибиторами моноаминоксидазы А,
бета-блокаторами, селективными ингибиторами обратного захвата
серотонина, блокаторами кальциевых каналов или ингибиторами
изоферментов цитохрома Р450 3А4 и 2D6. Не имеется исследований
взаимодействия in vivo,
оценивающих влияние алмотриптана на другие лекарственные средства.
Как и в случае
с другими агонистами 5-HT1,
нельзя исключать потенциальный риск развития серотонинергического
синдрома, из-за фармакодинамического взаимодействия в случае
сопутствующего лечения ИМАО.
Были сообщения о пациентах
с симптомами, совместимыми с серотониновым синдромом (включая
измененный психический статус, вегетативную нестабильность и
нервно-мышечные нарушения) после применения селективных ингибиторов
обратного захвата серотонина (СИОЗС) или ингибиторов обратного
захвата норадреналина (ИОЗНС) серотонина и триптанов.
Многократные
дозы с блокатором кальциевых каналов верапамилом, субстратом CYP3A4,
приводили к 20% увеличению Cmax
и AUC алмотриптана. Увеличение не считается клинически значимым.
Клинически значимых взаимодействий не наблюдалось.
Многократное
введение пропранолола не влияло на фармакокинетику алмотриптана.
Клинически значимых взаимодействий не наблюдалось.
Исследования
in vitro,
проведенные для оценки способности алмотриптана ингибировать основные
ферменты CYP в микросомах печени человека и моноаминоксидазы человека
(МАО), показали, что не ожидается, что алмотриптан изменит метаболизм
лекарств, метаболизируемых CYP или МАО-А и МАО- B ферменты.
Специальные
предупреждения
Беременность
и период лактации
Данные
для алмотриптана о беременных пациентах ограничены.
Следует
соблюдать осторожность при назначении алмотриптана беременным
женщинам.
Нет данных
относительно экскреции алмотриптана с грудным молоком. Следует
соблюдать осторожность при назначении во время кормления грудью.
Младенческое воздействие можно свести к минимуму, избегая грудного
вскармливания в течение 24 часов после лечения.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Учитывая
возможность возникновения побочных действий препарата, например,
головокружения, необходимо соблюдать осторожность при управлении
транспортным средством или механизмами, требующими повышенного
внимания.
Рекомендации
по применению
Режим
дозирования
Алмотриптан
не следует использовать для профилактики мигрени.
Взрослые
(18-65 лет)
Рекомендуемая
доза составляет одну таблетку, содержащую 12,5 мг алмотриптана.
Вторая доза может быть принята, если симптомы появятся в течение 24
часов. Эта вторая доза может быть принята при условии, что между
двумя дозами есть минимальный интервал в два часа.
Эффективность
второй дозы для лечения того же приступа, когда начальная доза
неэффективна, не была исследована в контролируемых испытаниях.
Поэтому если пациент не реагирует на первую дозу, не следует
принимать вторую дозу для того же приступа.
Максимальная
рекомендуемая доза составляет две дозы за 24 часа.
Дети
и подростки (до 18 лет)
Нет
никаких данных относительно использования алмотриптана у детей и
подростков, поэтому в этой возрастной группе его использование не
рекомендуется.
Пожилые
люди (старше 65 лет)
Регулировка
дозировки у пожилых людей не требуется. Безопасность и эффективность
алмотриптана у пациентов старше 65 лет систематически не оценивалась.
Почечная
недостаточность
Регулировка
дозировки не требуется и у пациентов с легкой или умеренной почечной
недостаточностью. Пациентам с тяжелой почечной недостаточностью
следует принимать не более одной таблетки по 12,5 мг в течение 24
часов.
Печеночная
недостаточность
Нет данных
относительно использования алмотриптана у пациентов с печеночной
недостаточностью.
Метод
и путь введения
Алмотриптан
следует принимать с жидкостями как можно раньше после появления
головной боли, связанной с мигренью, но он также эффективен при
приеме на более поздней стадии.
Таблетки можно
принимать с едой или без еды.
Меры,
которые необходимо принять в случае передозировки
Наиболее
частым побочным явлением у пациентов, получавших 150 мг (самая
высокая доза для пациентов), была сонливость.
Передозировка
должна лечиться симптоматически и осуществлять поддержку жизненно
важных функций. Поскольку период полувыведения составляет около 3,5
часов, мониторинг должен продолжаться не менее 12 часов или пока
сохраняются симптомы или признаки.
Описание
нежелательных реакций, которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
Алмотриптан
был оценен у более чем 2700 пациентов сроком до одного года в
клинических испытаниях. Наиболее частыми побочными реакциями в
терапевтической дозе были головокружение, сонливость, тошнота, рвота
и усталость. Ни одна из побочных реакций не имела частоты выше 1,5%.
Следующие
побочные реакции были оценены в клинических исследованиях и/или
зарегистрированы в постмаркетинговом опыте. Они перечислены в порядке
убывания частоты. Частота определена следующим образом: очень
часто (> 1/10),
часто
(от ≥1 / 100 до <1/10), нечасто
(от ≥1 / 1000 до <1/100), редко
(от ≥1 / 10000 до <1 / 1 000), очень
редко (<1/10 000) и
неизвестно
(не может быть оценена по имеющимся данным).
Часто (от
≥1 / 100 до <1/10)
—
головокружение,
сонливость
— тошнота,
рвота
— усталость
Нечасто (от
≥1 / 1000 до <1/100)
— парестезия,
головная боль
— тиннит
— учащенное
сердцебиение
— сжимание
горла
— диарея,
диспепсия,
сухость
во рту
— миалгия,
боль
в костях
— боль в
груди, астения
Очень редко
(< 1/10,000)
—
коронароспазм, инфаркт миокарда, тахикардия
Неизвестно
(невозможно установить частоту на основании имеющихся данных)
— реакции
чувствительности (включая ангионевротический отек), анафилактические
реакции
—
судороги
— нарушение
зрения*, расфокусированное
зрение*
*
Однако нарушения зрения могут возникать и во время самого приступа
мигрени.
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов
РГП на ПХВ
«Национальный центр экспертизы лекарственных средств и
медицинских изделий» Комитета медицинского и фармацевтического
контроля Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав
лекарственного препарата
Одна
таблетка содержит
активное
вещество —
алмотриптана D,
L-малат
17.50 мг (эквивалентно алмотриптана основанию 12.50 мг)
вспомогательные
вещества: маннитол, целлюлоза
микрокристаллическая PH
102, повидон К29/32, вода очищенная, натрия крахмала гликолят (тип
А), натрия стеарилфумарат.
Состав
пленочной оболочки Opadry
Y-1-7000:
гипромеллоза (Е464), титана диоксид (Е171),
ПЭГ 400.
Описание
внешнего вида, запаха, вкуса
Таблетки
круглой формы, покрытые пленочной оболочкой белого цвета, с
двояковыпуклой поверхностью, гладкие с обеих сторон.
Форма выпуска и упаковка
По
3 таблетки помещают в контурную ячейковую упаковку из пленки
поливинилхлоридной и фольги алюминиевой.
По 1 контурной
ячейковой упаковке вместе с инструкцией по медицинскому применению на
казахском и русском языках помещают в пачку из картона.
Срок хранения
4
года
Не
применять по истечении срока годности.
Условия хранения
Хранить
при температуре не выше 25°С.
Хранить
в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту
Сведения
о производителе
САГ
Мануфактуринг С.Л.У.
Carretera
Nacional I, Km 36 San Agustin de Guadalix, 28750 (Мадрид),
Испания
Тел.:
+34918488358
Факс:
+34918488622
Эл.
почта:
rfe@galenicum.com
Держатель
регистрационного удостоверения
Майлен
Фарма С.А.
Via
Crocicchio
Cortogna
6-6901, Лугано, Швейцария
Тел.:
+41916494741
Факс:
+41916494743
Эл.
почта: —
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан, принимающей претензии
(предложения) по качеству лекарственных средств от потребителей и
ответственной за пострегистрационное наблюдение за безопасностью
лекарственного средства
ТОО
«Биофармед»
050008,
г. Алматы, ул. Муканова д. 241, кв. 42
Тел./факс:
+7-727-313-74-96, +77717794502
Эл.
почта: too.biofarmed@mail.ru
| 3._ИМП_Алмовитае_.docx | 0.04 кб |
| Алмовитае_ИМП_каз.яз_.(1)_.doc | 0.12 кб |
Отправить прикрепленные файлы на почту
Алмотриптан
Almotriptan
Фармакологическое действие
Алмотриптан — препарат триптана для лечения мигрени, входит в класс селективных агонистов серотониновых рецепторов. Механизм действия проявляется сужением кровеносных сосудов в мозге, прекращением передачи болевых сигналов в мозг и прекращения выделения определённых природных веществ, которые вызывают боль, тошноту и другие симптомы мигрени.
Противопоказания
- Повышенная чувствительность к алмотриптану;
- гемиплегическая или базилярная мигрень;
- известная или подозреваемая ишемическая болезнь сердца;
- цереброваскулярные синдромы;
- заболевание периферических сосудов;
- неконтролируемая гипертония;
- одновременное применение в течение 24 часов другого агониста 5-HT1;
- одновременное применение в течение 24 часов производных эрготамина и/или эрготаминсодержащих препаратов.
Беременность и грудное вскармливание
Применение при беременности
Категория действия на плод по FDA — C.
Адекватных и строго контролируемых исследований по безопасности применения алмотриптана при беременности у человека не проведено. Исследования на животных, при применении в дозах от 80 до почти 1000-кратной рекомендуемой суточной дозы для человека, выявили признаки токсичности для развития.
В случае наступления беременности, отсутствия менструации или при подозрении на возможную беременность пациентка должна сообщить об этом своему лечащему врачу.
Применение алмотриптана при беременности допустимо по назначению врача, если ожидаемая польза для матери превышает потенциальный риск для плода.
Применение в период грудного вскармливания
Специальных исследований по безопасности применения алмотриптана в период грудного вскармливания не проведено.
Неизвестно, выделяется ли алмотриптан в грудное человеческое молоко. Экспериментальные исследования показали выделение алмотриптана в молоко лактирующих животных. Риск для грудного ребёнка не может быть исключён.
Рекомендуется прекратить грудное вскармливание в случае применения препарата.
Способ применения и дозы
Перорально.
Начальная доза — 6,25–12,5 мг однократно; если головная боль возвращается, повторить дозу через 2 часа; не более 2 доз в сутки.
Максимальная суточная доза — 25 мг.
Побочные действия
Частота встречаемости нежелательных реакций от 1 % до 10 %:
Со стороны центральной нервной системы: сонливость (≤5 %), головокружение (≤4 %), головная боль (≤2 %), парестезия (≤1 %).
Со стороны желудочно-кишечного тракта: тошнота (от 1 % до 3 %), рвота (≤2 %), ксеростомия (1 %).
Особые указания
Алмотриптан не предотвращает приступы мигрени.
Влияние на способность к вождению автотранспорта и управлению механизмами
В связи с тем, что алмотриптан может вызвать головокружение и сонливость необходимо воздержаться от управления транспортными средствами и занятий видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Классификация
-
АТХ
N02CC05
-
Фармакологическая группа
-
Код МКБ 10
-
Категория при беременности по FDA
C
(риск не исключается)
Информация о действующем веществе Алмотриптан предназначена для медицинских и фармацевтических специалистов, исключительно в справочных целях. Инструкция не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Содержащаяся здесь информация может меняться с течением времени. Наиболее точные сведения о применении препаратов, содержащих активное вещество Алмотриптан, содержатся в инструкции производителя, прилагаемой к упаковке.
Форма выпуска, упаковка и состав
препарата Тарка®
Таблетки с модифицированным высвобождением, покрытые пленочной оболочкой розового цвета, овальные, с гравировкой «Δ182» на одной стороне.
Вспомогательные вещества: слой верапамила гидрохлорида: целлюлоза микрокристаллическая — 59.1 мг, натрия алгинат — 240 мг, повидон (K30) — 36 мг, магния стеарат — 2.4 мг, вода — 22.5 мг; слой трандолаприла: крахмал кукурузный — 74.3 мг, лактозы моногидрат — 107 мг, повидон (К25) — 10.7 мг, гипромеллоза 6 мПа*с (тип 2910) — 4 мг, натрия стеарилфумарат — 2 мг.
Состав пленочной оболочки: гипромеллоза 6 мПа*с (тип 2910) — 11.608 мг, гипромеллоза 15 мПа*с — 1.152 мг, гипролоза 7 мПа*с — 1.152 мг, макрогол 400 — 1.8 мг, макрогол 6000 — 0.322 мг, тальк — 1.878 мг, кремния диоксид коллоидный — 0.03 мг, докузат натрия — 0.03 мг, титана диоксид (E171) — 1.912 мг, краситель железа оксид красный (Е172) — 0.112 мг, краситель железа оксид желтый (Е172) — 0.002 мг, краситель железа оксид черный (Е172) — 0.002 мг.
14 шт. — блистеры (1) — пачки картонные.
14 шт. — блистеры (2) — пачки картонные.
14 шт. — блистеры (4) — пачки картонные.
14 шт. — блистеры (7) — пачки картонные.
Фармакологическое действие
Комбинированное лекарственное средство.
Трандолаприл — ингибитор АПФ. Подавляет активность РААС в крови. Ингибирование АПФ приводит к снижению концентрации ангиотензина II в плазме крови, которое сопровождается уменьшением вазопрессорной активности и секреции альдостерона. Хотя выработка альдостерона уменьшается незначительно, тем не менее, может наблюдаться небольшое повышение концентрации калия в сыворотке в сочетании с потерей натрия и воды.
Снижение концентрации ангиотензина II по механизму обратной связи приводит к увеличению активности ренина в плазме крови. Другой функцией АПФ является разрушение кининов (брадикинина), обладающих мощным сосудорасширяющим свойством, до неактивных метаболитов. В связи с этим подавление АПФ приводит к повышению циркулирующих и тканевых концентраций калликреин-кининовой системы, что способствует расширению сосудов за счет активации системы простагландинов. Этот механизм, возможно, частично определяет гипотензивное действие ингибиторов АПФ и является причиной некоторых побочных эффектов.
У больных с артериальной гипертензией применение ингибиторов АПФ приводит к сопоставимому снижению АД в положении «лежа» и «стоя» без компенсаторного увеличения ЧСС. ОПСС снижается, сердечный выброс не меняется или увеличивается, почечный кровоток увеличивается, а скорость клубочковой фильтрации обычно не меняется. Резкое прекращение терапии не сопровождалось быстрым увеличением АД.
Антигипертензивный эффект трандолаприла проявляется через 1 ч после приема внутрь и сохраняется в течение, по крайней мере, 24 ч. В некоторых случаях оптимального контроля АД удается добиться только через несколько недель после начала лечения. При длительной терапии гипотензивный эффект сохраняется. Трандолаприл не ухудшает циркадный профиль АД.
Верапамил — блокатор кальциевых каналов, производное производное дифенилалкиламина. Ингибирует ток ионов кальция через медленные кальциевые канала мембран гладкомышечных клеток сосудов, проводящих и сократительных кардиомиоцитов. Верапамил вызывает снижение АД, как в покое, так и при физической нагрузке за счет расширения периферических артериол. В результате снижения ОПСС (постнагрузки) уменьшается потребность миокарда в кислороде и потребление энергии. Верапамил снижает сократимость миокарда. Отрицательный инотропный эффект препарата может компенсироваться уменьшением ОПСС. Сердечный индекс не снижается, за исключением больных с дисфункцией левого желудочка.
Фармакокинетика
Трандолаприл
После приема внутрь трандолаприл быстро всасывается. Абсолютная биодоступность около 10%. Тmax в плазме крови около 1 ч. Связывание трандолаприла с белками плазмы крови составляет около 80% и не зависит от концентрации. Vd трандолаприла около 18 л. T1/2 <1 ч. При многократном применении Css достигается примерно через 4 дня, как у здоровых добровольцев, так и у пациентов молодого и пожилого возраста с артериальной гипертензией.
В плазме крови трандолаприл подвергается гидролизу до образования активного метаболита трандолаприлата. Тmax трандолаприлата в плазме крови составляет 3-8 ч. Cmax и AUC не зависят от приема пищи. Абсолютная биодоступность трандолаприлата при приеме трандолаприла около 13%. Связь с белками крови зависит от концентрации и варьирует от 65% (при концентрации 1000 нг/мл) до 94% (при концентрации 0.1 нг/мл). В равновесном состоянии концентрация эффективного T1/2 трандолаприлата вместе с небольшой фракцией принятого препарата варьирует между 15 ч и 23 ч, что, вероятно, отражает связывание с плазменным и тканевым АПФ. Трандолаприлат обладает высоким сродством к АПФ. 9-14% дозы трандолаприла выводится в виде трандолаприлата почками. После приема меченного трандолаприла внутрь 33% препарата выводилось почками и 66% через кишечник. В незначительном количестве выводится в неизмененном виде через почки (менее 0.5 %). Почечный клиренс трандолаприлата варьирует от 0.15 до 4 л/ч в зависимости от дозы.
По сравнению со здоровыми добровольцами у пациентов на гемодиализе и с КК <30 мл/мин плазменная концентрация трандолаприлата примерно в 2 раза выше, а почечный клиренс снижен приблизительно на 85%. Пациентам с почечной недостаточностью рекомендована коррекция дозы.
По сравнению со здоровыми добровольцами у пациентов с алкогольным циррозом печени плазменная концентрация трандолаприла и трандолаприлата повышается в 9 и 2 раза соответственно, но АПФ-ингибирующая активность не изменяется. У пациентов с печеночной недостаточностью может потребоваться применение трандолаприла в меньших дозах.
Верапамил
Около 90% принятой внутрь дозы верапамила быстро всасывается в тонком кишечнике. Биодоступность составляет всего 22% из-за выраженного эффекта «первого прохождения» через печень. При повторном применении средняя биодоступность может возрастать до 30%. Прием пищи не оказывает влияния на биодоступность препарата. Тmax составляет 4-15 ч. Cmax норверапамила в плазме достигается примерно через 5-15 ч после приема. Css при многократном применении 1 раз/сут достигается через 3-4 дня. Связь с белками плазмы крови составляет около 90%. Одним из 12 метаболитов, обнаруженных в моче, является норверапамил, фармакологическая активность которого составляет 10-20% от таковой верапамила; его доля составляет 6% от выводимого препарата. Css норверапамила и верапамила сходные. T1/2 при повторном применении равен в среднем 8 ч. 3-4% дозы выводится почками в неизмененном виде. Метаболиты выводятся почками (70%) и через кишечник (16%). Биодоступность и T1/2 верапамила увеличиваются у пациентов с циррозом печени. Однако фармакокинетика верапамила остается без изменений у пациентов с компенсированным нарушением функции печени.
Показания активных веществ препарата
Тарка®
Эссенциальная артериальная гипертензия (у пациентов, которым показана комбинированная терапия).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Для приема внутрь. Разовую дозу принимают 1 раз/сут.
При длительном лечении максимальная суточная доза комбинации из расчета на верапамил не должна превышать 480 мг.
Побочное действие
Со стороны сердечно-сосудистой системы: часто — AV-блокада I степени, полная AV-блокада, стенокардия покоя, брадикардия, ощущение сердцебиения, тахикардия, артериальная гипотензия, гиперемия кожных покровов, приливы крови к коже лица, остановка синусового узла, сердечная недостаточность.
Со стороны нервной системы: часто — головная боль, головокружение, нарушение равновесия, парестезии, сонливость, обморок.
Нарушения психики: тревога, бессонница.
Со стороны органов чувств: нарушение зрения, «пелена» перед глазами; лабиринтное головокружение.
Со стороны дыхательной системы: часто — кашель, одышка, заложенность носа.
Со стороны пищеварительной системы: запор, тошнота, диарея, сухость слизистой оболочки полости рта, гиперплазия десен, боль в животе, дискомфорт в животе, рвота, панкреатит.
Инфекционные заболевания: бронхит.
Со стороны системы кроветворения: лейкопения, тромбоцитопения, агранулоцитоз.
Со стороны обмена веществ: гиперкалиемия.
Со стороны кожи и подкожных тканей: синдром Стивенса-Джонсона, ангионевротический отек, кожный зуд, сыпь, алопеция.
Со стороны костно-мышечной системы: артралгия, миалгия.
Со стороны мочевыделительной системы: поллакиурия, полиурия.
Со стороны половой системы: эректильная дисфункция.
Со стороны эндокринной системы: гиперпролактинемия, гинекомастия, галакторея.
Аллергические реакции: крапивница, гиперчувствительность.
Общие реакции: боль в груди, отеки, слабость, астения, лихорадка.
Результаты лабораторных исследований: повышение активности ЛДГ, активности ЩФ, концентрации креатинина, концентрации мочевины, активности АЛТ, АСТ в крови.
Противопоказания к применению
Ангионевротический отек в анамнезе, связанный с приемом ингибиторов АПФ; наследственный и идиопатический ангионевротический отек; кардиогенный шок; AV-блокада II или III степени (за исключением пациентов с искусственным водителем ритма); СССУ (за исключением пациентов с искусственным водителем ритма); сердечная недостаточность со сниженной фракцией выброса менее 35% и/или давления заклинивания легочной артерии более 20 мм рт.ст.; фибрилляция/трепетание предсердий при наличии дополнительных проводящих путей (в т.ч. у пациентов с синдромом WPW, Лауна-Ганонга-Левина — данные пациенты подвержены риску развития желудочковой тахиаритмии, в т.ч. фибрилляции желудочков в случае приема верапамила); аортальный стеноз или обструкция выносящего тракта левого желудочка; одновременное применение с бета-адреноблокаторами (в/в) (за исключением пациентов, проходящих лечение в отделении интенсивной терапии); тяжелые нарушения функции почек (КК менее 30 мл/мин), включая проведение гемодиализа; цирроз печени с асцитом; одновременное применение с алискиреном и алискиренсодержащими препаратами у пациентов с сахарным диабетом и/или нарушением функции почек (СКФ менее 60 мл/мин/1.73 м2); беременность, период грудного вскармливания; возраст до 18 лет; одновременное применение с ивабрадином; повышенная чувствительность к трандолаприлу, верапамилу или к любому другому ингибитору АПФ.
С осторожностью
Гиперкалиемия; при системных заболеваниях соединительной ткани (в т.ч. системная красная волчанка, склеродермия), особенно на фоне лечения кортикостероидами и антиметаболитами (риск развития агранулоцитоза и нейтропении); угнетение костномозгового кроветворения; острый инфаркт миокарда; AV блокада I степени; брадикардия; асистолия; симптоматическая артериальная гипотензия; состояния, сопровождающиеся снижением ОЦК (в т.ч. диарея, рвота); двусторонний стеноз почечных артерий; стеноз артерии единственной почки (например, после трансплантации почки); применение у представителей негроидной расы; нарушения функции печени; гипертрофическая обструктивная кардиомиопатия; заболевания, сопровождающиеся нарушением нервно-мышечной передачи (миастения, синдром Ламберта-Итона, мышечная дистрофия Дюшенна); у пациентов, соблюдающих диету с ограничением поваренной соли; перед процедурой афереза ЛПНП, одновременное проведение десенсибилизирующей терапии аллергенами (например, ядом перепончатокрылых) (риск развития анафилактоидных реакций (в некоторых случаях — жизнеугрожающих); хирургическое вмешательство (общая анестезия) (риск развития чрезмерного снижения АД); гемодиализ с применением высокопроточных полиакрилнитриловых мембран (риск развития анафилактоидных реакций); сердечная недостаточность с фракцией выброса более 35%; одновременное применение с дигоксином.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
С осторожностью следует назначать препарат пациентам с нарушением функции печени.
Применение при нарушениях функции почек
Противопоказано применение при тяжелом нарушении функции почек (КК<30 мл/мин.).
С осторожностью следует применять препарат при двустороннем стенозе почечных артерий, стенозе артерии единственной почки, состоянии после трансплантации почек.
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Применение у пожилых пациентов
У пациентов пожилого возраста возможно более выраженное снижение АД.
Особые указания
Поскольку трандолаприл метаболизируется в печени с образованием активного метаболита, пациентам с нарушением функции печени препарат следует назначать с осторожностью и при тщательном наблюдении врача.
У больных с неосложненной артериальной гипертензией после приема первой дозы трандолаприла или повышения дозы препарата отмечали развитие артериальной гипотензии, сопровождавшейся клиническими симптомами. Риск артериальной гипотензии более высокий при нарушении водно-электролитного баланса в результате длительной терапии диуретиками, ограничения потребления соли, диализа, диареи или рвоты. У таких пациентов перед началом терапии трандолаприлом следует прекратить терапию диуретиками и восполнить ОЦК и/или содержание натрия.
При лечении ингибиторами АПФ описаны случаи агранулоцитоза и угнетение функции костного мозга. Эти явления чаще встречаются у больных с нарушением функции почек, особенно с системными заболеваниями соединительной ткани. У таких пациентов (например, с системной красной волчанкой или склеродермией) целесообразно регулярно контролировать число лейкоцитов в крови и содержание белка в моче, особенно при нарушении функции почек, лечении кортикостероидами и антиметаболитами.
Трандолаприл может вызвать ангионевротический отек лица, языка, глотки и/или гортани. Есть данные о том, что ингибиторы АПФ чаще вызывают ангионевротический отек у пациентов негроидной расы.
На фоне лечения ингибиторами АПФ также были отмечены случаи ангионевротического отека кишечника. Такую возможность следует учитывать при развитии болей в животе (сопровождающихся тошнотой или рвотой, или без этих симптомов) на фоне приема трандолаприла.
Следует применения данной комбинации у пациентов с тяжелой дисфункцией левого желудочка (например, с фракцией выброса желудочка менее 30%, повышением давления заклинивания легочных капилляров более 20 мм рт.ст. или выраженными симптомами хронической сердечной недостаточности) и у больных с любой степенью дисфункции левого желудочка, если они получают бета-адреноблокаторы.
У некоторых больных, получающих диуретики (особенно в первые дни лечения), после назначения трандолаприла или увеличения его дозы, наблюдается резкое снижение АД.
При обследовании больных артериальной гипертензией следует всегда оценивать функцию почек. У пациентов с КК менее 30 мл/мин требуется назначение меньших доз трандолаприла.
У больных с нарушением функция почек, хронической сердечной недостаточностью, двусторонним стенозом почечных артерий или стенозом артерии единственной почки (например, после ее трансплантации) повышен риск ухудшения почечной функции. У некоторых больных артериальной гипертензией, без нарушения функции почек, при назначении трандолаприла в комбинации с диуретиком может наблюдаться повышение азота мочевины в крови и сывороточного креатинина.
При оперативных вмешательствах или проведении общей анестезии с применением препаратов, вызывающих артериальную гипотензию, трандолаприл может блокировать образование ангиотензина II, связанное с компенсаторным выбросом ренина.
У пациентов, получающих ингибиторы АПФ во время курса десенсибилизации (например, ядом перепончатокрылых), в редких случаях возможно развитие угрожающих жизни анафилактических реакций.
При проведении ЛПНП-афереза у пациентов, получающих ингибиторы АПФ, наблюдалось развитие жизнеугрожающих анафилактических реакций.
Данная комбинация может способствовать повышению содержания алкоголя в крови и замедлять его выведение. В связи с этим эффекты алкоголя могут быть усилены.
При применении во время гемодиализа высокопроточных мембран из полиакрилонитрила у больных, получавших ингибиторы АПФ, были описаны анафилактоидные реакции. У пациентов, получающих ингибиторы АПФ, следует избегать применения мембран подобного типа во время проведения гемодиализа.
Влияние на способность к управлению транспортными средствами и механизмами
Необходимо соблюдать осторожность при управлении транспортными средствами и занятии другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, особенно в начале лечения.
Лекарственное взаимодействие
Исследования in vitro свидетельствуют о том, что верапамил метаболизируется под действием изоферментов CYP3A4, CYP1A2, CYP2C8, CYP2C9 и CYP2C18.
Верапамил является ингибитором CYP3A4 и Р-гликопротеина. Клинически значимое взаимодействие было отмечено при одновременном применении с ингибиторами CYP3A4, при этом наблюдалось повышение уровня верапамила в плазме крови, в то время как индукторы CYP3A4 снижали концентрацию верапамила в плазме крови. Соответственно, при одновременном применении подобных средств следует учитывать возможность данного взаимодействия.
При одновременном применении верапамила с другими лекарственными препаратами возможны следующие эффекты.
Празозин — увеличение Cmax празозина (примерно 40%), не влияет на T1/2 празозина. Дополнительное антигипертензивное действие.
Теразозин — увеличение AUC теразозина (примерно 24%) и Cmax (примерно 25%).
Флекаинид — минимальное действие на плазменный клиренс флекаинида (<10%); не влияет на плазменный клиренс верапамила.
Хинидин — снижение перорального клиренса хинидина (примерно 35%). Усиление антигипертензивного действия. Может наблюдаться отек легких у пациентов с гипертрофической обструктивной кардиомиопатией.
Теофиллин — уменьшение перорального и системного клиренса (примерно 20%). У курящих — снижение примерно на 11%.
Карбамазепин — увеличение AUC карбамазепина (примерно 46%) у пациентов с резистентной парциальной эпилепсией. Увеличение концентрации карбамазепина, что может вызвать развитие побочных эффектов карбамазепина таких как диплопия, головная боль, атаксия или головокружение.
Фенитоин — уменьшение концентрации верапамила в плазме крови.
Имипрамин — увеличение AUC имипрамина (примерно 15%), не влияет на уровень активного метаболита, дезипрамина.
Глибурид — увеличивается Cmax глибурида (примерно 28%), AUC (примерно 26%).
Колхицин — увеличение AUC колхицина (примерно в 2 раза) и Сmax (примерно в 1.3 раза).
Кларитромицин, эритромицин, телитромицин — возможно повышение концентрации верапамила в плазме крови.
Рифампицин — уменьшение AUC (примерно 97%), Cmax (примерно 94%), биодоступности (примерно 92%) верапамила. Антигипертензивное действие может уменьшаться.
Доксорубицин — увеличение AUC (89%) и Cmax (61%) доксорубицина при приеме верапамила внутрь у пациентов с мелкоклеточным раком легких. Введение верапамила в/в у пациентов с прогрессирующими новообразованиями не влияет на плазменный клиренс доксорубицина.
Фенобарбитал — увеличение перорального клиренса верапамила примерно в 5 раз.
Буспирон — увеличение AUC и Cmax буспирона в 3.4 раза.
Мидазолам — увеличение AUC (примерно в 3 раза) и Cmax (примерно в 2 раза) мидазолама.
Метопролол — увеличение AUC (примерно 32.5%) и Cmax (примерно 41%) метопролола у пациентов со стенокардией.
Пропранолол — увеличение AUC (примерно 65%) и Cmax (примерно 94%) пропранолола у пациентов со стенокардией.
Дигитоксин — уменьшение общего клиренса (примерно 27%) и внепочечного клиренса (примерно 29%) дигитоксина.
Дигоксин — у здоровых добровольцев увеличиваются Cmax (примерно на 45-53%), Css (примерно на 42%) и AUC (примерно на 52%) дигоксина. Требуется снижение дозы дигоксина.
Циметидин — увеличивается AUC R- и S-верапамила (примерно 25% и 40% соответственно) с уменьшением клиренса R- и S-верапамила.
Циклоспорин — увеличиваются AUC, Css, Cmax (примерно на 45%) циклоспорина.
Сиролимус, такролимус, эверолимус — возможно повышение концентрации иммунодепрессантов в плазме крови.
Аторвастатин — возможно повышение концентрации аторвастатина, повышение концентрации верапамила примерно на 42.8% в плазме крови.
Ловастатин — возможно повышение концентрации ловастатина в плазме.
Симвастатин — увеличение AUC (примерно в 2.6 раз) и Cmax (примерно в 4.6 раз) симвастатина.
Алмотриптан — увеличение AUC (примерно 20%) и Cmax (примерно 24%) алмотриптана.
Сульфинпиразон — увеличение перорального клиренса верапамила (примерно в 3 раза), снижение его биодоступности (примерно 60%). Антигипертензивное действие может уменьшаться.
Дабигатран — увеличение Сmax (до 90%) и AUC (до 70%) дабигатрана. Может повышаться риск кровотечений.
Грейпфрутовый сок — увеличение AUC R- и S-верапамила (примерно 49% и 37% соответственно) и Cmax R- и S-верапамила (примерно 75% и 51% соответственно). T1/2 и почечный клиренс не изменялись.
Зверобой продырявленный — уменьшается AUC R- и S-верапамила (примерно 78% и 80% соответственно) с уменьшением Cmax.
При одновременном применении с комбинацией трандолаприл+верапамил антиаритмических средств и бета-адреноблокаторов возможно усиление неблагоприятного влияния на сердечно-сосудистую систему (более выраженная AV-блокада, более значительное снижение ЧСС, развитие сердечной недостаточности и усиление артериальной гипотензии).
При одновременном применении антигипертензивных средств, диуретиков и вазодилататоров с комбинацией трандолаприл+верапамил усиливается гипотензивное действие.
При одновременном применении с комбинацией трандолаприл+верапамил празозина, теразозина усиливается гипотензивное действие.
При одновременном применении с комбинацией трандолаприл+верапамил некоторые препараты для лечения ВИЧ-инфекции (ритонавир), могут ингибировать метаболизм верапамила, что приводит к увеличению его концентрации в плазме крови. При одновременном применении дозы верапамила должны быть снижены.
При одновременном применении лития с комбинацией трандолаприл+верапамил повышается нейротоксичность лития.
У пациентов с ИБС при назначении верапамила после приема дантролена были отмечены случаи гиперкалиемии и подавления функции миокарда. Совместное применением препаратов противопоказано.
При одновременном применении сульфинпиразона с комбинацией трандолаприл+верапамил возможно уменьшение гипотензивного действия верапамила.
При одновременном применении с комбинацией трандолаприл+верапамил эффект миорелаксантов может усилиться.
При одновременном применении ацетилсалициловой кислоты в качестве антиагрегантного средства с верапамилом может повыситься склонность к кровотечениям.
При одновременном применении с верапамилом уровень этанола в плазме крови повышается.
Диуретики или другие гипотензивные лекарственные средства могут усилить гипотензивное действие трандолаприла.
Калийсберегающие диуретики (спиронолактон, амилорид, триамтерен) или препараты калия повышают риск гиперкалиемии, особенно у больных почечной недостаточностью. Трандолаприл может уменьшить потерю калия при совместном применении с тиазидными диуретиками.
Одновременное применение трандолаприла (как и любых ингибиторов АПФ) с гипогликемическими средствами (инсулином или пероральными гипогликемическими средствами) может усилить гипогликемический эффект и привести к повышению риска гипогликемии.
Трандолаприл может ухудшить выведения лития. Необходим контроль уровня лития в сыворотке крови.
НПВС могут уменьшить гипотензивное действие трандолаприла, поэтому при присоединении НПВС к терапии трандолаприлом или их отмене необходим контроль АД.
Ингибиторы АПФ могут усилить гипотензивное действие некоторых средств для ингаляционного наркоза.
Аллопуринол, цитостатики, иммуносупрессивные средства и системные кортикостероиды или прокаинамид могут повысить риск развития лейкопении при лечении ингибиторами АПФ.
Антациды могут снизить биодоступность ингибиторов АПФ.
Антигипертензивное действие ингибиторов АПФ может быть снижено при совместном назначении симпатомиметиков. В таких случаях необходим тщательный мониторинг.
Как и в случае применения любых других гипотензивных средств, совместное назначение нейролептиков или трициклических антидепрессантов увеличивает риск развития ортостатической гипотензии.
From Wikipedia, the free encyclopedia
 |
|
 |
|
| Clinical data | |
|---|---|
| Trade names | Axert |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a603028 |
| License data |
|
| Routes of administration |
By mouth |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | 70% |
| Protein binding | 35% |
| Metabolism | Liver |
| Elimination half-life | 3–4 hours |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| IUPHAR/BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| Chemical and physical data | |
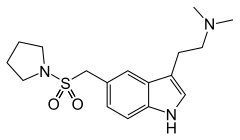
| Formula | C17H25N3O2S |
| Molar mass | 335.47 g·mol−1 |
| 3D model (JSmol) |
|
|
SMILES
|
|
|
InChI
|
|
| |
Almotriptan (trade name Axert and others) is a triptan medication discovered and developed by Almirall for the treatment of heavy migraine headache.
It was patented in 1992 and approved for medical use in 2000.[4]
Medical uses[edit]
Almotriptan is prescribed to treat the acute headache phase of migraine attacks with or without aura.[5] Almotriptan is the only oral triptan approved in the US for the treatment of migraine in adolescent from 12 to 17 years of age.[citation needed]
Efficacy[edit]
The efficacy and tolerability of almotriptan has been studied in numerous randomised, controlled trials totaling more than 4800 adults with either moderate or severe attacks of migraine. Its efficacy is significantly more effective than placebo and alleviates nausea, photophobia and phonophobia linked to migraine attacks. Almotriptan has similar efficacy as a standard dose of sumatriptan, another triptan drug, and fewer adverse effects.[6]
Contraindications[edit]
As with other triptans, almotriptan should not be used in patients with a history, symptoms or signs of ischaemic heart disease (myocardial infarction, angina pectoris, documented silent ischaemia, Prinzmetal’s angina) or severe hypertension and uncontrolled mild or moderate hypertension.
Other contraindications are previous cerebrovascular accident (CVA) or transient ischaemic attack (TIA), peripheral vascular disease, severe hepatic impairment, concomitant administration of ergotamine, ergotamine derivatives (including methysergide) and other 5-HT1B/D agonists.
Side effects[edit]
Almotriptan has proved to have an adverse effects profile similar to placebo when used following the Summary of Product Characteristics instructions (see references).
Pharmacology[edit]
Mechanism of action[edit]
Like all triptans, almotriptan has a high and specific affinity for serotonin 5-HT1B/1D receptors. Binding of the drug to the receptor leads to vasoconstriction of the cranial (brain) blood vessels and thus affects the redistribution of blood flow. Almotriptan significantly increases cerebral blood flow and reduces blood flow through extracerebral cranial vessels. Even though it affects cranial blood vessels a single standard dose of almotriptan has no clinically significant effect on blood pressure or heart rate in both young and elderly healthy volunteers. Larger doses seem to slightly increase blood pressure but not beyond clinical relevance.[6]
Pharmacokinetics[edit]
Almotriptan has linear pharmacokinetics up to the 16-fold standard dose. Its biological half-life is 3 hours, and its bioavailability 70%.
Cmax is observed 1.5–4 hours after oral administration, and approximately 50% of the drug is excreted unchanged in the urine. Metabolism is mediated through the enzymes MAO-A and CYP3A4 and CYP2D6 oxidation.
Almotriptan clearance is moderately reduced in the elderly but does not require dose adjustment. Sex does not alter the pharmacokinetics of the drug. People with moderate-to-severe renal dysfunction are recommended to use only half the dose.[7]
Interactions[edit]
Almotriptan is metabolized mainly by MAO-A and to lesser extent by CYP3A4 and CYP2D6. Studies of drugs used as preventive against migraine (propranolol and verapamil), anti-depressants (moclobemide and fluoxetine) yielded results that showed significant altering of the pharmacokinetics of almotriptan though they were deemed not clinically relevant.[6]
Society and culture[edit]
Brand names[edit]
Brand names include Axert (US, Canada), Almogran (Belgium, Denmark, Finland, France, Germany, Italy, Ireland Portugal, Spain, the United Kingdom, the Netherlands, Sweden, Switzerland, South Korea…), Almotrex (Italy), Almozen (Bulgaria and Poland) and Amignul (Spain).
References[edit]
- ^ «Almotriptan tablet, film coated». DailyMed. Retrieved 17 February 2021.
- ^ «Axert- almotriptan malate tablet, coated». DailyMed. Retrieved 17 February 2021.
- ^ «Active substance: almotriptan» (PDF). List of nationally authorised medicinal products. Europeans Medicines Agency. 11 February 2021.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 531. ISBN 9783527607495.
- ^ «Almotriptan Facts and Comparisons». Drugs.com. Retrieved 7 October 2012.
- ^ a b c Keam SJ, Goa KL, Figgitt DP (2002). «Almotriptan: a review of its use in migraine». Drugs. 62 (2): 387–414. doi:10.2165/00003495-200262020-00010. PMID 11817980. S2CID 242752549.
- ^ McEnroe JD, Fleishaker JC (2005). «Clinical pharmacokinetics of almotriptan, a serotonin 5-HT(1B/1D) receptor agonist for the treatment of migraine». Clinical Pharmacokinetics. 44 (3): 237–246. doi:10.2165/00003088-200544030-00002. PMID 15762767. S2CID 23136754.
External links[edit]
- «Almotriptan». Drug Information Portal. U.S. National Library of Medicine.
- «Almotriptan malate». Drug Information Portal. U.S. National Library of Medicine.
Суматриптан
(Sumatriptan)
0.027 ‰
Выбор описания
| Лек. форма | Дозировка |
|---|---|
|
таблетки, покрытые пленочной оболочкой |
50 мг 100 мг |
|
таблетки |
50 мг 100 мг |
таблетки, покрытые пленочной оболочкой
Суматриптан (таблетки, покрытые пленочной оболочкой, 50 мг), инструкция по медицинскому применению РУ № ЛП-003957
Дата последнего изменения: 08.11.2021
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Суматриптан
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Таблетки,
покрытые пленочной оболочкой.
Состав
На
одну таблетку 50 мг 100 мг
Активное вещество:
Суматриптана
сукцинат 70,0 мг 140,0 мг
в
пересчете на суматриптан 50,0 мг 100,0 мг
Вспомогательные вещества ядра таблетки:
Лактозы
моногидрат 125,0 мг 250,0 мг
Целлюлоза
микрокристаллическая 100,0 мг 200,0 мг
Магния
стеарат 1,5 мг 3,0 мг
Кроскармеллоза
натрия 2,0 мг 4,0 мг
Тальк 1,5 мг 3,0 мг
Вспомогательные вещества пленочной оболочки:
Гипромеллоза 5,9 мг 11,8 мг
Макрогол
6000 (полиэтиленгликоль 6000) 2,3 мг 4,6 мг
Титана
диоксид 0,92 мг 1,84 мг
Полисорбат-
80 0,88 мг 1,76 мг
Описание лекарственной формы
Таблетки
круглые, двояковыпуклые, покрытые пленочной оболочкой белого цвета.
Фармакокинетика
Приступы
мигрени не оказывают существенного влияния на фармакокинетику суматриптана,
принимаемого внутрь.
Всасывание
После
приема внутрь быстро всасывается, через 45 мин его концентрация в плазме
достигает 70% от максимальной. После приема 100 мг среднее значение
максимальной концентрации в плазме крови составляет 54 нг/мл.
Средняя величина абсолютной биодоступности составляет 14%,
частично вследствие пресистемного метаболизма, частично из-за неполной
абсорбции.
Распределение
Суматриптан
связывается с белками плазмы в незначительной степени (14–21%), средний общий
объем распределения 170 л.
Метаболизм
Главный
метаболит, индолуксусный аналог суматриптана, выводится, преимущественно, с мочой,
в виде свободной кислоты и глюкуронида. Этот метаболит не обладает активностью
по отношению к 5‑HT1‑
и 5‑HT2‑серотониновым
рецепторам. Второстепенные метаболиты суматриптана не обнаружены.
Выведение
Период
полувыведения составляет приблизительно 2 ч.
Средний общий плазменный клиренс составляет примерно 1160 мл/мин,
средний почечный клиренс составляет примерно 260 мл/мин;
внепочечный клиренс — около 80% от общего клиренса.
Суматриптан
метаболизируется под действием моноаминоксидазы А.
Особые группы пациентов
Пациенты с нарушением функции печени
Вследствие
снижения пресистемного клиренса суматриптана у пациентов с нарушением функции
печени повышается содержание суматриптана в плазме крови.
Пациенты разных возрастных групп
Фармакокинетика
у пациентов старше 65 лет значимо не отличается от таковой у пациентов более
молодого возраста.
Нет
значимых различий в фармакокинетики суматриптана у пациентов различных
этнических групп.
Фармакодинамика
Суматриптан
— селективный агонист сосудистых 5-гидрокситриптамин-1-рецепторов (5‑HT1D),
не влияет
на другие подтипы 5‑HT‑рецепторов
(5‑HT2–5‑HT7).
Рецепторы 5‑HT1D расположены,
главным образом, в краниальных кровеносных сосудах головного мозга, и их
стимуляция приводит к сужению этих сосудов.
У
животных суматриптан избирательно действует на вазоконстрикцию ветвей сонной
артерии, не влияя
на кровоток в сосудах головного мозга. Сосудистый бассейн сонной артерии
кровоснабжает экстракраниальные и интракраниальные ткани (в том числе
менингеальные оболочки), и считается, что расширение этих сосудов и/или отек их
стенок является основным механизмом возникновения мигрени у человека. Кроме
того, доклинические данные позволяют судить о том, что суматриптан снижает
чувствительность тройничного нерва. Оба эти эффекта могут лежать в основе
противомигренозного действия суматриптана. Суматриптан эффективен при лечении
менструальной мигрени, т.е. мигрени без ауры, которая возникает за 3 дня
до — 5 дней
после менструального цикла. Клинический эффект отмечается обычно через 30 минут
после перорального приема 100 мг препарата. Несмотря на то, что
рекомендованная доза при пероральном приеме составляет 50 мг, приступы
мигрени различаются по степени тяжести как у одного пациента, так и у разных
пациентов. Дозы от 25 мг до 100 мг показали большую эффективность по
сравнению с плацебо в клинических исследованиях, но доза 25 мг
статистически значительно менее эффективна, чем 50 мг и 100 мг.
Показания
Купирование
приступов мигрени с аурой или без нее, включая приступы
менструально-ассоциированной мигрени.
Назначают
только при верифицированном диагнозе мигрень.
Противопоказания
–
Гиперчувствительность
к любому из компонентов препарата.
–
Гемиплегическая,
базилярная или офтальмоплегическая формы мигрени.
–
Ишемическая
болезнь сердца (ИБС) (в том числе подозрение на нее), стенокардия (в том числе
стенокардия Принцметала), инфаркт миокарда (в том числе в анамнезе),
постинфарктный кардиосклероз, а также симптомы, позволяющие предположить
наличие ишемической болезни сердца.
–
Фармакологически
неконтролируемая артериальная гипертензия.
–
Окклюзионные
заболевания периферических сосудов.
–
Инсульт или
преходящее нарушение мозгового кровообращения (в том числе в анамнезе).
–
Тяжелые
нарушения функции печени и/или почек.
–
Одновременный
прием с эрготамином или его производными (включая метисергид) или другими
триптаминами/агонистами 5‑HT1‑серотониновых
рецепторов.
–
Применение на
фоне приема ингибиторов моноаминоксидазы не ранее, чем через 2 недели
после отмены этих препаратов.
–
Возраст до 18
лет и старше 65 лет (эффективность и безопасность не установлены).
–
В связи с
наличием в составе препарата лактозы, его прием противопоказан при врожденной
непереносимости лактозы, дефиците лактазы, глюкозо-галактозной мальабсорбции.
С осторожностью
–
Артериальная
гипертензия (контролируемая).
–
Эпилепсия (в том
числе любые состояния со сниженным эпилептическим порогом).
–
Заболевания, при
которых могут изменяться всасывание, метаболизм или выведение этого препарата
(например, нарушение функции почек или печени).
–
Беременность.
–
Период грудного
вскармливания.
–
У пациентов с
повышенной чувствительностью к сульфаниламидам (прием суматриптана может
вызвать аллергические реакции, выраженность которых варьируется от кожных
проявлений до анафилаксии). Данные о перекрестной чувствительности ограничены,
однако следует соблюдать осторожность при назначении суматриптана таким
пациентам.
Применение при беременности и кормлении грудью
Беременность
Применение
суматриптана при беременности возможно только в случае, если предполагаемая
польза для матери превосходит потенциальный риск для плода (адекватных и строго
контролируемых исследований безопасности применения не проведено).
Доступны
данные пострегистрационного наблюдения более 1000 женщин, принимавших
суматриптан во время I триместра
беременности. В связи с недостаточным объемом информации окончательные выводы о
повышении риска врожденных пороков делать преждевременно. Опыт применения
суматриптана во II и III триместрах беременности ограничен.
Результаты
экспериментальных исследований на животных не показали прямого тератогенного
действия суматриптана на плод или отрицательного влияния на пери- и
постнатальное развитие эмбриона или плода у крыс. Однако есть данные о влиянии
суматриптана на жизнеспособность эмбриона и плода у кроликов при приеме больших
доз суматриптана.
Период грудного вскармливания
Суматриптан
проникает в грудное молоко. Во избежание отрицательного воздействия на ребенка,
следует прекратить грудное вскармливание во время применения суматриптана и в
течение 24 ч
после окончания его применения.
Способ применения и дозы
Реклама: ООО «РЛС-Библиомед», ИНН 7714758963, erid=4CQwVszH9pUmKjt23pm
Внутрь.
Таблетку следует проглатывать целиком, запивая водой.
Суматриптан
применяется для интермиттирующей терапии приступов мигрени. Препарат не следует
применять в профилактических целях.
Начинают
лечение как можно раньше после возникновения приступа мигрени (хотя препарат
одинаково эффективен на любой стадии приступа). Для купирования острых
приступов мигрени взрослым — 50 мг, в некоторых случаях доза может быть
увеличена до 100 мг.
Для
купирования последующих приступов (при уменьшении или исчезновении симптомов, а
затем возобновлении) можно принять вторую дозу в течение следующих 24 ч
при условии, что интервал между приемом составляет не менее
2 ч.
В течение любого 24 ч
периода максимальная доза — 300 мг/сут. Если симптомы мигрени не исчезают
и не уменьшаются после приема первой дозы, то повторно для купирования
продолжающегося приступа вторую дозу не назначают. В этом случае может
назначаться парацетамол, ацетилсалициловая кислота или нестероидные
противовоспалительные препараты. Суматриптан может быть принят для купирования
последующих приступов. Суматриптан рекомендуется применять в качестве
монотерапии мигрени, не следует
применять суматриптан одновременно с эрготамином или его производными (включая
метисергид).
Пациентам с нарушением функции печени:
рекомендованная доза — 50 мг.
Дети
Эффективность
и безопасность суматриптана у детей в возрасте менее 10 лет не изучались. Нет
доступных клинических данных для этой возрастной группы.
Эффективность
и безопасность суматриптана у детей от 10 до 17 лет не были продемонстрированы
в клинических исследованиях, проведенных в этой возрастной группе. Поэтому
использование суматриптана у детей от 10 до 17 лет не рекомендовано.
Пожилые пациенты (старше 65 лет)
Опыт
использования суматриптана у пациентов в возрасте старше 65 лет ограничен.
Побочные действия
Нежелательные
реакции, представленные ниже, перечислены в соответствии с поражением систем
органов и частотой встречаемости. Частота определена следующим образом: очень часто (>1/10); часто (>1/100 и <1/10);
нечасто (>1/1000 и <1/100);
редко (>1/10000 и <1/1000);
очень редко (<1/10000); неизвестно (частота не может быть оценена
по имеющимся данным).
Данные клинических исследований
Нарушения со стороны нервной системы
Часто
— головокружение, сонливость, нарушения чувствительности (включая парестезии и
снижение чувствительности).
Нарушения со стороны сосудов
Часто
— преходящее повышение артериального давления (вскоре после приема препарата),
приливы.
Нарушения со стороны дыхательной системы, органов грудной
клетки и средостения
Часто
— одышка.
Нарушения со стороны желудочно-кишечного тракта
Часто
— тошнота, рвота (причинно-следственная связь возникновения нежелательных
реакций с приемом препарата не доказана).
Нарушения со стороны скелетно-мышечной и соединительной
ткани
Часто
— чувство тяжести (обычно преходящее, может быть интенсивным и возникать в
любой части тела, включая грудную клетку и горло).
Общие расстройства и нарушения в месте введения
Часто
— болевые ощущения, чувство холода или жара, чувство давления или стягивания
(обычно преходящие, могут быть интенсивными и возникать в любой части тела,
включая грудную клетку и горло), слабость, утомляемость (обычно слабо или
умеренно выраженные, преходящие).
Лабораторные и инструментальные данные
Очень
редко — незначительные отклонения показателей печеночных проб.
Данные пострегистрационных наблюдений
Нарушения со стороны иммунной системы
Неизвестно
— реакции повышенной чувствительности, которые варьируют от кожных проявлений
повышенной чувствительности до анафилаксии.
Нарушения со стороны нервной системы
Неизвестно
— судорожные припадки (в ряде случаев наблюдавшиеся у пациентов с судорожными
приступами в анамнезе или при сопутствующих состояниях, предрасполагающих к
возникновению судорог; у части пациентов факторов риска не было
выявлено), тремор, дистония, нистагм, скотома.
Нарушения со стороны органа зрения
Неизвестно
— мелькание, диплопия, снижение остроты зрения. Потеря зрения (обычно преходящая).
Однако расстройства зрения могут быть обусловлены собственно приступом мигрени.
Нарушения со стороны сердца
Неизвестно
— брадикардия, тахикардия, сердцебиение, аритмии, ЭКГ-признаки транзиторной
ишемии миокарда, коронарный вазоспазм, стенокардия, инфаркт миокарда.
Нарушения со стороны сосудов
Неизвестно
— снижение артериального давления, синдром Рейно.
Нарушения со стороны желудочно-кишечного тракта
Неизвестно
— ишемический колит, диарея.
Нарушения со стороны скелетно-мышечной и соединительной
ткани
Неизвестно
— ригидность шеи, артралгия.
Нарушения психики
Неизвестно
— тревога.
Нарушения со стороны кожи и подкожных тканей
Неизвестно
— гипергидроз.
Взаимодействие
Не
отмечено взаимодействия суматриптана с пропранололом, флунаризином, пизотифеном
и этиловым спиртом у здоровых добровольцев.
Противопоказано
одновременное применение суматриптана и эрготамина или других
триптанов/агонистов 5‑HT1‑серотониновых
рецепторов. Теоретически возможно повышение риска коронарного вазоспазма, и
совместное применение данных препаратов противопоказано (см. раздел
«Противопоказания»).
Период
времени, который должен пройти между применением суматриптана и
эрготаминсодержащих препаратов или другого триптана/агониста 5‑HT1‑рецепторов,
неизвестен. Он будет зависеть, в том числе, от дозы и типа назначаемых
препаратов. Действие может носить аддитивный характер. Рекомендуется выдержать,
по меньшей мере, 24 часа после применения препаратов, содержащих эрготамин
или другой триптан/агонист 5‑HT1‑рецепторов
перед применением суматриптана. И наоборот, рекомендуется выждать, по
меньшей мере, 6 часов после применения суматриптана перед применением
препаратов, содержащих эрготамин, и как минимум 24 часа до применения
другого триптана/5‑HT1‑агониста
рецепторов.
Возможно
взаимодействие между суматриптаном и ингибиторами МАО, их одновременное
применение противопоказано (см. раздел «Противопоказания»).
Имеются
редкие сообщения о развитии серотонинового синдрома (включая расстройства
психики, вегетативную лабильность и нервно-мышечные нарушения) в результате
одновременного применения селективных ингибиторов обратного захвата серотонина
(СИОЗС) и суматриптана. Также сообщалось о развитии серотонинового синдрома на
фоне одновременного применения триптанов с селективными ингибиторами обратного
захвата серотонина и норадреналина (СИОЗСН).
Побочные
реакции отмечаются чаще при одновременном применении триптанов с лекарственными
средствами, содержащими зверобой продырявленный.
Передозировка
Симптомы
При
приеме внутрь до 400 мг не наблюдается каких-либо других побочных реакций,
кроме перечисленных выше.
Лечение
Наблюдение
за состоянием пациента не менее 10 ч, при необходимости — поддерживающая
терапия. Нет данных о влиянии гемодиализа или перитонеального диализа на
концентрацию суматриптана в плазме.
Особые указания
Суматриптан
следует применять только у пациентов с установленным диагнозом мигрень.
Не показано применение суматриптана при гемиплегической, базилярной и
офтальмоплегической мигрени.
Не
следует превышать рекомендуемые дозы суматриптана. Как и в случае применения
других лекарственных препаратов для лечения острых приступов мигрени, перед
лечением приступа головной боли у пациентов, у которых ранее не
диагностировалась мигрень или у пациентов с атипичной формой мигрени необходимо
исключить другие потенциально серьезные виды неврологической патологии. Следует
отметить, что у пациентов с мигренью повышен риск развития определенных
цереброваскулярных нарушений (например, инсульта или транзиторных ишемических
атак (ТИА)).
После
приема препарата Суматриптан могут возникнуть такие преходящие симптомы, как
боль и давящее чувство в груди. Симптомы могут носить интенсивный характер и
распространяться на область шеи. Если есть основания полагать, что эти симптомы
являются проявлением ишемической болезни сердца (ИБС), дальнейшее применение
суматриптана следует прекратить и провести соответствующее диагностическое
обследование. Пациентам с факторами риска развития ишемической болезни сердца,
в т.ч. заядлым курильщикам или пациентам, использующим заместительную
никотиновую терапию, без предварительного обследования сердечно-сосудистой
системы, не следует назначать суматриптан. Особое внимание следует уделять
женщинам в постменопаузе и мужчинам в возрасте старше 40 лет, имеющим
перечисленные факторы риска. Однако обследование не всегда позволяет выявить
заболевание сердца, и в очень редких случаях серьезные кардиологические
осложнения возникали у пациентов без сопутствующих сердечно-сосудистых
заболеваний.
Препарат
Суматриптан следует применять с осторожностью у пациентов с контролируемой
артериальной гипертензией легкой степени, так как у небольшого количества
пациентов наблюдалось транзиторное повышение артериального давления и
периферического сосудистого сопротивления. Имеются редкие сообщения, полученные
в результате пострегистрационного наблюдения, о развитии серотонинового
синдрома (включая расстройства психического статуса, вегетативную лабильность и
нервно-мышечные нарушения) в результате одновременного применения селективных
ингибиторов обратного захвата серотонина (СИОЗС) и суматриптана. Также
сообщалось о развитии серотонинового синдрома на фоне одновременного применения
суматриптана с триптанами и селективными ингибиторами обратного захвата
норадреналина (СИОЗСН).
Если
у пациента клинически оправдано одновременное применение препаратов группы
СИОЗС и/или СИОЗСН, следует тщательно контролировать состояние пациента.
Препарат Суматриптан следует применять с осторожностью у пациентов, у которых
могут существенно изменяться всасывание, метаболизм или экскреция суматриптана,
например, у пациентов с печеночной недостаточностью или нарушением функции
почек. У пациентов с печеночной недостаточностью начальная доза должна
составлять 50 мг.
Препарат
Суматриптан необходимо применять с осторожностью у пациентов с судорогами в
анамнезе или другими факторами риска снижения порога судорожной готовности,
поскольку при приеме суматриптана были зарегистрированы случаи судорог.
У
пациентов с установленной гиперчувствительностью к сульфаниламидам прием
препарата Суматриптан может вызывать аллергические реакции, которые варьируют
от кожных реакций гиперчувствительности до анафилаксии. Данные о перекрестной
чувствительности ограничены, поэтому следует соблюдать осторожность перед применением
препарата Суматриптан этими пациентами.
Побочные
реакции могут отмечаться чаще при одновременном применении триптанов и
лекарственных средств, содержащих зверобой продырявленный. Длительное
применение любых типов болеутоляющих препаратов при головных болях может
приводить к их усилению. При возникновении данной ситуации или подозрении на
нее, необходимо прекратить терапию и провести дополнительное обследование.
Головная боль, вызванная чрезмерным использованием лекарственных препаратов,
может быть заподозрена у пациентов, страдающих периодическими или ежедневными
головными болями, несмотря на регулярный прием медикаментов от головной боли.
Пациенты с редкими наследственной непереносимостью лактозы, дефицитом лактазы и
глюкозо-галактозной мальабсорбцией не должны принимать препарат Суматриптан,
так как в его состав входит лактоза.
Влияние на способность управлять
транспортными средствами, механизмами
У
пациентов с мигренью может возникать сонливость, связанная как с самим
заболеванием, так и с приемом препарата Суматриптан. Пациенты должны быть
особенно осторожными при вождении автотранспорта и занятиями другими
потенциально опасными видами деятельности, требующими повышенной концентрации
внимания и быстроты психомоторных реакций.
Форма выпуска
Таблетки,
покрытые пленочной оболочкой 50 мг, 100 мг.
По
2 или 6 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и
фольги алюминиевой печатной лакированной.
По
2 или 6 таблеток в банку стеклянную для хранения лекарственных средств типа БТС
с треугольным венчиком, укупоренную крышкой натягиваемой с уплотняющим
элементом.
1
контурную ячейковую упаковку или банку с инструкцией по применению помещают в
пачку из картона.
Условия отпуска из аптек
Условия хранения
В
защищенном от света месте при температуре не выше 25 °C.
Хранить
в недоступном для детей месте.
Срок годности
3
года.
Не
применять по истечении срока годности.
Дата обновления: 29.08.2023
Аналоги (синонимы) препарата Суматриптан
Заказ в аптеках
| Название препарата | Цена за упак., руб. | Аптеки |
|---|---|---|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
105.00 |
|
|
|
123.00 |

|
|
|
140.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
524.00 |
|
|
|
524.00 |

|
|
|
721.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
85.00 |
|
|
|
136.00 |
|
|
|
212.00 |

|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
86.00 |
|
|
|
86.00 |

|
|
|
93.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
104.00 |
|
|
|
145.00 |
|
|
|
149.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
30.00 |
|
|
|
174.00 |
|
|
|
177.00 |

|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
132.00 |
|
|
|
191.00 |

|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
427.00 |
|
|
|
522.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
93.00 |
|
|
|
123.00 |

|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
122.00 |
|
|
|
151.00 |

|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
98.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
220.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
75.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
211.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
135.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
75.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
112.00 |
|
|
|
Суматриптан, таблетки, покрытые пленочной оболочкой, |
||
|
608.00 |
|
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.

